
OCTREOTIDA TEVA 10 MG POLVO Y DISOLVENTE PARA SUSPENSION INYECTABLE DE LIBERACION PROLONGADA EFG

Cómo usar OCTREOTIDA TEVA 10 MG POLVO Y DISOLVENTE PARA SUSPENSION INYECTABLE DE LIBERACION PROLONGADA EFG
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
OctreotidaTeva10 mg polvo y disolvente para suspensión inyectable de liberación prolongada EFG
OctreotidaTeva20 mg polvo y disolvente para suspensión inyectable de liberación prolongada EFG
OctreotidaTeva30 mg polvo y disolvente para suspensión inyectable de liberación prolongada EFG
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Octreotida Teva y para qué se utiliza
- Qué necesita saber antes de empezar a usar Octreotida Teva
- Cómo usar Octreotida Teva
- Posibles efectos adversos
- Conservación de Octreotida Teva
- Contenido del envase e información adicional
1. Qué es Octreotida Teva y para qué se utiliza
Octreotida es un compuesto sintético derivado de la somatostatina. La somatostatina se encuentra normalmente en el cuerpo humano, donde inhibe la liberación de algunas hormonas como la hormona del crecimiento. Las ventajas de octreotida respecto a somatostatina son que es más potente y sus efectos son más duraderos.
Para qué se utiliza
- para tratar la acromegalia,
La acromegalia es una enfermedad en la que el cuerpo produce demasiada hormona del crecimiento. Normalmente la hormona del crecimiento controla el crecimiento de los tejidos, los órganos y los huesos. Un exceso de hormona del crecimiento supone un aumento en el tamaño de los huesos y los tejidos, especialmente en las manos y los pies. Octreotida reduce notablemente los síntomas de la acromegalia, que incluyen dolor de cabeza, exceso de sudoración, adormecimiento de las manos y los pies, cansancio y dolor en las articulaciones. En la mayoría de los casos, la sobreproducción de hormona del crecimiento está causada por aumento del tamaño de la glándula pituitaria (adenoma pituitario); el tratamiento con este medicamento puede reducir el tamaño del adenoma.
Este medicamento se utiliza para tratar personas que sufren acromegalia:
- cuando otros tipos de tratamiento para la acromegalia (cirugía o radioterapia) no son adecuados o no han funcionado correctamente;
- después de la radioterapia, para cubrir el periodo de tiempo intermedio hasta que la radioterapia es completamente eficaz.
- para aliviar los síntomas asociados con la sobreproducción de algunas hormonas específicas y otras sustancias relacionadas en el estómago, intestino o páncreas.
La sobreproducción de unas hormonas específicas y de otras sustancias naturales relacionadas puede estar causada por algunas alteraciones raras del estómago, intestino o páncreas. Esto altera el equilibrio hormonal natural y provoca una serie de síntomas como sofocos, diarrea, baja tensión arterial, erupción cutánea y pérdida de peso. El tratamiento con este medicamento ayuda a controlar estos síntomas.
- para tratar tumores neuroendocrinos localizados en el intestino (p.ej. apéndice, intestino delgado o colon),
Los tumores neuroendocrinos son tumores raros que se pueden encontrar en diferentes partes del cuerpo. Octreotida también se utiliza para controlar el crecimiento de estos tumores, cuando están localizados en el intestino (p.ej. apéndice, intestino delgado o colon)
- para tratar tumores pituitarios que producen demasiada hormona estimulante del tiroides (TSH).
Un exceso de hormona estimulante del tiroides (TSH) provoca hipertiroidismo. Octreotida se utiliza para tratar personas con tumores pituitarios que producen demasiada hormona estimulante del tiroides (TSH):
- cuando otros tipos de tratamiento (cirugía o radioterapia) no son adecuados o no han funcionado;
- después de la radioterapia, para cubrir el periodo hasta que la radioterapia es completamente efectiva.
2. Qué necesita saber antes de empezar a usar Octreotida Teva
Siga todas las instrucciones que le dé su médico cuidadosamente. Pueden ser diferentes de la información contenida en este prospecto.
Lea las siguientes indicaciones antes de utilizar este medicamento.
No useOctreotidaTeva
- si es alérgico a octreotida o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico antes de empezar a usar Octreotida Teva:
- si sabe que tiene actualmente cálculos en la vesícula biliar, o los ha tenido en el pasado presenta alguna complicación como fiebre, escalofríos, dolor abdominal, o coloración amarillenta de la piel o los ojos; informe a su médico, pues el uso prolongado de este medicamento puede provocar la formación de cálculos biliares. Su médico podría querer controlar su vesícula biliar periódicamente.
- si sabe que tiene diabetes, ya que este medicamento puede afectar los niveles de azúcar en la sangre. Si es diabético, debe controlar regularmente sus niveles de azúcar.
- si tiene antecedentes de deficiencia de vitamina B12 su médico puede controlar el nivel de B12 periódicamente.
Análisis y controles
Si recibe tratamiento con este medicamento durante un periodo prolongado de tiempo, su médico puede controlar su función tiroidea periódicamente.
Su médico controlará la función de su hígado.
Su médico podrá comprobar el funcionamiento de sus enzimas pancreáticas.
Niños
Existe poca experiencia con el uso de este medicamento en niños.
Uso de Octreotida Teva con otros medicamentos
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
Normalmente puede continuar tomando otros medicamentos mientras esté en tratamiento con este medicamento. Sin embargo, se han notificado que algunos medicamentos como cimetidina, ciclosporina, bromocriptina, quinidina y terfenadina se ven afectados por este medicamento.
Si está tomando un medicamento para controlar la presión arterial (p.ej. un beta bloqueante o un antagonista de los canales del calcio) o un agente para controlar el equilibrio de líquidos y electrolitos, su médico puede necesitar ajustar la dosis.
Si es diabético, su médico puede necesitar ajustar su dosis de insulina.
Si va a recibir tratamiento con lutecio (177Lu) oxodotreotida, un radiofármaco, su médico puede interrumpir y/o adaptar el tratamiento con Sandostatin LAR durante un periodo corto de tiempo.
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento.
Sólo se debe utilizar octreotida durante el embarazo si es estrictamente necesario.
Las mujeres en edad fértil deben utilizar un método anticonceptivo eficaz durante el tratamiento.
No debe dar lactancia durante el tratamiento con este medicamento. Se desconoce si octreotida pasa a la leche materna.
Conducción y uso de máquinas
Octreotida Teva no tiene efectos o éstos son insignificantes sobre la capacidad de conducir o utilizar máquinas. Sin embargo algunos de estos efectos adversos que puede sufrir durante el tratamiento con este medicamento, como dolor de cabeza y cansancio, pueden reducir su capacidad para conducir y utilizar máquinas de forma segura.
OctreotidaTevacontiene sodio
Octreotida Teva contiene menos de 23 mg de sodio (1 mmol) por dosis; esto es esencialmente “exento de sodio”.
3. Cómo usar Octreotida Teva
Este medicamento se debe administrar siempre como una inyección en el músculo de los glúteos. Con la administración repetida, se debe utilizar el glúteo derecho e izquierdo alternativamente.
Si usa másOctreotidaTevadel que debe
No se han notificado reacciones adversas que suponen una amenaza vital después de una sobredosis con Octreotida Teva.
Los síntomas de sobredosis son: sofocos, micciones frecuentes, cansancio, depresión, ansiedad y falta de concentración.
Si piensa que ha sufrido una sobredosis y presenta alguno de estos síntomas, informe a su médico inmediatamente. También puede llamar al Servicio de Información Toxicológica, Tel. 91 562 0420.
Si olvidó usarOctreotidaTeva
Si ha olvidado su inyección, se recomienda que se la administren tan pronto como se acuerde, y después continuar con la pauta habitual. No va a provocarle ningún daño el hecho de recibir una dosis unos días más tarde, pero pueden reaparecer temporalmente los síntomas hasta que vuelva a la pauta habitual de tratamiento.
Si interrumpe el tratamiento conOctreotidaTeva
Si interrumpe su tratamiento con este medicamento pueden reaparecer sus síntomas. Por tanto, no interrumpa el tratamiento con octreotida a menos que se lo indique su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, enfermero o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Algunos efectos adversos pueden ser graves. Si usted tiene algunos de los efectos adversos indicados a continuación, acudan inmediatamente a su médico:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Cálculos biliares, que conllevan dolor de espalda repentino.
- Demasiado azúcar en la sangre.
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
- Disminución de la actividad de la glándula tiroidea (hipotiroidismo) que causa cambios en el ritmo del corazón, el apetito o el peso; cansancio, sensación de frío, o hinchazón en la parte de delante del cuello.
- Cambios en los análisis de la función tiroidea.
- Inflamación de la vesícula biliar (colecistitis); los síntomas pueden incluir dolor en la parte superior derecha del abdomen, fiebre, náuseas, coloración amarilla de la piel y los ojos (ictericia).
- Muy poco azúcar en la sangre.
- Alteración de la tolerancia a la glucosa.
- Latido del corazón lento.
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- Sed, baja eliminación de orina, color oscuro en la orina, piel seca enrojecida.
- Latido del corazón rápido.
Otros efectos adversos graves
- Reacciones de hipersensibilidad (alérgicas) incluyendo urticaria en la piel.
- Un tipo de reacción alérgica (anafilaxis) que puede causar dificultad para tragar o respirar, hinchazón y hormigueo, posiblemente con una disminución de la tensión arterial con mareo o pérdida de conciencia.
- Una inflamación de la glándula del páncreas (pancreatitis); los síntomas pueden incluir dolor repentino en la parte superior del abdomen, náuseas, vómitos, diarrea.
- Inflamación del hígado (hepatitis); síntomas que pueden incluir color amarillento de la piel y los ojos (ictericia), náuseas, vómitos, pérdida de apetito, sensación general de malestar, picor, orina ligeramente coloreada.
- Latido del corazón irregular.
- Nivel bajo en el recuento de plaquetas en la sangre; esto puede suponer un aumento en el sangrado o en la aparición de moratones.
Informe a su médico inmediatamente si nota alguno de las reacciones adversas anteriores.
Otros efectos adversos:
Informe a su médico, farmacéutico o enfermero si nota alguno de los efectos adversos enumerados a continuación. Normalmente son leves y tienden a desaparecer al avanzar el tratamiento.
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Diarrea.
- Dolor abdominal.
- Náuseas.
- Estreñimiento.
- Flatulencia (gases).
- Dolor de cabeza.
- Dolor local en el lugar de inyección.
Frecuentes(puede afectar hasta 1 de cada 10 personas):
- Molestia en el estómago después de comer (dispepsia).
- Vómitos.
- Sensación de tener el estómago lleno.
- Heces grasas.
- Heces líquidas.
- Cambio de color de las heces.
- Mareo.
- Pérdida de apetito.
- Cambios en los análisis sobre la función del hígado.
- Pérdida de pelo.
- Dificultad para respirar.
- Debilidad.
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, enfermero o farmacéutico.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: http://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Octreotida Teva
Mantener este medicamento fuera de la vista y del alcance de los niños.
Conservar en el embalaje original para protegerlo de la luz.
Conservar en nevera (entre 2ºC y 8ºC). No congelar.
Este medicamento se puede conservar por debajo de 25ºC el día de la inyección.
No se debe conservar Octreotida Teva después de la reconstitución (se debe utilizar inmediatamente).
No utilice este medicamento después de la fecha de caducidad que aparece en el envase y en la etiqueta después de CAD. La fecha de caducidad es el último día del mes que se indica.
No utilice este medicamento si observa presencia de partículas o un cambio de color.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Octreotida Teva
- El principio activo es octreotida.
Un vial contiene 10 mg, 20 mg o 30 mg de octreotida (como octreotida acetato).
- Los demás componentes son:
En el polvo (vial): poli(DL-láctido-co-glicólido) y manitol (E-421).
En el disolvente (jeringa precargada): carmelosa sódica, manitol (E-421), poloxamer y agua para preparaciones inyectables
Aspecto de Octreotida Teva y contenido del envase
Octreotida 10 mg: Cada envase contiene un vial de vidrio con 10 mg de octreotida con un tapón de goma sellado con un tapón de aluminio con una lengüeta azul oscuro, 1 jeringa precargada de vidrio con 2 ml de disolvente, 1 aguja de inyección de seguridad y un adaptador al vial o 3 viales con 10 mg de octreotida cada uno, 3 jeringas precargadas de vidrio con 2 ml de disolvente, 3 agujas de inyección de seguridad y 3 adaptadores al vial.
Octreotida 20 mg: Cada envase contiene un vial de vidrio con 20 mg de octreotida con un tapón de goma sellado con un tapón de aluminio con una lengüeta naranja, 1 jeringa precargada de vidrio con 2 ml de disolvente, 1 aguja de inyección de seguridad y un adaptador al vial o 3 viales con 20 mg de octreotida cada uno, 3 jeringas precargadas de vidrio con 2 ml de disolvente, 3 agujas de inyección de seguridad y 3 adaptadores al vial.
Octreotida 30 mg: Cada envase contiene un vial de vidrio con 30 mg de octreotida con un tapón de goma sellado con un tapón de aluminio con una lengüeta rojo oscuro, 1 jeringa precargada de vidrio con 2 ml de disolvente,1 aguja de inyección de seguridad y un adaptador al vial o 3 viales con 30 mg de octreotida cada uno, 3 jeringas precargadas de vidrio con 2 ml de disolvente, 3 agujas de inyección de seguridad y 3 adaptadores al vial.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Teva B.V.
Swensweg 5,
2031GA Haarlem,
Países Bajos
Responsable de la fabricación
Merckle GmbH
Ludwig-Merckle-Str. 3,
Blaubeuren
89143, Alemania
ó
PLIVA HRVATSKA d.o.o. (PLIVA CROATIA Ltd.)
Prilaz baruna Filipovicá 25,
Zagreb, 10000
Croacia
ó
PHARMATHEN INTERNATIONAL S.A
Industrial Park Sapes,
Rodopi Prefecture, Block No 5,
Rodopi 69300,
Grecia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Teva Pharma, S.L.U.
C/ Anabel Segura, 11, Edificio Albatros B, 1ª planta
28108, Alcobendas, Madrid (España)
Fecha de la última revisión de este prospecto: Marzo 2022
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) http://www.aemps.gob.es
------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Cuánto Octreotida Teva se debe utilizar
Acromegalia
Se recomienda iniciar el tratamiento con la administración de 20 mg de este medicamento a intervalos de 4 semanas durante 3 meses. Los pacientes en tratamiento con octreotida s.c. pueden iniciar el tratamiento con este medicamento el día después de la última dosis de octreotida s.c.. El ajuste de dosis subsiguiente se debe basar en las concentraciones séricas de la hormona del crecimiento (GH) y el factor de crecimiento 1 de tipo insulina/somatomedina C (IGF-1) y los síntomas clínicos.
Para los pacientes en los que no están controlados completamente los síntomas clínicos y los parámetros bioquímicos (GH; IGF-1) en un periodo de 3 meses (concentraciones de GH todavía por encima de 2,5 microgramos/L), se puede aumentar la dosis a 30 mg cada 4 semanas. Si después de 3 meses, no están controlados adecuadamente GH, IGF-1, y/o los síntomas a la dosis de 30 mg, la dosis se puede aumentar a 40 mg cada 4 semanas.
Para pacientes con concentraciones de GH que se encuentran de forma constante por debajo de 1 microgramo/L, y con concentraciones séricas de IGF-1 normalizadas, y en los cuales la mayoría de los signos/síntomas reversibles de acromegalia han desaparecido después de 3 meses de tratamiento con 20 mg, se pueden administrar 10 mg de este medicamento cada 4 semanas. Sin embargo, especialmente en este grupo de pacientes, se recomienda controlar estrechamente las concentraciones séricas de GH e IGF-1, y los signos/síntomas a esta dosis baja de este medicamento.
Para pacientes que están tratados con una dosis estable de este medicamento, la valoración de GH e IGF-1 se debe realizar cada 6 meses.
Tumores endocrinos gastroenteropancreáticos
- Tratamiento de pacientes con síntomas asociados con tumores neuroendocrinos gastroenteropancreáticos funcionales
Se recomienda iniciar el tratamiento con la administración de 20 mg de este medicamento a intervalos de 4 semanas. Los pacientes en tratamiento con octreotida s.c. deben continuar a la dosis previamente efectiva durante 2 semanas después de la primera inyección de este medicamento.
Para pacientes en los que los síntomas y los marcadores biológicos están bien controlados después de 3 meses de tratamiento, se puede reducir la dosis a 10 mg de este medicamento cada 4 semanas.
Para pacientes en los que los síntomas están sólo parcialmente controlados después de 3 meses de tratamiento, se puede aumentar la dosis a 30 mg de este medicamento cada 4 semanas.
Para los días en que pueden aumentar los síntomas asociados con tumores gastroenteropancreáticos durante el tratamiento con este medicamento, se recomienda la administración adicional de octreotida s.c. a la dosis utilizada antes del tratamiento con este medicamento. Esto puede aparecer principalmente en los 2 primeros meses de tratamiento hasta que se alcancen las concentraciones terapéuticas de octreotida.
- Tratamiento de pacientes con Tumores Neuroendocrinos avanzados del intestino o de origen desconocido donde se ha excluido los lugares de origen que no sean del intestino
La dosis recomendada de octreotida es de 30 mg administrado cada 4 semanas. El tratamiento con este medicamento para controlar el tumor se debe continuar en ausencia de progresión del tumor.
Tratamiento de adenomas secretores de TSH
El tratamiento con octreotida se debe iniciar a la dosis de 20 mg a intervalos de 4 semanas durante 3 meses antes de considerar un ajuste de dosis. Después la dosis se ajusta en base de la TSH y de la respuesta de la hormona tiroidea.
Instrucciones para la preparación y la inyección intramuscular de OctreotidaTeva
SÓLO PARA INYECCIÓN INTRAMUSCULAR
Componentes del kit de inyección:
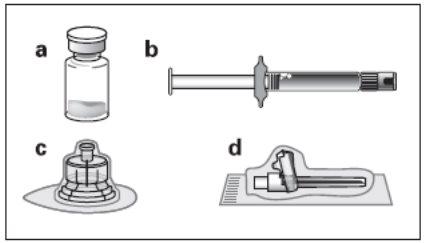
a Un vial que contiene el polvo de este medicamento
b Una jeringa precargada que contiene el disolvente para la reconstitución
c Un adaptador al vial para la reconstitución del medicamento
d Una aguja de inyección de seguridad
Siga cuidadosamente las instrucciones que se indican a continuación para asegurar la reconstitución de este medicamento antes de la inyección intramuscular profunda.
Hay tres pasos críticos en el proceso de reconstitución de Octreotida Teva. Si no se realizan correctamente, podría suponer que no se administre el medicamento de forma adecuada.
- El kit de inyección debe alcanzar la temperatura ambiente.Sacar el kit de inyección de la nevera y dejar que el kit alcance la temperatura ambiente durante un mínimo de 30 minutos antes de la reconstitución, pero sin que se superen las 24 h.
- Después de añadir la solución del diluyente, dejar reposar el vial durante 5 minutos para asegurar que el polvo queda completamente saturado.
- Después de la saturación, agitar el vial moderadamenteen dirección horizontal durante un mínimo de 30 segundos, hasta que se forme una suspensión uniforme. La suspensión de octreotida sólo se debe preparar inmediatamenteantes de la administración.
Octreotida Teva debe ser administrado sólo por un profesional sanitario experto.
Paso 1
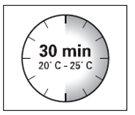
- Sacar de la nevera el kit de inyección de este medicamento.
ATENCIÓN: es esencial iniciar el proceso de reconstitución
sólo después de que el kit de inyección haya alcanzado la
temperatura ambiente. Dejar que el kit alcance la temperatura
ambiente durante un mínimo de 30 minutos antes de la reconstitución
pero no exceder las 24 h.
Nota: El Kit de inyección puede refrigerarse de nuevo, en caso necesario.
Paso 2
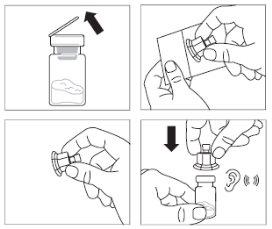
- Retirar la lengüeta de plástico del vial y limpiar
el tapón de caucho del vial con una toallita con alcohol.
- Retirar la lámina protectora del envoltorio y retirar
el adaptador del vial de su embalaje sujetando entre
el tapón luer blanco y el embalaje de plástico.
NOtoque la punta del dispositivo de acceso
en ningún lugar.
- Coloque el vial en una superficie plana. Coloque el
adaptador del vial en la parte superior del vial y
apretarlo completamente hacia abajo para que encaje
encima del vial. Esto lo confirmará cuando escuche un “click”.
- Limpiar la punta del adaptador del vial con algodón con alcohol.
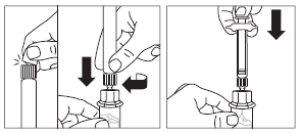 Paso 3
Paso 3
- Retirar el tapón blanco liso de la jeringa precargada
que contiene el disolvente y enroscar la jeringa en
el adaptador de vial.
- Presionar lentamente el émbolo hasta el fondo hasta
transferir toda la solución diluyente al vial.
Paso 4
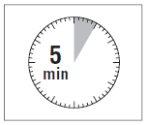
ATENCIÓN:Es esencial dejar reposar el vial durante 5 minutos
para asegurar que el disolvente ha saturado completamente el polvo.
Nota: es normal que el émbolo se desplace hacia arriba, ya que puede
haber una sobrepresión en el vial.
- En este punto, preparar al paciente para administrarle la inyección.
Paso 5
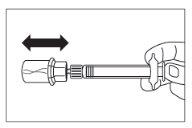 Después del periodo de saturación, asegurarse que se presiona
Después del periodo de saturación, asegurarse que se presiona
el émbolo hacia el fondo de la jeringa.
ATENCIÓN: Mantener el émbolo presionado y agitar el vial
moderadamenteen sentido horizontal durante un mínimo de
30 segundospara que el polvo esté completamente suspendido
en el disolvente (suspensión uniforme de consistencia lechosa).
Repetir la agitación moderada durante otros 30 segundos más
si el polvo no está completamente suspendido.
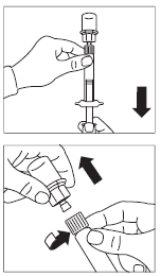
Paso 6
- Girar la jeringa y el vial boca abajo, y lentamente tirar del émbolo
hasta transferir el contenido completo del vial a la jeringa.
- Desenroscar la jeringa del adaptador del vial.
Paso 7
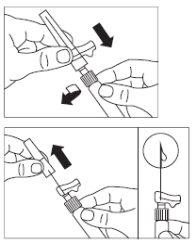
- Preparar el lugar de inyección con un algodón con alcohol.
- Enroscar la aguja de inyección de seguridad en la jeringa.
- Si se retrasa la administración inmediata, re-agitar
moderadamente la jeringa para asegurar la suspensión
uniforme, de consistencia lechosa.
- Retirar la cubierta protectora de la aguja.
- Golpear suavemente la jeringa para desplazar cualquier burbuja
visible y expulsarla fuera de la jeringa.
- Pasar inmediatamenteal Paso 8 para la administración al paciente.
Cualquier retraso en la administración puede producir unasedimentación.
Paso 8
- Octreotida debe administrarse sólo mediante inyección
intramuscular profunda, NUNCAse debe administrar por vía intravenosa.
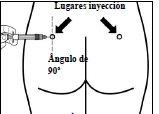 Insertar la aguja completamente en el glúteo derecho o izquierdo,
Insertar la aguja completamente en el glúteo derecho o izquierdo,
formando un ángulo de 90º con la piel.
- Lentamente aspirar con el émbolo para comprobar que no se ha
penetrado un vaso sanguíneo (si fuera así, cambiar la zona de punción).
- Utilizando una presión constantesobre el émbolo, administrar lentamente hasta que la jeringa esté vacía. Extraer la aguja del lugar de inyección y
- activar el mecanismo de seguridad (tal como se muestra en el Paso 9).
 Paso 9
Paso 9
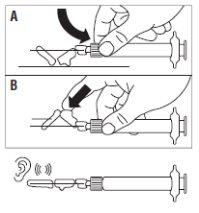
- Activar el mecanismo de seguridad sobre la aguja, utilizando
uno de los dos métodos siguientes:
- o bien presionando la sección articulada del dispositivo de
seguridad hacia abajo sobre una superficie rígida (figura A)
- o bien presionando la parte articulada con un dedo (figura B)
- El sonido de un “click” confirma la activación adecuada.
- Nota: Registre el sitio de inyección en el registro del paciente y
alterne mensualmente
Desechar la jeringa inmediatamente (en un contenedor de objetos punzante).
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a OCTREOTIDA TEVA 10 MG POLVO Y DISOLVENTE PARA SUSPENSION INYECTABLE DE LIBERACION PROLONGADA EFGForma farmacéutica: INYECTABLE, Octreotida 100 microgramos/mlPrincipio activo: OctreotidaFabricante: Gp Pharm S.A.Requiere recetaForma farmacéutica: INYECTABLE, Octreotida 500 microgramos/mlPrincipio activo: OctreotidaFabricante: Gp Pharm S.A.Requiere recetaForma farmacéutica: INYECTABLE, 200 microgramos/mlPrincipio activo: OctreotidaFabricante: Gp Pharm S.A.Requiere receta
Médicos online para OCTREOTIDA TEVA 10 MG POLVO Y DISOLVENTE PARA SUSPENSION INYECTABLE DE LIBERACION PROLONGADA EFG
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de OCTREOTIDA TEVA 10 MG POLVO Y DISOLVENTE PARA SUSPENSION INYECTABLE DE LIBERACION PROLONGADA EFG, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes






