NEMLUVIO 30 MG POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN PLUMA PRECARGADA

Cómo usar NEMLUVIO 30 MG POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN PLUMA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Nemluvio 30 mg polvo y disolvente para solución inyectable en pluma precargada
nemolizumab
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Nemluvio y para qué se utiliza
- Qué necesita saber antes de empezar a usar Nemluvio
- Cómo usar Nemluvio
- Posibles efectos adversos
- Conservación de Nemluvio
- Contenido del envase e información adicional
1. Qué es Nemluvio y para qué se utiliza
Nemluvio contiene el principio activo nemolizumab, un anticuerpo monoclonal (una proteína especializada que reconoce una diana específica y se une a ella).
Nemluvio se utiliza en adultos y adolescentes de 12 años en adelante para tratar la dermatitis atópica de moderada a grave (también llamada eccema atópico cuando la piel presenta picor, enrojecimiento y sequedad). Se puede utilizar cuando los pacientes pueden recibir tratamientos sistémicos (un medicamento administrado por vía oral o mediante inyección).
Nemluvio también se utiliza en adultos para tratar el prurigo nodular (PN) de moderado a grave, también llamado prurigo nodular crónico (PNC), una afección de la piel de larga duración asociada a un sarpullido que provoca urticaria. Se utiliza cuando los pacientes pueden recibir tratamientos sistémicos.
Nemolizumab, el principio activo de Nemluvio, bloquea la acción de una proteína llamada interleucina (IL)-31. La IL-31 desempeña un papel importante en la inflamación y el picor de la piel que se observan en las personas con dermatitis atópica y prurigo nodular. Al bloquear la IL-31, este medicamento puede reducir estos síntomas.
2. Qué necesita saber antes de empezar a usar Nemluvio
No use Nemluvio
- Si es alérgico al nemolizumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Si cree que podría tener alergia o no lo sabe con seguridad, consulte a su médico, farmacéutico o enfermero antes de usar Nemluvio.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Nemluvio.
Trazabilidad
Es importante llevar un registro del número de lote de Nemluvio. Cada vez que obtenga un nuevo envase de Nemluvio, anote la fecha y el número de lote (se indica en el envase después de “Lote”) y guarde esta información en un lugar seguro.
Reacciones alérgicas
Nemluvio puede causar reacciones alérgicas (hipersensibilidad) que pueden ser graves. Las reacciones alérgicas se producen poco después de utilizar este medicamento, pero también pueden producirse más tarde. Debe estar alerta a los signos de estas reacciones mientras esté utilizando Nemluvio. Estas pueden ser:
- problemas para respirar
- hinchazón de la cara, la boca y la lengua
- desmayos, mareos o sensación de mareo debido a tensión arterial baja
- urticaria
- picor
- erupción cutánea
Si nota algún signo de reacción alérgica, deje de utilizar Nemluvio y avise a su médico o solicite atención médica de inmediato.
Empeoramiento del asma
Si tiene una enfermedad respiratoria grave como el asma, la enfermedad pulmonar obstructiva crónica (EPOC) o la bronquitis crónica, consulte a su médico antes de tomar Nemluvio. Si su enfermedad respiratoria empeora después de iniciar el tratamiento con Nemluvio, informe a su médico inmediatamente.
Vacunación
Se aconseja completar el plan de vacunación recomendado en su caso antes de empezar a tomar Nemluvio. Debe evitar la vacunación con vacunas con microorganismos vivos cuando use Nemluvio. Hable con su médico sobre su plan de vacunación actual.
Niños y adolescentes
- No administre este medicamento a niños con dermatitis atópica menores de 12 años y peso corporal inferior a 30 kg; no se ha estudiado en este grupo de edad.
- No administre este medicamento a niños y adolescentes con prurigo nodular menores de 18 años; no se ha estudiado en este grupo de edad.
Otros medicamentos y Nemluvio
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
- Informe a su médico o farmacéutico si se ha vacunado recientemente o tiene previsto hacerlo.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Embarazo
Se desconocen los efectos de este medicamento en mujeres embarazadas; por tanto, es preferible evitar el uso de Nemluvio durante el embarazo a menos que su médico le aconseje utilizarlo.
Lactancia
Se desconoce si Nemluvio pasa a la leche materna. Nemluvio puede pasar a la leche materna en los primeros días después del parto. Por tanto, debe informar a su médico si está amamantando o tiene previsto hacerlo, para que usted y su médico puedan decidir si se le puede administrar Nemluvio.
Conducción y uso de máquinas
Es improbable que Nemluvio influya sobre la capacidad para conducir y utilizar máquinas.
3. Cómo usar Nemluvio
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
El tratamiento debe ser iniciado y supervisado por un médico con experiencia en el diagnóstico y el tratamiento de la dermatitis atópica y el prurigo nodular.
Cuánto Nemluvio se administra y durante cuánto tiempo
Su médico decidirá cuánto Nemluvio necesita y durante cuánto tiempo lo utilizará.
Pacientes adultos y adolescentes con dermatitis atópica (a partir de 12 años de edad)
La dosis recomendada de Nemluvio es:
- Una primera dosis de 60 mg (dos inyecciones de 30 mg)
- Dosis posteriores de 30 mg cada 4 semanas durante 16 semanas
Después de 16 semanas de tratamiento, su médico comprobará la eficacia del medicamento para usted. Si el médico decide que continuar usándolo le será beneficioso, seguirá tomando una dosis de 30 mg cada 8 semanas.
Nemluvio puede utilizarse con o sin medicamentos para el eccema que se usan en la piel (tópicos).
Adultos con prurigo nodular (PN)
La dosis recomendada se basa en el peso corporal.
Si pesa menos de 90 kg:
- Una primera dosis de 60 mg (dos inyecciones de 30 mg)
- Dosis posteriores de 30 mg cada 4 semanas
Si pesa 90 kg o más:
- Una primera dosis de 60 mg (dos inyecciones de 30 mg)
- Dosis posteriores de 60 mg (dos inyecciones de 30 mg) cada 4 semanas
Después de 16 semanas de tratamiento, su médico comprobará la eficacia del medicamento para usted para decidir si continuar usándolo le será beneficioso.
Cómo usar Nemluvio
Lea atentamente las instrucciones de uso incluidas al final de este prospecto antes de utilizar Nemluvio. Las instrucciones presentan paso a paso cómo debe usar el medicamento.
Nemluvio se administra en forma de inyección bajo la piel (inyección subcutánea) utilizando la pluma precargada. Se debe inyectar en la parte delantera alta del muslo o en el vientre, evitando la zona de 5 cm alrededor del ombligo. Si es otra persona quien le administra la inyección, también se puede administrar en la parte superior del brazo.
Usted y su médico o enfermero decidirán si puede inyectarse este medicamento usted mismo/a. Solo podrá inyectarse usted mismo/a después de que su médico o enfermero le hayan enseñado a hacerlo. Asimismo, un cuidador puede administrarle la inyección después de haber recibido la formación adecuada.
Se recomienda ir cambiando el lugar de la inyección con cada inyección. Nemluvio no se debe inyectar en zonas de piel sensible, inflamada, hinchada, sensible o dañada, ni de piel con moratones, cicatrices o heridas abiertas.
Si usa más Nemluvio del que debe
Si ha usado más Nemluvio del que debe o ha tomado la dosis siguiente demasiado pronto, consulte a su médico, farmacéutico o enfermero.
Si olvidó usar Nemluvio
No tome una dosis doble para compensar las dosis olvidadas. Si olvida inyectarse una dosis de Nemluvio, adminístresela lo antes posible y continúe con su calendario original.
Si interrumpe el tratamiento con Nemluvio
No deje de usar Nemluvio sin hablar primero con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos graves
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
Nemluvio puede causar reacciones alérgicas (hipersensibilidad). Deje de utilizar Nemluvio y avise a un médico o solicite atención médica de inmediato si nota algún signo de reacción alérgica.Los signos pueden ser, entre otros:
- problemas para respirar
- hinchazón de la cara, la boca y la lengua
- desmayos, mareos, sensación de mareo debido a tensión arterial baja
- urticaria
- picor
- erupción cutánea
Otros efectos adversos
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
- Infecciones de la piel por hongos como la dermatofitosis corporal (tiña corporal) o el pie de atleta (tiña de pie), las infecciones de las uñas por hongos y la tiña inguinal
- Dolor de cabeza
- Empeoramiento del asma (en las personas con asma preexistente)
- Eccema
- Dermatitis atópica (piel con picor, enrojecimiento y sequedad en las personas propensas a las alergias)
- Eccema discoide (eccema numular) (afección de la piel que causa zonas de piel inflamada con picor y sequedad de forma redondeada u ovalada)
- Reacciones en el lugar de la inyección, que incluyen enrojecimiento, picor, moratones, dolor, irritación e hinchazón en el lugar de la inyección
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- Aumento del número de glóbulos blancos, que puede observarse en el análisis de sangre (eosinofilia)
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Nemluvio
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja después de CAD. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 °C y 8 °C). No congelar.
Conservar en el embalaje original para protegerlo de la luz.
Si es necesario, Nemluvio se puede conservar a temperatura ambiente (hasta 25 °C) durante un único periodo de 90 días como máximo. Anote la fecha en que sacó la pluma de la nevera en el espacio proporcionado en la caja exterior. No utilice Nemluvio si se ha pasado la fecha de caducidad o si han transcurrido 90 días desde que lo sacó de la nevera (lo que ocurra antes).
Una vez finalizados los pasos para la reconstitución, Nemluvio se debe utilizar en un plazo de 4 horas o desecharse.
No utilice este medicamento si observa que el polvo no es blanco.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenidodel envase e información adicional
Composición de Nemluvio
- El principio activo es nemolizumab.Cada pluma precargada de un solo uso contiene 30 mg de nemolizumab.
- Los demás componentes son:
- Polvo:sacarosa, trometamol, clorhidrato de trometamol (para ajustar el pH), hidrocloruro de arginina, poloxámero 188.
- Disolvente:agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Nemluvio polvo y disolvente para solución inyectable en pluma precargada consiste en una pluma precargada de un solo uso que contiene un cartucho de vidrio que suministra un polvo blanco y un líquido transparente e incoloro. El líquido no es visible desde la ventana de inspección antes de la disolución.
Nemluvio se presenta en una pluma precargada de 30 mg en un envase que contiene 1 pluma precargada o en envases múltiples que contienen 2 o 3 cajas, cada una con 1 pluma precargada.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Galderma International
La Defense 4, Tour Europlaza
20 Avenue Andre Prothin
92927 Paris La Defense Cedex
Francia
Responsables de la fabricación
Q-Med AB
Seminariegatan 21
Uppsala Lan
752 28 Uppsala
Suecia
Nuvisan France S.A.R.L.
2400 Route Des Colles
06410 Biot
Francia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien Luxembourg/Luxemburg Galderma Benelux BV Tél/Tel: +31 183691919 e-mail: [email protected] | Ireland Galderma (UK) Ltd. Tel: +44 (0)300 3035674 e-mail: [email protected] |
| Latvija
Tel: +371/67/103205 e-mail: [email protected] |
Ceská republika Slovenská republika Galenoderm s.r.o. Tel: +421 2 49 10 90 10 e-mail: [email protected] | Lietuva
Tel: +370/52/711710 e-mail: [email protected] |
Danmark Norge Ísland Suomi/Finland Sverige Galderma Nordic AB Tlf/Sími/Puh/Tel: + 46 18 444 0330 e-mail: [email protected] | Magyarország Ewopharma Hungary Kft. Tel.: +36 1 200 4650 e-mail: [email protected] |
Deutschland Galderma Laboratorium GmbH Tel: + 49 (0) 800 – 5888850 e-mail: [email protected] | Malta Prohealth Limited Tel. +356 21461851, +356 21460164 e-mail: [email protected] |
Eesti
Tel: + 372/6/460980 e-mail: [email protected] | Nederland Galderma Benelux BV Tel: + 31 183691919 e-mail: [email protected] |
Ελλáδα Κúπρος Pharmassist Ltd Τηλ: + 30 210 6560700 e-mail: [email protected] | Österreich Galderma Austria GmbH Tel: 0043 732 715 993 e-mail: [email protected] |
España Laboratorios Galderma SA Tel: + 34 902 02 75 95 e-mail: [email protected] | Polska Galderma Polska Sp. z o.o. Tel.: + 48 22 331 21 80 e-mail: [email protected] |
France Galderma International Tél: +33 (0)1 58 86 45 45 e-mail: [email protected] | Portugal Laboratorios Galderma SA – Sucursal em Portugal Tel: + 351 21 315 19 40 e-mail: [email protected] |
Hrvatska Medical Intertrade d.o.o. T: +385 1 333 6036 e-mail: [email protected] | România Neola pharma SRL Tel: + 40 21 233 17 81 e-mail: [email protected] |
Italia Galderma Italia S.p.A. Tel: +39 3371176197 e-mail: [email protected] | Slovenija Medical Intertrade d.o.o. T: +386 1 2529 113 F: +386 1 2529 114 e-mail: [email protected] |
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu.
-----------------------------------------------------------------------------------------------------------------------------------
Instrucciones de uso
IMPORTANTE: leer el prospecto antes de utilizar este medicamento. Esta pluma requiere unos pasos específicos antes de la inyección.
Nemluvio 30 mg polvo y disolvente para solución inyectable en pluma precargada (nemolizumab)
No se debe poner la inyección de Nemluvio ni ponérsela a otra persona hasta que un profesional sanitario le haya enseñado a hacerlo.
En caso de duda, consulte a un profesional sanitario.
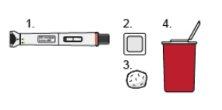
Nemluvio se presenta en una pluma precargada de doble cámara de un solo uso (denominada “pluma de Nemluvio” o “pluma” en estas instrucciones).
La pluma contiene dos cámaras, una con el medicamento (el polvo) y otra con agua para disolver el polvo.
Antes de inyectarse el medicamento, debe mezclar el polvo con el agua siguiendo la descripción que figura a continuación.
Descripción general del dispositivo
Pluma precargada de doble cámara de Nemluvio
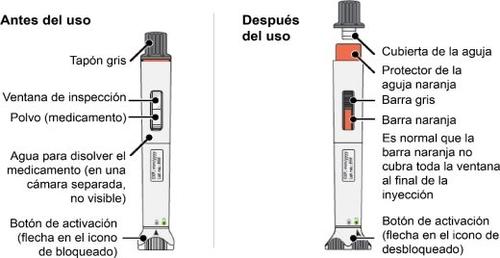
Información importante
Qué necesita saber antes del uso
- Lea detenidamente todas las instrucciones antes de usar la pluma de Nemluvio.
- Marque su calendariocon antelación para recordar cuándo debe recibir Nemluvio.
- Siga todos los pasos exactamente como se describen. Así se asegurará de recibir la dosis correcta de medicamento.
- Noutilice la pluma de Nemluvio si se ha caído sobre una superficie dura o si está dañada, agrietada o rota.
Información sobre la conservación
- Mantenga la pluma de Nemluvio y todos los medicamentos fuera de la vista y del alcance de los niños.
- Conserve la pluma de Nemluvio en la nevera entre 2 °C y 8 °C.
- Nocongele la pluma de Nemluvio.
- Conserve la pluma de Nemluvio en el embalaje original para protegerla de la luz.
- La pluma de Nemluvio se puede conservar en el embalaje original a temperatura ambiente de hasta 25 °C durante un único periodo de 90 días como máximo. Si la saca de la nevera, anote la fecha de extracción en la caja y utilice Nemluvio en un plazo de 90 días.
- No utilice Nemluvio si se ha pasado la fecha de caducidad o si han transcurrido 90 días desde que lo sacó de la nevera (lo que ocurra antes).
- Una vez finalizados los pasos para la reconstitución, Nemluvio se debe utilizar en un plazo de 4 horas.
Paso 1: Deje que Nemluvio alcance la temperatura ambiente La inyección de medicamentos fríos puede provocar dolor en el lugar de la inyección. Saque la caja de Nemluvio de la nevera y espere de 30 a 45 minutos para que alcance la temperatura ambiente antes de comenzar con el Paso 2. No debe:
microondas, luz solar directa), ya que podría dañar el medicamento.
Nota:En algunos casos, es posible que su médico le recete dos plumas para que las utilice al mismo tiempo. En ese caso, debe extraer dos plumas y utilizar una pluma después de la otra. | |
Paso 2: Lávese las manos con jabón y séqueselas bien. | |
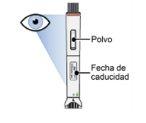
Paso 3: Prepare los suministros Saque la pluma de la caja y coloque los siguientes materiales sobre una superficie limpia, plana y bien iluminada:
punzocortantes*
|
|
Paso 4: Compruebe la pluma de Nemluvio para asegurarse de que: | |
agrietada Noutilice la pluma a menos que se cumplan todas las condiciones anteriores. Si nose cumple alguna de las condiciones, tire la pluma y utilice una nueva (ver paso 13.5 “Desechar”). |
|
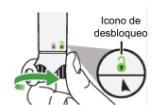
Paso 5: Activación de la pluma de Nemluvio Sujete la pluma en posición vertical y gire el botón de activación hacia la derecha hasta que se detenga. Esto inicia el proceso de transferencia de agua a la cámara donde está contenido el polvo. |
|
Paso 6: Espere hasta que la barra gris deje de moverse Observe la ventana de inspección hasta que la barra gris se haya detenido. Noagite la pluma antes de que la barra gris se haya detenido por completo para permitir la administración de la dosis exacta. |
|
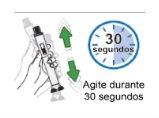
Paso 7: Agite para disolver el medicamento Cuando la barra gris se haya detenido por completo, agite la pluma arriba y abajo durante 30 segundos. |
|
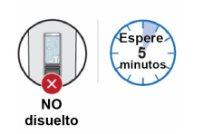
Paso 8: Espere 5 minutos a que disminuyan las burbujas Espere a que disminuyan las burbujas y a que el polvo se disuelva por completo. Tardará unos 5 minutos. Nota:Si el medicamento no se ha disuelto por completo, agítelo de nuevo durante 30 segundos y espere 5 minutos. Nota:Es normal que quede una pequeña capa de espuma o algunas burbujas de aire pequeñas en el medicamento disuelto. |
|
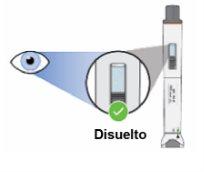
Paso 9: Compruebe el medicamento en la ventana de inspección Compruebe que el medicamento disuelto:
amarillo.
Noutilice la pluma si el medicamento disuelto está turbio o contiene partículas. Tire la pluma y utilice una nueva (ver paso 13.5 “ Desechar”). Nota:Una vez disuelto el medicamento, se debe utilizar en un plazo de 4 horas. Durante este tiempo, se debe mantener a temperatura ambiente (hasta 25 °C). Si no lo ha utilizado en 4 horas, deséchelo. |
|
| |
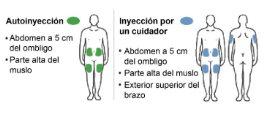
Paso 10: Seleccione un lugar de inyección Puede administrarse la inyección en el abdomen o en la parte alta del muslo. Un cuidador también puede administrarle la inyección en la cara externa superior del brazo. Dónde noinyectar:
del ombligo.
enrojecida o con cicatrices o estrías.
ejemplo, a 2,5 cm). |
|
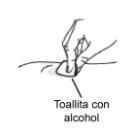
Paso 11: Limpie el lugar de la inyección
para limpiar el lugar de la inyección. De este modo se evitan la contaminación y las infecciones.
No debe:
limpiado.
limpio.
|
|
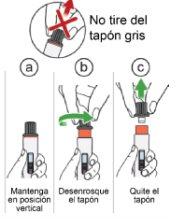
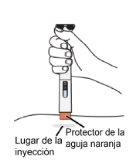
Paso 12: Gire el tapón gris para exponer el protector de la aguja
para evitar fugas
aparezca el protector de la aguja naranja.
protector de la aguja naranja.
recipiente para eliminar objetos punzocortantes (ver paso 13.5 “Desechar”). No debe:
Nota:Si no puede quitar el tapón, vuelva al paso 5y asegúrese de que el botón de activación esté completamente girado hacia la derecha hasta que se detenga. |
|
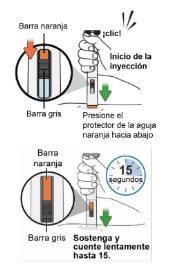
Paso 13: Inyección del medicamento
inyección en posición verticalpara que el protector de la aguja naranja quede plano contra la piel. Nota:Asegúrese de poder ver fácilmente la ventana de inspección durante la inyección.
abajo hasta que el protector de la aguja naranja quede completamente hacia dentro. La inyección se inicia de inmediato con un clic. Debe observar que la barra naranja y la barra gris se mueven. Siga empujando la pluma hacia abajo durante 15 segundos.
verificar que la barra naranja y la barra gris se han detenido. Esto significa que la inyección se ha completado Nolevante la pluma hasta que la barra naranja y la barra gris hayan dejado de moverse. Si la barra naranja no es visible, tire la pluma y utilice una nueva (ver paso 13.5 “Desechar”). Nota:Es normal que la barra naranja no cubra toda la ventana de inspección al final de la inyección.
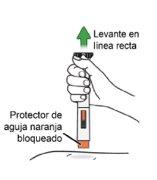
en vertical El protector de la aguja naranja se bloqueará para cubrir la aguja. Nota:Si sangra, haga presión sobre el lugar de la inyección con una bola de algodón o una gasa. Nofrote el lugar de la inyección.
recipiente para eliminar objetos punzocortantes inmediatamente después de su uso. Evite el contacto con la aguja. |
|
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a NEMLUVIO 30 MG POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN PLUMA PRECARGADAForma farmacéutica: INYECTABLE, 1 mlPrincipio activo: TralokinumabFabricante: Leo Pharma A/SRequiere recetaForma farmacéutica: INYECTABLE, 300 mgPrincipio activo: TralokinumabFabricante: Leo Pharma A/SRequiere recetaForma farmacéutica: CAPSULA, 10 mgPrincipio activo: AlitretinoinaFabricante: Industrial Farmaceutica Cantabria S.A.Requiere receta
Médicos online para NEMLUVIO 30 MG POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN PLUMA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de NEMLUVIO 30 MG POLVO Y DISOLVENTE PARA SOLUCION INYECTABLE EN PLUMA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes