MOUNJARO 5 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA


Cómo usar MOUNJARO 5 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Mounjaro 2,5mg solución inyectable en pluma precargada
Mounjaro 5mg solución inyectable en pluma precargada
Mounjaro 7,5mg solución inyectable en pluma precargada
Mounjaro 10mg solución inyectable en pluma precargada
Mounjaro 12,5mg solución inyectable en pluma precargada
Mounjaro 15mg solución inyectable en pluma precargada
tirzepatida
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, enfermero o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, enfermero o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Mounjaro y para qué se utiliza
- Qué necesita saber antes de empezar a usar Mounjaro
- Cómo usar Mounjaro
- Posibles efectos adversos
- Conservación de Mounjaro
- Contenido del envase e información adicional
1. Qué es Mounjaro y para qué se utiliza
Mounjaro contiene un principio activo llamado tirzepatida y se utiliza para tratar adultos con diabetes mellitus tipo 2. Mounjaro reduce el nivel de azúcar en el cuerpo solo cuando los niveles de azúcar están altos.
Mounjaro también se utiliza para tratar a adultos con obesidad o sobrepeso (con un IMC de al menos 27 kg/m2). Mounjaro influye en la regulación del apetito, lo que puede ayudarle a comer menos alimentos y a reducir su peso corporal.
En diabetes tipo 2, Mounjaro se utiliza:
- por sí solo cuando no pueda tomar metformina (otro medicamento para la diabetes).
- o en combinación con otros medicamentos para la diabetes cuando estos no son suficientes para controlar los niveles de azúcar en su sangre. Estos otros medicamentos pueden ser tomados por vía oral y/o puede ser una inyección de insulina.
Mounjaro también se utiliza junto con dieta y ejercicio para perder peso y ayudar a mantener el peso bajo control en adultos, que tienen:
- un IMC igual o superior a 30 kg/m² (obesidad) o
- un IMC de, al menos, 27 kg/m², pero inferior a 30 kg/m² (sobrepeso) y problemas de salud relacionados con el peso (como prediabetes, diabetes tipo 2, hipertensión arterial, niveles anormales de grasa en la sangre, problemas respiratorios durante el sueño denominados "apnea obstructiva del sueño" o antecedentes de infarto de miocardio, ictus o problemas vasculares)
El IMC (Índice de Masa Corporal) es una medida de su peso en relación con su estatura.
En pacientes con apnea obstructiva del sueño (AOS) y obesidad, Mounjaro se puede usar con o sin tratamiento de presión positiva en las vías respiratorias (PAP).
Es importante que mantenga los consejos sobre su alimentación y la actividad física que le proporcionen su médico, enfermero o farmacéutico.
2. Qué necesita saber antes de empezar a usar Mounjaro
No use Mounjaro
- si es alérgico a tirzepatida o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico, enfermero o farmacéutico antes de empezar a usar Mounjaro si:
- tiene problemas graves con la digestión de la comida o la comida permanece en su estómago más tiempo de lo normal (incluyendo gastroparesia grave).
- alguna vez ha tenido pancreatitis (inflamación del páncreas, que puede provocar dolor intenso en el estómago y la espalda que no desaparece).
- si tiene algún problema en los ojos (retinopatía diabética o edema macular).
- está tomando una sulfonilurea (otro medicamento para la diabetes) o insulina para la diabetes, ya que puede ocurrir una bajada de azúcar en sangre (hipoglucemia). Su médico puede tener que cambiar la dosis de estos medicamentos para reducir este riesgo.
Al inicio del tratamiento con Mounjaro, podría experimentar en algunos casos pérdida de fluidos/deshidratación, como en caso de vómitos, náuseas y/o diarrea, que pueden provocar un descenso de la función renal. Para evitar la deshidratación, es importante la ingesta de abundantes líquidos. Contacte con su médico si tiene alguna pregunta o inquietud.
Si sabe que va a someterse a una intervención quirúrgica en la que se someterá a anestesia (estado de sueño), informe a su médico de que está tomando Mounjaro.
Niños y adolescentes
Este medicamento no se debe administrar a niños y adolescentes menores de 18 años porque no se ha estudiado en este grupo de edad.
Otros medicamentos y Mounjaro
Informe a su médico, enfermero o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Embarazo
Si está embarazada, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento. Este medicamento no debe usarse durante el embarazo ya que se desconocen los efectos de este medicamento en el feto. Por tanto, se recomienda utilizar métodos anticonceptivos mientras se usa este medicamento.
Lactancia
Se desconoce si tirzepatida pasa a la leche materna. No se puede descartar un riesgo para los recién nacidos/niños. Si está en periodo de lactancia o planea estarlo, consulte a su médico antes de utilizar este medicamento. Usted y su médico deben decidir si debe interrumpir la lactancia o retrasar el uso de Mounjaro.
Conducción y uso de máquinas
Es poco probable que este medicamento afecte a su capacidad para conducir y utilizar máquinas. Sin embargo, si usa Mounjaro en combinación con una sulfonilurea o insulina, puede producirse un nivel bajo de azúcar en sangre (hipoglucemia) que puede reducir su capacidad de concentración. Evite conducir o utilizar máquinas si tiene cualquier indicio de bajada de azúcar en sangre, por ejemplo, dolor de cabeza, somnolencia, debilidad, mareos, sensación de hambre, confusión, irritabilidad, latidos rápidos del corazón y sudoración (ver sección 4). Ver la sección 2, “Advertencias y precauciones” para obtener información sobre el aumento del riesgo de tener una bajada de azúcar en sangre. Consulte con su médico para más información.
Mounjaro contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis; esto es, esencialmente “exento de sodio”.
3. Cómo usar Mounjaro
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
Cuánto hay que usar
- La dosis inicial es de 2,5 mg una vez a la semana durante cuatro semanas. Después de cuatro semanas, su médico le aumentará la dosis a 5 mg una vez a la semana.
- Su médico puede aumentar su dosis en incrementos de 2,5 mg hasta 7,5 mg, 10 mg, 12,5 mg o 15 mg una vez a la semana si lo necesita. En cada caso, su médico le indicará que permanezca en una dosis concreta durante al menos 4 semanas antes de pasar a una dosis más alta.
No cambie su dosis a menos que su médico se lo haya indicado.
Cada pluma contiene una dosis de Mounjaro de 2,5 mg, 5 mg, 7,5 mg, 10 mg, 12,5 mg o 15 mg.
Elegir cuándo usar Mounjaro
Puede usar su pluma a cualquier hora del día, con o sin alimentos. Si puede, debe utilizarla el mismo día de cada semana. Para ayudarle a recordar cuándo usar Mounjaro, puede anotar el día de la semana cuando se inyecte su primera dosis en la caja de su pluma o en un calendario.
Si es necesario, puede cambiar el día de su inyección semanal de Mounjaro, siempre que hayan pasado al menos 3 días desde su última inyección. Después de seleccionar un nuevo día de dosificación, continúe con la administración una vez a la semana en ese nuevo día.
Cómo inyectar Mounjaro
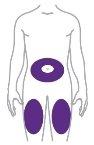
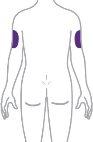
Mounjaro se inyecta debajo de la piel (inyección subcutánea) de la zona del abdomen a una distancia mínima de 5 cm del ombligo o en la parte superior de la pierna (muslo) o en la parte superior del brazo. Es posible que necesite ayuda de otra persona si desea inyectarse en la parte superior del brazo.
Si usted quiere, puede inyectarse en la misma zona de su cuerpo cada semana. Pero en este caso, asegúrese de elegir dentro de la misma zona diferentes sitios de inyección. Si también se inyecta insulina, elija un sitio de inyección diferente para esa inyección.
Antes de usar Mounjaro, lea atentamente las “Instrucciones de uso” de la pluma.
Control de los niveles de glucosa en sangre
Si está utilizando Mounjaro con una sulfonilurea o insulina, es importante que controle sus niveles de glucosa en sangre siguiendo las instrucciones de su médico, enfermero o farmacéutico (ver sección 2, “Advertencias y precauciones”).
Si usa más Mounjaro del que debe
Si usa más Mounjaro del que debe, consulte a su médico inmediatamente. Demasiado medicamento puede hacer que la cantidad de azúcar en su sangre baje demasiado (hipoglucemia) y también puede hacer que tenga náuseas o vómitos.
Si olvidó usar Mounjaro
Si olvida inyectarse una dosis y,
- han pasado 4días o menosdesde que debería haber usado Mounjaro, úselo tan pronto como lo recuerde. Luego inyecte su próxima dosis como de costumbre en su día programado.
- Si han pasado más de 4díasdesde que debería haber usado Mounjaro, omita la dosis olvidada. Luego inyecte su próxima dosis como de costumbre en su día programado.
No se inyecte una dosis doble para compensar la dosis olvidada. El tiempo mínimo entre dos dosis debe ser de al menos 3 días.
Si interrumpe el tratamiento con Mounjaro
No interrumpa el uso de Mounjaro sin consultar con su médico. Si usted interrumpe el tratamiento con Mounjaro, y tiene diabetes tipo 2, los niveles de azúcar en su sangre pueden aumentar.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, enfermero o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos graves
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- Inflamación del páncreas (pancreatitis aguda) que podría causar dolor intenso en el estómago y la espalda que no desaparece. Acuda a su médico de forma inmediata si experimenta estos síntomas.
Raros(pueden afectar hasta 1 de cada 1 000 personas)
- Reacciones alérgicas graves (por ejemplo, reacción anafiláctica, angioedema). Debe obtener ayuda médica inmediata e informar a su médico si experimenta síntomas como problemas respiratorios, hinchazón rápida de los labios, la lengua y/o la garganta con dificultad para tragar y latidos cardíacos rápidos.
Otros efectos adversos
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas)
- Náuseas
- Diarrea
- Dolor de estómago (abdominal) notificado en pacientes tratados para el control del peso
- Náuseas (vómitos) notificadas en pacientes tratados para el control del peso
- Estreñimiento notificado en pacientes tratados para el control del peso
Estos efectos adversos normalmente no son graves. Las náuseas, diarrea y vómitos son más frecuentes cuando se empieza a usar tirzepatida, pero disminuyen con el tiempo en la mayoría de los pacientes.
- Las bajadas de azúcar en sangre (hipoglucemia) son muy frecuentes cuando tirzepatida se usa junto con otros medicamentos que contienen una sulfonilurea y/o insulina. Si está tomando una sulfonilurea o insulina para la diabetes tipo 2, puede que necesite que le reduzcan la dosis mientras usa tirzepatida (ver sección 2, “Advertencias y precauciones”). Los síntomas de una bajada de azúcar en sangre pueden incluir dolor de cabeza, somnolencia, debilidad, mareos, sensación de hambre, confusión, irritabilidad, latidos rápidos del corazón y sudoración. Su médico debe indicarle cómo puede tratar los niveles bajos de azúcar en sangre.
Frecuentes(puede afectar hasta 1 de cada 10 personas)
- Bajadas de azúcar en sangre (hipoglucemia) cuando tirzepatida se usa para diabetes tipo 2 con metformina junto con un inhibidor del cotransportador sodio-glucosa tipo 2 (otro medicamento para la diabetes)
- Reacción alérgica (hipersensibilidad) (por ejemplo, sarpullido, picor y eccema)
- Mareos notificados en pacientes tratados para el control del peso
- Presión arterial baja notificada en pacientes tratados para el control del peso
- Tener menos hambre (disminución del apetito) notificado en pacientes tratados para diabetes tipo 2
- Dolor de estómago (abdominal) notificado en pacientes tratados para diabetes tipo 2
- Vómitos notificados en pacientes tratados para diabetes tipo 2– normalmente disminuyen con el tiempo
- Indigestión (dispepsia)
- Estreñimiento notificado en pacientes tratados para diabetes tipo 2
- Hinchazón de estómago
- Eructos
- Gases (flatulencia)
- Reflujo o acidez estomacal (también llamado enfermedad por reflujo gastroesofágico – ERGE)– una enfermedad causada por la acidez del estómago que sube hacia el conducto que conecta el estómago con la boca
- Pérdida de cabello notificada en pacientes tratados para el control del peso
- Cansancio (fatiga)
- Reacciones en la zona de inyección (por ejemplo, picor o enrojecimiento)
- Pulso rápido
- Aumento de los niveles de enzimas pancreáticas (como la lipasa y la amilasa) en sangre
- Aumento de los niveles de calcitonina en sangre en pacientes tratados para el control del peso.
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- Bajadas de azúcar en sangre (hipoglucemia) cuando tirzepatida se usa con metformina para diabetes tipo 2
- Piedras en la vesícula biliar
- Inflamación de la vesícula biliar
- Pérdida de peso notificada en pacientes tratados para diabetes tipo 2
- Dolor en la zona de inyección
- Aumento de los niveles de calcitonina en sangre en pacientes tratados para diabetes tipo 2 o para AOS con obesidad
- Sentido del gusto modificado
- Cambio en la sensibilidad de la piel
- Retraso en el vaciado del estómago
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, enfermero o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Mounjaro
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta de la pluma y en el embalaje después de CAD. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 ºC y 8 ºC). No congelar. Si la pluma se ha congelado, NO LA USE.
Conservar en el envase original para protegerlo de la luz.
Mounjaro se puede almacenar sin refrigerar por debajo de 30 ºC hasta un máximo de 21 días consecutivos, después la pluma debe desecharse.
No utilice este medicamento si observa que la pluma está deteriorada o el medicamento está turbio, tiene color o contiene partículas.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Mounjaro
El principio activo es tirzepatida.
- Mounjaro 2,5mg:Cada pluma precargada contiene 2,5 mg de tirzepatida en 0,5 ml de solución (5 mg/ml).
- Mounjaro 5mg:Cada pluma precargada contiene 5 mg de tirzepatida en 0,5 ml de solución (10 mg/ml).
- Mounjaro 7,5mg:Cada pluma precargada contiene 7,5 mg de tirzepatida en 0,5 ml de solución (15 mg/ml).
- Mounjaro 10mg:Cada pluma precargada contiene 10 mg de tirzepatida en 0,5 ml de solución (20 mg/ml).
- Mounjaro 12,5mg:Cada pluma precargada contiene 12,5 mg de tirzepatida en 0,5 ml de solución (25 mg/ml).
- Mounjaro 15mg:Cada pluma precargada contiene 15 mg de tirzepatida en 0,5 ml de solución (30 mg/ml).
Los demás componentes son hidrógeno fosfato disódico heptahidratado (E339), cloruro de sodio, hidróxido de sodio (para mayor información ver sección 2 “Mounjaro contiene sodio”), ácido clorhídrico concentrado y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Mounjaro es una solución inyectable transparente, entre incolora y ligeramente amarilla, en pluma precargada.
La pluma precargada tiene una aguja oculta que se introducirá automáticamente en la piel cuando se pulsa el botón de inyección. La pluma precargada retraerá la aguja cuando se haya completado la inyección.
Cada pluma precargada contiene 0,5 ml de solución.
La pluma precargada es de un solo uso.
Los tamaños de envase son 2 plumas precargadas, 4 plumas precargadas o envase múltiple de 12 (3 paquetes de 4) plumas precargadas. Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Eli Lilly Nederland B.V., Papendorpseweg 83, 3528 BJ Utrecht, Países Bajos.
Responsable de la fabricación
Eli Lilly Italia S.p.A.,Via Gramsci 731/733, 50019, Sesto Fiorentino, Florencia (FI), Italia.
Lilly France, 2, rue du Colonel Lilly, 67640 Fegersheim, Francia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgique/België/Belgien Eli Lilly Benelux S.A./N.V. Tél/Tel: + 32-(0)2 548 84 84 | Lietuva Eli Lilly Lietuva Tel. +370 (5) 2649600 |
???????? ?? "??? ???? ?????????" ?.?. - ???????? ???. + 359 2 491 41 40 | Luxembourg/Luxemburg Eli Lilly Benelux S.A./N.V. Tél/Tel: + 32-(0)2 548 84 84 |
Ceská republika ELI LILLY CR, s.r.o. Tel: + 420 234 664 111 | Magyarország Lilly Hungária Kft. Tel: + 36 1 328 5100 |
Danmark Eli Lilly Danmark A/S Tlf.: +45 45 26 60 00 | Malta Charles de Giorgio Ltd. Tel: + 356 25600 500 |
Deutschland Lilly Deutschland GmbH Tel. + 49-(0) 6172 273 2222 | Nederland Eli Lilly Nederland B.V. Tel: + 31-(0) 30 60 25 800 |
Eesti Eli Lilly Nederland B.V. Tel: +372 6 817 280 | Norge Eli Lilly Norge A.S. Tlf: + 47 22 88 18 00 |
Ελλ?δα ΦΑΡΜΑΣΕΡΒ-ΛΙΛΛΥ Α.Ε.Β.Ε. Τηλ: +30 210 629 4600 | Österreich Eli Lilly Ges.m.b.H. Tel: + 43-(0) 1 20609 1270 |
España Lilly S.A. Tel: + 34-91 663 50 00 | Polska Eli Lilly Polska Sp. z o.o. Tel: +48 22 440 33 00 |
France Lilly France Tél: +33-(0) 1 55 49 34 34 | Portugal Lilly Portugal Produtos Farmacêuticos, Lda Tel: + 351-21-4126600 |
Hrvatska Eli Lilly Hrvatska d.o.o. Tel: +385 1 2350 999 | România Eli Lilly România S.R.L. Tel: + 40 21 4023000 |
Ireland Eli Lilly and Company (Ireland) Limited Tel: + 353-(0) 1 661 4377 | Slovenija Eli Lilly farmacevtska družba, d.o.o. Tel: +386 (0)1 580 00 10 |
Ísland Icepharma hf. Sími + 354 540 8000 | Slovenská republika Eli Lilly Slovakia s.r.o. Tel: + 421 220 663 111 |
Italia Eli Lilly Italia S.p.A. Tel: + 39- 055 42571 | Suomi/Finland Oy Eli Lilly Finland Ab Puh/Tel: + 358-(0) 9 85 45 250 |
Κ?προς Phadisco Ltd Τηλ: +357 22 715000 | Sverige Eli Lilly Sweden AB Tel: + 46-(0) 8 7378800 |
Latvija Eli Lilly (Suisse) S.A Parstavnieciba Latvija Tel: +371 67364000 |
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu, y en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/).
Instrucciones de uso |
Mounjaro 2,5mg solución inyectable en pluma precargada Mounjaro 5mg solución inyectable en pluma precargada Mounjaro 7,5mg solución inyectable en pluma precargada Mounjaro 10mg solución inyectable en pluma precargada Mounjaro 12,5mg solución inyectable en pluma precargada Mounjaro 15mg solución inyectable en pluma precargada |
tirzepatida
|
Información importante que debe conocer antes de inyectarse Mounjaro.
Lea estas instrucciones de uso y el prospecto antes de usar su pluma precargada de Mounjaro (pluma) y cada vez que obtenga una nueva pluma.Es posible que haya nueva información. Esta información no reemplaza la conversación con su médico, enfermero o farmacéutico acerca de su situación médica o tratamiento.
Consulte a su médico, enfermero o farmacéutico sobre cómo inyectar Mounjaro de forma adecuada.
- Mounjaro es una pluma precargada de dosis única.
- La pluma tiene una aguja oculta que se introducirá automáticamente en su piel cuando presione el botón de inyección. La pluma precargada retraerá la aguja cuando se haya completado la inyección.
- Mounjaro se utiliza una vez cada semana.
- Se inyecta solamente bajo la piel (vía subcutánea).
- Usted u otra persona puede inyectarle en la zona del abdomen, en la parte superior de la pierna (muslo) o en la parte superior del brazo.
- Es posible que necesite la ayuda de otra persona si quiere inyectarse en la parte superior del brazo.
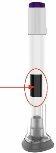
Partes de la pluma
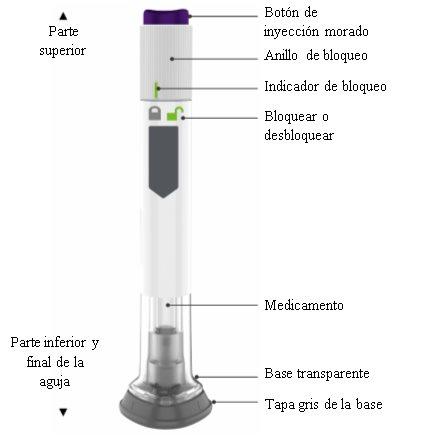
Preparación para inyectarse Mounjaro
Saquela pluma de la nevera. Deje puesta la tapa gris de la base hasta que esté preparado para inyectarse. | |
Compruebela etiqueta de la pluma para asegurarse de que es el medicamento y la dosis correcta y que no está caducado. Examinela pluma para asegurarse de que no está dañada. |
|
Asegúrese de que el medicamento: | |
|
|
Lavesus manos. |
Elija su zona de inyección
Su médico, enfermero o farmacéutico pueden ayudarle a elegir la mejor zona de inyección para usted.
| Usted u otra persona puede inyectarle el medicamento en la zona del abdomen a una distancia mínima de 5 cm del ombligo o en el muslo. |
| Otra persona puede inyectarle en la parte de atrás de la zona superior del brazo. Cambie (rote) la zona de inyección cada semana. Puede utilizar la misma zona del cuerpo, pero asegúrese de elegir un sitio de inyección diferente en esa zona. |
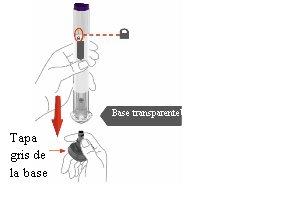
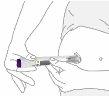
Paso 1 | Retire la tapa de color gris de la base |
| Asegúrese de que la pluma está bloqueada. Nodesbloquee la pluma hasta que coloque la base transparente en su piel y esté preparado para inyectarse. |
Retirela tapa gris de la base y tírela. Novuelva a colocar la tapa de la base – esto podría dañar la aguja. Notoque la aguja. |
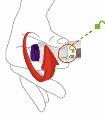
Paso 2 | Coloque la base transparente sobre la piel, luego desbloquee |
| Coloquela base transparente de forma plana sobre su piel en la zona de inyección. |
| Desbloqueargirando el anillo de bloqueo. |
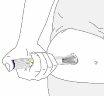
Paso 3 | Presione y mantenga pulsado hasta 10segundos |
| Presione y mantenga pulsadoel botón de inyección morado. Escuche:
|
| Sabrá que la inyección ha terminado cuando el émbolo gris sea visible. |
Tras su inyección, deposite la pluma usada en un contenedor para desechar objetos punzantes. |

Eliminación de su pluma usada
|
|
Conservación y manipulación
- Para las instrucciones de conservación, consulte la sección 5 del prospecto.
- La pluma tiene partes de vidrio. Manéjela con cuidado. Si se le cae la pluma sobre una superficie dura, nola utilice. Utilice una pluma nueva para su inyección.
Preguntas frecuentes
¿Qué sucede si veo burbujas de aire en mi pluma?
Las burbujas de aire son normales.
¿Qué sucede si mi pluma no está a temperatura ambiente?
No es necesario templar la pluma a temperatura ambiente.
¿Qué sucede si desbloqueo la pluma y pulso el botón de inyección morado antes de retirar la tapa de la base gris?
Noretire la tapa gris de la base. Tire la pluma y obtenga una pluma nueva.
¿Qué sucede si hay una gota de líquido en la punta de la aguja cuando retiro la tapa gris de la base?
Una gota de líquido en la punta de la aguja es normal. Notoque la aguja.
¿Necesito mantener el botón de inyección pulsado hasta que la inyección finalice?
No es necesario, pero puede ayudarle a mantener la pluma estable sobre su piel.
Escuché más de dos clics durante la inyección – dos clics altos y uno bajo. ¿La inyección ha terminado?
Algunas personas pueden escuchar un clic bajo justo antes del segundo clic alto. Esto es por el funcionamiento normal de la pluma. Noretire la pluma de su piel hasta que no escuche el segundo clic más alto.
No estoy seguro de si mi pluma ha funcionado correctamente.
| Compruebe si ha recibido su dosis. La dosis se ha administrado correctamente si la parte gris es visible. Además, ver Paso3de las instrucciones. Si no ve el émbolo gris, contacte con Lilly para información adicional. Hasta entonces, conserve su pluma de forma segura para evitar una herida accidental con la aguja. |
¿Qué sucede si hay una gota de líquido o sangre en mi piel tras la inyección?
Esto es normal. Presione una bola de algodón o gasa sobre la zona de inyección. Nofrote la zona de inyección.
Otra información
- Si tiene problemas de visión, no use su pluma sin la ayuda de otra persona entrenada en el uso de la pluma de Mounjaro.
Dónde obtener más información
- Si tiene alguna pregunta o problema con su pluma de Mounjaro, contacte con Lilly o con su médico, enfermero o farmacéutico.
Última revisión en
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a MOUNJARO 5 MG SOLUCION INYECTABLE EN PLUMA PRECARGADAForma farmacéutica: INYECTABLE, 10 MGPrincipio activo: TirzepatidaFabricante: Eli Lilly Nederland B.V.Requiere recetaForma farmacéutica: INYECTABLE, 10 mgPrincipio activo: TirzepatidaFabricante: Eli Lilly Nederland B.V.Requiere recetaForma farmacéutica: INYECTABLE, 10 MG/DOSISPrincipio activo: TirzepatidaFabricante: Eli Lilly Nederland B.V.Requiere receta
Médicos online para MOUNJARO 5 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de MOUNJARO 5 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes