
LASTIFLUNO 137 MICROGRAMOS/50 MICROGRAMOS/ APLICACIÓN SUSPENSION PARA PULVERIZACION NASAL

Cómo usar LASTIFLUNO 137 MICROGRAMOS/50 MICROGRAMOS/ APLICACIÓN SUSPENSION PARA PULVERIZACION NASAL
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Lastifluno 137 microgramos/50 microgramos/ aplicación,
suspensión para pulverización nasal
hidrocloruro de azelastina / propionato de fluticasona
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Lastifluno y para qué se utiliza
- Qué necesita saber antes de empezar a usar Lastifluno
- Cómo usar Lastifluno
- Posibles efectos adversos
- Conservación de Lastifluno
- Contenido del envase e información adicional
1. Qué es Lastifluno y para qué se utiliza
Lastifluno contiene dos sustancias activas: hidrocloruro de azelastina y propionato de fluticasona.
- El hidrocloruro de azelastina pertenece a un grupo de medicamentos llamados antihistamínicos. Los antihistamínicos actúan previniendo los efectos de sustancias tales como histamina, producidas por el organismo como parte de una reacción alérgica; de esta forma, reduce los síntomas de la rinitis alérgica.
- El propionato de fluticasona pertenece a un grupo de medicamentos llamados corticosteroides, que reducen la inflamación.
Lastifluno se utiliza para aliviar los síntomas de la rinitis alérgica estacional de moderada a grave y la rinitis alérgica perenne, si el tratamiento con antihistamínico o corticosteroide intranasal por separado se consideran insuficientes.
La rinitis alérgica estacional o perenne son reacciones alérgicas frente a sustancias tales como el polen (fiebre del heno), ácaros del hogar, mohos, polvo o animales domésticos.
Lastifluno alivia los síntomas de las alergias, por ejemplo: rinorrea, goteo post-nasal, estornudos, picor o taponamiento nasal.
2. Qué necesita saber antes de empezar a usar Lastifluno
No use Lastifluno
- Si es alérgico al hidrocloruro de azelastina o al propionato de fluticasona, o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Lastifluno si:
- Ha sufrido una reciente operación o herida en nariz o boca.
- Padece una infección nasal. Las infecciones nasales se deben tratar con antibacterianos o antifúngicos. Si a usted le han dado medicación para una infección nasal, puede continuar usando Lastifluno para tratar su alergia.
- Tiene tuberculosis o una infección no tratada.
- Tiene cambios de visión o antecedentes de presión intraocular elevada, glaucoma y/o cataratas. Si usted padece alguna de estas enfermedades, será vigilado/a estrechamente durante el uso de Lastifluno.
- Tiene deteriorada la función adrenal. Se debe tener precaución cuando se cambie un tratamiento sistémico de esteroides por Lastifluno.
- Padece enfermedad grave del hígado. Se incrementará el riesgo de presentar efectos adversos sistémicos.
En estos casos, su médico decidirá si puede utilizar Lastifluno.
Es importante que tome la dosis indicada en la sección 3 o la indicada por su médico. El tratamiento con dosis mayores a las recomendadas de corticoides nasales puede llevar a una supresión adrenal, lo cual puede producir pérdida de peso, fatiga, debilidad muscular, niveles bajos de glucosa en sangre, necesidad de sal, dolor de articulaciones, depresión y oscurecimiento de la piel. Si le ocurre alguno de estos efectos adversos, su médico le puede recomendar otro medicamento durante periodos de estrés o cirugía selectiva.
Para evitar la supresión adrenal, su médico le aconsejará que tome la dosis más baja que mantenga un control eficaz de los síntomas de la rinitis.
El uso de corticosteroides nasales (como Lastifluno) puede causar un crecimiento más lento en niños y adolescentes cuando lo usen durante un largo periodo de tiempo. El médico controlará de forma regular el crecimiento de los niños y se asegurará de que tomen la menor dosis efectiva posible.
Contacte con su médico si experimenta visión borrosa u otras alteraciones visuales.
Si no está seguro de si se encuentra en cualquiera de las situaciones anteriores, consulte con su médico o farmacéutico antes de usar Lastifluno.
Niños
No se recomienda el uso de este medicamento en niños menores de 12 años.
Uso de Lastifluno con otros medicamentos
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento, incluso los adquiridos sin receta.
Algunos medicamentos pueden aumentar los efectos de Lastifluno, por lo que su médico le hará controles minuciosos si está tomando estos medicamentos (incluidos algunos para el VIH: ritonavir, cobicistat y medicamentos para el tratamiento de las infecciones por hongos: ketoconazol). No use Lastifluno si toma medicamentos sedantes o que afecten al sistema nervioso central.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Conducción y uso de máquinas
Lastifluno ejerce una mínima influencia sobre la capacidad para conducir y usar máquinas.
Muy raramente, puede experimentar fatiga, debilidad o mareos debido a la propia enfermedad o durante el uso de Lastifluno. En estos casos, no conduzca ni maneje maquinaria. Tenga en cuenta que el consumo de alcohol puede potenciar estos efectos.
Lastifluno contiene cloruro de benzalconio.
Este medicamento contiene 14 microgramos de cloruro de benzalconio en cada pulverización.
El cloruro de benzalconio puede causar irritación o inflamación dentro de la nariz, especialmente cuando se usa durante periodos largos de tratamiento.
Informe a su médico o farmacéutico si nota disconfort al usar el pulverizador.
3. Cómo usar Lastifluno
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
Es esencial que el uso de Lastifluno sea regular para que el beneficio terapéutico sea completo.
Evite el contacto con los ojos.
Adultos y adolescentes (mayores de 12 años)
- La dosis recomendada es de una aplicación en cada fosa nasal, por la mañana y por la noche.
Uso en niños menores de 12 años
- No se recomienda el uso de este medicamento en niños menores de 12 años.
Uso en caso de insuficiencia renal y hepática
- No hay datos disponibles en pacientes con insuficiencia renal y hepática.
Forma de administración
Vía nasal.
Lea detenidamente las siguientes instrucciones y utilice el producto sólo como está indicado.
INSTRUCCIONES DE USO
Preparación de la pulverización
- Agite el frasco suavemente durante 5 segundos inclinándolo de arriba hacia abajo y, seguidamente, retire el tapón de protección (ver figura 1).
Figura 1

- La primera vez que se usa el pulverizador nasal, se debe activar la bomba pulverizando al aire.
- Active la bomba colocando dos dedos a cada lado de la bomba de pulverización y poniendo el pulgar en la base del frasco.
- Pulse y libere la bomba 6 veces, hasta que aparezca una pulverización fina (ver figura 2).
- Ahora, la bomba está activada y lista para ser usada.
Figura 2
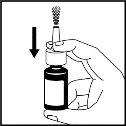
- Si no se ha utilizado el pulverizador nasal durante más de 7 días, tendrá que volver a activar la bomba, presionando y liberando la misma. Agite el frasco suavemente durante 5 segundos inclinándolo de arriba hacia abajo y, seguidamente, retire el tapón de protección (ver figura 1) y presione y libere la bomba una vez.
Uso del pulverizador
- Agite el frasco suavemente durante 5 segundos inclinándolo de arriba hacia abajo y, seguidamente, retirar el tapón de protección (ver figura 1).
- Suénese la nariz para despejar las fosas nasales.
- Mantenga la cabeza inclinada hacia sus pies. No eche la cabeza hacia atrás.
- Mantenga el frasco en posición recta e inserte con cuidado la punta del pulverizador en una fosa nasal.
- Tape con el dedo la otra fosa nasal, pulse rápidamente una sola vez y, al mismo tiempo, efectúe una suave inspiración (ver figura 3).
- Respire por la boca.
Figura 3
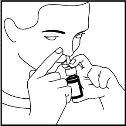
- Repita la operación en la otra fosa nasal.
- Respire suavemente y no eche la cabeza hacia atrás después de la aplicación. Así, se impide que el medicamento llegue a su garganta, provocando un sabor desagradable (ver figura 4).
Figura 4
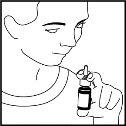
- Después de cada uso, limpie la punta del pulverizador con un pañuelo o paño limpio, y vuelva a colocar el tapón de protección.
- No pinche la boquilla en caso de que no se obtenga la pulverización. Limpie la válvula con agua.
Es importante que utilice la dosis prescrita por su médico. Use solamente la cantidad que le ha recomendado su médico.
Duración del tratamiento
Lastifluno es apropiado para el uso prolongado. La duración del tratamiento se corresponde con el periodo en el que experimente síntomas alérgicos.
Si usa más Lastiflunodel que debe
Si se aplica más cantidad de este medicamento en la nariz, es improbable que sufra algún tipo de problema. En caso de duda, o si ha usado una dosis mayor a la recomendada durante un largo periodo de tiempo, consulte con su médico. Si una persona, sobre todo un niño, bebe accidentalmente Lastifluno, consulte inmediatamente a su médico o acuda al centro médico más cercano, o llame al Servicio de Información Toxicológica. Teléfono (91) 562 04 20, indicando el medicamento y la cantidad ingerida.
Si olvidó usar Lastifluno
Use el pulverizador nasal en cuanto lo recuerde y, seguidamente, adminístrese la dosis siguiente a la hora habitual. No utilice una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento con Lastifluno
No interrumpa el tratamiento sin consultar con su médico porque pone en riesgo el éxito de su tratamiento.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- Hemorragia nasal.
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 personas):
- Dolor de cabeza.
- Sabor amargo en la boca, especialmente si echa la cabeza hacia atrás durante el uso del pulverizador nasal. Este sabor debe desaparecer si bebe un refresco algunos minutos después de usar este medicamento.
- Olor desagradable.
Efectos adversos poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
- Ligera irritación del interior de la nariz, que puede causar leve escozor, picor o estornudos.
- Sequedad nasal, tos, sequedad de garganta o irritación de garganta.
Efectos adversos raros (pueden afectar hasta 1 de cada 1.000 personas):
- Sequedad de boca.
Efectos adversos muy raros (pueden afectar hasta 1 de cada 10.000 personas):
- Aturdimiento o somnolencia.
- Cataratas, glaucoma o aumento de la presión en el ojo, con posible pérdida de la visión y/o enrojecimiento y dolor de ojos. Estos efectos adversos se han observado con tratamientos prolongados con pulverizaciones nasales de propionato de fluticasona.
- Lesiones de la piel y mucosa de la nariz.
- Sensación de malestar, cansancio, agotamiento o debilidad.
- Exantema, enrojecimiento o picor de la piel, urticaria.
- Broncoespasmo (estrechamiento de las vías aéreas de los pulmones).
Solicite inmediatamente atención médica si desarrolla alguno de los siguientes síntomas:
- Hinchazón del rostro, labios, lengua o garganta, que puedan dificultar la deglución/respiración y repentina aparición de exantema en la piel. Estos podrían ser signos de una reacción alérgica grave. Tenga en cuenta que esto es muy raro.
Efectos adversos con frecuencia no conocida (la frecuencia no se puede estimar a partir de los datos disponibles)
- Visión borrosa
- Úlceras en la nariz
Cuando este medicamento se administra a dosis elevadas durante un periodo prolongado de tiempo, pueden producirse efectos adversos sistémicos (efectos adversos que afectan a todo el organismo). La probabilidad de que se produzcan estos efectos es mucho menor si se utiliza una pulverización nasal de corticosteroides en lugar de corticosteroides por vía oral. Estos efectos pueden variar entre pacientes individuales y entre las diferentes preparaciones de corticosteroides (ver sección 2).
Los corticosteroides nasales pueden afectar a la producción normal de hormonas en su cuerpo, especialmente si se usan altas dosis durante largo tiempo. En niños y adolescentes éste efecto adverso puede provocarles un crecimiento más lento.
En raros casos, se produce una reducción de la densidad ósea (osteoporosis) cuando los corticosteroides son administrados por vía nasal durante un largo periodo de tiempo.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Lastifluno
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta del frasco y en el envase después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
No refrigerar o congelar.
Caducidad después de su apertura: Deseche cualquier resto no utilizado del medicamento 6 meses después de abrir por primera vez el pulverizador nasal.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición deLastifluno
Los principios activos son: hidrocloruro de azelastina y propionato de fluticasona.
Cada ml de suspensión contiene 1.000 microgramos de hidrocloruro de azelastina y 365 microgramos de propionato de fluticasona.
Cada aplicación (0,14 g) libera 137 microgramos de hidrocloruro de azelastina (equivalentes a 125 microgramos de azelastina) y 50 microgramos de propionato de fluticasona.
Los demás componentes son: edetato de disodio, glicerol (E422), celulosa microcristalina, carmelosa sódica, polisorbato 80, cloruro de benzalconio, alcohol feniletílico y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Lastifluno es una suspensión nasal de color blanco que se presenta en un frasco de vidrio de color ámbar, equipado con una bomba pulverizadora, un aplicador y un tapón de protección.
Cada frasco de 25 ml contiene 23 g de suspensión para pulverización nasal (al menos 120 aplicaciones).
Cada envase contiene 1 frasco con 23 g de suspensión para pulverización nasal o envases múltiples que contienen 3 frascos, cada uno conteniendo 23 g de suspension para pulverización nasal.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Day Zero ehf.
Reykjavikurvegi, 62
Hafnarfjoerdur 220
Islandia
Responsable de la fabricación
Teva Czech Industries s.r.o.
Ostravska 305/29
747 70 Opava - Komárov,
República Checa
Fecha de la última revisión de este prospecto:
Septiembre 2023
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/).
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a LASTIFLUNO 137 MICROGRAMOS/50 MICROGRAMOS/ APLICACIÓN SUSPENSION PARA PULVERIZACION NASALForma farmacéutica: PRODUCTO USO NASAL, 137 microgramos/50 microgramos/aplicaciónPrincipio activo: fluticasone, combinationsFabricante: Laboratorios Cinfa S.A.Requiere recetaForma farmacéutica: PRODUCTO USO NASAL, 137 microgramos/50 microgramos/actuationPrincipio activo: fluticasone, combinationsFabricante: Teva B.V.Requiere recetaForma farmacéutica: PRODUCTO USO NASAL, 137 microgramos/50 microgramos/aplicaciónPrincipio activo: fluticasone, combinationsFabricante: Especialidades Farmaceuticas Centrum S.A.Requiere receta
Médicos online para LASTIFLUNO 137 MICROGRAMOS/50 MICROGRAMOS/ APLICACIÓN SUSPENSION PARA PULVERIZACION NASAL
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de LASTIFLUNO 137 MICROGRAMOS/50 MICROGRAMOS/ APLICACIÓN SUSPENSION PARA PULVERIZACION NASAL, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes











