
JUNOD 60 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA

Cómo usar JUNOD 60 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Junod 60 mg solución inyectable en jeringa precargada
denosumab
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
- Su médico le proporcionará una tarjeta recordatorio para el paciente, que contiene información importante de seguridad que debe conocer antes y durante su tratamiento con Junod.
Contenido del prospecto
- Qué es Junod y para qué se utiliza
- Qué necesita saber antes de empezar a usar Junod
- Cómo usar Junod
- Posibles efectos adversos
- Conservación de Junod
- Contenido del envase e información adicional
1. Qué es Junod y para qué se utiliza
Qué es Junod y cómo funciona
Junod contiene denosumab, una proteína (anticuerpo monoclonal) que interfiere en la acción de otra proteína con el objetivo de tratar la pérdida ósea y la osteoporosis. El tratamiento con Junod refuerza los huesos y reduce las posibilidades de fractura.
El hueso es un tejido vivo que se renueva continuamente. Los estrógenos contribuyen a la conservación de la salud de los huesos.
En las mujeres, después de la menopausia, el nivel de estrógenos desciende, lo que puede provocar que los huesos se vuelvan más finos y frágiles. A la larga esto puede provocar una enfermedad llamada osteoporosis.
La osteoporosis también puede ocurrir en varones debido a varias causas incluyendo la edad y/o un nivel bajo de la hormona masculina, testosterona. También, se puede dar en pacientes en tratamiento con glucocorticoides.
Muchos pacientes con osteoporosis no presentan síntomas, aunque siguen teniendo riesgo de fracturarse los huesos, sobre todo en la columna, la cadera y las muñecas.
Las intervenciones quirúrgicas o los medicamentos que detienen la producción de estrógeno o testosterona, utilizados para tratar pacientes con cáncer de próstata o de mama, también pueden provocar la pérdida ósea. Con ello, los huesos se hacen más débiles y se rompen con más facilidad.
Para qué se utiliza Junod
Junod se utiliza para tratar:
- la osteoporosis posterior a la menopausia (posmenopáusica) en mujeres y en varones que tienen un riesgo incrementado de fractura (rotura de huesos), reduciendo el riesgo de fracturas de la cadera, de la columna y en localizaciones que no son la columna.
- la pérdida ósea causada por la reducción del nivel hormonal (testosterona) como consecuencia de una operación quirúrgica o un tratamiento con medicamentos en pacientes con cáncer de próstata.
- la pérdida ósea resultante del tratamiento a largo plazo con glucocorticoides en pacientes que tienen riesgo elevado de fractura.
2. Qué necesita saber antes de empezar a usar Junod
No use Junod
- si tiene niveles bajos de calcio en la sangre (hipocalcemia).
- si es alérgico a denosumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Junod
Durante el tratamiento con denosumab usted podría desarrollar una infección de la piel con síntomas como una zona inflamada y enrojecida en la piel, más frecuentemente en la parte inferior de la pierna, que nota caliente y sensible al tacto (celulitis), y que puede ir acompañada de fiebre. Informe a su médico inmediatamente si presenta cualquiera de estos síntomas.
Además, debe tomar suplementos de calcio y vitamina D durante el tratamiento con Junod. Su médico le comentará este aspecto.
Su nivel de calcio en sangre puede descender durante el tratamiento con denosumab. Informe a su médico inmediatamente si nota cualquiera de los siguientes síntomas: espasmos, contracciones o calambres musculares, y/o entumecimiento u hormigueo en los dedos de las manos, de los pies o alrededor de la boca, y/o convulsiones, confusión o pérdida de la conciencia.
En raras ocasiones, se han notificado casos de niveles muy bajos de calcio en sangre que han requerido hospitalización e, incluso, reacciones potencialmente mortales. Por lo tanto, antes de la administración de cada dosis y, en pacientes con predisposición a la hipocalcemia, en un plazo de dos semanas tras la dosis inicial, se comprobarán sus niveles de calcio en sangre (mediante un análisis de sangre).
Informe a su médico si tiene o ha tenido problemas renales graves, insuficiencia renal, si ha necesitado someterse a diálisis o si está tomando medicamentos llamados glucocorticoides (como prednisolona o dexametasona), ya que podrían incrementar el riesgo de tener niveles bajos de calcio en sangre si no toma suplementos de calcio.
Problemas en la boca, dientes o mandíbula
En pacientes que reciben denosumab para la osteoporosis se ha notificado en raras ocasiones (puede afectar hasta 1 de cada 1 000 personas) un efecto adverso llamado osteonecrosis mandibular (ONM) (daño en el hueso de la mandíbula). El riesgo de ONM aumenta en pacientes tratados durante mucho tiempo (puede afectar hasta 1 de cada 200 personas si son tratadas durante 10 años). La ONM también puede ocurrir después de interrumpir el tratamiento. Es importante intentar prevenir el desarrollo de la ONM ya que puede ser una afección dolorosa que puede ser difícil de tratar. Para reducir el riesgo de desarrollar ONM, siga estas precauciones:
Antes de recibir el tratamiento, informe a su médico o enfermero (profesional sanitario) si:
- tiene algún problema en su boca o dientes como mala salud dental, enfermedad de las encías, o una extracción dental planeada.
- no recibe revisiones dentales periódicas o hace tiempo que no se ha sometido a una revisión dental.
- es fumador (ya que puede incrementar el riesgo de problemas dentales).
- ha estado tratado previamente con un bisfosfonato (utilizado para prevenir o tratar trastornos óseos).
- está tomando medicamentos llamados corticosteroides (como prednisolona o dexametasona).
- tiene cáncer.
Su médico puede pedirle que se someta a una revisión dental antes de iniciar el tratamiento con Junod.
Mientras esté siendo tratado, debe mantener una buena higiene bucal y someterse a revisiones dentales rutinarias. Si utiliza prótesis dental debe asegurarse de que esta se ajuste adecuadamente. Si está en tratamiento dental o se va a someter a cirugía dental (p. ej. extracciones dentales), informe a su médico sobre su tratamiento dental e informe a su dentista que está en tratamiento con Junod.
Contacte con su médico y su dentista inmediatamente si experimenta cualquier problema en su boca o dientes como dientes móviles, dolor o inflamación, o úlceras que no curan o que supuran, ya que podrían ser síntomas de ONM.
Fracturas inusuales del fémur
Algunas personas han desarrollado fracturas inusuales en el fémur mientras estaban en tratamiento con denosumab. Consulte con su médico si sufre un dolor nuevo o inusual en la cadera, ingle o muslo.
Niños y adolescentes
Junod no debería utilizarse en menores de 18 años de edad.
Otros medicamentos y Junod
Informe a su médico o farmacéutico si está tomando, ha tomado utilizado recientemente o pudiera tener que tomar cualquier otro medicamento.
Es especialmente importante que informe a su médico si está en tratamiento con otro medicamento que contenga denosumab. No debe usar Junod junto con otro medicamento que contenga denosumab.
Informe a su médico si está tomando medicamentos denominados glucocorticoides (como prednisolona o dexametasona), ver también la sección, “Advertencias y precauciones”.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Denosumab no se ha probado en mujeres embarazadas. No se recomienda utilizar Junod durante el embarazo. Las mujeres en edad fértil deben utilizar métodos anticonceptivos efectivos durante el tratamiento con Junod y al menos 5 meses después de interrumpir el tratamiento con Junod.
Si se queda embarazada durante el tratamiento con Junod o menos de 5 meses después de interrumpir el tratamiento con Junod, informe a su médico.
Se desconoce si denosumab se excreta en la leche materna. Es importante que le comunique a su médico si está en periodo de lactancia o si planea estarlo. Su médico le ayudará a decidir sobre si debe abandonar la lactancia materna, o si debe dejar de usar Junod, teniendo en cuenta el beneficio de la lactancia materna para el niño y el beneficio de Junod para usted.
Conducción y uso de máquinas
La influencia de Junod sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Junod contiene sorbitol, polisorbato 20 y sodio
Este medicamento contiene 46 mg de sorbitol en cada ml de solución.
Este medicamento contiene 0,1 mg de polisorbato 20 en cada ml de solución. Los polisorbatos pueden causar reacciones alérgicas. Informe a su médico si usted o su hijo tienen cualquier alergia conocida.
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por ml; esto es, esencialmente “exento de sodio”.
3. Cómo usar Junod
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada es una jeringa precargada de 60 mg administrada bajo la piel (vía subcutánea) en una única inyección una vez cada 6 meses.
Los mejores lugares para ponerse la inyección son la parte superior de los muslos y el abdomen. Si la inyección se la pone un cuidador (persona que le atiende), también puede administrarle la inyección en la cara externa de la parte superior del brazo.
Consulte con su médico la fecha de la siguiente posible inyección.
Cada envase de Junod contiene una tarjeta de recordatorio que puede despegarse del cartón y utilizarse para mantener un registro de la fecha de la siguiente inyección.
Además, debe tomar suplementos de calcio y vitamina D durante el tratamiento con Junod. Su médico le comentará este aspecto.
Su médico podrá decidir si es mejor que la inyección de Junod la administre usted o un cuidador. Su médico o profesional sanitario le mostrará a usted o a su cuidador cómo utilizar Junod. Si desea obtener instrucciones sobre cómo inyectar Junod, lea el último apartado de este prospecto.
No agitar.
Si olvidó usar Junod
Si se salta una dosis de Junod, la inyección deberá administrarse lo antes posible. Posteriormente, las inyecciones deberán programarse cada 6 meses a partir de la fecha de la última inyección.
Si interrumpe el tratamiento con Junod
Para sacar el máximo beneficio de su tratamiento y reducir el riesgo de fracturas, es importante que utilice Junod durante todo el periodo que le prescriba el médico. No interrumpa el tratamiento sin hablar antes con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Los pacientes tratados con denosumab pueden desarrollar infecciones en la piel (principalmente celulitis) con poca frecuencia (pueden afectar hasta 1 de cada 100 personas). Informe a su médico inmediatamentesi aparece alguno de estos síntomas durante el tratamiento con Junod: zona hinchada y enrojecida en la piel, normalmente en la parte inferior de la pierna, caliente y sensible al tacto y que puede ir acompañada de fiebre.
Raramente (pueden afectar hasta 1 de cada 1 000 personas), los pacientes que reciben denosumab pueden desarrollar dolor en la boca y/o mandíbula, inflamación o úlceras que no se curan en la boca o mandíbula, supuración, entumecimiento o sensación de pesadez en la mandíbula, o movilidad de un diente. Estos podrían ser síntomas de daño óseo en la mandíbula (osteonecrosis). Informe a su médico y a su dentista inmediatamentesi experimenta tales síntomas mientras está en tratamiento con Junod o después de interrumpir el tratamiento.
Raramente (pueden afectar hasta 1 de cada 1 000 personas), los pacientes que reciben denosumab pueden presentar niveles bajos de calcio en sangre (hipocalcemia); los niveles muy bajos de calcio en sangre pueden requerir hospitalización e, incluso, podrían poner en peligro la vida. Los síntomas incluyen espasmos, contracciones o calambres en los 34 músculos, y/o entumecimiento u hormigueo en los dedos de las manos, en los dedos de los pies o alrededor de la boca y/o convulsiones, confusión o pérdida de la conciencia. Si presenta alguno, informe a su médico inmediatamente. Los niveles bajos de calcio en la sangre también pueden provocar un cambio en el ritmo del corazón llamado prolongación del QT, que se puede observar realizando un electrocardiograma (ECG).
Raramente (pueden afectar hasta 1 de cada 1 000 personas), pueden darse fracturas inusuales del fémur en pacientes que reciben denosumab. Consulte con su médicosi sufre un dolor nuevo o inusual en la cadera, ingle o muslo ya que ello puede ser una indicación temprana de una posible fractura del fémur.
Raramente (pueden afectar hasta 1 de cada 1 000 personas), pueden darse reacciones alérgicas en pacientes que reciben denosumab. Los síntomas incluyen hinchazón en la cara, labios, lengua, garganta u otras partes del cuerpo; erupción, picor o urticaria en la piel, sibilancias o dificultad al respirar.
Informe a su médicosi experimenta tales síntomas mientras está en tratamiento con Junod.
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- dolor de huesos, articulaciones y/o músculos que a veces es intenso,
- dolor de piernas o brazos (dolor en las extremidades).
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 personas):
- micción dolorosa, micción frecuente, presencia de sangre en la orina, incontinencia urinaria,
- infección del tracto respiratorio superior,
- dolor, hormigueo o insensibilidad que se extiende hacia la parte inferior de la pierna (ciática),
- estreñimiento,
- molestias abdominales,
- erupción cutánea,
- afección cutánea con picor, enrojecimiento y/o sequedad (eccema),
- pérdida del pelo (alopecia).
Efectos adversos poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
- fiebre, vómitos y dolor o molestias abdominales (diverticulitis),
- infección del oído,
- erupción en la piel o úlceras en la boca (erupciones liquenoides inducidas por medicamentos).
Efectos adversos muy raros (pueden afectar hasta 1 de cada 10 000 personas):
- reacción alérgica que puede dañar los vasos sanguíneos, principalmente de la piel (p. ej. manchas color púrpura o rojo parduzco, urticaria o úlceras de la piel) (vasculitis por hipersensibilidad).
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- consulte a su médico si tiene dolor de oído, el oído le supura y/o sufre una infección de oído. Estos podrían ser síntomas de daño en los huesos del oído.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Junod
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja después de “EXP”. La fecha de caducidad es el último día del mes que se indica.
No utilice este medicamento si observa que la solución contiene partículas, o si está turbia o descolorida.
Conservar en nevera (entre 2 °C y 8 °C). No congelar.
Conservar la jeringa precargada en el embalaje exterior para protegerla de la luz.
Una vez fuera de la nevera, Junod puede conservarse a temperatura ambiente (hasta 25 °C) durante un máximo de 30 días en el envase original y en el embalaje exterior para protegerla de la luz. Se debe utilizar dentro de un plazo de 30 días.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Junod
- El principio activo es denosumab. Cada ml de jeringa precargada contiene 60 mg de denosumab.
- Los demás componentes son ácido acético glacial, hidróxido de sodio, sorbitol (E420), polisorbato 20 (E432) y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Junod es una solución inyectable transparente, de incolora a ligeramente amarilla suministrada en una jeringa precargada lista para usar.
Un ml de Junod se presenta en una jeringa precargada de vidrio individual (vidrio Tipo I) con tapón de émbolo FluroTec®, encajada una aguja (27 G × 12,7 mm), y un protector rígido de la aguja (carcasa rígida de elastómero + polipropileno).
El envase contiene una jeringa precarga con protector de seguridad.
Titular de la autorización de comercialización
Gedeon Richter Plc.
Gyömroi út 19-21.
1103 Budapest Hungary
Responsable de la fabricación
Gedeon Richter Plc.
Gyömroi út 19-21.
1103 Budapest Hungría
Chemical Works of Gedeon Richter Plc.
(Gedeon Richter Plc.)
Richter Gedeon utca 20. Debrecen
4031
Hungría
Fecha de la última revisión de este prospecto:
Otras fuentes de información
La información detallada de este producto está también disponible escaneando el código QR incluido más abajo o en el embalaje exterior con el móvil. La misma información está también disponible en la siguiente URL: www.junodinfo.com
Código QR debe ser incluido
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: https://www.ema.europa.eu , y en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/.
INSTRUCCIONES DE USO
Guía de las partes
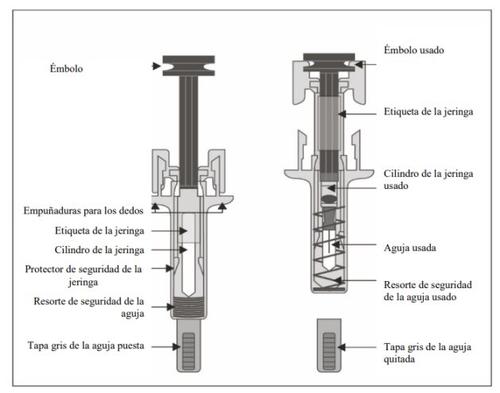
Importante
Antes de usar la jeringa precargada Junod con el protector automático de la aguja, lea toda esta información importante hasta el final.Siga las instrucciones cuidadosamente cuando utilice la jeringa.
- Es importante que no intente administrarse la inyección a sí mismo a menos que haya recibido la formación por parte de su médico o profesional sanitario.
- Junod se presenta como una inyección que atraviesa el tejido bajo la piel (inyección subcutánea).
- Noretire la tapa gris de la aguja de la jeringa precargada hasta que esté listo para inyectar.
- Noutilice la jeringa precargada si se ha caído sobre una superficie dura. Utilice una nueva jeringa precargada y contacte con su médico o profesional sanitario.
- Nointente activar la jeringa precargada antes de la inyección.
- Nointente eliminar el protector de seguridad de la jeringa precargada de esta.
Contacte con su médico o profesional sanitario si tiene cualquier pregunta.
Paso 1: Preparación
- Abra el envase que contiene la jeringa precargada y reúna los materiales necesarios para su inyección: toallitas con alcohol, una bola de algodón o gasa, una tirita y un contenedor para desechar objetos punzantes (no incluidos).
Para una inyección más cómoda, deje la jeringa precargada a temperatura ambiente alrededor de 15 – 30 minutos antes de inyectarla. Lávese sus manos minuciosamente con jabón y agua.
Sobre una superficie de trabajo limpia y bien iluminada, coloque la nueva jeringa precargada y los demás materiales.
- Nointente calentar la jeringa precargada utilizando una fuente de calor como agua caliente o microondas.
- Nodeje la jeringa precargada expuesta a la luz solar directa.
- Noagite la jeringa precargada.
Mantener la jeringa precargada fuera de la vista y del alcance de los niños.
- Agarre el protector de seguridad de la jeringa para retirarla del envase.
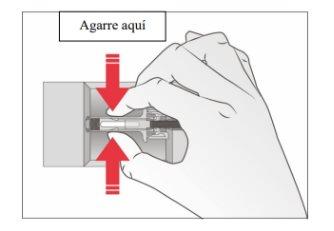
Por motivos de seguridad:
- Noagarre el émbolo.
- Noagarre la tapa gris de la aguja.
- Examine el medicamento y la jeringa precargada.
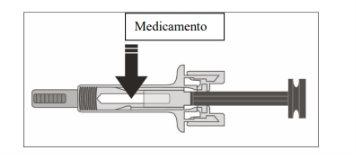
Nouse la jeringa precargada si:
- El medicamento está turbio o si hay partículas en él. Debe ser una solución transparente, de incolora a ligeramente amarillenta.
- Cualquier parte aparece agrietada o rota.
- La tapa gris de la aguja está perdida o no está bien sujeta.
- La fecha de caducidad impresa en la etiqueta ha superado el último día del mes indicado.
En todos los casos, consulte con su médico o profesional sanitario.
Paso 2: Prepárese
- Lave sus manos cuidadosamente. Prepare y limpie la zona de inyección.
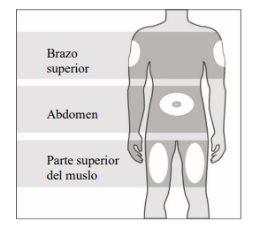
Puedes usar:
- Parte superior del muslo.
- Abdomen, a excepción de un área de 5 cm alrededor del ombligo.
- Área externa del brazo superior (solamente si alguien te administra la inyección).
Limpie la zona de la inyección con una toallita con alcohol. Deje que la piel se seque.
- Notoque la zona de inyección antes de inyectarse.
- Nose inyecte en áreas donde la piel esté sensible, contusionada, enrojecida o con durezas.
Evite inyectarse en áreas con cicatrices o estrías.
- Tire cuidadosamente la tapa gris de la aguja hacia fuera y lejos de su cuerpo.
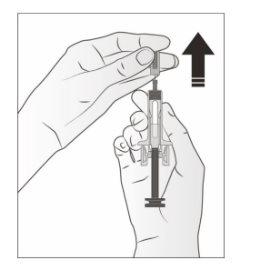
- Pellizque la zona de inyección para crear una superficie firme.
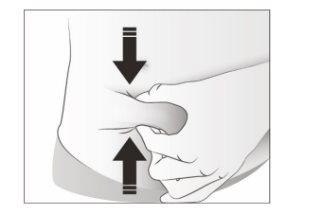
Es importante mantener la piel pellizcada cuando se inyecta.
Paso 3: Inyecte
- Sostenga el pellizco. INSERTE la aguja con un ángulo de 45 a 90 grados en la piel.
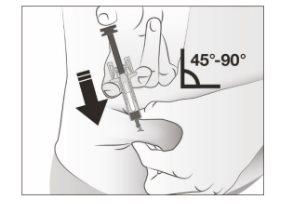
- Notoque el área limpia de la piel.
- Empujeel émbolo con presión lenta y constante hasta que sienta o escuche un “clic”. Empuje completamente hacia abajo hasta oír el “clic”.
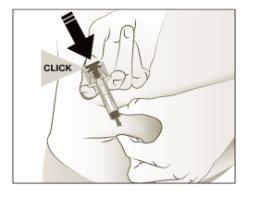
Nota:Es importante empujar hacia abajo hasta oír “clic” para administrar la dosis completa.
- Suelteel pulgar. A continuación, separela jeringa de la piel.
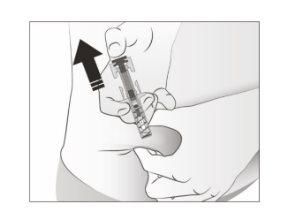
Tras soltar el émbolo, el protector de seguridad de la jeringa precargada cubrirá de forma segura la aguja de inyección.
Novuelva a poner la tapa gris de la aguja en la jeringa precargada usada.
Paso 4: Final
- Deseche la jeringa precargada usada y los demás materiales en un contenedor para desechar objetos punzantes.
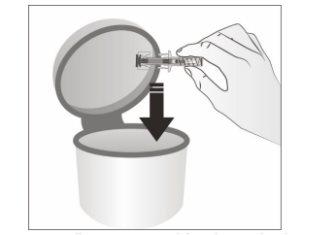
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
Mantener la jeringa y el contenedor para desechar objetos punzantes fuera de la vista y del alcance de los niños.
- Noreutilice la jeringa precargada.
- Norecicle las jeringas precargadas ni las arroje a la basura.
- Examine la zona de inyección.
Si hay sangre, presione una bola de algodón o una gasa en el sitio de inyección. Nofrote el sitio de la inyección. Aplique una tirita si es necesario.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a JUNOD 60 MG SOLUCION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 120 mgPrincipio activo: DenosumabFabricante: Fresenius Kabi Deutschland GmbhRequiere recetaForma farmacéutica: INYECTABLE, 120 mgPrincipio activo: DenosumabFabricante: Fresenius Kabi Deutschland GmbhRequiere recetaForma farmacéutica: INYECTABLE, 60 mgPrincipio activo: DenosumabFabricante: Fresenius Kabi Deutschland GmbhRequiere receta
Médicos online para JUNOD 60 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de JUNOD 60 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes












