
HUKYNDRA 40 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA

Cómo usar HUKYNDRA 40 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Hukyndra 40mg solución inyectable en pluma precargada
adalimumab
- Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Puede contribuir comunicando los efectos adversos que pudiera usted tener. La parte final de la sección 4 incluye información sobre cómo comunicar estos efectos adversos.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Su médico le dará una tarjeta de información para el paciente, que contiene información de seguridad importante que necesita conocer antes de empezar a usar y durante el tratamiento con Hukyndra. Conserve esta tarjeta de información para el paciente durante su tratamiento y los 4 meses posteriores a su última inyección de Hukyndra.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted y no debe dárselo a otras personas, aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Hukyndra y para qué se utiliza
- Qué necesita saber antes de empezar a usar Hukyndra
- Cómo usar Hukyndra
- Posibles efectos adversos
- Conservación de Hukyndra
- Contenido del envase e información adicional
- Instrucciones de uso
1. Qué es Hukyndra y para qué se utiliza
Hukyndra contiene como sustancia activa adalimumab
Hukyndra se usa para tratar:
- Artritis reumatoide
- Artritis idiopática juvenil poliarticular
- Artritis asociada a entesitis
- Espondilitis anquilosante
- Espondiloartritis axial sin evidencia radiográfica de espondilitis anquilosante
- Artritis psoriásica
- Psoriasis en placas
- Hidradenitis supurativa
- Enfermedad de Crohn
- Colitis ulcerosa
- Uveítis no infecciosa
La sustancia activa de Hukyndra, adalimumab, es un anticuerpo monoclonal humano. Los anticuerpos monoclonales son proteínas que atacan a una diana específica.
La diana de adalimumab es una proteína llamada factor de necrosis tumoral (TNFα), que interviene en el sistema inmune (defensa) y se encuentra en niveles elevados en las enfermedades inflamatorias descritas arriba. Mediante el ataque al TNFα, Hukyndra disminuye el proceso de inflamación en esas enfermedades.
Artritis reumatoide
La artritis reumatoide es una enfermedad inflamatoria de las articulaciones.
Hukyndra se utiliza para tratar la artritis reumatoide de moderada a grave en adultos. Puede que se le administren antes otros medicamentos modificadores de la enfermedad tales como metotrexato. En caso de que la respuesta a estos medicamentos no sea suficiente, se le administrará Hukyndra.
Hukyndra también puede usarse en el tratamiento de la artritis reumatoide grave, activa y progresiva sin tratamiento previo con metotrexato.
Hukyndra puede reducir el daño de las articulaciones producido por la enfermedad inflamatoria y puede ayudar a que se muevan con más libertad.
Su médico decidirá si Hukyndra debe utilizarse con metotrexato o en monoterapia.
Artritis idiopática juvenil poliarticular
La artritis idiopática juvenil poliarticular es una enfermedad inflamatoria de las articulaciones.
Hukyndra se utiliza para tratar la artritis idiopática juvenil poliarticular en pacientes desde los 2 años de edad. Puede haber recibido primero otros fármacos modificadores de la enfermedad, como metotrexato. Si no responde suficientemente bien a esos medicamentos, recibirá Hukyndra.
Su médico decidirá si Hukyndra debe utilizarse con metotrexato o en monoterapia.
Artritis asociada a entesitis
La artritis asociada a entesitis es una enfermedad inflamatoria de las articulaciones y los lugares de fijación de los tendones en el hueso.
Hukyndra se usa para tratar la artritis asociada a entesitis en pacientes desde los 6 años de edad. Puede haber recibido primero otros fármacos modificadores de la enfermedad, como metotrexato. Si no responde suficientemente bien a esos medicamentos, se le administrará Hukyndra.
Espondilitis anquilosante y espondiloartritis axial sin evidencia radiográfica de espondilitis anquilosante
La espondilitis anquilosante y la espondiloartritis axial sin evidencia radiográfica de espondilitis anquilosante son enfermedades inflamatorias que afectan a la columna vertebral.
Hukyndra se utiliza para tratar la espondilitis anquilosante grave y la espondiloartritis axial sin evidencia radiográfica de espondilitis anquilosante en adultos. Puede que se le trate primero con otros medicamentos. Si no responde suficientemente bien a esos medicamentos, se le administrará Hukyndra.
Artritis psoriásica
La artritis psoriásica es una enfermedad inflamatoria de las articulaciones que suele ir asociada con la psoriasis.
Hukyndra se utiliza para tratar la artritis psoriásica en adultos. Hukyndra puede reducir el daño que produce la enfermedad en las articulaciones y puede ayudar a que se muevan con más libertad. Puede que se le trate primero con otros medicamentos. Si no responde suficientemente bien a esos medicamentos, se le administrará Hukyndra.
Psoriasis en placas
La psoriasis en placas es una enfermedad de la piel que causa áreas enrojecidas, escamosas, con costras y cubiertas por escamas plateadas. La psoriasis en placas también puede afectar las uñas, provocando que se deterioren, se engrosen y se levanten del lecho de la uña, lo cual puede ser doloroso.
Hukyndra se utiliza para tratar
- la psoriasis crónica en placas de moderada a grave en adultos y
- la psoriasis crónica en placas grave en niños y adolescentes entre 4 y 17 años de edad que no hayan respondido o no sean buenos candidatos para terapia tópica y fototerapias.
Hidradenitis supurativa
La hidradenitis supurativa (a veces denominada acné inverso) es una enfermedad inflamatoria de la piel crónica y a menudo dolorosa. Los síntomas pueden incluir nódulos sensibles (bultos) y abscesos (forúnculos) que pueden secretar pus. Normalmente afecta a áreas específicas de la piel, como debajo del pecho, de las axilas, zona interior de los muslos, ingle y nalgas. También puede haber cicatrices en las áreas afectadas.
Hukyndra se utiliza para tratar
- la hidradenitis supurativa de moderada a grave en adultos y
- la hidradenitis supurativa de moderada a grave en adolescentes desde 12 a 17 años.
Hukyndra puede reducir el número de nódulos y abscesos provocados por la enfermedad y el dolor que normalmente va asociado a esta enfermedad. Puede que se le trate primero con otros medicamentos. Si no responde suficientemente bien a esos medicamentos, se le administrará Hukyndra.
Enfermedad de Crohn
La enfermedad de Crohn es una enfermedad inflamatoria del tracto digestivo.
Hukyndra se utiliza para tratar
- la enfermedad de Crohn de moderada a grave en adultos y
- la enfermedad de Crohn de moderada a grave en niños y adolescentes desde los 6 hasta los 17 años.
Puede haber recibido otros medicamentos previamente. Si no responde lo suficientemente bien a esos medicamentos, recibirá Hukyndra.
Colitis ulcerosa
La colitis ulcerosa es una enfermedad inflamatoria del intestino grueso.
Hukyndra se utiliza para tratar
- la colitis ulcerosa de moderada a grave en adultos
- la colitis ulcerosa de moderada a grave en niños y adolescentes desde los 6 hasta los 17 años
Puede haber recibido otros medicamentos previamente. Si no responde lo suficientemente bien a esos medicamentos, recibirá Hukyndra.
Uveítis no infecciosa
La uveítis no infecciosa es una enfermedad inflamatoria que afecta a ciertas partes del ojo.
Hukyndra se utiliza para tratar
- adultos con uveítis no infecciosa con inflamación que afecta a la parte posterior del ojo.
- niños desde los 2 años de edad con uveítis crónica no infecciosa con inflamación que
- afecta a la parte frontal del ojo.
Esta inflamación puede conducir a una disminución de la visión y/o la presencia de motas en el ojo (puntos negros o líneas delgadas que se mueven a lo largo del campo de visión). Hukyndra actúa reduciendo esta inflamación.
Puede haber recibido otros medicamentos previamente. Si no responde lo suficientemente bien a esos medicamentos, recibirá Hukyndra.
2. Qué necesita saber antes de empezar a usar Hukyndra
No use Hukyndra
- Si es alérgico a adalimumab o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si padece tuberculosis activa u otras infecciones graves (ver “Advertencias y precauciones”). En caso de tener síntomas de cualquier infección, por ejemplo, fiebre, heridas, cansancio, problemas dentales, es importante que informe a su médico.
- Si padece insuficiencia cardiaca moderada o grave. Es importante que le diga a su médico si ha tenido o tiene algún problema cardiaco serio (ver “Advertencias y precauciones”).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Hukyndra.
Reacciones alérgicas
- Si tuviera una reacción alérgica con síntomas como opresión en el pecho, dificultad para respirar, mareo, hinchazón o sarpullido, interrumpa la administración de Hukyndra y póngase en contacto con su médico inmediatamente ya que, en casos raros, estas reacciones pueden poner en peligro la vida.
Infecciones
- Si padece cualquier infección, incluyendo infección crónica o una infección localizada en alguna parte del cuerpo (por ejemplo: una úlcera en la pierna), consulte a su médico antes de comenzar el tratamiento con Hukyndra. Si no está seguro, póngase en contacto con su médico.
- Con el tratamiento con Hukyndra podría contraer infecciones con más facilidad. Este riesgo puede ser mayor si tiene dañados los pulmones. Estas infecciones pueden ser graves e incluyen:
- tuberculosis
- infecciones causadas por virus, hongos, parásitos o bacterias
- infección grave en la sangre (sepsis)
En casos raros, estas infecciones podrían poner en peligro su vida. Es importante que en el caso de que tenga síntomas como fiebre, heridas, cansancio o problemas dentales, se lo diga a su médico. Su médico puede indicar que deje de utilizar Hukyndra durante algún tiempo.
- Informe a su médico si reside o viaja por regiones en las que las infecciones fúngicas (como, por ejemplo, histoplasmosis, coccidiomicosis o blastomicosis) son muy frecuentes.
- Informe a su médico si ha sufrido infecciones recurrentes u otros trastornos que aumenten el riesgo de infecciones.
- Si tiene más de 65 años puede ser más susceptible de padecer infecciones mientras está en tratamiento con Hukyndra. Tanto usted como su médico deben prestar especial atención a la aparición de signos de infección mientras esté siendo tratado con Hukyndra. Es importante informar a su médico si tiene síntomas de infecciones, como fiebre, heridas, sensación de cansancio o problemas dentales.
Tuberculosis
- Es muy importante que avise a su médico si ha sufrido tuberculosis en alguna ocasión o si ha estado en estrecho contacto con alguien que haya padecido tuberculosis. Si tiene tuberculosis activa, no debe usar Hukyndra.
- Dado que se han descrito casos de tuberculosis en pacientes en tratamiento con adalimumab, su médico le examinará en busca de signos o síntomas de tuberculosis antes de comenzar su tratamiento con Hukyndra. Esto incluirá la realización de una evaluación médica minuciosa, incluyendo su historia médica y las pruebas apropiadas de diagnóstico (por ejemplo radiografía de tórax y la prueba de la tuberculina). La realización y resultados de estas pruebas debe anotarse en su tarjeta de información para el paciente.
- Se puede desarrollar tuberculosis durante el tratamiento incluso si usted ha recibido el tratamiento para prevenir la tuberculosis.
- Si apareciesen síntomas de tuberculosis (como por ejemplo, tos que no se va, pérdida de peso, falta de energía, febrícula) o de cualquier otra infección durante o una vez finalizado el tratamiento, póngase en contacto inmediatamente con su médico.
Hepatitis B
- Informe a su médico si es usted portador del virus de la hepatitis B (VHB), si ha tenido infecciones activas con VHB o si piensa que podría correr riesgo de contraer el VHB.
- Su médico le debe realizar un análisis para el VHB. En las personas portadoras del VHB, adalimumab puede causar que el virus vuelva a ser activo.
- En casos raros, especialmente si está tomando otros medicamentos que suprimen el sistema inmune, la reactivación del VHB puede poner en peligro su vida.
Cirugía o intervención dental
- Si le van a realizar una intervención quirúrgica o dental, diga a su médico que está usando Hukyndra. Su médico le puede recomendar que interrumpa temporalmente el tratamiento con Hukyndra.
Enfermedad desmielinizante
- Si padece o desarrolla una enfermedad desmielinizante (una enfermedad que afecta a la capa de aislamiento alrededor de los nervios, como la esclerosis múltiple), su médico decidirá si debe ser tratado o continuar en tratamiento con Hukyndra. Informe inmediatamente a su médico si experimenta síntomas tales como cambios en la visión, debilidad en brazos o piernas o entumecimiento u hormigueo en cualquier parte del cuerpo.
Vacunas
- Ciertas vacunas pueden causar infecciones y no deben administrarse si se está en tratamiento con Hukyndra.
- Consulte con su médico antes de la administración de cualquier tipo de vacuna.
- Si es posible, se recomienda que los niños reciban las vacunas previstas para su edad antes de iniciar el tratamiento con Hukyndra.
- Si recibió Hukyndra mientras estaba embarazada, su bebé puede tener un riesgo mayor de sufrir infecciones durante aproximadamente los cinco meses siguientes a la última dosis que haya recibido de Hukyndra durante su embarazo. Es importante que informe al médico de su bebé y a otros profesionales sanitarios sobre el uso de Hukyndra durante el embarazo, para que ellos puedan decidir si su bebé debe recibir alguna vacuna.
Insuficiencia cardiaca
- Si tiene insuficiencia cardiaca leve y está en tratamiento con Hukyndra, puede ser monitorizado estrechamente por su médico. Es importante que le diga a su médico si ha tenido o tiene problemas cardíacos graves. Si desarrolla síntomas nuevos o empeoran sus síntomas (por ejemplo, dificultad al respirar, o hinchazón de los pies), debe ponerse en contacto con su médico inmediatamente. Su médico decidirá si debe seguir recibiendo Hukyndra.
Fiebre, hematomas, sangrado o aspecto pálido
- En algunos pacientes, el organismo puede ser incapaz de producir un número suficiente del tipo de células sanguíneas que ayudan al cuerpo a luchar contra las infecciones o de las que contribuyen a parar las hemorragias. Su médico puede decidir si interrumpe el tratamiento. Si desarrolla fiebre persistente, ligeros hematomas o sangra muy fácilmente o está muy pálido, llame a su médico inmediatamente.
Cáncer
- En muy raras ocasiones se han dado casos de ciertos tipos de cáncer en niños y adultos tratados con adalimumab u otros agentes que bloquean el TNF.
- Las personas con artritis reumatoide de grados más graves y que padezcan la enfermedad desde hace mucho tiempo pueden tener un riesgo mayor que la media de desarrollar un linfoma (un cáncer que afecta al sistema linfático) y leucemia (un cáncer que afecta a la sangre y a la médula ósea).
- Si está en tratamiento con Hukyndra el riesgo de padecer linfoma, leucemia u otros tipos de cáncer puede incrementarse. Se ha observado, en raras ocasiones, un tipo de linfoma poco frecuente y grave en pacientes en tratamiento con adalimumab. Algunos de estos pacientes recibían tratamiento también con azatioprina o 6- mercaptopurina.
- Informe a su médico si está tomando azatioprina o 6-mercaptopurina con Hukyndra.
- Se han observado casos de cáncer de piel tipo no melanoma en pacientes que usan adalimumab.
- Informe a su médico si durante o después del tratamiento aparecen nuevas lesiones en su piel o si las lesiones existentes cambian de apariencia.
- Se han registrado cánceres, diferentes del linfoma, en pacientes con una determinada enfermedad pulmonar, denominada Enfermedad Pulmonar Obstructiva Crónica (EPOC), tratados con otro agente bloqueante del TNF. Si tiene EPOC, o fuma mucho, debe consultar a su médico si el tratamiento con un bloqueante del TNF es adecuado en su caso.
Enfermedad autoimmune
- En raras ocasiones el tratamiento con Hukyndra podría dar lugar a un síndrome similar al lupus. Contacte con su médico si tiene síntomas como erupción persistente sin explicación, fiebre, dolor de las articulaciones o cansancio.
Niños y adolescentes
- Vacunas: si es posible su hijo debe ponerse al día con todas las vacunas antes de usar Hukyndra.
Otros medicamentos y Hukyndra
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
No debe tomar Hukyndra con medicamentos que contengan los siguientes principios activos debido a un incremento del riesgo de infecciones graves:
- anakinra
- abatecept
Hukyndra se puede tomar junto con:
- metotrexato
- ciertos medicamentos antirreumáticos modificadores de la enfermedad (como por ejemplo, sulfasalazina, hidroxicloroquina, leflunomida y preparaciones inyectables a base de sales de oro)
- esteroides o medicamentos para el dolor, incluidos los antiinflamatorios no esteroideos (AINEs).
Si tiene alguna duda, consulte a su médico.
Embarazo y lactancia
- Debe considerar el uso de métodos anticonceptivos adecuados para evitar quedarse embarazada y continuar con su uso durante al menos 5 meses después del último tratamiento con Hukyndra.
- Si está embarazada, cree que podría estar embarazada o tiene intención de tener un bebé, pida consejo a su médico sobre el uso de este medicamento.
- Hukyndra debe usarse durante el embarazo solo si es necesario.
- Según un estudio en embarazo, no hubo un mayor riesgo de defectos congénitos cuando la madre había recibido tratamiento con adalimumab durante el embarazo comparado con las madres con la misma enfermedad que no recibieron tratamiento con adalimumab.
- Hukyndra puede usarse durante la lactancia.
- Si utiliza Hukyndra mientras está embarazada, su hijo puede tener un riesgo más alto de contraer una infección.
- Es importante que informe al pediatra y a otros profesionales sanitarios sobre el uso de Hukyndra durante el embarazo antes de que el bebé reciba ninguna vacuna. Para más información sobre vacunas ver la sección “Advertencias y precauciones”.
Conducción y uso de máquinas
La influencia de Hukyndra sobre la capacidad para conducir, montar en bicicleta o utilizar máquinas es pequeña. Puede producirse sensación de que la habitación da vueltas y alteraciones de la visión después de utilizar Hukyndra.
Hukyndra contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por 0,4 ml; esto es, esencialmente “exento de sodio”.
3. Cómo usar Hukyndra
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
En la siguiente tabla se indican las dosis recomendadas de Hukyndra para cada uno de sus usos aprobados. Su médico le puede prescribir otra dosis de Hukyndra si necesita una dosis diferente.
Artritis reumatoide, artritis psoriásica, espondilitis anquilosante o espondiloartritis axial sin evidencia radiográfica de espondilitis anquilosante | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Adultos | 40 mg en semanas alternas | En la artritis reumatoide, continúa el tratamiento con metotrexato durante el uso de Hukyndra. Si su médico decide que el metotrexato es inapropiado, puede administrarse Hukyndra en monoterapia. Si presenta artritis reumatoide y no recibe metotrexato con su tratamiento con Hukyndra, su médico puede decidir administrarle 40 mg de Hukyndra cada semana u 80 mg cada dos semanas. |
Artritis idiopática juvenil poliarticular | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Niños, adolescentes y adultos desde los 2 años de edad con peso de 30 kg o más | 40 mg en semanas alternas | No procede |
Artritis asociada a entesitis | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Niños, adolescentes y adultos desde 6 años de edad con peso de 30 kg o más | 40 mg en semanas alternas | No procede |
Psoriasis en placas | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Adultos | La dosis inicial es de 80 mg (dos inyecciones de 40 mg en un día), seguida de 40 mg en semanas alternas comenzando una semana después de la primera dosis. | Si obtiene una respuesta inadecuada, su médico puede aumentar la dosis a 40 mg cada semana u 80 mg cada dos semanas. |
Niños y adolescentes desde los 4 a 17 años de edad con peso de 30 kg o más | La dosis inicial es de 40 mg, seguida de 40 mg una semana después. A partir de entonces, la dosis habitual es de 40 mg en semanas alternas. | No procede |
Hidradenitis supurativa | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Adultos | La dosis inicial es de 160 mg (cuatro inyecciones de 40 mg en un día o dos inyecciones de 40 mg al día durante dos días consecutivos), seguida de una dosis de 80 mg (dos inyecciones de 40 mg en un día) dos semanas más tarde. Después de dos semanas más, continuar con una dosis de 40 mg cada semana u 80 mg cada dos semanas, según se lo haya recetado su médico. | Se recomienda que use un líquido antiséptico diario en las zonas afectadas. |
Adolescentes a partir de 12 a 17 años de edad, con un peso de 30 kg o más | La dosis inicial es de 80 mg (2 inyecciones de 40 mg en un día), seguido de 40 mg en semanas alternas comenzando una semana después. | Si obtiene una respuesta inadecuada con Hukyndra 40 mg en semanas alternas, su médico puede aumentar la dosis a 40 mg semanales u 80 mg cada dos semanas. Se recomienda que utilice un líquido antiséptico diario en las zonas afectadas. |
Enfermedad de Crohn | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Niños, adolescentes y adultos a partir de los 6 años de edad con peso de 40 kg o más | La dosis inicial es de 80 mg (dos inyecciones de 40 mg en un día), seguida de 40 mg dos semanas más tarde. Si se necesita una respuesta más rápida, el médico puede prescribir una primera dosis de 160 mg (cuatro inyecciones de 40 mg en un día o dos inyecciones de 40 mg al día durante dos días consecutivos) seguida de 80 mg (dos inyecciones de 40 mg en un día) dos semanas más tarde. A partir de entonces, la dosis habitual es de 40 mg en semanas alternas. | Su médico puede aumentar la dosis a 40 mg cada semana u 80 mg cada dos semanas. |
Niños y adolescentes desde los 6 a 17 años de edad que pesen menos de 40 kg | La dosis inicial es de 40 mg, seguida de 20 mg dos semanas más tarde. Si se necesita una respuesta más rápida, el médico puede prescribir una primera dosis de 80 mg (dos inyecciones de 40 mg en un día), seguida de 40 mg dos semanas más tarde. A partir de entonces, la dosis habitual es de 20 mg en semanas alternas. | Su médico puede aumentar la frecuencia de la dosis a 20 mg cada semana. |
- Hukyndra solo está disponible jeringa pregargada de 40 mg, pluma precargada de 40 mg y jeringa precargada de 80 mg. Por lo tanto, no es posible administrar Hukyndra a pacientes que requieran menos de una dosis completa de 40 mg.
Colitis ulcerosa | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Adultos | La dosis inicial es de 160 mg (cuatro inyecciones de 40 mg en un día o dos inyecciones de 40 mg al día durante dos días consecutivos), seguidas de una dosis de 80 mg (dos inyecciones de 40 mg en un día) dos semanas más tarde. A partir de entonces, la dosis habitual es de 40 mg en semanas alternas. | Su médico puede aumentar la dosis a 40 mg cada semana u 80 mg cada dos semanas. |
Niños y adolescentes desde los 6 años de edad con un peso inferior a 40 kg | Primera dosis de 80 mg (dos inyecciones de 40 mg en un día), seguida de 40 mg (una inyección de 40 mg) dos semanas después. A partir de entonces, la dosis habitual es de 40 mg en semanas alternas. | Debe continuar utilizando adalimumab a la dosis habitual, incluso después de cumplir los 18 años. |
Niños y adolescentes desde los 6 años de edad con un peso de 40 kg o superior | Primera dosis de 160 mg (cuatro inyecciones de 40 mg en un día o dos inyecciones de 40 mg al día en dos días consecutivos), seguida de 80 mg (dos inyecciones de 40 mg en un día) dos semanas después. A partir de entonces, la dosis habitual es de 80 mg en semanas alternas. | Debe continuar utilizando adalimumab a la dosis habitual, incluso después de cumplir los 18 años. |
Uveitis no infecciosa | ||
Edad o peso corporal | Cuánto y con qué frecuencia se debe tomar | Notas |
Adultos | La dosis inicial es de 80 mg (dos inyecciones de 40 mg en un día), seguidos de 40 mg en semanas alternas comenzando una semana después de la dosis inicial. | Se puede continuar el tratamiento con corticoesteroides u otros medicamentos que afectan el sistema inmune. Hukyndra también se puede administrar sólo. |
Niños y adolescentes desde los 2 años de edad con peso de al menos 30 kg | 40 mg en semanas alternas | Su médico le puede prescribir una dosis inicial de 80 mg que puede ser administrada una semana antes de empezar con la pauta habitual de 40 mg en semanas alternas. Se recomienda el uso de Hukyndra en combinación con metotrexato. |
Forma y vía de administración
Hukyndra se inyecta bajo la piel (vía subcutánea).
En la sección 7 «Instrucciones de uso» se proporcionan las instrucciones detalladas sobre cómo inyectar Hukyndra.
Si usa más Hukyndra del que debe
Si accidentalmente se inyecta Hukyndra con más frecuencia que la pautada por su médico o farmacéutico, informe de ello a su médico o farmacéutico. Siempre lleve la caja del medicamento consigo, incluso si está vacía.
Si olvidó usar Hukyndra
Si olvida administrarse una inyección, debe inyectarse la siguiente dosis de Hukyndra tan pronto como lo recuerde. Después se administrará la siguiente dosis como habitualmente, como si no se hubiese olvidado una dosis.
Si interrumpe el tratamiento con Hukyndra
La decisión de dejar de usar Hukyndra debe ser discutida con su médico. Sus síntomas pueden volver si deja de utilizar Hukyndra.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. La mayoría de los efectos adversos son leves a moderados. Sin embargo, algunos pueden ser graves y requerir tratamiento. Los efectos adversos pueden aparecer al menos hasta 4 meses después de la última inyección de Hukyndra.
Póngase en contacto con su médico inmediatamente si nota cualquiera de los siguientes efectos
- erupción grave, urticaria u otros signos de reacción alérgica
- hinchazón de la cara, manos, pies
- dificultad para respirar, tragar
- falta de aliento con la actividad física o al estar tumbado o hinchazón de pies.
Póngase en contacto con su médico tan pronto como sea posible si nota alguno de los siguientes efectos
- signos de infección tales como fiebre, ganas de vomitar, heridas, problemas dentales, sensación de quemazón al orinar
- sensación de debilidad o cansancio
- tos
- hormigueo
- entumecimiento
- visión doble
- debilidad en brazos o piernas
- una protuberancia o una herida abierta que no se cura
- signos y síntomas de alteraciones en la sangre como fiebre persistente, cardenales, hemorragias y palidez
Los síntomas descritos anteriormente pueden ser signos de los efectos adversos listados a continuación, que se han observado con adalimumab.
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas)
- reacciones en el lugar de inyección (incluyendo dolor, hinchazón, enrojecimiento o picor)
- infecciones del tracto respiratorio inferior (incluyendo resfriado, moqueo, sinusitis, neumonía)
- dolor de cabeza
- dolor abdominal
- náuseas y vómitos
- sarpullido
- dolor muscular
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
- infecciones graves (incluyendo envenenamiento sanguíneo y gripe)
- infecciones intestinales (incluyendo gastroenteritis)
- infecciones de la piel (incluyendo celulitis y herpes)
- infección de oído
- infecciones orales (incluyendo infección dental y dolor frío)
- infecciones en el sistema reproductor
- infección del tracto urinario
- infecciones por hongos
- infección en las articulaciones
- tumores benignos
- cáncer de piel
- reacciones alérgicas (incluyendo alergia estacional)
- deshidratación
- cambios de humor (incluyendo depresión)
- ansiedad
- dificultad para dormir
- alteraciones sensoriales como hormigueo, escozor o entumecimiento
- migraña
- compresión de la raíz nerviosa (incluyendo dolor en la parte baja de la espalda y la pierna)
- alteraciones visuales
- inflamación del ojo
- inflamación del párpado e hinchazón del ojo
- vértigo (sensación de mareo o de que todo da vueltas)
- sensación de pulso acelerado
- alta presión sanguínea
- rubor
- hematomas (acumulación de sangre fuera de los vasos sanguíneos)
- tos
- asma
- dificultad para respirar
- sangrado gastrointestinal
- dispepsia (indigestión, hinchazón y ardor)
- reflujo ácido
- síndrome del ojo seco (incluyendo sequedad en ojos y boca)
- picores
- sarpullido con picor
- moratones
- inflamación de la piel (como eczema)
- rotura de uñas de las manos y los pies
- aumento de la transpiración
- pérdida de pelo
- psoriasis de nueva aparición o empeoramiento de la psoriasis existente
- espasmos musculares
- sangre en orina
- problemas renales
- dolor de pecho
- edema (hinchazón)
- fiebre
- disminución de plaquetas en sangre, lo que incrementa el riesgo de sangrado o moratones
- problemas de cicatrización
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- infecciones oportunistas (que incluyen tuberculosis y otras infecciones que ocurren cuando la resistencia a la enfermedad disminuye)
- infecciones neurológicas (incluyendo meningitis viral)
- infecciones del ojo
- infecciones bacterianas
- diverticulitis (inflamación e infección del intestino grueso)
- cáncer
- cáncer que afecta al sistema linfático
- melanoma
- alteraciones inmunológicas que pueden afectar a los pulmones, piel y ganglios linfáticos (la presentación más frecuente es sarcoidosis)
- vasculitis (inflamación de los vasos sanguíneos)
- temblor (sentirse tembloroso)
- neuropatía (trastorno del sistema nervioso)
- derrame cerebral
- pérdida de oído, zumbidos
- sensación de pulso irregular como brincos
- problemas del corazón que pueden causar dificultad para respirar o hinchazón de tobillos
- ataque al corazón
- saco en la pared de una arteria mayor, inflamación y coagulación en una vena, bloqueo de un vaso sanguíneo
- enfermedades pulmonares que pueden causar dificultad para respirar (incluyendo inflamación)
- embolia pulmonar (bloqueo de una arteria del pulmón)
- derrame pleural (almacenamiento anormal de fluido en el espacio pleural)
- inflamación del páncreas que causa un dolor grave en el abdomen y la espalda
- dificultad para tragar
- edema facial (hinchazón de la cara)
- inflamación de la vesícula; piedras en la vesícula
- grasa en el hígado
- sudores nocturnos
- cicatrices
- crisis muscular anormal
- lupus eritematoso sistémico (incluyendo inflamación de la piel, corazón, pulmones, articulaciones y otros órganos)
- interrupciones del sueño
- impotencia
- inflamaciones
Raros(pueden afectar hasta 1 de cada 1000 personas)
- leucemia (cáncer que afecta a la sangre y la médula ósea)
- reacción alérgica grave con shock
- esclerosis múltiple
- alteraciones nerviosas (como inflamación del nervio óptico y síndrome de Guillain-Barré que puede provocar debilidad muscular, sensaciones anormales, hormigueo en los brazos y la parte superior del cuerpo)
- parada cardiaca
- fibrosis pulmonar (cicatriz en el pulmón)
- perforación intestinal (orificio en el intestino)
- hepatitis
- reactivación del virus de la hepatitis B
- hepatitis autoinmune (inflamación del hígado causada por el propio sistema inmunológico del cuerpo)
- vasculitis cutánea (inflamación de los vasos sanguíneos en la piel)
- síndrome de Stevens-Johnson (los síntomas tempranos incluyen malestar, fiebre, dolor de cabeza y sarpullido)
- edema facial (hinchazón de la cara) asociado con reacciones alérgicas
- eritema multiforme (erupción inflamatoria en la piel)
- síndrome similar al lupus
- angioedema (inflamación localizada de la piel)
- reacción liquenoide en la piel (sarpullido rojizo-morado con picor)
Frecuencia no conocida(no se puede estimar la frecuencia a partir de los datos disponibles)
- linfoma hepatoesplénico de células T (cáncer sanguíneo raro que a menudo es mortal)
- carcinoma de células de Merkel (un tipo de cáncer de piel)
- sarcoma de Kaposi, un cáncer poco común relacionado con la infección por el virus del herpes humano 8. El sarcoma de Kaposi suele manifestarse con mayor frecuencia como lesiones cutáneas de color púrpura.
- fallo hepático
- empeoramiento de una enfermedad llamada dermatomiositis (visto como erupción cutánea acompañada de debilidad muscular)
- aumento de peso (para la mayoría de pacientes, el aumento de peso fue reducido)
Algunos efectos adversos observados con adalimumab no tienen síntomas y sólo pueden ser identificados mediante un análisis de sangre. Estos incluyen:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas)
- bajo recuento sanguíneo de células blancas
- bajo recuento sanguíneo de células rojas
- aumento de lípidos en sangre
- aumento de enzimas hepáticas
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
- alto recuento sanguíneo de células blancas
- bajo recuento sanguíneo de plaquetas
- aumento de ácido úrico en sangre
- valores anormales de sodio en sangre
- bajo nivel de calcio en sangre
- bajo nivel de fosfato en sangre
- azúcar en sangre alto
- valores altos de lactato deshidrogenasa en sangre
- presencia de autoanticuerpos en sangre
- bajo nivel de potasio en sangre
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
- valores de bilirrubina elevados (análisis de función hepática)
Raros(pueden afectar hasta 1 de cada 1000 personas)
- recuentos bajos en sangre para células blancas, células rojas y plaquetas
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte con su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede
comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Hukyndra
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y en el envase después de “EXP”. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 °C y 8 °C). No congelar.
Conservar la pluma precargada en el embalaje exterior para protegerla de la luz.
Almacenamiento alternativo:
Cuando sea necesario (por ejemplo cuando esté de viaje), puede almacenar una pluma precargada individual de Hukyndra a 20 ºC hasta 25 ºC durante un periodo máximo de hasta 30 días - asegúrese de protegerla de la luz). Una vez que se ha sacado de la nevera para almacenar la pluma a 20 ºC hasta 25 ºC, debe usarla en los siguientes 30 días o desecharla, incluso si la vuelve a meter en la nevera.
Debe anotar la fecha en la que retiró la pluma de la nevera, y la fecha después de la cual debe desechar la pluma.
No utilice este medicamento si el líquido está turbio, decolorado o contiene escamas o partículas.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Hukyndra
El principio activo es adalimumab.
Los demás componentes son: cloruro de sodio, sacarosa, polisorbato 80, agua para preparaciones inyectables, ácido clorhídrico (para ajustar el pH), hidróxido de sodio (para ajustar el pH).
Aspecto de Hukyndra y contenido del envase
Hukyndra 40 mg solución inyectable en pluma precargada se suministra como 0,4 ml de solución inyectable en un sistema de inyección precargado con aguja (autoinyector) que contiene una jeringa de vidrio precargada con una aguja fija y un émbolo (caucho de bromobutilo). La pluma es un dispositivo de inyección mecánico de mano, desechable y de un solo uso.
Cada envase contiene 1, 2 o 6 plumas precargadas envasadas en un blíster con 1, 2 o 6 toallitas impregnadas con alcohol.
Puede que solamente estén comercializados algunos tamaños de envases.
Hukyndra puede estar disponible en jeringa precargada y/o en pluma precargada.
Titular de la autorización de comercialización
STADA Arzneimittel AG
Stadastrasse 2-18
61118 Bad Vilbel
Alemania
Responsables de la fabricación
Ivers-Lee CSM
Marie-Curie-Str.8
79539 Lörrach
Alemania
Alvotech Hf
Sæmundargata 15-19
Reykjavik, 101
Islandia
STADA Arzneimittel AG
Stadastrasse 2-18
61118 Bad Vilbel
Alemania
Pueden solicitar más información respecto a este medicamento, dirigiéndose al representante local del titular de la autorización de comercialización:
België/Belgique/Belgien EG (Eurogenerics) NV Tél/Tel: +32 24797878 | Lietuva UAB „STADA Baltics“ Tel: +370 52603926 |
| Luxembourg/Luxemburg EG (Eurogenerics) NV Tél/Tel: +32 4797878 |
Ceská republika STADA PHARMA CZ s.r.o. Tel: +420 257888111 | Magyarország STADA Hungary Kft Tel.: +36 18009747 |
Danmark STADA Nordic ApS Tlf: +45 44859999 | Malta Pharma.MT Ltd Tel: +356 21337008 |
Deutschland STADAPHARM GmbH Tel: +49 61016030 | Nederland Centrafarm B.V. Tel.: +31 765081000 |
Eesti UAB „STADA Baltics“ Tel: +370 52603926 | Norge STADA Nordic ApS Tlf: +45 44859999 |
Ελλ?δα STADA Arzneimittel AG Τηλ: +30 2106664667 | Österreich STADA Arzneimittel GmbH Tel: +43 136785850 |
España Laboratorio STADA, S.L. Tel: +34 934738889 | Polska STADA Poland Sp. z.o o. Tel: +48 227377920 |
France EG LABO - Laboratoires EuroGenerics Tél: +33 146948686 | Portugal Stada, Lda. Tel: +351 211209870 |
Hrvatska STADA d.o.o. Tel: +385 13764111 | România STADA M&D SRL Tel: +40 213160640 |
Ireland Clonmel Healthcare Ltd. Tel: +353 526177777 | Slovenija Stada d.o.o. Tel: +386 15896710 |
Ísland STADA Arzneimittel AG Sími: +49 61016030 | Slovenská republika STADA PHARMA Slovakia, s.r.o. Tel: +421 252621933 |
Italia EG SpA Tel: +39 028310371 | Suomi/Finland STADA Nordic ApS, Suomen sivuliike Puh/Tel: +358 207416888 |
Κ?προς STADA Arzneimittel AG Τηλ: +30 2106664667 | Sverige STADA Nordic ApS Tel: +45 44859999 |
Latvija UAB „STADA Baltics“ Tel: +370 52603926 | United Kingdom (Northern Ireland) STADA Arzneimittel AG Tel: +49 61016030 |
Fecha de la última revisión de este prospecto
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Puede acceder a información detallada y actualizada sobre este medicamento, que incluye un vídeo sobre cómo utilizar la pluma precargada, escaneando con su teléfono móvil (smartphone) el código QR incluido debajo o en el envase exterior. También puede acceder a esta información en la siguiente dirección de internet: hukyndrapatients.com
Incluir código QR
- Instrucciones de uso
INSTRUCCIONES DE USO
Hukyndra (adalimumab) pluma precargada
Solución inyectable de 40mg/0,4ml, para uso subcutáneo
Lea atentamente estas instrucciones de uso antes de usar Hukyndra pluma precargada de un solo uso
Antes de inyectar
Su profesional sanitario debe mostrarle cómo usar Hukyndra pluma precargada de un solo uso antes de usarla por primera vez.
Si usted ha utilizado anteriormente otra pluma de adalimumab, esta pluma funciona de manera diferente a otras plumas comercializadas en el mercado. Por favor, lea estas instrucciones de uso completamente para que entienda cómo utilizar correctamente la pluma precargada Hukyndra antes de inyectarse.
Información importante
Noutilice la pluma y llame a su profesional sanitario o farmacéutico si
- El líquido está turbio, decolorado o tiene escamas o partículas en él.
- La fecha de caducidad ha vencido.
- La pluma se ha dejado a la luz solar directa.
- La pluma se ha caído o aplastado.
Mantenga la tapa transparente puesta hasta justo antes de la inyección. Mantenga la pluma precargada de un solo uso Hukyndra fuera del alcance de los niños.
Lea las instrucciones de todas las páginas antes de usar la pluma precargada de un solo uso Hukyndra.
Consulte la sección "Información de almacenamiento" al final de estas instrucciones sobre cómo almacenar la pluma precargada de un solo uso Hukyndra.
Hukyndra pluma precargada
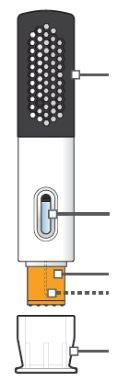
¿Cómo debo almacenar la pluma precargada de un solo uso Hukyndra?
Guarde la pluma precargada de un solo uso Hukyndra en la caja original dentro de la nevera entre 2 °C y 8 °C. Si es necesario, por ejemplo, cuando viaje, también puede almacenar la pluma precargada Hukyndra entre 20 °C y 25 °C durante un tiempo de hasta 30días.
Consulte la sección "Información de almacenamiento" al final de estas instrucciones para mayor detalle.
PASO 1: Saque la pluma precargada Hukyndra de la nevera y déjela entre 20°C y 25°C durante 15 a 30 minutos antes de inyectarse
Paso 1a.Saque la pluma precargada Hukyndra de la nevera (ver Figura A).
Paso 1b.Deje la pluma precargada Hukyndra entre 20 °C y 25 °C durante 15 a 30 minutos antes de inyectarse (ver Figura B).
- Noretire la tapa transparente mientras deja que la pluma precargada Hukyndra alcance entre 20 °C y 25 °C.
- Nocaliente la pluma precargada Hukyndra de ninguna otra manera. Por ejemplo, nola caliente en un microondas o con agua caliente.
- Noutilice la pluma precargada si el líquido se ha congelado (incluso si se ha descongelado).
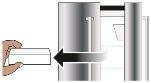
Figura A
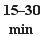

Figura B
PASO 2: Compruebe la fecha de caducidad, recopile los dispositivos y lávese las manos
Paso 2a.Compruebe la fecha de caducidad en la etiqueta de la pluma precargada Hukyndra (consulte la Figura C).
Noutilice la pluma precargada Hukyndra si la fecha de caducidad ha vencido.
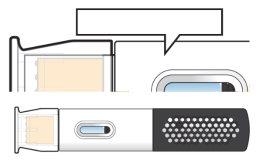
Figura C
Paso 2b.Coloque lo siguiente sobre una superficie limpia y plana (consulte la Figura D):
- 1 pluma precargada Hukyndra y toallita impregnada en alcohol.
- 1 bola de algodón o gasa (no incluida).
- Contenedor de eliminación de objetos punzantes resistentes a la punción (no incluido). Consulte el paso 9 al final de estas instrucciones de uso sobre cómo tirar (deshacerse de) su pluma precargada Hukyndra.
Paso 2c.Lávese y séquese las manos (ver Figura E).
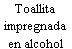
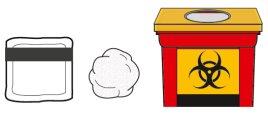
Figura D
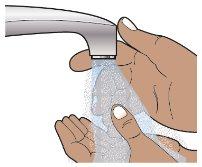
Figura E
PASO 3: Elegir y limpiar el lugar de inyección
Paso 3a.Elija un lugar de inyección (véase la Figura F):
- En la parte delantera de los muslos o,
- En la barriga (abdomen) al menos a 5 cm de distancia del ombligo.
- Al menos a 3 cm de distancia de su último lugar de inyección.
Paso 3b.Limpie el lugar de inyección con un movimiento circular utilizando la toallita impregnada en alcohol (ver Figura G).
Nose inyecte a través de la ropa.
Nose inyecte en la piel dolorida, magullada, roja, dura, cicatrizada, con estrías o áreas con placas de psoriasis.
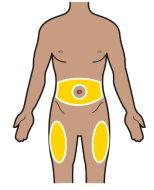
Figura F
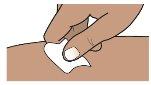
Figura G
PASO 4: Compruebe el medicamento en la ventana de inspección
Paso 4a.Sostenga la pluma precargada Hukyndra con el área de sujeción del mango gris hacia arriba. Revise la ventana de inspección (véase la figura H).
- Es normal ver 1 o más burbujas en la ventana.
- Asegúrese de que el líquido esté transparente e incoloro.
Noutilice la pluma precargada Hukyndra si el líquido está turbio o tiene partículas.
Noutilice la pluma precargada Hukyndra si se ha caído o aplastado.
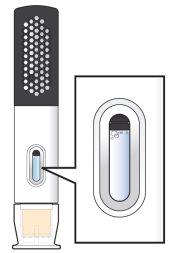
Figura H
PASO 5: Retire la tapa transparente
Paso 5a.Tire de la tapa transparente (ver Figura I).
Es normal ver salir de la aguja algunas gotas de líquido.
Paso 5b.Deseche la tapa transparente.
Novuelva a poner la tapa transparente en la pluma. Esto puede dañar la aguja. La pluma está lista para usarse después de que se haya quitado la tapa transparente.
Paso 5c.Gire la pluma precargada Hukyndra para que la cubierta naranja de la aguja apunte hacia el lugar de inyección.
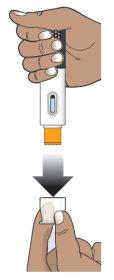
Figura I
PASO 6: Pellizque la piel y coloque la pluma precargada Hukyndra sobre el lugar de inyección
Paso 6a.Apriete la piel para hacer un área elevada en el lugar de inyección y sosténgala firmemente.
Paso 6b.Coloque la cubierta naranja de la aguja recta (ángulo de 90°) contra el lugar de inyección (ver Figura J).
Sujete la pluma de forma que pueda ver la ventana de inspección.
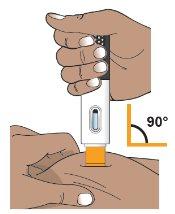
Figura J
PASO 7: Administrar inyección
Paso 7a.Empuje y siga empujando la pluma hacia abajo contra el lugar de inyección (consulte la Figura K).
- El primer 'clic' marcará el inicio de la inyección (véase la figura K). Puede tardar en completarse hasta 10 segundos después del primer 'clic'.
- Siga empujando la pluma hacia abajo contra el lugar de inyección.
- La inyección se completa cuando el indicador naranja ha dejado de moverse y puede oír un segundo 'clic' (consulte la figura L).
Nolevante ni quite la presión del lugar de inyección hasta que haya confirmado que la inyección se ha completado.

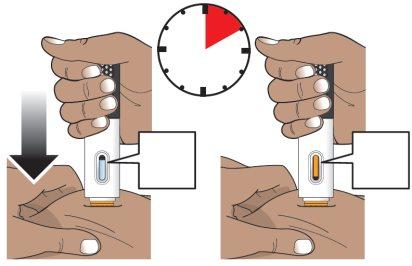
Figura K Figura L
PASO 8: Retirar la pluma precargada Hukyndra de la piel y cuidado de la piel
Paso 8a.Cuando se complete la inyección, retire lentamente la pluma precargada Hukyndra de la piel. La cubierta naranja de la aguja cubrirá la punta de la aguja (ver Figura M).
Si hay más de unas gotas de líquido en el lugar de la inyección, póngase en contacto con su profesional sanitario para obtener ayuda.
Paso 8b.Después de completar la inyección, coloque una bola de algodón o una gasa sobre la piel en el lugar de inyección.
Nofrote.
El sangrado leve en el lugar de la inyección es normal.
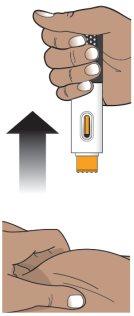
Figura M
PASO 9: ¿Cómo debo deshacerme de la pluma precargada Hukyndra usada?
Paso 9a.Coloque sus agujas, plumas y objetos punzantes usados en un recipiente de eliminación de objetos punzantes de inmediato después de su uso (consulte la Figura N).
No tire (deseche) la pluma en la basura del hogar.
Paso 9b.Las tapas transparentes, la toallita impregnada en alcohol, la bola de algodón o la gasa y el envase pueden tirarse en la basura de su hogar.
Si no tiene un recipiente de eliminación de objetos punzantes, puede utilizar un recipiente doméstico que sea:
- hecho de un plástico resistente,
- se puede cerrar con una tapa ajustada y resistente a la perforación, sin que los objetos punzantes puedan salir,
- vertical y estable durante el uso,
- resistente a fugas y
- debidamente etiquetado para advertir de residuos peligrosos dentro del contenedor.
Cuando su contenedor de eliminación de objetos punzantes esté casi lleno, deberá seguir las directrices locales sobre la forma correcta de deshacerse de su contenedor de eliminación de objetos punzantes.
Nodeseche su recipiente de eliminación de objetos punzantes usados en la basura de su hogar.
Norecicle el recipiente de eliminación de objetos punzantes usados.
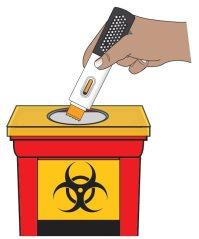
Figura N
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a HUKYNDRA 40 MG SOLUCION INYECTABLE EN PLUMA PRECARGADAForma farmacéutica: INYECTABLE, 20 mgPrincipio activo: AdalimumabFabricante: Amgen Europe B.V.Requiere recetaForma farmacéutica: INYECTABLE, 20 mgPrincipio activo: AdalimumabFabricante: Amgen Europe B.V.Requiere recetaForma farmacéutica: INYECTABLE, 40 mgPrincipio activo: AdalimumabFabricante: Amgen Europe B.V.Requiere receta
Médicos online para HUKYNDRA 40 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de HUKYNDRA 40 MG SOLUCION INYECTABLE EN PLUMA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes







