
FULVESTRANT VISO FARMACEUTICA 250 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA EFG


Cómo usar FULVESTRANT VISO FARMACEUTICA 250 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA EFG
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
- Introducción
- Qué es Fulvestrant Viso Farmacéutica y para qué se utiliza
- Qué necesita saber antes de empezar a usar Fulvestrant Viso Farmacéutica
- Cómo usar Fulvestrant Viso Farmacéutica
- Posibles efectos adversos
- Conservación de Fulvestrant Viso Farmacéutica
- Contenido del envase e información adicional
Introducción
Prospecto: información para el paciente
Fulvestrant Viso Farmacéutica 250 mg solución inyectable en jeringa precargada EFG
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento,porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Fulvestrant Viso Farmacéutica y para qué se utiliza
- Qué necesita saber antes de empezar usar Fulvestrant Viso Farmacéutica
- Cómo usar Fulvestrant Viso Farmacéutica
- Posibles efectos adversos
- Conservación de Fulvestrant Viso Farmacéutica
- Contenido del envase e información adicional
1. Qué es Fulvestrant Viso Farmacéutica y para qué se utiliza
Este medicamento contiene el principio activo fulvestrant, que pertenece al grupo de bloqueantes de estrógeno.
Los estrógenos, un tipo de hormonas sexuales femeninas, pueden estar en algunos casos implicados en el desarrollo del cáncer de mama.
Fulvestrant se utiliza:
- en monoterapia, para el tratamiento de mujeres posmenopáusicas con un tipo de cáncer de mama llamado cáncer de mama con receptor estrogénico positivo, que es localmente avanzado o que se ha extendido a otras partes del cuerpo (metastásico), o
- en combinación con palbociclib para tratar a mujeres con un tipo de cáncer de mama llamado cáncer de mama con receptor hormonal positivo y cáncer de mama con receptor 2 del factor de crecimiento epidérmico humano negativo, que está localmente avanzado o que se ha extendido a otras partes del cuerpo (metastásico). Las mujeres que no hayan llegado a la menopausia también serán tratadas con un medicamento llamado agonista de la hormona liberadora de la hormona luteinizante (LHRH).
Cuando Fulvestrant se administre en combinación con palbociclib, es importante que usted también lea el prospecto de palbociclib. Si tiene cualquier duda sobre palbociclib, consulte a su médico.
2. Qué necesita saber antes de empezar a usar Fulvestrant Viso Farmacéutica
No useFulvestrant Viso Farmacéutica:
- si es alérgico a fulvestrant o a alguno de los demás componentes de este medicamento (incluidos en la sección 6),
- si está embarazada o en periodo de lactancia,
- si presenta problemas graves de hígado.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Fulvestrant Viso Farmacéutica si algo de esto le aplica:
- problemas de riñón o hígado,
- recuento bajo de plaquetas (que ayudan a la coagulación de la sangre) o alteraciones hemorrágicas,
- problemas previos de coágulos sanguíneos,
- osteoporosis (pérdida de densidad ósea),
- alcoholismo.
Niños y adolescentes
Fulvestrant no está indicado en niños y adolescentes menores de 18 años.
Otros medicamentos yFulvestrant Viso Farmacéutica
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento.
En particular, debe informar a su médico si está utilizando anticoagulantes (medicamentos para prevenir los coágulos sanguíneos).
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
No debe utilizar este medicamento si está embarazada. Si se puede quedar embarazada, debe utilizar un método anticonceptivo eficaz mientras esté en tratamiento con este medicamento y durante dos años después de la última dosis.
No debe dar el pecho mientras esté en tratamiento con Fulvestrant Viso Farmacéutica.
Conducción y uso de máquinas
No se espera que este medicamento afecte a su capacidad para conducir o utilizar máquinas. Sin embargo, si se siente cansada después del tratamiento no conduzca ni utilice máquinas.
Uso en deportistas
Este medicamento contiene fulvestrant que puede producir un resultado positivo en las pruebas de control de dopaje.
Fulvestrant Viso Farmacéuticacontiene etanol
Este medicamento contiene 500 mg de alcohol (etanol) en cada jeringa que equivale a 100 mg/ml (10 % m/v). La cantidad en cada jeringa de este medicamento es equivalente a menos de 13 ml de cerveza o 5 ml de vino.
Es poco probable que la cantidad de alcohol que contiene este medicamento tenga algún efecto perceptible en adultos o adolescentes. Podría tener algunos efectos en niños pequeños, como por ejemplo somnolencia.
La cantidad de alcohol contenida en este medicamento puede alterar el efecto de otros medicamentos. Consulte con su médico o farmacéutico si está tomando otros medicamentos.
Si está embarazada o en periodo de lactancia, consulte con su médico o farmacéutico antes de usar este medicamento.
Si tiene adicción al alcohol, consulte con su médico o farmacéutico antes de usar este medicamento.
Fulvestrant Viso Farmacéutica contiene alcohol bencílico
Este medicamento contiene 500 mg de alcohol bencílico en cada jeringa precargada equivalente a 100 mg / ml (10 % m/v). El alcohol bencílico puede provocar reacciones alérgicas.
Consulte a su médico o farmacéutico si está embarazada o en periodo de lactancia. Esto es debido a que se pueden acumular grandes cantidades de alcohol bencílico en su organismo y provocar efectos adversos (acidosis metabólica).
Consulte a su médico o farmacéutico si tiene enfermedades de hígado o riñón. Esto es debido a que se pueden acumular en el organismo grandes cantidades de alcohol bencílico y provocar efectos adversos (acidosis metabólica).
Fulvestrant Viso Farmacéutica contiene benzoato de bencilo
Este medicamento contiene 750 mg de benzoato de bencilo por inyección equivalente a 150 mg/ml.
3. Cómo usar Fulvestrant Viso Farmacéutica
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada es de 500 mg de fulvestrant (dos inyecciones de 250 mg/5ml) administrada una vez al mes con una dosis adicional de 500 mg administrada 2 semanas después de la dosis inicial.
Su médico o enfermero le administrará Fulvestrant Viso Farmacéutica mediante una inyección intramuscular lenta en cada uno de sus glúteos.
En caso de sobredosis o ingestión accidental, consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20, indicando el medicamento y la cantidad ingerida.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Puede necesitar tratamiento médico urgente si experimenta alguno de los siguientes efectos adversos:
- reacciones alérgicas (hipersensibilidad), incluyendo hinchazón de la cara, labios, lengua y/o garganta, que pueden ser síntomas de reacciones anafilácticas,
- tromboembolismo (aumento del riesgo de coágulos sanguíneos)*,
- inflamación del hígado (hepatitis),
- fallo hepático.
Informe inmediatamente a su médico, farmacéutico o enfermero si nota alguno de los siguientes efectos adversos:
Efectos adversos muy frecuentes(puede afectar a más de 1 de cada 10 pacientes)
- reacciones en el lugar de la inyección, como dolor y/o inflamación,
- niveles anómalos de enzimas hepáticos (en análisis de sangre)*,
- náuseas (sensación de malestar),
- debilidad, cansancio*,
- dolor articular y musculoesquelético,
- sofocos,
- erupción cutánea,
- reacciones alérgicas (hipersensibilidad), incluyendo hinchazón de la cara, labios, lengua y/o garganta.
Todos los efectos adversos restantes:
Efectos adversos frecuentes(puede afectar hasta a 1 de cada 10 pacientes)
- dolor de cabeza,
- vómitos, diarrea o pérdida del apetito*,
- infecciones del tracto urinario,
- dolor de espalda*,
- aumento de bilirrubina (un pigmento de la bilis producido por el hígado),
- tromboembolismo (aumento del riesgo de coágulos sanguíneos)*,
- niveles disminuidos de plaquetas (trombocitopenia),
- hemorragia vaginal,
- dolor lumbar que se refleja en un lado de la pierna (ciática),
- debilidad repentina, entumecimiento, hormigueo o pérdida de movimiento en su pierna, especialmente en un solo lado del cuerpo, problemas repentinos para caminar o de equilibrio (neuropatía periférica).
Efectos adversos poco frecuentes(puede afectar hasta a 1 de cada 100 pacientes)
- flujo vaginal espeso, blanquecino y candidiasis (infección),
- hematoma y hemorragia en el lugar de la inyección,
- aumento de gamma-GT, un enzima hepático que se identifica en un análisis de sangre,
- inflamación del hígado (hepatitis),
- fallo hepático,
- entumecimiento, hormigueo y dolor,
- reacciones anafilácticas.
- Incluye efectos adversos para los cuales no se puede evaluar el papel exacto de fulvestrant debido a la enfermedad subyacente.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Fulvestrant Viso Farmacéutica
Este medicamento no requiere condiciones especiales de conservación.
Conservar la jeringa precargada en el embalaje original para protegerla de la luz.
Su profesional sanitario será el responsable de la conservación, uso y eliminación correctos de Fulvestrant Viso farmacéutica.
Este medicamento puede presentar un riesgo para el medio acuático. Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Fulvestrant Viso Farmacéutica
- El principio activo es fulvestrant. Cada jeringa precargada (5 ml) contiene 250 mg de fulvestrant.
- Los demás componentes son etanol (96%), alcohol bencílico (E1519), benzoato de bencilo y aceite de ricino refinado.
Aspecto del producto y contenido del envase
Fulvestrant Viso farmacéutica es una solución viscosa, transparente, de incolora a amarilla en una jeringa precargada que contiene 5 ml de solución inyectable. Deben administrarse dos jeringas para recibir la dosis mensual recomendada de 500 mg..
Fulvestrant Viso farmacéutica presenta 3 formatos de envase, un envase que contiene 1 jeringa precargada de vidrio, un envase que contiene 2 jeringas precargadas de vidrio y un envase que contiene 6 jeringas precargadas de vidrio. Se proporcionan además una, dos o seis agujas de seguridad (BD SafetyGlide) para su conexión al cuerpo de cada jeringa.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización:
Glenmark Arzneimittel GmbH
Industriestr. 31
82194 Gröbenzell
Alemania
Responsable de la fabricación:
Laboratorios Farmalán, S.A.
C/ La Vallina s/n, Edificio 2
Polígono Industrial Navatejera
24193, Villaquilambre, León
España
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Glenmark Farmacéutica, S.L.U.
C/ Retama 7, 7ª planta
28045 Madrid
España
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Holanda: Fulvestrant Glenmark 250 mg oplossing voor injectie in een voorgevulde spuit
Alemania: Fulvestrant Glenmark 250 mg Injektionslösung in einer Fertigspritze
Dinamarca: Fulvestrant Glenmark
España: Fulvestrant Viso Farmacéutica 250 mg solución inyectable en jeringa precargada EFG
Noruega: Fulvestrant Glenmark
Suecia: Fulvestrant Glenmark
Reino Unido: Fulvestrant 250 mg solution for injection in pre-filled syringe |
Fecha de la última revisión de este prospecto: abril 2025
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/)
---------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Fulvestrant Viso Farmacéutica 500 mg (2 x 250 mg/5 ml solución inyectable) se debe administrar usando dos jeringas precargadas. Ver sección 3.
Instrucciones de administración
Advertencia – No esterilizar en autoclave la aguja de seguridad (aguja hipodérmica de seguridad BD SafetyglideTM) antes de su uso. Las manos deben permanecer por detrás de la aguja en todo momento durante su uso y eliminación.
Para cada una de las dos jeringas:
-Retire el cilindro de vidrio de la jeringa de la bandeja y verifique que no esté dañado.
-Despegue el embalaje exterior de la aguja de seguridad (SafetyGlide).
-Las soluciones parenterales deben inspeccionarse visualmente para detectar partículas y decoloración antes de su administración.
-Sostenga la jeringa en posición vertical sobre la parte acanalada (C). Con la otra mano, agarre el tapón (A) y gire con cuidado el tapón de punta rígida de plástico en sentido antihorario. (ver figura 1):
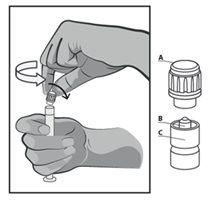
Figura 1
-Retire la tapa de la punta rígida de plástico (A) en dirección recta hacia arriba. Para mantener la esterilidad, no toque la punta de la jeringa (B) (ver figura 2)
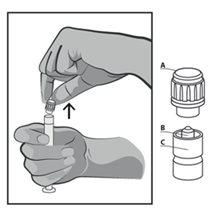
Figura 2
Conecte la aguja de seguridad al Luer-Lok y gírela hasta que quede firmemente asentada (ver figura 3).
- Compruebe que la aguja esté bloqueada en el conector Luer antes de salir del plano vertical.
- Extraiga el protector de la aguja para evitar dañar la punta de la aguja.
- Lleve la jeringa llena hasta el punto de administración.
- Retire la funda de la aguja.
- Expulsar el exceso de gas de la jeringa.
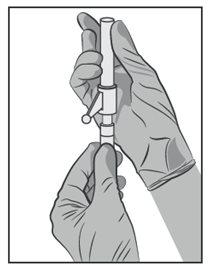
Figura 3
- Administrar por vía intramuscular lentamente (1-2 minutos /inyección) en la nalga (zona de los glúteos). Para comodidad del usuario, la posición de bisel de la aguja está orientada hacia el brazo de palanca (ver figura 4).
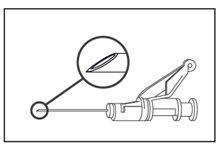
Figura 4
Tras la inyección, dé inmediatamente un toque con el dedo en el brazo de la palanca para activar el mecanismo de seguridad (ver Figura 5).
NOTA: Actívelo alejado de su cuerpo y de los demás. Escuche el clic y confirme visualmente que la punta de la aguja está totalmente protegida.
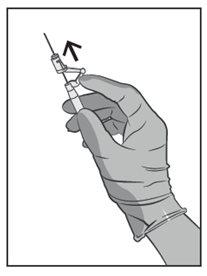
Figura 5
Disposición
Las jeringas precargadas son para un solo uso.
Este medicamento puede suponer un riesgo para el medio acuático. Cualquier medicamento no utilizado o material de desecho debe eliminarse de acuerdo con los requisitos locales.
- País de registro
- Precio medio en farmacia225.7 EUR
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a FULVESTRANT VISO FARMACEUTICA 250 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA EFGForma farmacéutica: INYECTABLE, 250 mg/5 mlPrincipio activo: FulvestrantFabricante: Bexal Farmaceutica S.A.Requiere recetaForma farmacéutica: INYECTABLE, 250 mgPrincipio activo: FulvestrantFabricante: Ever Valinject GmbhRequiere recetaForma farmacéutica: INYECTABLE, 250 mgPrincipio activo: FulvestrantFabricante: Astrazeneca AbRequiere receta
Médicos online para FULVESTRANT VISO FARMACEUTICA 250 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA EFG
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de FULVESTRANT VISO FARMACEUTICA 250 MG SOLUCION INYECTABLE EN JERINGA PRECARGADA EFG, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes













