FLUARIX TETRA SUSPENSION INYECTABLE EN JERINGA PRECARGADA

Cómo usar FLUARIX TETRA SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Fluarix Tetra suspensión inyectable en jeringa precargada
Vacuna antigripal (de virus fraccionados e inactivados)
Este prospecto se ha escrito asumiendo que la persona que va a recibir la vacuna es quien lo va a leer. Sin embargo, la vacuna se puede administrar a adolescentes y niños, de modo que puede que lo esté leyendo para su hijo.
Lea todo el prospecto detenidamente antes de que usted o su hijo reciba esta vacuna,porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Esta vacuna se le ha recetado solamente a usted o a su hijo, y no debe dársela a otras personas.
- Si usted o su hijo experimenta efectos adversos, consulte a su médico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
- Qué es Fluarix Tetra y para qué se utiliza
- Qué necesita saber antes de recibir Fluarix Tetra
- Cómo se administra Fluarix Tetra
- Posibles efectos adversos
5Conservación de Fluarix Tetra
- Contenido del envase e información adicional
1. Qué es Fluarix Tetra y para qué se utiliza
Fluarix Tetra es una vacuna que le ayuda a protegerse frente a la gripe, especialmente en personas con elevado riesgo de complicaciones asociadas. El uso de Fluarix Tetra debe basarse en las recomendaciones oficiales.
Cuando se administra Fluarix Tetra a una persona, su sistema inmunitario (el sistema de defensa natural del organismo), producirá su propia protección (anticuerpos) frente a la enfermedad. Ninguno de los componentes de la vacuna puede provocar la gripe.
La gripe es una enfermedad que se propaga rápidamente y está causada por diferentes tipos de cepas que pueden cambiar cada año. Por tanto, ésta es la razón por la que puede que necesite vacunarse anualmente. El periodo con mayor riesgo de contraer la gripe es durante los meses fríos, entre octubre y marzo. Si no se vacunó en otoño, es recomendable que lo haga antes de primavera, puesto que hasta entonces corre el riesgo de contagiarse. Su médico le recomendará el mejor momento para vacunarse.
Fluarix Tetra le protegerá frente a las cuatro cepas del virus a partir de, aproximadamente, las 2 o 3 semanas después de la inyección.
El periodo de incubación de la gripe es de unos pocos días, de modo que, si se expone a la gripe inmediatamente antes o después de vacunarse, aún puede desarrollar la enfermedad.
La vacuna no le protegerá frente al resfriado común, aunque algunos de los síntomas sean parecidos a los de la gripe.
2. Qué necesita saber antes de recibir Fluarix Tetra
Para asegurarse de que Fluarix Tetra es apropiado para usted, es importante que informe a su médico o farmacéutico si cualquiera de los puntos que se tratan a continuación le afecta. Si hay algo que no entiende, pida a su médico o farmacéutico que se lo explique.
No use Fluarix Tetra
- Si es alérgico a los principios activos o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6) o a cualquier componente que pueda estar presente en cantidades muy pequeñas tales como huevos (ovoalbúmina o proteínas de pollo), formaldehído, sulfato de gentamicina o desoxicolato de sodio.
- Si padece cualquier enfermedad acompañada de fiebre elevada o una infección aguda, se deberá retrasar la vacunación hasta que se haya recuperado.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de recibir Fluarix Tetra:
- si tiene una respuesta inmunitaria débil (debido a una inmunodeficiencia o a medicamentos que afecten al sistema inmunitario)
- si, por cualquier razón, se le va a practicar un análisis de sangre pocos días después de la vacunación antigripal. Esto es debido a que se han observado resultados falsos positivos en los análisis de sangre de algunos pacientes que habían sido recientemente vacunados
- si tiene un problema de coagulación o le aparecen moratones con facilidad.
Su médico decidirá si debe recibir la vacuna.
Antes o después de cualquier inyección, podría producirse un desmayo (especialmente en los adolescentes), por lo que debe informar a su médico o enfermero si se ha desmayado en anteriores ocasiones tras la administración de una inyección.
Al igual que todas las vacunas, puede que Fluarix Tetra no proteja completamente a todas las personas vacunadas.
Uso deFluarix Tetra con otros medicamentos
Comunique a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento.
Fluarix Tetra puede administrarse al mismo tiempo que otras vacunas si se inyectan en diferentes extremidades.
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Su médico o farmacéutico podrá decidir si debe recibir Fluarix Tetra. Pida consejo a su médico o farmacéutico antes de tomar cualquier medicamento.
Conducción y uso de máquinas
La influencia de Fluarix Tetra sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Fluarix Tetra contiene sodio
Este medicamento contiene menos de 23 mg de sodio (1 mmol) por dosis; esto es, esencialmente "exento de sodio".
Fluarix Tetra contiene potasio
Este medicamento contiene menos de 39 mg (l mmol) de potasio por dosis, por lo que se considera esencialmente "exento de potasio".
3. Cómo se administra Fluarix Tetra
Dosis
Los adultos recibirán una dosis de 0,5 ml.
Uso en niños:
Los niños de 6 meses en adelante recibirán una dosis de 0,5 ml.
Si su hijo es menor de 9 años y no ha sido vacunado previamente frente a la gripe, se le debe administrar una segunda dosis después de un intervalo de al menos 4 semanas.
Forma y/o vía de administración
Su médico le administrará la dosis recomendada de la vacuna mediante una inyección en el músculo.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, esta vacuna puede producir efectos adversos, aunque no todas las personas los sufran.
Los siguientes efectos adversos se han observado durante los ensayos clínicos:
Efectos adversos ocurridos en niños entre 6 y 36 meses de edad
Muy frecuentes(pueden ocurrir con más de 1 de cada 10 dosis de la vacuna): pérdida de apetito, irritabilidad, somnolencia, dolor y/o enrojecimiento en el lugar de la inyección.
Frecuentes(pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna): fiebre, hinchazón en el lugar de la inyección.
Efectos adversos ocurridos en niños entre 3 y 6 años de edad
Muy frecuentes(pueden ocurrir con más de 1 de cada 10 dosis de la vacuna): dolor y/o enrojecimiento y/o hinchazón en el lugar de la inyección, irritabilidad.
Frecuentes(pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna): pérdida de apetito, somnolencia, fiebre.
Poco frecuentes(pueden ocurrir hasta con 1 de cada 100 dosis de la vacuna): erupción en la piel, picor en el lugar de la inyección.
Efectos adversos ocurridos en niños entre 6 y 18 años de edad
Muy frecuentes(pueden ocurrir con más de 1 de cada 10 dosis de la vacuna): dolor muscular, dolor y/o enrojecimiento y/o hinchazón en el lugar de la inyección, cansancio.
Frecuentes(pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna): náuseas, diarrea, vómitos, dolor de estómago, dolor de cabeza, dolor de las articulaciones, escalofríos, fiebre.
Poco frecuentes(pueden ocurrir hasta con 1 de cada 100 dosis de la vacuna): erupción en la piel, picor en el lugar de la inyección.
Efectos adversos ocurridos en adultos ≥18 años de edad
Muy frecuentes(pueden ocurrir con más de 1 de cada 10 dosis de la vacuna): dolor en el lugar de la inyección, cansancio, dolor muscular (mialgia).
Frecuentes(pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna): dolor de cabeza, náuseas, diarrea, vómitos, dolor de estómago, dolor de las articulaciones (artralgia), fiebre, escalofríos, enrojecimiento y/o hinchazón en el lugar de la inyección.
Poco frecuentes(pueden ocurrir hasta con 1 de cada 100 dosis de la vacuna): cardenales (hematomas), picor (prurito) alrededor del área donde se inyecta la vacuna, mareo.
Además, los efectos adversos ocurridos durante los estudios en sujetos a partir de los 3 años de edad con Fluarix (vacuna antigripal trivalente) fueron:
Frecuentes(pueden ocurrir hasta con 1 de cada 10 dosis de la vacuna): endurecimiento (induración) alrededor del área donde se inyecta la vacuna, sudoración.
Estas reacciones desaparecen normalmente en 1-2 días sin tratamiento.
Además de los efectos adversos mencionados anteriormente, los siguientes efectos adversos ocurrieron durante el uso rutinario de Fluarix y/o Fluarix Tetra:
Raros(pueden ocurrir hasta con 1 de cada 1000 dosis de la vacuna):
- Reacciones alérgicas:
- conducen a una urgencia médica por un fallo del sistema circulatorio que impide que se proporcione un flujo sanguíneo adecuado a los diferentes órganos del cuerpo (shock),
- hinchazón, más evidente en la cabeza y el cuello, incluyendo la cara, labios, lengua, garganta o cualquier otra parte del cuerpo (angioedema).
- Reacciones cutáneas que pueden extenderse por el cuerpo, incluyendo picor de la piel (prurito, urticaria) y enrojecimiento (eritema) de la piel.
- Trastornos neurológicos que pueden ocasionar rigidez en el cuello, confusión, entumecimiento, dolor y debilidad en las extremidades, pérdida del equilibrio, pérdida de reflejos, parálisis parcial o total del cuerpo (encefalomielitis, neuritis, síndrome de Guillain-Barré).
- Hinchazón temporal de los ganglios del cuello, axilas o ingles (linfadenopatía transitoria).
- Síntomas parecidos a los de la gripe, malestar general.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano, www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Fluarix Tetra
Mantener esta vacuna fuera de la vista y del alcance de los niños.
No utilice esta vacuna después de la fecha de caducidad que aparece en el envase después de CAD. La fecha de caducidad es el último día del mes que se indica.
Conservar en nevera (entre 2 °C y 8 ºC).
No congelar.
Conservar en el embalaje exterior para protegerla de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Fluarix Tetra
Los principios activos son: virus de la gripe (fraccionados, inactivados) de las siguientes cepas*:
Cepa similar aA/Victoria/4897/2022(H1N1)pdm09:
(IVR-238) derivada deA/Victoria/4897/202215 microgramos de HA**
Cepa similar a A/Croatia/10136RV/2023(H3N2):
(X-425A) derivada deA/Croatia/10136RV/202315 microgramos de HA**
Cepa similar aB/Austria/1359417/2021:
(BVR-26) derivada de B/Austria/1359417/202115 microgramos de HA**
Cepa similar aB/Phuket/3073/2013:
(salvaje)derivada deB/Phuket/3073/201315 microgramos de HA**
por dosis de 0,5 ml
- propagados en huevos embrionados de gallina procedentes de grupos de pollos sanos
**hemaglutinina
Esta vacuna cumple con la recomendación de la Organización Mundial de la Salud (OMS) para el hemisferio Norte y con la recomendación de la Unión Europea para la campaña 2025/2026.
Los demás componentes son: cloruro de sodio, hidrógeno fosfato de sodio dodecahidrato, dihidrogenofosfato de potasio, cloruro de potasio, cloruro de magnesio hexahidrato, hidrógeno succinato de α-tocoferilo, polisorbato 80, octoxinol 10 y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Fluarix Tetra es una suspensión inyectable en jeringa precargada.
Fluarix Tetra está disponible en jeringa precargada de 1 dosis con o sin agujas separadas; tamaños de envase de 1 y 10.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Responsable de la fabricación
GlaxoSmithKline Biologicals NL der SmithKline Beecham Pharma GmbH & Co. KG
Zirkusstrasse 40
D-01069 Dresden
Alemania
Representante local
GlaxoSmithKline, S.A.
P.T.M. C/ Severo Ochoa, 2
28760 Tres Cantos (Madrid)
Tel.: +34 900 202 700
Este medicamento está autorizado en los Estados miembros del Espacio Económico Europeo con los siguientes nombres:
Estado miembro | Nombre |
Austria, Bulgaria, Chipre, Croacia, Dinamarca, Eslovaquia, Eslovenia, España, Estonia, Finlandia, Grecia, Hungría, Irlanda, Islandia, Italia, Letonia, Lituania, Malta, Noruega, Países Bajos, Polonia, Portugal, República Checa, Suecia | Fluarix Tetra |
Bélgica, Luxemburgo | Alpharix-Tetra |
Alemania | Influsplit Tetra |
Francia | FluarixTetra |
Fecha de la última revisión de este prospecto:07/2025
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/)
--------------------------------------------------------------------------------------------------------------------Esta información está destinada únicamente a profesionales del sector sanitario:
Al igual que con todas las vacunas inyectables, debe disponerse en todo momento del tratamiento y supervisión médica adecuados, para el caso de aparición de reacciones anafilácticas tras la administración de la vacuna.
La inmunización se debe realizar por inyección intramuscular.
En ningún caso se debe administrar Fluarix Tetra por vía intravascular.
Fluarix Tetra se puede administrar al mismo tiempo que otras vacunas. La inmunización se debe realizar en diferentes extremidades.
Permitir que la vacuna alcance la temperatura ambiente antes de su utilización.
Agitar antes de usar. Inspeccionar visualmente antes de la administración.
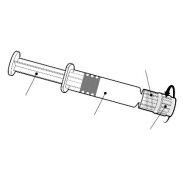
Instrucciones para la jeringa precargada
| Sostenga la jeringa por el cuerpo, no por el émbolo. Desenrosque el tapón de la jeringa girándola en sentido contrario a las agujas del reloj. |
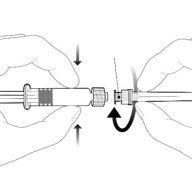
| Para insertar la aguja, conecte la base al adaptador luer-locky gírelo un cuarto de vuelta en el sentido de las agujas del reloj hasta que sienta que se bloquea. No saque el émbolo de la jeringa del cuerpo. Si esto ocurre, no administre la vacuna. |
Eliminación de residuos
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a FLUARIX TETRA SUSPENSION INYECTABLE EN JERINGA PRECARGADAForma farmacéutica: INYECTABLE, 3,75 microgramosPrincipio activo: influenza, inactivated, split virus or surface antigenFabricante: Glaxosmithkline BiologicalsRequiere recetaForma farmacéutica: INYECTABLE, 0,5 mlPrincipio activo: influenza, inactivated, split virus or surface antigenFabricante: Sanofi Winthrop IndustrieRequiere recetaForma farmacéutica: INYECTABLE, 60 microgramos de HAPrincipio activo: influenza, inactivated, split virus or surface antigenFabricante: Sanofi Winthrop IndustrieRequiere receta
Médicos online para FLUARIX TETRA SUSPENSION INYECTABLE EN JERINGA PRECARGADA
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de FLUARIX TETRA SUSPENSION INYECTABLE EN JERINGA PRECARGADA, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes