
DORZOLAMIDA/TIMOLOL STULLN PF 20 MG/ML + 5 MG/ML COLIRIO EN SOLUCION EN ENVASE UNIDOSIS


Cómo usar DORZOLAMIDA/TIMOLOL STULLN PF 20 MG/ML + 5 MG/ML COLIRIO EN SOLUCION EN ENVASE UNIDOSIS
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
- Introducción
- Qué es Dorzolamida/Timolol Stulln PF y para qué se utiliza
- Qué necesita saber antes de empezar a usar Dorzolamida/Timolol Stulln PF
- Cómo usar Dorzolamida/Timolol Stulln PF
- Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico. La posología apropiada y la duración del tratamiento serán establecidas por su médico.
- Posibles efectos adversos
- Conservación de Dorzolamida/Timolol Stulln PF
- Mantener este medicamento fuera de la vista y del alcance de los niños.
- Contenido del envase e información adicional
Introducción
Prospecto: información para el usuario
Dorzolamida/Timolol Stulln PF 20 mg/ml + 5 mg/ml colirio en solución en envase unidosis
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Dorzolamida/Timolol Stulln PF y para qué se utiliza
- Qué necesita saber antes de empezar a usar Dorzolamida/Timolol Stulln PF
- Cómo usar Dorzolamida/Timolol Stulln PF
- Posibles efectos adversos
- Conservación de Dorzolamida/Timolol Stulln PF
- Contenido del envase e información adicional
1. Qué es Dorzolamida/Timolol Stulln PF y para qué se utiliza
Dorzolamida/Timolol Stulln PF contiene dos medicamentos: dorzolamida y timolol.
- Dorzolamida pertenece a un grupo de medicamentos llamados "inhibidores de la anhidrasa carbónica".
- Timolol pertenece a un grupo de medicamentos llamados "betabloqueantes".
Estos medicamentos disminuyen la presión en el ojo de distintas maneras.
Este medicamento se prescribe para reducir la presión ocular elevada en el tratamiento del glaucoma cuando el uso de un solo colirio betabloqueante no sea adecuado.
2. Qué necesita saber antes de empezar a usar Dorzolamida/Timolol Stulln PF
No use Dorzolamida/Timolol Stulln PF
- si es alérgico a dorzolamida hidrocloruro, timolol maleato o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- si tiene ahora o ha tenido en el pasado problemas respiratorios, como asma o bronquitis obstructiva crónica grave (enfermedad del pulmón grave que puede causar pitidos, dificultad para respirar y/o tos persistente durante mucho tiempo).
- si tiene un latido cardiaco lento, insuficiencia cardiaca o alteraciones del ritmo cardiaco (latidos irregulares del corazón).
- si sufre enfermedad o trastornos del riñón graves, o tiene antecedentes de piedras en el riñón.
- si tiene exceso de acidez de la sangre causada por un acúmulo de cloruros en la sangre (acidosis hiperclorémica).
Si no está seguro si debe usar este medicamento, consulte a su médico o farmacéutico.
Advertencias y precauciones
Consulte a su médico antes de empezar a usar este medicamento si padece o ha padecido en el pasado:
- cardiopatía coronaria (los síntomas pueden incluir dolor torácico u opresión en el pecho, dificultad para respirar o ahogo), insuficiencia cardiaca, tensión arterial baja.
- alteraciones del ritmo cardiaco tales como enlentecimiento del latido cardiaco.
- problemas respiratorios, asma o enfermedad pulmonar obstructiva crónica.
- enfermedad por mala circulación de la sangre (tal como enfermedad de Raynaud o síndrome de Raynaud).
- diabetes, ya que el timolol puede enmascarar signos y síntomas de un descenso de azúcar en sangre.
- hiperactividad de la glándula tiroides, ya que el timolol puede enmascarar signos y síntomas.
Informe a su médico, antes de que tenga una intervención quirúrgica, que está usando este medicamento, ya que el timolol puede cambiar los efectos de algunos medicamentos usados durante la anestesia.
También informe a su médico sobre cualquier alergia o reacciones alérgicas incluyendo ronchas, hinchazón de la cara, labios, lengua y/o garganta que puede causar dificultad en la respiración o al tragar.
Informe a su médico si padece debilidad muscular o si le han diagnosticado miastenia grave.
Si desarrolla cualquier otra irritación ocular o problema nuevo en los ojos, como enrojecimiento de los ojos o hinchazón de los párpados, consulte inmediatamente a su médico.
Si sospecha que este medicamento le está causando una reacción alérgica o hipersensibilidad (por ejemplo, erupción cutánea, reacción cutánea grave o enrojecimiento y picor de ojos), deje de utilizar este medicamento y consulte inmediatamente a su médico.
Informe a su médico si se produce una infección ocular, si sufre una lesión en el ojo, si se somete a una intervención quirúrgica ocular o si desarrolla una reacción que incluya nuevos síntomas o empeoramiento de los existentes.
Cuando este medicamento se instila en el ojo puede afectar a todo el cuerpo.
Este medicamento no se ha estudiado en pacientes que usen lentes de contacto.
Si lleva lentes de contacto blandas, debe consultar con su médico antes de usar este medicamento.
Uso en niños
Se dispone de experiencia limitada con dorzolamida/timolol, colirio en solución (formulación con conservante) en lactantes y en niños.
Uso en pacientes de edad avanzada
En estudios con dorzolamida/timolol, colirio en solución (formulación con conservante), los efectos fueron semejantes tanto en los pacientes de edad avanzada como en los más jóvenes.
Uso en pacientes con deterioro hepático
Informe a su médico si sufre o ha sufrido problemas del hígado.
Uso en deportistas
Este medicamento contiene timolol que puede producir un resultado positivo en las pruebas de control de dopaje.
Uso deDorzolamida/Timolol StullnPF con otros medicamentos
Este medicamento puede afectar o ser afectado por otros medicamentos que esté usando, incluyendo otros colirios para el tratamiento del glaucoma. Informe a su médico si está usando o tiene intención de usar medicamentos para reducir la presión arterial, medicamentos para el corazón o medicamentos para tratar la diabetes. Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento. Esto es particularmente importante si está:
- tomando medicamentos para reducir la presión arterial o para tratar enfermedades cardíacas tales como bloqueadores de los canales de calcio, betabloqueantes o digoxina.
- tomando medicamentos para tratar una alteración o irregularidad del latido cardiaco tales como bloqueadores de los canales de calcio, betabloqueantes o digoxina.
- usando otro colirio que contiene betabloqueantes.
- tomando otro inhibidor de la anhidrasa carbónica tal como acetazolamida.
- tomando inhibidores de la monoamino oxidasa (IMAO).
- tomando un fármaco parasimpaticomimético que pudiera haber sido prescrito para ayudarle a orinar. Los parasimpaticomiméticos son también un tipo particular de medicamento que en algunas ocasiones se utiliza para ayudar a restaurar los movimientos normales a través del intestino.
- tomando narcóticos, tal como la morfina utilizada para tratar el dolor moderado a grave.
- tomando medicamentos para tratar la diabetes.
- tomando antidepresivos conocidos como fluoxetina y paroxetina.
- tomando una sulfamida.
- tomando quinidina (usada para tratar trastornos del corazón y algunos tipos de malaria).
Embarazo y lactancia
Consulte a su médico o farmacéutico antes de utilizar cualquier medicamento.
Embarazo
No use este medicamento si está embarazada, a no ser que su médico lo considere necesario.
Lactancia
No use este medicamento si está dando el pecho a su hijo. Timolol puede llegar a la leche materna. Pida a su médico consejo antes de tomar cualquier medicamento durante la lactancia.
Conducción y uso de máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir o utilizar máquinas. Hay efectos adversos asociados con este medicamento, tales como visión borrosa, que pueden afectar a su capacidad para conducir y/o manejar máquinas. No conducir o manejar máquinas hasta que se sienta bien o su visión sea clara.
3. Cómo usar Dorzolamida/Timolol Stulln PF
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico. La posología apropiada y la duración del tratamiento serán establecidas por su médico.
La dosis recomendada es de una gota en el ojo u ojos afectados por la mañana y por la noche.
Si está utilizando este medicamento al mismo tiempo que otro colirio, las gotas deben instilarse al menos con 10 minutos de diferencia.
No cambie la dosis del medicamento sin consultar a su médico.
Si tienen dificultad en la administración de las gotas, busque ayuda en un miembro de la familia o cuidador.
No deje que la punta del envase unidosis toque los ojos o las zonas que los rodean. Esto podría causar lesión en los ojos. Puede estar contaminada con bacterias capaces de causar infecciones oculares que originen graves daños en los ojos, e incluso la pérdida de la visión. Para evitar una posible contaminación del envase unidosis, lávese las manos antes de utilizar este medicamento y evite que la punta del envase entre en contacto con cualquier superficie. El envase unidosis debe abrirse inmediatamente antes de su uso. En caso de que su médico le haya indicado usar el colirio en ambos ojos, un envase unidosis contiene suficiente solución para ambos ojos.
Deseche el envase una vez abierto inmediatamente después de su uso con su contenido restante
Instrucciones de uso
- Lávase las manos.
- Abra el sobre de aluminio y extraiga una tira de envases unidosis.
- Separe un envase unidosis de la tira (Fig. 1).
- Abra el envase unidosis girando la punta. No toque la punta después de abrir el envase (Fig. 2).
- Incline la cabeza hacia atrás (Fig. 3).
- Tire del párpado inferior hacia abajo con el dedo y sostenga el envase unidosis con la otra mano. Apriete el envase para que caiga una gota en el ojo (Fig. 4).
- Cierre el ojo y presione con el dedo la esquina interna del ojo con su dedo durante aproximadamente dos minutos. Esto ayuda a evitar que el medicamento llegue al resto del cuerpo (Fig. 5). Si es necesario, repita los pasos 5 a 7 con su otro ojo.
- Deseche el envase unidosis después de su uso.
- Vuelva a colocar los envases unidosis restantes en el sobre y cierre el sobre doblando el borde. Coloque el sobre en la caja. Si quedan envases unidosis 3 meses después de abrir el sobre, deben desecharse adecuadamente y abrirse un nuevo sobre. Es importante continuar usando el colirio según lo prescrito por su médico.
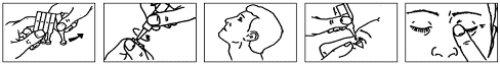
Fig. 1 Fig. 2 Fig. 3 Fig. 4 Fig. 5
Si usa másDorzolamida/Timolol StullnPF del que debe
Si se aplica demasiadas gotas en el ojo o traga algo del contenido del envase, entre otros efectos, puede sentir aturdimiento, tener dificultad para respirar o notar que el corazón le late más despacio. Contacte con su médico inmediatamente.
En caso de sobredosis o ingestión accidental consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20. Indicando el medicamento y la cantidad tomada.
Si olvidó usarDorzolamida/Timolol StullnPF
Es importante usar este medicamento como le ha prescrito su médico.
Si olvida aplicar una dosis, debe administrársela lo antes posible. Sin embargo, si es casi la hora de la siguiente dosis, no se administre la dosis olvidada y continúe con el programa de dosis previsto normalmente.
No utilice una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento conDorzolamida/Timolol StullnPF
Si quiere interrumpir el tratamiento con este medicamento, consulte primero con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Por lo general usted puede continuar usando las gotas, a menos que los efectos sean graves. Si está preocupado, consulte al médico o farmacéutico. No deje de usar este medicamento sin hablar con su médico.
Pueden ocurrir reacciones alérgicas generalizadas que incluyen hinchazón debajo de la piel en zonas como la cara y las extremidades, y pueden obstruir las vías respiratorias, pudiendo causar dificultad al tragar o al respirar, ronchas o erupción con picor, erupción generalizada y localizada, picazón, reacción alérgica grave repentina que puede llegar a ser mortal.
Las siguientes reacciones adversas se han notificado con dorzolamida/timolol, colirio en solución (formulación sin conservante) o con uno de sus componentes durante los ensayos clínicos o durante la experiencia tras la comercialización:
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas)
Quemazón y escozor en los ojos, alteración del sabor.
Frecuentes(pueden afectar hasta 1 de cada 10 personas)
Enrojecimiento en y alrededor del ojo(s), lagrimeo o picor en el ojo(s), erosión de la córnea (daño en la capa delantera del globo ocular), inflamación y/o irritación en y alrededor del ojo(s), sensación de cuerpo extraño en el ojo (sensación de que tienen algo en el ojo), disminución de la sensibilidad de la córnea (no aprecia que tiene algo en el ojo y no siente dolor), dolor en el ojo, ojos secos, visión borrosa, dolor de cabeza, sinusitis (sensación de tensión o congestión en la nariz), náuseas, debilidad/cansancio y fatiga.
Poco frecuentes(pueden afectar hasta 1 de cada 100 personas)
Mareos, depresión, inflamación del iris, alteraciones de la visión incluyendo las modificaciones de la refracción (en algunos casos debido a la supresión de la terapia miótica), disminución de los latidos cardiacos, desfallecimiento, dificultad en la respiración (disnea), indigestión, piedras en el riñón (a menudo marcado por un inicio repentino de dolor insoportable y calambres en la parte baja de la espalda y / o en los costados, la ingle o el abdomen).
Raros(pueden afectar hasta 1 de cada 1.000 personas)
Lupus eritematoso sistémico (una enfermedad inmune que puede causar una inflamación de los órganos internos), hormigueo o entumecimiento de las manos o los pies, insomnio, pesadillas, pérdida de memoria, incremento en los signos y síntomas de mistenia gravis (trastorno muscular), disminución del deseo sexual, accidente cerebro vascular, miopía transitoria que remite al cesar la terapia, desprendimiento de la capa de debajo de la retina que contiene vasos sanguíneos después de la cirugía de filtración que puede causar alteraciones visuales, párpado caído (haciendo que el ojo permanezca medio cerrado), visión doble, costras en el párpado, hinchazón de la córnea (con síntomas de alteraciones visuales), presión baja en el ojo, sonidos de campanilleo en el oído, presión arterial baja, cambios en el ritmo o velocidad con la que late el corazón, insuficiencia cardiaca congestiva (enfermedad del corazón con respiración entrecortada e hinchazón de pies y piernas debido a la acumulación de líquidos), edema (acumulación de líquidos), isquemia cerebral (llegada reducida de sangre al cerebro), dolor del pecho, latidos cardíacos fuertes que pueden ser rápidos o irregulares (palpitaciones), ataque cardiaco, fenómeno de Raynaud, manos y pies hinchados o fríos y disminución de la circulación en sus brazos y piernas, calambres en las piernas y/o dolor de pierna cuando se camina (claudicación), dificultad para respirar, insuficiencia respiratoria, rinitis, sangrado de nariz, constricción de las vías respiratorias en los pulmones, tos, irritación de la garganta, boca seca, diarrea, dermatitis de contacto, pérdida de pelo, erupción cutánea con apariencia de color blanco plateado (erupción psoriasiforme), enfermedad de Peyronie (que puede causar un encorvamiento del pene), reacciones de tipo alérgico tales como erupción cutánea, ronchas, picor, en raros casos posible hinchazón de los labios, ojos y boca, sibilancias, o reacciones cutáneas graves (síndrome de Stevens Johnson, necrólisis epidérmica tóxica).
Al igual que otros medicamentos aplicados en los ojos, timolol se absorbe en la sangre. Esto puede causar efectos secundarios similares como los que se observan con los agentes beta-bloqueantes orales. La incidencia de efectos adversos tras la administración tópica oftálmica es menor que cuando por ejemplo, los medicamentos son administrados vía oral o inyectados. Los siguientes efectos adversos fueron observados con medicamentos betabloqueantes para el tratamiento de trastornos oculares:
No conocida(la frecuencia no puede estimarse a partir de los datos disponibles)
Niveles de glucosa bajos en sangre, alucinaciones, insuficiencia cardíaca, un tipo de trastorno del ritmo cardíaco, aumento de la frecuencia cardiaca, aumento de la tensión arterial, dolor abdominal, vómitos, dolor muscular no causado por el ejercicio, disfunción sexual.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Dorzolamida/Timolol Stulln PF
Mantener este medicamento fuera de la vista y del alcance de los niños.
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la luz.
No utilizar más de 3 meses después de la primera apertura del sobre de aluminio.
Este medicamento no contiene conservantes. Una vez abierto, el contenido del envase unidosis debe usarse inmediatamente y no puede almacenarse. Debe desecharse la solución restante en el envase unidosis después de su aplicación.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja, el sobre y el envase unidosis después de CAD. La fecha de caducidad es el último día del mes que se indica.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición deDorzolamida/Timolol Stulln PF
- Los principios activos son dorzolamida y timolol.
Cada ml contiene 20 mg de dorzolamida (como 22,26 mg de dorzolamida hidrocloruro) y 5 mg de timolol (como 6,83 mg de timolol maleato).
- Los demás componentes son hidroxietilcelulosa (4000 ‑ 5000 mPa·s), manitol, citrato de sodio, hidróxido de sodio (para ajustar el pH) y agua para preparaciones inyectables.
Aspecto del producto y contenido del envase
Dorzolamida/Timolol Stulln PF es una solución transparente, casi incolora, ligeramente viscosa, prácticamente libre de partículas visibles. Un envase unidosis contiene 0,2 ml o 0,3 ml.
Dorzolamida/Timolol Stulln PF se encuentra disponible en envases de 10, 20, 30, 50, 60, 100 o 120 envases unidosis. Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización y responsable de la fabricación
Pharma Stulln GmbH
Werksstrasse 3
92551 Stulln
Alemania
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Austria: Dorzolamid + Timolol Stulln sine 20 mg/ml + 5 mg/ml Augentropfen, Lösung im Einzeldosisbehältnis
Alemania: Dorzocomp-Stulln sine 20 mg/ml + 5 mg/ml Augentropfen, Lösung im Einzeldosisbehältnis
Francia: DORTIRUS 20 mg/ml + 5 mg/ml collyre en solution en récipient unidose
Grecia: DORZYLEA 20 mg/ml + 5 mg/ml Οφθαλμικ?ς σταγ?νες, δι?λυμα σε περι?κτη μ?ας δ?σης
Holanda: Dorzolamide + Timolol Stulln zonder conserveermiddel 20 mg/ml + 5 mg/ml oogdruppels, oplossing in verpakking voor éénmalig gebruik
Polonia: Dorzolamidum + Timololum Stulln
España: Dorzolamida/Timolol Stulln PF 20 mg/ml + 5 mg/ml colirio en solución en envase unidosis
Fecha de la última revisión de este prospecto:Noviembre 2023
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/)
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a DORZOLAMIDA/TIMOLOL STULLN PF 20 MG/ML + 5 MG/ML COLIRIO EN SOLUCION EN ENVASE UNIDOSISForma farmacéutica: COLIRIO, 10 mg/ml + 5 mg/mlPrincipio activo: timolol, combinationsFabricante: Novartis Europharm LimitedRequiere recetaForma farmacéutica: COLIRIO, 0,3 mg/ml + 5 mg/mlPrincipio activo: timolol, combinationsFabricante: Brill Pharma S.L.Requiere recetaForma farmacéutica: COLIRIO, 0,3 mg/ml+5mg/mlPrincipio activo: timolol, combinationsFabricante: Laboratorio Stada S.L.Requiere receta
Médicos online para DORZOLAMIDA/TIMOLOL STULLN PF 20 MG/ML + 5 MG/ML COLIRIO EN SOLUCION EN ENVASE UNIDOSIS
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de DORZOLAMIDA/TIMOLOL STULLN PF 20 MG/ML + 5 MG/ML COLIRIO EN SOLUCION EN ENVASE UNIDOSIS, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















