DITRALIA 25.000 UI PELICULAS BUCODISPERSABLES


Cómo usar DITRALIA 25.000 UI PELICULAS BUCODISPERSABLES
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Ditralia 25000 UIpelículasbucodispersables
colecalciferol (vitamina D3)
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Ditralia y para qué se utiliza
- Qué necesita saber antes de empezar a tomar Ditralia
- Cómo tomar Ditralia
- Posibles efectos adversos
- Conservación de Ditralia
- Contenido del envase e información adicional
1. Qué es Ditralia y para qué se utiliza
Ditralia contiene colecalciferol (vitamina D3). La función principal de la vitamina D es garantizar una correcta absorción intestinal del calcio y favorecer la adecuada mineralización de los huesos.
Ditralia está indicado para el tratamiento inicial de la deficiencia de vitamina D clínicamente relevante en adultos.
2. Qué necesita saber antes de empezar a tomar Ditralia
No tome Ditralia
- si es alérgico al colecalciferol o a alguno de los demás componentes de este medicamento (incluidos en la sección 6)
- si tiene una sensibilidad particular a la vitamina D (lesiones tisulares en varios órganos provocadas por sobredosis de vitamina D) (hipervitaminosis D)
- si presenta altos niveles de calcio en sangre
- si presenta altos niveles de calcio en orina, en especial si tiene cálculos renales
- si tiene depósitos de calcio en los riñones (nefrocalcinosis)
- si tiene una función renal muy reducida (insuficiencia renal grave)
Si se encuentra en alguna de las situaciones anteriores, consulte a su médico o farmacéutico antes de empezar a tomar Ditralia.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Ditralia.
Informe a su médico si está tomando otros productos que contienen vitamina D, como alimentos y leche enriquecidos con vitamina D, ya que la vitamina D se acumula en el organismo y una sobredosis puede causar efectos tóxicos. Ditralia debe utilizarse con precaución en pacientes inmovilizados.
Por eso es importante no superar la dosis recomendada.
Consulte a su médico antes de empezar a tomar Ditralia:
- si tiene tendencia elevada a la formación de cálculos (piedras) en el riñón
- si tiene un desequilibrio de la hormona paratiroidea (pseudohipoparatiroidismo)
Si tiene alguna de las siguientes condiciones, su médico controlará sus niveles de calcio o fosfato en sangre, o el nivel de calcio en orina:
- si tiene problemas de riñón,
- si padece «sarcoidosis», una enfermedad del sistema inmunitario que puede afectar al hígado, los pulmones, la piel o los ganglios linfáticos,
- si es una persona de edad avanzada en tratamiento con glucósidos o diuréticos.
- si está inmovilizado.
Niños y adolescentes
Este medicamento no está recomendado en niños y adolescentes menores de 18 años.
Otros medicamentos y Ditralia
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o pudiera tener que tomar cualquier otro medicamento, incluidos los adquiridos sin receta.
En particular, consulte con su médico si está tomando alguno de los siguientes medicamentos:
- diuréticos tiazídicos: se controlarán regularmente sus niveles de calcio en sangre;
- corticoesteroides («esteroides», por ejemplo, prednisolona o dexametasona): puede ser necesario aumentar su dosis de vitamina D;
- colestiramina (un medicamento para reducir el colesterol) o laxantes (por ejemplo, aceite de parafina): reducen la absorción de vitamina D;
- medicamentos para el corazón (glucósidos cardíacos): deberá estar bajo la supervisión de un médico y es posible que supervise su ECG y sus niveles de calcio en sangre;
- anticonvulsivos (para el tratamiento de la epilepsia; por ejemplo, fenitoína), medicamentos para dormir (por ejemplo, hidantoína, barbitúricos) o primidona: reducen los efectos de la vitamina D;
- rifampicina, isoniazida (antibióticos): pueden reducir la efectividad de la vitamina D;
- actinomicina (un medicamento que se utiliza para tratar algunos tipos de cáncer) y antifúngicos derivados del imidazol (por ejemplo, clotrimazol y ketoconazol, medicamentos que se utilizan para tratar infecciones producidas por hongos): pueden reducir la efectividad de la vitamina D;
- productos que contienen calcio en dosis elevadas: aumentan el riesgo de niveles altos de calcio en sangre;
- productos que contienen magnesio (por ejemplo, antiácidos): no deben utilizarse durante el tratamiento con vitamina D por el riesgo de niveles elevados de magnesio;
- productos que contienen fósforo en dosis elevadas: su uso concomitante con vitamina D puede incrementar el riesgo de niveles elevados de fosfatos en sangre;
- orlistat (un medicamento que se utiliza para tratar la obesidad, incluida la pérdida de peso): podría reducir la absorción de vitamina D. Debe haber un intervalo de 2 horas (antes y después) entre la administración de la vitamina D y la administración de orlistat.
Toma de Ditralia con alimentos y bebidas
Ver sección 3 «Cómo tomar Ditralia».
Embarazo, lactancia y fertilidad
Durante el embarazo y la lactancia no deben utilizarse dosis altas de este producto, sino dosis más bajas. Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de tomar vitamina D. La vitamina D3 pasa a la leche materna. Esto debe tenerse en cuenta cuando se administra al lactante vitamina D de forma adicional. No existen datos acerca de los efectos de la vitamina D3 sobre la fertilidad. Sin embargo, no se prevé que unos niveles normales de vitamina D tengan efectos negativos sobre la fertilidad.
Conducción y uso de máquinas
La influencia de Ditralia sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Ditralia contiene amarillo anaranjado:
Amarillo anaranjado (E110), que puede provocar reacciones de tipo alérgico.
3. Cómo tomar Ditralia
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, pregunte a su médico o farmacéutico.
Uso en adultos
Su médico supervisará el tratamiento, ya que la dosis y la duración de la terapia dependen de su nivel de 25-hidroxicolecalciferol (25(OH)D) en sangre, la gravedad de su enfermedad y su respuesta al tratamiento.
Dosis recomendada: 1 película bucodispersable de 25 000 UI a la semana durante el primer mes. Después del primer mes de tratamiento, el médico puede considerar bajar la dosis
Como alternativa, se pueden seguir las recomendaciones nacionales de posología para el tratamiento de la deficiencia de vitamina D.
Uso en niños y adolescentes
No está previsto el uso de Ditralia en niños y adolescentes menores de 18 años.
Instrucciones de uso
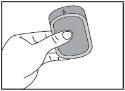
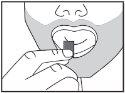
La película bucodispersable debe colocarse en la boca, sobre la lengua, y dejar que se disuelva antes de tragar. Debe tomarse inmediatamente después de sacarla del sobre. Ditralia puede tomarse con o sin alimentos.
Importante: No manipule la película bucodispersable con las manos húmedas.
|
|
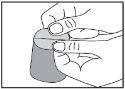
Para ello sostenga cada parte con una mano, con ayuda de sus dedos pulgar e índice. |
|
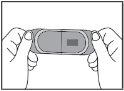
Verá la película bucodispersable colocada en una de las partes separadas del sobre. |
|
|
|
Si toma más Ditralia del que debe
Si toma una dosis excesiva de Ditralia, consulte inmediatamente a su médico o farmacéutico. El exceso de vitamina D provoca una alteración del ciclo del calcio en el organismo. Pueden experimentarse los siguientes síntomas: debilidad, fatiga, dolor de cabeza, náuseas, vómitos, diarrea (y en fases posteriores, estreñimiento), producción excesiva de orina, calcio urinario, sequedad bucal, nicturia, sed intensa, pérdida de apetito, dolor muscular y articular, dolor abdominal y arritmia.
En caso de sobredosis o ingestión accidental, consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono 91 562 04 20, indicando el medicamento y la cantidad ingerida
Tratamiento de urgencia:
Calcitonina, corticoterapia (que evita la absorción intestinal del calcio), hidratación abundante, diuréticos para incrementar el contenido de calcio en la orina (furosemida), una dieta baja en calcio. Los niveles elevados de calcio en sangre requieren ingreso hospitalario inmediato.
Si olvidó tomar Ditralia
No tome una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento con Ditralia
No debe interrumpir el tratamiento a menos que experimente efectos adversos. Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Interrumpa el tratamiento con Ditralia y consulte inmediatamente a su médico
- Si experimenta cualquiera de los siguientes síntomas, ya que pueden ser un signo de reacción alérgica (hipersensibilidad):
- hinchazón de la cara, los labios, la lengua o la garganta
- dificultad para tragar
- urticaria
- dificultad para respirar.
Efectos adversos poco frecuentes (pueden afectar a hasta 1 de cada 100 personas):
- exceso de calcio en la sangre (hipercalcemia)
- exceso de calcio en la orina (hipercalciuria)
Efectos adversos raros (pueden afectar a hasta 1 de cada 1.000 personas):
- prurito, erupción cutánea y urticaria
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- estreñimiento, flatulencia, náuseas, dolor abdominal, diarrea.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Ditralia
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja después de CAD.
No conservar a temperatura superior a 30 °C.
Conservar el producto en el embalaje original para protegerlo de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Ditralia
El principio activo es colecalciferol. Cada película contiene 625 microgramos de colecalciferol (vitamina D3), equivalente a 25 000 UI.
Los demás componentes (excipientes) son aceite de oliva refinado, agua purificada, maltodextrina, hidroxipropilbetadex, copovidona, manitol (E421), glicerol (E422), polisorbato 80 (E433), monolinoleato de glicerol, dióxido de titanio (E171), sucralosa (E955), aroma de naranja*, ácido ascórbico (E300), todo-rac-alfa-tocoferol (E307), amarillo anaranjado (E110).
*contiene:
Aroma: aceite esencial de naranja, aceite de naranja sin terpenos, aceite de limón sin terpenos, aceite de mandarina sin terpenos, hexanoato de etilo, 2-metilbutirato de etilo, butirato de etilo, acetaldehído
Aditivos: bultilhidroxianisol (E320), ácido cítrico (E330)
Agentes de carga: maltodextrina, goma arábiga (E414)
Aspecto del producto y contenido del envase
Ditralia 25 000 UI es una película rectangular y flexible de color naranja claro (15 mm x 30 mm).
La película bucodispersable se presenta en un envase que contiene 2 o 4 películas para cada concentración. Cada sobre contiene una película bucodispersable.
Titular de la Autorización de Comercialización:
IBSA Farmaceutici Italia S.r.l.
Via Martiri di Cefalonia 2
26900 Lodi, Italia
Responsable de la fabricación:
IBSA Farmaceutici Italia S.r.l
S.S. n. 11 Padana Superiore Km 160
20051 Cassina de’ Pecchi (Mi), Italia
o
Altergon Italia Srl
Zona Industriale
83040 Morra de Sanctis (AV), Italia
Puede solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Instituto Bioquimico Iberico IBSA S.L.
Avenida Diagonal 605,
Planta 8, Local 1,
08028 Barcelona (España)
Fecha de la última revisión de este prospecto:
Agosto 2024
La información detallada y actualizada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a DITRALIA 25.000 UI PELICULAS BUCODISPERSABLESForma farmacéutica: CAPSULA, 25.000 UIPrincipio activo: colecalciferolFabricante: Laboratorios Alter S.A.Requiere recetaForma farmacéutica: CAPSULA, 50.000 UIPrincipio activo: colecalciferolFabricante: Laboratorios Alter S.A.Requiere recetaForma farmacéutica: CAPSULA, 50,000 UIPrincipio activo: colecalciferolFabricante: Consilient Health LimitedRequiere receta
Médicos online para DITRALIA 25.000 UI PELICULAS BUCODISPERSABLES
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de DITRALIA 25.000 UI PELICULAS BUCODISPERSABLES, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes