CABAZITAXEL ZENTIVA 60 MG CONCENTRADO Y DISOLVENTE PARA SOLUCION PARA PERFUSION EFG

Cómo usar CABAZITAXEL ZENTIVA 60 MG CONCENTRADO Y DISOLVENTE PARA SOLUCION PARA PERFUSION EFG
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el paciente
Cabazitaxel Zentiva 60 mg concentrado y disolvente para solución para perfusión EFG
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Cabazitaxel Zentiva y para qué se utiliza
- Qué necesita saber antes de que le administren Cabazitaxel Zentiva
- Cómo usar Cabazitaxel Zentiva
- Posibles efectos adversos
- Conservación de Cabazitaxel Zentiva
- Contenido del envase e información adicional
1. Qué es Cabazitaxel Zentiva y para qué se utiliza
Cabazitaxel Zentiva contiene el principio activo cabazitaxel que pertenece a un grupo de medicamentos denominado “taxanos”, utilizados para tratar cánceres.
Cabazitaxel se utiliza para el tratamiento del cáncer de próstata que ha progresado después de haber recibido otra quimioterapia. Actúa deteniendo el crecimiento de las células y su multiplicación.
Como parte de su tratamiento, tomará también cada día un corticosteroide (prednisona o prednisolona), por vía oral. Pida información a su médico sobre este otro medicamento.
2. Qué necesita saber antes de empezar a usar Cabazitaxel Zentiva
No use Cabazitaxel Zentiva:
- si es alérgico (hipersensible) a cabazitaxel, a otros taxanos, al polisorbato 80 o a alguno de los demás componentes de este medicamento (incluidos en la sección 6),
- si el número de sus glóbulos blancos es muy bajo (número de neutrófilos menor o igual a 1.500/mm3),
- si tiene problemas graves de hígado,
- si recientemente ha sido o va a ser vacunado contra la fiebre amarilla.
No debe recibir Cabazitaxel Zentiva si le sucede alguna de las circunstancias anteriores. Si no está seguro, consulte a su médico antes de recibir Cabazitaxel Zentiva.
Advertencias y precauciones
Antes de iniciar el tratamiento con Cabazitaxel Zentiva, le harán análisis de sangre para comprobar que tiene suficientes células sanguíneas y que sus riñones e hígado funcionan adecuadamente para recibir Cabazitaxel Zentiva.
Informe a su médico inmediatamente si:
- tiene fiebre. Durante el tratamiento con Cabazitaxel Zentiva es más probable que se reduzca el número de sus glóbulos blancos. El médico controlará su sangre y su estado general para detectar signos de infecciones. Podría administrarle otros medicamentos para mantener el número de sus células sanguíneas. Las personas con recuentos celulares bajos pueden desarrollar infecciones que pueden poner en peligro la vida. El primer signo de infección podría ser fiebre, por lo que si tiene fiebre, informe a su médico inmediatamente.
- alguna vez ha tenido cualquier alergia. Durante el tratamiento con Cabazitaxel Zentiva pueden producirse reacciones alérgicas graves.
- tiene diarrea grave o duradera, se siente mal (náuseas) o está mal (vómitos). Cualquiera de estas situaciones puede producir deshidratación grave. Su médico tendría que ponerle un tratamiento.
- tiene sensación de insensibilidad, hormigueo, ardor o disminución de las sensaciones en manos y pies.
- tiene algún problema de sangrado en el intestino o tiene cambios en el color de sus heces o dolor de estómago. Si el sangrado o el dolor es grave, su médico interrumpirá su tratamiento con Cabazitaxel Zentiva. Esto es porque Cabazitaxel Zentiva podría incrementar el riesgo de sangrado o desarrollo de perforaciones en la pared intestinal.
- tiene problemas de riñón.
- tiene piel y ojos amarillentos, orina oscura, áuseas intensas (sensación de malestar) o vómitos, ya que pueden ser signos o síntomas de problemas hepáticos.
- nota que el volumen de su orina aumenta o disminuye significativamente.
- tiene sangre en su orina.
Si le sucede cualquiera de las circunstancias anteriores, informe a su médico inmediatamente. Su médico podría reducir la dosis de Cabazitaxel Zentiva o interrumpir el tratamiento.
Uso de Cabazitaxel Zentivacon otros medicamentos
- Informe a su médico, farmacéutico o enfermero si está utilizando o ha utilizado recientemente otros medicamentos, incluso los adquiridos sin receta. Esto se debe a que algunos medicamentos pueden afectar la eficacia de Cabazitaxel Zentiva o Cabazitaxel Zentiva puede afectar la eficacia de otros medicamentos. Estos medicamentos incluyen los siguientes:
- ketoconazol, rifampicina (para infecciones);
- carbamazepina, fenobarbital o fenitoína (para convulsiones);
- Hierba de San Juan o hipérico (Hypericum perforatum) (planta medicinal utilizada para tratar la depresión y otros problemas);
- estatinas (tales como simvastatina, lovastatina, atorvastatina, rosuvastatina, o pravastatina) (para reducir el colesterol en su sangre);
- valsartan (para la hipertensión);
- repaglinida (para la diabetes).
Mientras esté en tratamiento con Cabazitaxel Zentiva, consulte con su médico antes de vacunarse.
Embarazo, lactancia y fertilidad
Cabazitaxel Zentiva no está indicado para el uso en mujeres.
Use preservativos en sus relaciones sexuales si su pareja está o pudiera estar embarazada. Cabazitaxel puede estar preesente en su semen y afectar al feto. Se recomienda no engendrar un hijo durante y hasta 4 meses despues del tratamiento y solicitar información sobre la conservación del esperma antes del tratamiento, ya que Cabazitaxel Zentiva podría alterar la fertilidad masculina.
Conducción y uso de máquinas
Durante el tratamiento con este medicamento podría sentirse cansado o mareado. Si esto sucede, no conduzca ni use herramientas o máquinas hasta que se sienta mejor.
Cabazitaxel Zentivacontiene etanol (alcohol)
Este medicamento contiene 709,8 mg de alcohol (etanol) en cada vial de disolvente. La cantidad en la dosis de este medicamento es equivalente a 14 ml de cerveza o 6 ml de vino. La pequeña cantidad de alcohol que contiene este medicamento no produce ningún efecto perceptible. Si tiene adicción al alcohol, tiene una enfermedad hepática o epilepsia, consulte a su médico o farmacéutico antes de tomar este medicamento.
3. Cómo usar Cabazitaxel Zentiva
Instrucciones de uso
Antes de recibir cabazitaxel le administrarán medicamentos antialérgicos para reducir el riesgo de reacciones alérgicas.
- Cabazitaxel será administrado por un médico o un enfermero.
- Cabazitaxel se debe preparar (diluir) antes de administrarse. Con este prospecto se proporciona información práctica para la manipulación y administración de cabazitaxel para médicos, enfermeros y farmacéuticos.
- Cabazitaxel se administrará en el hospital mediante un gotero (perfusión) en una de sus venas (vía intravenosa) durante aproximadamente 1 hora.
- Como parte de su tratamiento, tomará también un medicamento corticosteroide (prednisona o prednisolona) por vía oral todos los días.
Cuánto y con qué frecuencia se administra
- La dosis habitual depende de su área de superficie corporal. Su médico calculará su área de superficie corporal en metros cuadrados (m2) y decidirá la dosis que debe recibir.
- Habitualmente recibirá una perfusión cada 3 semanas.
En caso de sobredosis o ingestión accidental, consulte a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20, indicando el medicamento y la cantidad ingerida.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
4. Posibles efectos adversos
Al igual que todos los medicamentos, Cabazitaxel Zentiva puede producir efectos adversos, aunque no todas las personas los sufran. Su médico comentará esto con usted y le explicará los riesgos y los beneficios potenciales de su tratamiento.
Acuda inmediatamente al médico si nota cualquiera de los siguientes efectos adversos:
- fiebre (temperatura alta). Esto es frecuente (podría afectar hasta de 1 de cada 10 personas).
- pérdida grave de fluidos corporales (deshidratación). Esto es frecuente (podría afectar hasta 1 de cada 10 personas). Esto puede ocurrir si tiene diarrea grave o duradera, o fiebre, o si ha estado vomitando.
- dolor de estómago grave o dolor de estómago que no se resuelve. Esto puede suceder si usted tiene una perforación en el estómago, esófago, intestino (perforación gastrointestinal). Esto puede causar la muerte.
Si le sucede alguna de las circunstancias anteriores, comuníquelo inmediatamente a su médico.
Otros efectos adversos incluyen:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- reducción del número de células sanguíneas rojas (anemia), o blancas (que son importantes para combatir las infecciones)
- reducción del número de plaquetas (lo cual resulta en un aumento del riesgo de tener hemorragias)
- pérdida de apetito (anorexia)
- molestias de estómago, incluyendo náuseas, vómitos, diarrea o estreñimiento
- dolor de espalda
- sangre en la orina
- cansancio, debilidad o falta de energía
Frecuentes (pueden afectar hasta 1 de cada 10 personas):
- alteración del gusto
- respiración entrecortada
- tos
- dolor abdominal
- pérdida de cabello a corto plazo (en la mayoría de los casos el pelo vuelve a crecer con normalidad)
- dolor de las articulaciones
- infección del tracto urinario
- escasez de glóbulos blancos asociada con fiebre e infecciones
- sensación de insensibilidad, hormigueo, ardor o disminución de las sensaciones en manos y pies
- mareo
- dolor de cabeza
- aumento o disminución de la tensión arterial
- malestar de estómago, ardor de estómago o eructos
- dolor de estómago
- hemorroides
- espasmos musculares
- orinar con frecuencia o con dolor
- incontinencia urinaria
- problemas o alteración de los riñones
- úlceras en la boca o en los labios
- infecciones o riesgo de infecciones
- nivel de azúcar en sangre elevado
- insomnio
- confusión mental
- sensación de ansiedad
- sensación rara o pérdida de sensación o dolor en manos y pies
- problemas de equilibrio
- latidos rápidos o irregulares del corazón
- coágulos de sangre en las piernas o en el pulmón
- sensación de sofoco en la piel
- dolor de boca o garganta
- hemorragia rectal
- molestias, trastornos, debilidad o dolores musculares
- inflamación de pies o piernas
- escalofríos.
- trastornos en las uñas (cambio de color en sus uñas; las unas se podrían desprender).
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
- nivel de potasio en sangre bajo
- zumbido en los oidos
- sensación de calor en la piel
- inflamacion de la vejiga, que puede ocurrir cuando su vejiga ha estado previamente exuesta a radioterapia (cistitis debida a fenómenos de recuerdo de radiación).
Frecuencia no conocida (no puede estimarse a partir de los datos disponibles):
- enfermedad pulmonar intersticial (inflamación de los pulmones causando tos y dificultad para respirar).
Comunicación de efectos adversos:
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Cabazitaxel Zentiva
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el envase y en la etiqueta de los viales después de CAD. La fecha de caducidad es el último día del mes que se indica.
No refrigerar.
En la sección “Información práctica para médicos o profesionales sanitarios sobre la preparación, administracion y manipulación de Cabazitaxel Zentiva” se incluye información sobre la conservacion y el tiempo de uso de Cabazitaxel Zentiva, una vez que se ha diluido y está listo para usar.
La eliminación del medicamento no utilizado se realizará de acuerdo con la normativa local. Estas medidas ayudarán a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Cabazitaxel Zentiva
El principio activo es cabazitaxel. Un ml de concentrado contiene 40 mg de cabazitaxel. Un vial de concentrado contiene 60 mg de cabazitaxel.
Los demás componentes son: polisorbato 80, ácido cítrico y etanol absoluto en el concentrado, y etanol 96% y agua para preparaciones inyectables en el disolvente (ver sección 2 “Cabazitaxel Zentiva contiene etanol (alcohol)”).
Nota: tanto el vial del concentrado de Cabazitaxel Zentiva 60 mg/1,5 ml (volumen de llenado: 1,83 ml) como el del vial de disolvente (volumen de llenado: 5,67 ml) contienen un sobrellenado para compensar la pérdida de líquido durante la preparación. Este sobrellenado asegura que después de la dilución con el contenido completo del disolvente proporcionado, haya una solución conteniendo 10 mg/ml de cabazitaxel para inyección.
Aspecto del producto y contenido del envase
Cabazitaxel Zentiva es un concentrado y disolvente para solución para perfusión (concentrado estéril).
El concentrado es una solución viscosa transparente entre incolora y amarilla pálida.
El disolvente es una solución transparente e incolora.
Un envase de Cabazitaxel Zentiva contiene:
Concentrado: 1,5 ml de concentrado en un vial de 15 ml de vidrio tubular transparente (tipo I), cerrado con un cierre de elastómero de caucho de color gris, sellado con un sello de aluminio abatible con un disco de plástico de color amarillo. Cada vial contiene 60 mg de cabazitaxel en1,5 ml (volumen nominal).
Disolvente: 5,67 ml en un vial de vidrio de 15 ml transparente (tipo I), cerrado con un cierre de elastómero de caucho de color gris, sellado con un sello de aluminio abatible con un disco de plástico de color azul oscuro. Cada vial contiene 5,67 ml (volumen nominal).
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
Zentiva, k.s.,
U kabelovny 130,
Praga 10 – Dolní Mecholupy,
102 37 República Checa
Responsable de la fabricación
Mias Pharma Limited
Suite 2, Stafford House, Strand Road
Portmarnock, Co. Dublin
Irlanda
Tillomed Malta Limited,
Malta Life Sciences
Park, LS2.01.06
Industrial Estate,
San Gwann, SGN 3000,
Malta
Puedensolicitar más información respecto a estemedicamentodirigiéndose al representante local del titular de la autorización de comercialización:
Zentiva Spain S.L.U.
Avenida de Europa, 19, Edificio 3, Planta 1.
28224 Pozuelo de Alarcón, Madrid
España
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo y en el Reino Unido (Irlanda del Norte) con los siguientes nombres:
País | Nombre del producto |
Alemania | Cabazitaxel Tillomed 60 mg Konzentrat und Lösungsmittel zur Herstellung einer Infusionslösung |
España | Cabazitaxel Zentiva 60 mg concentrado y disolvente para solución para perfusión EFG |
Italia | Cabazitaxel Tillomed |
Francia | Cabazitaxel Tillomed 60 mg solution à diluer et solvant pour solution pour perfusion |
Fecha de la última revisión de este prospecto:julio 2023
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es/
<------------------------------------------------------------------------------------------------------>
La siguiente información está destinada únicamente a profesionales sanitarios.
INFORMACIÓN PRÁCTICA PARA MÉDICOS O PROFESIONALES SANITARIOS SOBRE LA PREPARACIÓN, ADMINISTRACIÓN Y MANIPULACIÓN DE Cabazitaxel Zentiva60 mg CONCENTRADO Y DISOLVENTE PARA SOLUCIÓN PARA PERFUSIÓN
Esta información complementa las secciones 3 y 5 para el usuario.
Es importante que lea el contenido completo de este procedimiento antes de preparar la solución para perfusión.
Incompatibilidades
Este medicamento no debe mezclarse con otros medicamentos excepto los utilizados para las diluciones.
Periodo de validez y precauciones especiales de conservación
Para el envase de Cabazitaxel Zentiva 60 mg concentrado y disolvente
No refrigerar.
Después de la apertura del vial
Los viales de concentrado y disolvente deben utilizarse inmediatamente. Si no se utilizan inmediatamente, el tiempo y las condiciones de conservación son responsabilidad del usuario. Desde un punto de vista microbiológico, el proceso de dilución en dos etapas debe realizarse en condiciones controladas y asépticas (ver a continuación “Precauciones de preparación y administración”).
Después de la dilución inicialde Cabazitaxel Zentiva 60 mg concentrado con el contenido completodel vial de disolvente se ha demostrado la estabilidad química y física en uso durante 1 hora, a temperatura ambiente (15ºC - 30ºC).
Después de la dilución final en la bolsa/botella de perfusión
Se ha demostrado la estabilidad química y física de la solución de perfusión durante 8 horas a temperatura ambiente (15°C – 30°C) incluyendo 1 hora de tiempo de perfusión y durante 48 horas en nevera incluyendo 1 hora de tiempo de perfusión.
Desde un punto de vista microbiológico, la solución de perfusión debe utilizarse inmediatamente. Si no se utiliza inmediatamente, los tiempos y las condiciones de conservación son responsabilidad del usuario y normalmente no deberían ser más de 24 horas a 2ºC - 8ºC, a menos que la dilución se haya realizado en condiciones asépticas controladas y validadas.
Precauciones de preparación y administración
Al igual que otros agentes antineoplásicos, se debe actuar con precaución durante la preparación y administración de las soluciones de cabazitaxel, teniendo en cuenta el uso de dispositivos de seguridad, equipo de protección personal (por ej. guantes) y procedimientos de preparación.
Si en cualquiera de las etapas de preparación, cabazitaxel entrara en contacto con la piel, lavar inmediata y minuciosamente con agua y jabón. Si entrara en contacto con membranas mucosas, lavar inmediata y minuciosamente con agua.
Cabazitaxel solo debe ser preparado y administrado por personal entrenado en el manejo de agentes citotóxicos. Las trabajadoras embarazadas no deben manipularlo.
Diluir siempre el concentrado para solución para perfusión con el disolvente completo que se proporciona antes de añadirlo a las soluciones de perfusión.
Etapas de la preparación
Lea detenidamente TODAesta sección antes de mezclar y diluir. Cabazitaxel Zentiva requiere DOSdiluciones antes de la administración. Siga las instrucciones de preparación que se proporcionan a continuación.
Nota: tanto el vial del concentrado de Cabazitaxel Zentiva 60 mg/1,5 ml (volumen de llenado: 1,83 ml) como el vial de disolvente (volumen de llenado: 5,67 ml) contienen un sobrellenado para compensar la pérdida de líquido durante la preparación. Este sobrellenado asegura que después de la dilución con el contenido COMPLETOdel disolvente proporcionado, haya una solución conteniendo 10 mg/ml de cabazitaxel.
Para preparar la solución para perfusión, el siguiente proceso de dilución se debe realizar en dos etapas de forma aséptica.
Etapa 1: dilución inicial del concentrado de solución para perfusión con el disolvente proporcionado.
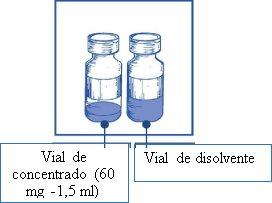
Etapa 1.1 Inspeccionar el vial de concentrado y el disolvente proporcionado. La solución de concentrado y de disolvente deben ser transparentes |
|
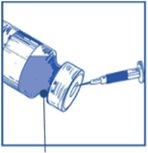
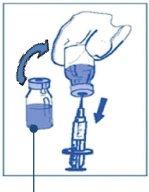
Etapa 1.2 Utilizando una jeringa provista de una aguja fija, extraer de forma aséptica el contenido completodel disolvente proporcionado invirtiendo parcialmente el vial. |
|
| |
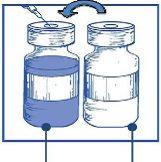
Etapa 1.3 Inyectar el contenido completoen el correspondiente vial de concentrado. Para limitar todo lo posible la formación de espuma al inyectar el disolvente, dirigir la aguja hacia la pared interior del vial de solución de concentrado e inyectar lentamente. Una vez reconstituido, la solución resultante contiene 10 mg/ml de cabazitaxel. |
|
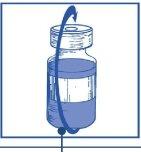
Etapa 1.4 Sacar la jeringa y la aguja y mezclar manual y suavemente, mediante inversiones repetidas, hasta que se obtenga una solución transparente y homogénea. Se pueden tardar unos 45 segundos. |
|
| |
Etapa 1.5 Dejar reposar la solución durante aproximadamente 5 minutos y a continuación comprobar que la solución es homogénea y transparente. Es normal que persista la espuma pasado este tiempo. |
|
Esta mezcla concentrado-disolvente resultante contiene 10 mg/ml de cabazitaxel (al menos 6 ml de volumen liberado). La segunda dilución se debe realizar inmediatamente (antes de 1 hora) como se detalla en la Etapa 2.
Podría ser necesario más de un vial de mezcla concentrado-disolvente para administrar la dosis prescrita.
Etapa 2: segunda dilución (final) para perfusión
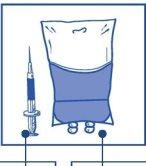
Etapa 2.1 De forma aséptica extraer la cantidad requerida de mezcla concentrado-disolvente (10 mg/ml de cabazitaxel), con una jeringa graduada provista de una aguja fija. Como ejemplo, una dosis de 45 mg de Cabazitaxel Zentiva requeriría 4,5 ml de la mezcla de concentrado-disolvente preparada en la Etapa 1. Como puede seguir habiendo espuma en la pared del vial de esta solución, después de la preparación descrita en la Etapa 1, es preferible situar la aguja de la jeringa en la mitad del contenido durante la extracción. |
|
Etapa 2.2 Inyectar en un envase estéril sin PVC de solución de glucosa al 5% o solución de cloruro sódico 9 mg/ml (0,9%) para perfusión. La concentración de la solución para perfusión debe estar entre 0,10 mg/ml y 0,26 mg/ml. |
|
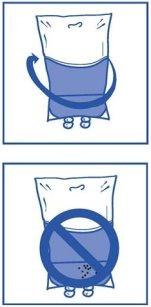
Etapa 2.3 Sacar la jeringa y mezclar el contenido de la bolsa o botella de perfusión manualmente, mediante movimiento de balanceo. Etapa 2.4 Al igual que todos los productos parenterales, la solución de perfusión resultante se debe inspeccionar visualmente antes de usarla. Como la solución de perfusión está sobresaturada, puede cristalizar con el tiempo. En este caso, no se debe utilizar la solución y debe eliminarse. |
|
La solución para perfusión debe utilizarse inmediatamente. No obstante, el tiempo de conservación en uso puede ser más largo bajo las condiciones específicas mencionadas en la sección Periodo de validez y precauciones especiales de conservación.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
Método de administración
Cabazitaxel Zentiva se administra en perfusión durante 1 hora.
Se recomienda el uso de un filtro en línea de 0,22 micrómetros de tamaño de poro nominal (también denominado 0,2 micrómetros) durante la administración.
No deben utilizarse envases de perfusión de PVC o sets de perfusión de poliuretano para la preparación y administración de la solución para perfusión .
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a CABAZITAXEL ZENTIVA 60 MG CONCENTRADO Y DISOLVENTE PARA SOLUCION PARA PERFUSION EFGForma farmacéutica: INYECTABLE PERFUSION, 20 mg/mlPrincipio activo: CabazitaxelFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: INYECTABLE PERFUSION, 20 MGPrincipio activo: CabazitaxelFabricante: Eugia Pharma (Malta) LimitedRequiere recetaForma farmacéutica: INYECTABLE PERFUSION, 60 mgPrincipio activo: CabazitaxelFabricante: Reddy Pharma Iberia S.A.Requiere receta
Médicos online para CABAZITAXEL ZENTIVA 60 MG CONCENTRADO Y DISOLVENTE PARA SOLUCION PARA PERFUSION EFG
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de CABAZITAXEL ZENTIVA 60 MG CONCENTRADO Y DISOLVENTE PARA SOLUCION PARA PERFUSION EFG, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes