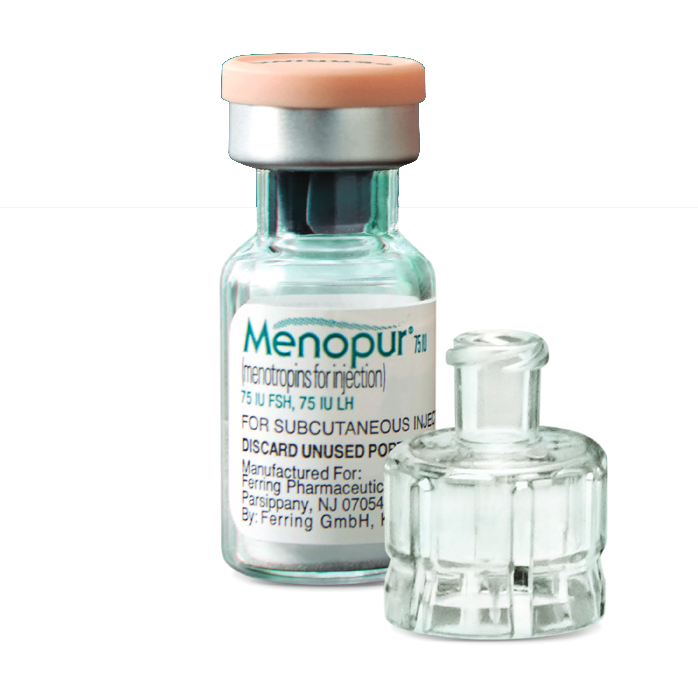
Cómo usar Menopur
Hoja de instrucciones del paquete: información para el paciente
MENOPUR, 150 IU FSH + 150 IU LH, polvo y disolvente para preparar una solución
para inyección
Menotropina
Es importante leer el folleto antes de tomar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar este folleto para poder volver a leerlo si es necesario.
- En caso de dudas, debe consultar a su médico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en este folleto, debe informar a su médico. Véase el punto 4.
Índice del folleto:
- 1. Qué es Menopur y para qué se utiliza
- 2. Información importante antes de tomar Menopur
- 3. Cómo tomar Menopur
- 4. Posibles efectos adversos
- 5. Cómo conservar Menopur
- 6. Contenido del paquete y otra información
1. Qué es Menopur y para qué se utiliza
Menopur es un polvo (en este caso, es una masa compacta y sólida) que debe disolverse en un líquido (disolvente) antes de su uso. El medicamento se administra por inyección subcutánea o intramuscular. Menopur (menotropina altamente purificada obtenida de la orina de mujeres posmenopáusicas) contiene dos hormonas: hormona folitropina (FSH) y hormona luteinizante (LH). FSH y LH son hormonas producidas en el cuerpo de la mujer y el hombre. Permiten el funcionamiento normal de los órganos reproductivos. Menopur se utiliza para tratar la infertilidad en las siguientes situaciones: en mujeres que no pueden quedar embarazadas porque sus ovarios no producen óvulos (también en el caso del síndrome de ovario poliquístico). Menopur se utiliza en mujeres a las que se les ha administrado citrato de clomifeno para tratar la infertilidad, pero el medicamento no ha sido efectivo; en mujeres que participan en programas de reproducción asistida, como la fecundación in vitro y la transferencia de embriones, la transferencia de gametos al oviducto y la inyección citoplasmática de espermatozoides en el óvulo. Menopur ayuda a producir múltiples folículos ováricos en los que pueden desarrollarse óvulos (desarrollo de múltiples folículos ováricos); en hombres que tienen un número insuficiente de espermatozoides debido a una deficiencia de gonadotropinas (hormonas producidas por la glándula pituitaria y que afectan los testículos).
2. Información importante antes de tomar Menopur
Antes de comenzar a tomar Menopur, es necesario que el médico evalúe las causas de la infertilidad en ambos partners. Especialmente, debe verificar si no hay enfermedades que requieran un tratamiento diferente: hipotiroidismo y enfermedad de Addison; niveles altos de prolactina (hiperprolactinemia); tumores pituitarios (glándula ubicada en la base del cerebro); tumores hipotalámicos (área ubicada debajo de la parte del cerebro llamada tálamo). Si el paciente tiene alguna de estas enfermedades, debe informar a su médico antes de comenzar el tratamiento con Menopur.
Contraindicaciones
En mujeres y hombres: si el paciente es alérgico a la menotropina o a alguno de los demás componentes de este medicamento (enumerados en el punto 6); si se han detectado tumores pituitarios o hipotalámicos. En mujeres: si la paciente está embarazada o en período de lactancia; si la paciente tiene quistes ováricos o ovarios agrandados no causados por el síndrome de ovario poliquístico; si la paciente tiene sangrado vaginal de causa desconocida; si la paciente tiene tumores uterinos, ováricos o mamarios; si la paciente tiene malformaciones genitales que impiden el desarrollo del embarazo; si la paciente tiene miomas uterinos que impiden el desarrollo del embarazo; si la paciente ha entrado en la menopausia prematuramente. En hombres: si el paciente tiene cáncer de próstata; si el paciente tiene tumores testiculares.
Precauciones y advertencias
Se debe tener cuidado si la paciente tiene: dolor abdominal; hinchazón abdominal; náuseas; vómitos; diarrea; aumento de peso; dificultades para respirar; disminución de la frecuencia o cantidad de orina. Debe informar a su médico de inmediato si experimenta alguno de estos síntomas, incluso si aparecen varios días después de la última dosis del medicamento. Pueden ser síntomas de hiperestimulación ovárica, que puede ser grave. Si los síntomas empeoran, debe suspender el tratamiento de infertilidad y recibir tratamiento en un hospital. Seguir la dosis recomendada y observar atentamente el curso del tratamiento reduce la probabilidad de que aparezcan estos síntomas. Estos síntomas también pueden aparecer cuando se suspende el tratamiento con Menopur. Si aparece alguno de estos síntomas, debe contactar a su médico de inmediato. Durante el tratamiento con Menopur, el médico generalmente ordena exámenes de ultrasonido (con ultrasonido) y sometimes análisis de sangre para verificar la respuesta al tratamiento. El tratamiento con hormonas como Menopur puede aumentar el riesgo de: embarazo ectópico (fuera del útero) en mujeres con enfermedades tubáricas preexistentes; aborto; embarazo múltiple (gemelos, trillizos, etc.); malformaciones congénitas (defectos físicos presentes en el niño al nacer). En algunas mujeres tratadas por infertilidad, se han desarrollado quistes ováricos o tumores de otros órganos reproductivos. No se sabe si esto se debió al tratamiento con hormonas como Menopur. El riesgo de trombosis en las venas o arterias es mayor en mujeres embarazadas. El tratamiento de infertilidad puede aumentar el riesgo de trombosis, especialmente si la paciente tiene sobrepeso o si ha tenido trombosis previamente o si hay antecedentes familiares de trombosis. La paciente debe informar a su médico si cree que esto la afecta. Menopur, junto con una hormona llamada gonadotropina coriónica humana (hCG), puede ser administrado para tratar la infertilidad en hombres.
Niños y adolescentes
No se recomienda el uso de Menopur en niños y adolescentes.
Menopur y otros medicamentos
Debe informar a su médico sobre todos los medicamentos que está tomando actualmente o que planea tomar. El citrato de clomifeno es otro medicamento utilizado para tratar la infertilidad. Si Menopur se administra al mismo tiempo que el citrato de clomifeno, el efecto en los ovarios puede aumentar. Menopur puede ser administrado junto con el medicamento Bravelle. Véase el punto 3.
Embarazo y lactancia
No se debe tomar Menopur durante el embarazo o la lactancia.
Conducción de vehículos y uso de máquinas
Es poco probable que Menopur afecte la capacidad de conducir vehículos o operar máquinas.
Menopur contiene cloruro de sodio
Menopur contiene menos de 1 mmol de cloruro de sodio (23 mg) por dosis, es decir, el medicamento se considera "libre de sodio".
3. Cómo tomar Menopur
Este medicamento debe ser tomado siempre según las indicaciones de su médico. En caso de dudas, debe consultar a su médico. Mujeres que no ovulan (no producen óvulos) El tratamiento debe comenzar dentro de los primeros 7 días del ciclo menstrual (día 1 es el primer día de la menstruación). El medicamento debe ser administrado diariamente durante al menos 7 días. La dosis inicial es generalmente de 75 IU (unidades internacionales) de FSH + 75 IU de LH a 150 IU de FSH + 150 IU de LH (es decir, de ½ a 1 ampolla de polvo) por día, pero puede ser ajustada según la respuesta de la paciente hasta un máximo de 225 IU de FSH + 225 IU de LH (es decir, 1 ampolla y ½ ampolla de polvo) por día. La dosis determinada debe ser administrada durante al menos 7 días antes de que se produzca un cambio en la dosis. Se recomienda que, en cada cambio, la dosis se aumente en 37,5 IU de FSH + 37,5 IU de LH (es decir, ¼ de ampolla de polvo), pero no más de 75 IU de FSH + 75 IU de LH (es decir, ½ ampolla de polvo). El ciclo de tratamiento debe ser interrumpido si no se produce respuesta después de 4 semanas. Cuando se produce una respuesta satisfactoria, al día siguiente de la última inyección de Menopur, se debe administrar una sola inyección de hCG en una dosis de 5000 IU a 10 000 IU. Se recomienda tener relaciones sexuales el día de la inyección y al día siguiente de la inyección de hCG. Alternativamente, se puede realizar una inseminación (introducción de semen en el útero). La paciente permanece bajo estrecha supervisión del médico durante al menos 2 semanas después de la inyección de hCG. El médico verificará los resultados del tratamiento con Menopur. Dependiendo del progreso del tratamiento, el médico puede decidir interrumpir la administración de Menopur y omitir la inyección de hCG. En este caso, la paciente será informada sobre la necesidad de usar un método anticonceptivo mecánico (por ejemplo, condón) o abstenerse de tener relaciones sexuales hasta la próxima menstruación. Mujeres que participan en programas de reproducción asistida Si la paciente también ha recibido tratamiento con un agonista de GnRH (un medicamento que ayuda a la acción de la hormona que libera gonadotropina, GnRH), la administración de Menopur debe comenzar aproximadamente 2 semanas después del inicio del tratamiento con el agonista de GnRH. Si la paciente también ha recibido tratamiento con un antagonista de GnRH, la administración de Menopur debe comenzar el día 2 o 3 del ciclo menstrual (día 1 es el primer día de la menstruación). El medicamento debe ser administrado diariamente durante al menos 5 días. La dosis inicial de Menopur es generalmente de 150 IU de FSH + 150 IU de LH a 225 IU de FSH + 225 IU de LH (es decir, de 1 a 1 y ½ ampolla de polvo) por día. Dependiendo de la respuesta de la paciente al tratamiento, la dosis puede ser aumentada hasta un máximo de 450 IU de FSH + 450 IU de LH (es decir, 3 ampollas de polvo) por día. No se debe aumentar la dosis en más de 150 IU de FSH + 150 IU de LH (es decir, 1 ampolla de polvo) a la vez. El tratamiento generalmente no debe durar más de 20 días. Cuando se produce una respuesta satisfactoria, se administra una sola inyección de hCG en una dosis de hasta 10 000 IU para inducir la ovulación (liberación del óvulo). La paciente permanece bajo estrecha supervisión del médico durante al menos 2 semanas después de la inyección de hCG. El médico verificará los resultados del tratamiento con Menopur. Dependiendo del progreso del tratamiento, el médico puede decidir interrumpir la administración de Menopur y omitir la inyección de hCG. En este caso, la paciente será informada sobre la necesidad de usar un método anticonceptivo mecánico (por ejemplo, condón) o abstenerse de tener relaciones sexuales hasta la próxima menstruación. Hombres El tratamiento comienza con la administración de hCG 3 veces a la semana en una dosis de 1000 IU a 3000 IU, hasta que se produzca un nivel normal de testosterona en la sangre. Luego, se administra Menopur por vía intramuscular en una dosis de 75 IU de FSH + 75 IU de LH a 150 IU de FSH + 150 IU de LH (es decir, de ½ a 1 ampolla de polvo) 3 veces a la semana durante varios meses.
INSTRUCCIONES PARA LA ADMINISTRACIÓN
Si el médico ha recetado la autoadministración de Menopur, debe seguir todas las instrucciones proporcionadas. La primera inyección de Menopur debe ser administrada bajo la supervisión de un médico. RECONSTITUCIÓN (DISOLUCIÓN) DE MENOPUR:Menopur es un polvo y debe ser reconstituido (disuelto) antes de la inyección. El líquido utilizado para disolver el polvo se suministra con el polvo. Menopur debe ser reconstituido justo antes de su uso. Para ello, debe:
- Colocar firmemente en la jeringa una aguja gruesa y larga (aguja para reconstitución).
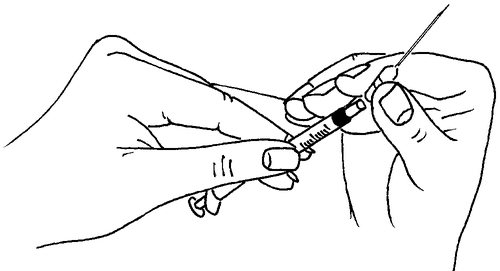
reconstitución).
- Romper la parte superior del frasco con el disolvente en el lugar indicado por el punto.
- Introducir la aguja en el frasco con el disolvente.
- Extraer todo el líquido del frasco con el disolvente a la jeringa.
- Introducir la aguja a través del tapón de goma de la ampolla con el polvo y, lentamente, inyectar todo el líquido.
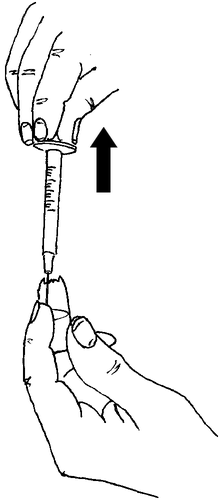
El polvo debe disolverse rápidamente (en 2 minutos), formando una solución transparente.
- Para facilitar la reconstitución del polvo, se puede agitar suavemente la ampolla. No
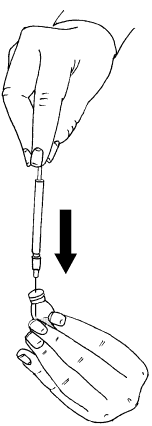
- debe agitarse, ya que esto puede causar la formación de burbujas de aire. Si la solución no es transparente osi contiene partículas, no debe ser utilizada.
- Extraer la solución de regreso a la jeringa.
Si el médico ha recetado más de una ampolla de Menopur por inyección, la solución obtenida después de la reconstitución del polvo de la primera ampolla se puede inyectar en la segunda ampolla con el polvo. Esta acción se puede repetir con las ampollas de polvo adicionales, hasta un máximo de 3 ampollas de polvo, pero solo si el médico lo ha recetado. Si el médico ha recetado el medicamento Bravelle junto con Menopur, se pueden mezclar los dos medicamentos. Para ello, se debe reconstituir Menopur, inyectar lentamente la solución resultante en la ampolla con Bravelle, esperar a que Bravelle se disuelva, extraer la solución que contiene ambos medicamentos a la jeringa y administrarla por vía subcutánea. Este procedimiento permite evitar la inyección de cada medicamento por separado. ADMINISTRACIÓN DE MENOPUR:
- Después de extraer la dosis prescrita de Menopur a la jeringa, debe cambiar la aguja
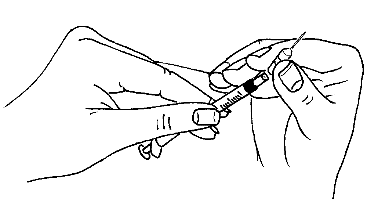
por una aguja corta y delgada (aguja para inyección).
- Colocar la jeringa en posición con la aguja hacia arriba y golpear suavemente con el dedo la jeringa para que las burbujas de aire se acumulen en la parte superior. Presionar suavemente el émbolo de la jeringa hasta que aparezca la primera gota de líquido en la punta de la aguja.
- La paciente es informada por el médico o la enfermera sobre dónde debe inyectar el medicamento (por ejemplo, parte delantera del muslo, abdomen, etc.).
- Desinfectar (desinfectar) la piel en el lugar de la inyección.
- Para realizar la inyección, debe crear un pliegue en la piel entre
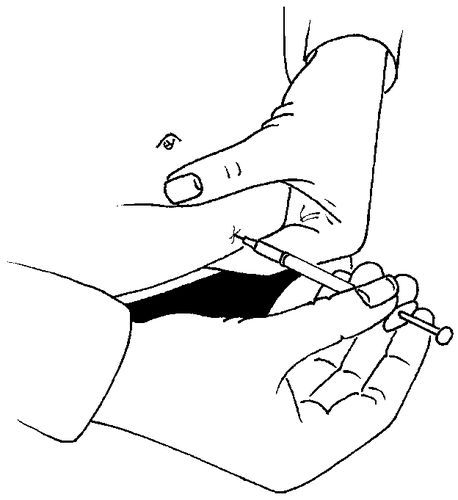
los dedos y, con un movimiento rápido, insertar la aguja en un ángulo de 90 grados (perpendicularmente). Inyectar la solución, presionando el émbolo de la jeringa, y luego retirar la aguja.
- Después de retirar la aguja, presionar el lugar de la inyección para evitar el sangrado. Un masaje suave en el lugar de la inyección ayuda a que la solución se disperse bajo la piel.
- No debe desechar los artículos usados en los contenedores de basura domésticos, sino eliminarlos de manera adecuada.
Sobredosis de Menopur
En caso de sobredosis de Menopur, debe informar a su médico.
Olvido de una dosis de Menopur
No debe tomar una dosis doble para compensar una dosis olvidada. En caso de olvido de una dosis de Menopur, debe informar a su médico.
4. Posibles efectos adversos
Como cualquier medicamento, Menopur puede causar efectos adversos, aunque no todos los pacientes los experimentarán. Las hormonas utilizadas para tratar la infertilidad, como Menopur, pueden causar una hiperestimulación ovárica, lo que puede llevar a una enfermedad llamada síndrome de hiperestimulación ovárica (OHSS), especialmente en mujeres con síndrome de ovario poliquístico. Los síntomas incluyen: dolor abdominal, hinchazón abdominal, náuseas, vómitos, diarrea e aumento de peso. En casos graves de OHSS, se han observado complicaciones como la acumulación de líquido en la cavidad abdominal, la cavidad pélvica y (o) la cavidad pleural, dificultades para respirar y disminución de la frecuencia o cantidad de orina, formación de coágulos en los vasos sanguíneos (trastornos trombóticos) y torsión ovárica. Si aparece alguno de estos síntomas, debe contactar a su médico de inmediato, incluso si aparecen varios días después de la última dosis del medicamento. Durante el tratamiento, pueden ocurrir reacciones alérgicas (hipersensibilidad). Los síntomas de estas reacciones pueden incluir: erupción, picazón, hinchazón de la garganta y dificultades para respirar. Si aparece alguno de estos síntomas, debe contactar a su médico de inmediato. Los siguientes efectos adversosson frecuentes, es decir, ocurren en 1 de cada 10 pacientes tratados: dolor abdominal; dolor de cabeza; náuseas; hinchazón abdominal; dolor pélvico; hiperestimulación ovárica; reacciones en el lugar de la inyección, como dolor, enrojecimiento, moretones, hinchazón y (o) picazón. Los siguientes efectos adversosson poco frecuentes, es decir, ocurren en 1 de cada 100 pacientes tratados: vómitos; trastornos abdominales; diarrea; fatiga; mareos; quistes ováricos; trastornos mamarios, incluyendo dolor mamario, sensibilidad mamaria, incomodidad, dolor en los pezones y hinchazón mamaria; sofocos. Los siguientes efectos adversosson raros, es decir, ocurren en 1 de cada 1000 pacientes tratados: acné; erupción. Además de los anteriormente mencionados, se han observado los siguientes efectos adversosdespués de la comercialización de Menopur, cuya frecuenciaes desconocida: trastornos de la visión; fiebre; malestar general; reacciones alérgicas; aumento de peso; dolor muscular y articular (por ejemplo, dolor de espalda, dolor de cuello y dolor en las extremidades); torsión ovárica, como complicación de la hiperestimulación ovárica; picazón; urticaria; coágulos sanguíneos, como complicación de la hiperestimulación ovárica.
Notificación de efectos adversos
Si aparecen efectos adversos, incluidos los efectos adversos no mencionados en este folleto, debe informar a su médico. Los efectos adversos pueden ser notificados directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad: calle, ciudad, código postal, teléfono, fax, correo electrónico. Los efectos adversos también pueden ser notificados al titular de la autorización de comercialización.
5. Cómo conservar Menopur
El medicamento debe ser conservado en un lugar fuera del alcance de los niños. No conservar a temperaturas superiores a 25°C. Conservar en el embalaje original para protegerlo de la luz. No usar este medicamento después de la fecha de caducidad indicada en el paquete y en las etiquetas de la ampolla y el frasco con el disolvente después de "EXP". La fecha de caducidad es el último día del mes indicado. Los medicamentos no deben ser tirados por el desagüe ni a los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se necesitan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Menopur
- El principio activo de Menopur es menotropina altamente purificada (gonadotropina menopáusica humana, hMG) en una cantidad equivalente a 150 IU de FSH (hormona folitropina) y 150 IU de LH (hormona luteinizante).
- Los demás componentes son:
- polvo: lactosa monohidratada, polisorbato 20, hidróxido de sodio (para ajustar el pH), ácido clorhídrico (para ajustar el pH)
- disolvente: cloruro de sodio, ácido clorhídrico al 10% (para ajustar el pH), agua para inyección
Cómo se presenta Menopur y qué contiene el paquete
Menopur es un polvo y disolvente para preparar una solución para inyección. En una caja de cartón hay 1 o 5 ampollas de vidrio incoloro que contienen el polvo. En una caja de cartón hay la misma cantidad de frascos de vidrio incoloro que contienen el disolvente. No todas las presentaciones pueden estar comercializadas.
Título de la autorización de comercialización
Ferring GmbH Wittland 11 D-24109 Kiel Alemania
Fabricante/Importador
Ferring GmbH Wittland 11 D-24109 Kiel Alemania
Fecha de la última revisión de este folleto
Para obtener más información sobre este medicamento, debe consultar al representante del titular de la autorización de comercialización: Ferring Pharmaceuticals Poland Sp. z o.o. ul. Szamocka 8, 01-748 Varsovia Tel.: +48 22 246 06 80, Fax: +48 22 246 06 81
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorFerring GmbH
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a MenopurForma farmacéutica: Polvo, 75 UI FSH + 75 UI LHPrincipio activo: human menopausal gonadotrophinFabricante: Ferring GmbHRequiere recetaForma farmacéutica: Polvo, 600 UI FSH + 600 UI LHPrincipio activo: human menopausal gonadotrophinRequiere recetaForma farmacéutica: Polvo, 1200 UI FSH + 1200 UI LHPrincipio activo: human menopausal gonadotrophinRequiere receta
Alternativas a Menopur en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Menopur en España
Alternativa a Menopur en Ucrania
Médicos online para Menopur
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Menopur – sujeta a valoración médica y normativa local.