

Fulvestrant Sandoz

Consulta con un médico sobre la receta médica de Fulvestrant Sandoz

Cómo usar Fulvestrant Sandoz
Hoja de instrucciones del paquete: información para el paciente
Fulvestrant Sandoz, 250 mg/5 ml, solución inyectable en jeringa precargada
Fulvestrant
Es importante leer detenidamente el contenido de la hoja de instrucciones antes de tomar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico, farmacéutico o enfermera.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos todos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Fulvestrant Sandoz y para qué se utiliza
- 2. Información importante antes de tomar Fulvestrant Sandoz
- 3. Cómo tomar Fulvestrant Sandoz
- 4. Posibles efectos adversos
- 5. Cómo conservar Fulvestrant Sandoz
- 6. Contenido del paquete y otra información
1 Qué es Fulvestrant Sandoz y para qué se utiliza
Fulvestrant Sandoz contiene el principio activo fulvestrant, que pertenece a una clase de medicamentos que bloquean la acción de los receptores de estrógeno.
Los estrógenos, hormonas femeninas, pueden participar en el desarrollo del cáncer de mama en algunos casos.
Fulvestrant Sandoz se utiliza:
- como medicamento único para el tratamiento de mujeres posmenopáusicas con un tipo específico de cáncer de mama, es decir, cáncer de mama con receptores de estrógeno, que es localmente avanzado o se ha extendido a otras partes del cuerpo (metástasis),
- en combinación con palbociclib para el tratamiento de mujeres con un tipo específico de cáncer de mama, es decir, cáncer de mama con receptores hormonales, sin sobreexpresión del receptor de crecimiento epidérmico humano 2, que es localmente avanzado o se ha extendido a otras partes del cuerpo (metástasis). Las mujeres premenopáusicas también recibirán un medicamento llamado agonista del hormona liberadora de lutropina (LHRH).
Cuando se administra Fulvestrant Sandoz con palbociclib, es importante leer también la hoja de instrucciones del paquete del medicamento que contiene palbociclib. En caso de dudas sobre palbociclib, debe consultar a su médico.
2. Información importante antes de tomar Fulvestrant Sandoz
Cuándo no tomar Fulvestrant Sandoz
si el paciente es alérgico al fulvestrant o a alguno de los demás componentes de este medicamento (enumerados en el punto 6);
si el paciente está embarazada o en período de lactancia;
si el paciente tiene trastornos hepáticos graves.
Precauciones y advertencias
Antes de tomar Fulvestrant Sandoz, debe discutir con su médico, farmacéutico o enfermera si alguno de los siguientes problemas de salud se aplica al paciente:
trastornos renales o hepáticos;
baja cantidad de plaquetas en la sangre (que participan en la coagulación) o trastornos de la coagulación;
enfermedad tromboembólica en el pasado;
osteoporosis (densidad ósea reducida);
enfermedad alcohólica.
Niños y adolescentes
Fulvestrant Sandoz no está indicado para su uso en niños y adolescentes menores de 18 años.
Fulvestrant Sandoz y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente o que planea tomar.
En particular, debe informar a su médico sobre el uso de medicamentos anticoagulantes (medicamentos que evitan la formación de coágulos sanguíneos).
Embarazo y lactancia
Si una mujer está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener un hijo, debe consultar a su médico antes de tomar este medicamento.
No se debe tomar Fulvestrant Sandoz durante el embarazo. Las mujeres en edad reproductiva deben usar métodos anticonceptivos efectivos durante el tratamiento y durante 2 años después de la última dosis.
No se debe amamantar durante el tratamiento con Fulvestrant Sandoz.
Conducción de vehículos y uso de máquinas
No se espera que Fulvestrant Sandoz afecte la capacidad de conducir vehículos o usar máquinas. Sin embargo, si el tratamiento causa somnolencia, no debe realizar estas actividades.
Fulvestrant Sandoz contiene etanol, alcohol bencílico y benzoato de bencilo
Este medicamento contiene 1000 mg de etanol (96%) por dosis, lo que equivale a 100 mg/ml (10% v/v). La cantidad de etanol en una dosis de este medicamento es equivalente a menos de 24 ml de cerveza o 10 ml de vino. La pequeña cantidad de etanol en este medicamento no causará efectos notables.
Este medicamento contiene 1000 mg de alcohol bencílico por dosis, lo que equivale a 100 mg/ml.
El alcohol bencílico puede causar reacciones alérgicas.
La administración de alcohol bencílico a niños pequeños se asocia con un riesgo de efectos adversos graves, incluyendo trastornos respiratorios (síndrome de "gasping").
No se debe administrar a recién nacidos (hasta 4 semanas de vida) sin la recomendación de un médico.
No se debe administrar a niños pequeños (menores de 3 años) durante más de una semana sin la recomendación de un médico o farmacéutico.
Los pacientes con enfermedades hepáticas o renales deben consultar a su médico antes de tomar el medicamento, ya que una gran cantidad de alcohol bencílico puede acumularse en su organismo y causar efectos adversos (acidosis metabólica).
Este medicamento contiene 1500 mg de benzoato de bencilo por dosis, lo que equivale a 150 mg/ml.
El benzoato de bencilo puede aumentar el riesgo de ictericia (decoloración amarilla de la piel y las membranas mucosas) en recién nacidos (hasta 4 semanas de vida).
3. Cómo tomar Fulvestrant Sandoz
Este medicamento debe tomarse siempre según las indicaciones de su médico o farmacéutico. En caso de dudas, debe consultar a su médico o farmacéutico.
La dosis recomendada de fulvestrant es 500 mg (dos inyecciones de 250 mg), administradas una vez al mes, y una dosis adicional de 500 mg administrada 2 semanas después de la primera dosis.
Fulvestrant Sandoz se administra por un médico o enfermera en una inyección lenta intramuscular, una en cada glúteo.
En caso de dudas adicionales sobre la administración de este medicamento, debe consultar a su médico, farmacéutico o enfermera.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
En caso de que se produzca alguno de los siguientes efectos adversos, puede ser necesario buscar ayuda médica de inmediato:
reacciones de hipersensibilidad (alergia), incluyendo hinchazón de la cara, los labios, la lengua y/o la garganta, que pueden ser síntomas de una reacción anafiláctica
coágulos con émbolos (aumento del riesgo de formación de coágulos sanguíneos)*
hepatitis
insuficiencia hepática
Debe informar a su médico, farmacéutico o enfermera sobre la ocurrencia de alguno de los siguientes efectos adversos:
Efectos adversos muy frecuentes(pueden ocurrir en más de 1 de cada 10 personas)
reacción en el lugar de la inyección, como dolor y/o inflamación;
actividad anormal de las enzimas hepáticas (detectada en análisis de sangre)*
náuseas
debilidad, fatiga*
dolor en las articulaciones y dolores óseos
calores
erupción cutánea
reacciones alérgicas (hipersensibilidad), incluyendo hinchazón de la cara, los labios, la lengua y/o la garganta
Todos los demás efectos adversos
Efectos adversos frecuentes(pueden ocurrir en menos de 1 de cada 10 personas)
dolor de cabeza
vómitos, diarrea o pérdida de apetito*
infecciones del tracto urinario
dolor de espalda*
aumento de la bilirrubina (pigmento de la bilis producido en el hígado)
coágulos con émbolos (aumento del riesgo de formación de coágulos sanguíneos)*
disminución de la cantidad de plaquetas en la sangre (trombocitopenia)
sangrado vaginal
dolor en la parte inferior de la espalda, que irradia a una pierna (ciática)
debilidad repentina, entumecimiento, hormigueo o pérdida de movilidad en una pierna (especialmente en un lado del cuerpo), dificultad para caminar o mantener el equilibrio (neuropatía periférica)
Efectos adversos poco frecuentes(pueden ocurrir en menos de 1 de cada 100 personas):
descarga vaginal espesa y blanquecina y candidiasis (infección)
formación de moretones y sangrado en el lugar de la inyección del medicamento
aumento de la actividad de la enzima hepática gamma-GT (detectada en análisis de sangre)
hepatitis
insuficiencia hepática
entumecimiento, hormigueo y dolor
reacciones anafilácticas
* efectos adversos en los que el papel exacto de Fulvestrant Sandoz no se ha establecido debido a la enfermedad subyacente
Notificación de efectos adversos
Si se producen efectos adversos, incluidos todos los efectos adversos no mencionados en la hoja de instrucciones, debe informar a su médico, farmacéutico o enfermera. Los efectos adversos se pueden notificar directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad:
tel.: +34 91 596 24 50 / fax: +34 91 596 24 51 / sitio web: https://www.aemps.gob.es/
Los efectos adversos también se pueden notificar al titular de la autorización de comercialización.
La notificación de efectos adversos permite recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Fulvestrant Sandoz
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
No se debe tomar este medicamento después de la fecha de caducidad que figura en el paquete de cartón o en la etiqueta de la jeringa precargada, después de "EXP". La fecha de caducidad es el último día del mes indicado.
Este medicamento no requiere condiciones de conservación especiales.
El personal sanitario es responsable de la conservación, uso y eliminación adecuados del paquete y el contenido del medicamento Fulvestrant Sandoz después de su uso.
No se debe tomar el medicamento si se observan signos de daño en la jeringa precargada o deterioro de su contenido, como turbidez de la solución, partículas flotando en ella o cambio de color.
No se deben tirar los medicamentos por el desagüe ni depositarlos en los contenedores de basura doméstica. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se necesitan. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Fulvestrant Sandoz?
El principio activo es fulvestrant.
Una jeringa precargada contiene 250 mg de fulvestrant en 5 ml de solución (50 mg/ml).
Los demás componentes son: etanol (96%), alcohol bencílico, benzoato de bencilo y aceite de ricino.
Cómo se presenta Fulvestrant Sandoz y qué contiene el paquete?
Fulvestrant Sandoz es una solución inyectable transparente, incolora a amarillenta, viscosa en una jeringa precargada.
El paquete contiene una o dos jeringas precargadas individuales. Además, el paquete contiene una aguja estéril.
Titular de la autorización de comercialización y fabricante
Titular de la autorización de comercialización
Sandoz GmbH
Biochemiestrasse 10
6250 Kundl, Austria
Fabricante
Lek Pharmaceuticals d.d.
Verovškova 57
1526 Liubliana, Eslovenia
EBEWE Pharma Ges.m.b.H. Nfg.KG
Mondseestrasse 11
4866 Unterach, Austria
Fareva Unterach GmbH
Mondseestraße 11
4866 Unterach, Austria
Para obtener información más detallada sobre el medicamento y sus nombres en los países del Espacio Económico Europeo, debe dirigirse a:
Sandoz España
Calle de María de Molina, 46
28006 Madrid
tel. 91 456 55 00
Fecha de la última revisión de la hoja de instrucciones:01/2022
Logotipo de Sandoz
Información destinada exclusivamente al personal sanitario:
La dosis de Fulvestrant Sandoz de 500 mg (2 x 250 mg/5 ml solución inyectable) debe administrarse utilizando dos jeringas precargadas (véase el punto 3).
Instrucciones de administración
Advertencia: no esterilizar la aguja con sistema de protección en el autoclave antes de su uso.
Al manipular el medicamento y eliminar los residuos, debe evitar el contacto de las manos con la aguja.
Las jeringas se suministran con una aguja con sistema de protección BD SafetyGlide o Terumo SurGuard .
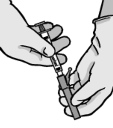
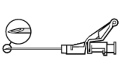
Instrucciones para la aguja con sistema de protección BD SafetyGlide
| |
| |
| |
|  |
| |
|
| |
|  |
| 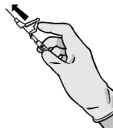 |
| ATENCIÓN: Proceda de esta manera para asegurar su propia seguridad y la de los demás. Escuche el clic y asegúrese visualmente de que la punta de la aguja esté completamente cubierta. | |
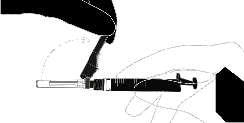
Instrucciones para la aguja con sistema de protección Terumo SurGuard
Se aplica a cada jeringa:
| |
|  |
|  |
| |
| |
| |
| 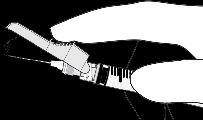 |
| o activación con el dedo índice | |
| o activación con el pulgar | 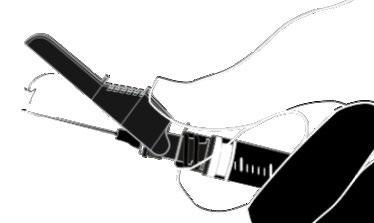 |
| o activación sobre la superficie | 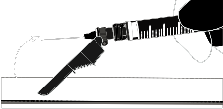 |
| La activación se confirma con un clic audible y/o palpable, y también se puede verificar visualmente. En caso de duda sobre si la cubierta ha cubierto completamente la aguja, debe repetir el paso final. | |
Eliminación
Las jeringas precargadas están destinadas únicamentepara un uso único.
Todos los residuos del producto o sus desechos deben eliminarse de acuerdo con las regulaciones locales.
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorEbewe Pharma Ges.m.b.H Nfg. KG Fareva Unterach GmbH LEK Pharmaceuticals d.d.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a Fulvestrant SandozForma farmacéutica: Solución, 250 mgPrincipio activo: FulvestrantNo requiere recetaForma farmacéutica: Solución, 250 mgPrincipio activo: FulvestrantRequiere recetaForma farmacéutica: Solución, 250 mg/ 5 mlPrincipio activo: FulvestrantRequiere receta
Alternativas a Fulvestrant Sandoz en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Fulvestrant Sandoz en España
Alternativa a Fulvestrant Sandoz en Ucrania
Médicos online para Fulvestrant Sandoz
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Fulvestrant Sandoz – sujeta a valoración médica y normativa local.












