
Cómo usar Divina
Hoja de instrucciones del paquete: información para el paciente
Es importante leer atentamente el contenido de la hoja de instrucciones antes de tomar el medicamento, ya que contiene
información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a su médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Divina y para qué se utiliza
- 2. Información importante antes de tomar Divina
- 3. Cómo tomar Divina
- 4. Posibles efectos adversos
- 5. Cómo conservar Divina
- 6. Contenido del paquete y otra información
1. Qué es Divina y para qué se utiliza
Divina es un medicamento cíclico, bifásico, destinado a ser utilizado en terapia hormonal sustitutiva (THS). El medicamento contiene dos tipos de hormonas femeninas, valerato de estradiol (estrógeno) y acetato de medroxiprogesterona (progestágeno).
Divina se utiliza para:
Aliviar los síntomas que ocurren después de la menopausia
Durante la menopausia, disminuye la cantidad de estrógeno producido por el organismo de la mujer. Esto puede provocar síntomas como sensación de calor en la cara, cuello y pecho („olas de calor”). Divina alivia estos síntomas que ocurren después de la menopausia. Divina se prescribe solo en casos en que los síntomas afectan significativamente la vida diaria de la paciente.
Prevenir la osteoporosis
Después de la menopausia, algunas mujeres desarrollan fragilidad ósea (osteoporosis). Todas las opciones disponibles deben ser discutidas con el médico. Si la paciente tiene un mayor riesgo de fracturas debido a la osteoporosis y otros medicamentos no son adecuados, se puede utilizar Divina para prevenir la osteoporosis.
La experiencia en el tratamiento de pacientes mayores de 65 años es limitada.
2. Información importante antes de tomar Divina
Historia médica y exámenes de control regulares
El uso de terapia hormonal sustitutiva (THS) conlleva un riesgo que debe ser considerado al tomar la decisión de iniciar o continuar la terapia.
Los casos de uso de terapia en mujeres con menopausia prematura (causada por insuficiencia ovárica o procedimientos quirúrgicos) son raros. En el caso de mujeres con menopausia prematura, el riesgo de usar THS puede ser diferente. Debe consultar a su médico.
Antes de iniciar (o reiniciar) la THS, el médico realizará una historia clínica y un examen físico de la paciente y su familia. El médico también puede realizar un examen físico, incluyendo un examen de los senos y (o) órganos internos, si es necesario.
Después de iniciar el tratamiento con Divina, debe asistir a controles regulares (al menos una vez al año). Durante estas visitas, debe discutir con su médico los beneficios y riesgos de continuar tomando Divina.
Debe realizar exámenes de los senos de acuerdo con las recomendaciones de su médico.
Cuándo no tomar Divina:
Si alguna de las siguientes condiciones se aplica a la paciente o si la paciente tiene dudas sobre alguna de las siguientes condiciones, debe consultar a su médicoantes de tomar Divina.
No debe tomar Divina:
- si es alérgica a los principios activoso a alguno de los demás componentes de este medicamento (enumerados en el punto 6),
- si ha tenido o tiene cáncer de mamao si se sospecha que lo tiene,
- si tiene cáncer de úteroo si se sospecha que lo tiene,
- si tiene sangrado vaginal de causa desconocida,
- si tiene hiperplasia endometrial no tratada,
- si ha tenido o tiene trombosis venosa(enfermedad tromboembólica venosa) de las extremidades inferiores (trombosis venosa profunda) o pulmonar (embolia pulmonar),
- si tiene trastornos de coagulación(como deficiencia de proteína C, proteína S o antitrombina),
- si ha tenido o tiene enfermedad arterial(como infarto de miocardio o accidente cerebrovascular),
- si tiene enfermedad hepáticay los resultados de las pruebas hepáticas no han vuelto a los valores normales,
- si tiene porfiria, una enfermedad hepática rara.
Si alguno de los factores anteriores ocurre por primera vez mientras toma Divina, debe dejar de tomar el medicamento y consultar a su médico de inmediato.
Precauciones y advertencias
Antes de iniciar el tratamiento con Divina, debe discutirlo con su médico o farmacéutico.
Antes de iniciar el tratamiento, debe informar a su médico sobre cualquier condición que tenga o haya tenido, ya que pueden empeorar o reaparecer durante el tratamiento con Divina. En los siguientes casos, debe aumentar la frecuencia de los controles:
- miomas uterinos (fibromas uterinos),
- endometriosis o hiperplasia endometrial previa,
- aumento del riesgo de trombosis,
- aumento del riesgo de cáncer de mama,
- hipertensión,
- enfermedad hepática,
- diabetes con o sin complicaciones vasculares,
- colelitiasis,
- cefalea o migraña,
- enfermedad autoinmune que afecta a muchos órganos (lupus eritematoso sistémico),
- epilepsia,
- asma,
- enfermedad que afecta la membrana del oído y la audición (otosclerosis),
- triglicéridos muy altos en la sangre,
- retención de líquidos debido a enfermedad cardíaca o renal,
- edema angioneurótico hereditario o adquirido.
Debe dejar de tomar Divina y consultar a su médico de inmediato
Si la paciente experimenta alguno de los siguientes síntomas mientras toma THS:
- cualquiera de las enfermedades enumeradas en el punto „Cuándo no tomar Divina”,
- ictericia (decoloración amarilla de la piel y los ojos); puede ser un signo de enfermedad hepática,
- edema de la cara, lengua y (o) garganta y (o) dificultad para tragar o erupción cutánea, junto con dificultad para respirar, que puede indicar angioedema,
- aumento significativo de la presión arterial; los síntomas pueden incluir dolor de cabeza, fatiga, mareo,
- cefalea de tipo migrañoso que aparece por primera vez,
- si la paciente queda embarazada,
- si nota signos de trombosis, como:
- hinchazón y enrojecimiento doloroso de las extremidades inferiores,
- dolor agudo en el pecho,
- dificultad para respirar. Más información está disponible en el punto „Trombosis venosa (trombosis)”.
Advertencia:Divina no es un medicamento anticonceptivo. Si han pasado menos de 12 meses desde la última menstruación o si la paciente tiene menos de 50 años, pueden ser necesarias medidas anticonceptivas adicionales para prevenir el embarazo. Debe consultar a su médico.
THS y cáncer
Hiperplasia endometrial y cáncer de endometrio
El uso de THS con solo estrógenos aumenta el riesgo de hiperplasia endometrial y cáncer de endometrio.
El uso de estrógenos en combinación con progestágeno, durante al menos 12 días por ciclo o de manera continua, reduce significativamente este riesgo adicional.
En mujeres con útero conservado que no toman THS, se diagnostica cáncer de endometrio en aproximadamente 5 de cada 1000 mujeres de 50 a 65 años.
En mujeres con útero conservado que toman THS con solo estrógenos, se diagnostica cáncer de endometrio en 10 a 60 de cada 1000 mujeres (es decir, de 5 a 55 casos adicionales), dependiendo de la dosis y la duración del tratamiento.
Sangrado irregular
Pueden ocurrir sangrados irregulares o manchados durante los primeros 3-6 meses de tratamiento con Divina. Si el sangrado irregular:
- dura más de 6 meses,
- aparece después de 6 meses de tratamiento con Divina,
- persiste después de dejar de tomar Divina, debe consultar a su médico de inmediato.
Cáncer de mama
Los datos confirman que tomar THS en forma de combinación de estrógeno y progestágeno o solo estrógeno aumenta el riesgo de cáncer de mama. El riesgo adicional depende de la duración del tratamiento con THS. Este riesgo adicional se hace evidente después de 3 años de tratamiento con THS. Después de dejar de tomar THS, el riesgo adicional disminuirá con el tiempo, pero puede persistir durante 10 años o más si la THS duró más de 5 años.
Comparación
En mujeres de 50 a 54 años que no toman THS, se diagnostica cáncer de mama en aproximadamente 13 a 17 de cada 1000 mujeres en un período de 5 años.
En mujeres de 50 años que comienzan una THS con estrógenos durante 5 años, el número de casos es de 16 a 17 de cada 1000 pacientes (es decir, 0 a 3 casos adicionales).
En mujeres de 50 años que comienzan una THS con estrógenos y progestágenos durante 5 años, el número de casos es de 21 de cada 1000 pacientes (es decir, 4 a 8 casos adicionales).
En mujeres de 50 a 59 años que no toman THS, se diagnostica cáncer de mama en aproximadamente 27 de cada 1000 mujeres en un período de 10 años.
En mujeres de 50 años que comienzan una THS con estrógenos durante 10 años, el número de casos es de 34 de cada 1000 pacientes (es decir, 7 casos adicionales).
En mujeres de 50 años que comienzan una THS con estrógenos y progestágenos durante 10 años, el número de casos es de 48 de cada 1000 pacientes (es decir, 21 casos adicionales).
Debe realizar exámenes de los senos de manera regular.Debe consultar a su médico si nota cambios como:
- arrugas en la piel,
- cambios en el pecho,
- cualquier bulto visible o palpable.
Además, se recomienda participar en programas de detección de cáncer de mama.
Es importante informar al personal médico que realiza la mammografía de que está tomando THS, ya que este medicamento puede causar un aumento en la densidad radiológica de los senos, lo que puede afectar el resultado de la mammografía. En áreas con mayor densidad, la mammografía puede no detectar todos los bultos.
Cáncer de ovario
El cáncer de ovario es raro, mucho menos común que el cáncer de mama. El uso de THS que incluye solo estrógenos o una combinación de estrógenos y progestágenos se asocia con un riesgo ligeramente aumentado de cáncer de ovario.
El riesgo de cáncer de ovario depende de la edad. Por ejemplo, en mujeres de 50 a 54 años que no toman THS, se diagnostica cáncer de ovario en aproximadamente 2 de cada 2000 mujeres en un período de 5 años. En mujeres que tomaron THS durante 5 años, se diagnostica en aproximadamente 3 de cada 2000 pacientes (es decir, 1 caso adicional).
Efecto de la THS en el corazón y la circulación
Trombosis venosa (trombosis)
El riesgo de desarrollar trombosis venosaes aproximadamente 1,3 a 3 veces mayor en mujeres que toman THS que en aquellas que no la toman, especialmente durante el primer año de tratamiento.
Las trombosis pueden tener consecuencias graves y, si un coágulo llega a los pulmones, puede causar dolor en el pecho, dificultad para respirar, pérdida de conocimiento o incluso la muerte.
La probabilidad de formación de coágulos en las venas aumenta con la edad y depende de la presencia de factores como:
- no poder caminar durante un período prolongado debido a una cirugía importante, lesión o enfermedad (véase también el punto 3 „Si necesita una operación”),
- obesidad (IMC > 30 kg/m2),
- trastornos de coagulación que requieren tratamiento a largo plazo con medicamentos anticoagulantes,
- si algún familiar cercano ha tenido un coágulo en una extremidad inferior, pulmón o otro órgano,
- ha tenido una cirugía importante,
- tiene lupus eritematoso sistémico,
- tiene cáncer,
- si está embarazada o en el posparto.
Los síntomas de trombosis se pueden encontrar en el punto „Debe dejar de tomar Divina y consultar a su médico de inmediato”.
Comparación
En mujeres de 50 a 59 años que no toman THS, es probable que ocurra una trombosis venosa en aproximadamente 4 a 7 de cada 1000 mujeres en un período de 5 años.
En mujeres de 50 a 59 años que tomaron THS con estrógenos y progestágenos durante más de 5 años, es probable que ocurra una trombosis venosa en 9 a 12 de cada 1000 pacientes (es decir, 5 casos adicionales).
Enfermedad cardíaca (infarto de miocardio)
No hay evidencia científica que respalde que la THS pueda prevenir los infartos de miocardio.
Las mujeres mayores de 60 años que toman THS con estrógenos y progestágenos tienen un riesgo ligeramente mayor de enfermedad cardíaca que aquellas que no toman THS.
Accidente cerebrovascular
El riesgo de sufrir un accidente cerebrovascular es aproximadamente 1,5 veces mayor en mujeres que toman THS que en aquellas que no la toman. El número de casos adicionales de accidente cerebrovascular debido a la THS aumenta con la edad.
Comparación
En mujeres de 50 a 59 años que no toman THS, es probable que ocurra un accidente cerebrovascular en aproximadamente 8 de cada 1000 mujeres en un período de 5 años. En mujeres de 50 a 59 años que toman THS, es probable que ocurra un accidente cerebrovascular en 11 de cada 1000 pacientes en un período de 5 años (es decir, 3 casos adicionales).
Otras afecciones
- La THS no previene la pérdida de función cognitiva. Hay evidencia de que el riesgo de demencia aumenta en mujeres que comienzan la THS después de los 65 años. Debe consultar a su médico.
- Los estrógenos pueden causar retención de líquidos, especialmente en pacientes con enfermedad cardíaca o renal.
- La THS puede afectar los resultados de algunas pruebas endocrinológicas y de función hepática. Debe informar a su médico sobre la ingesta de Divina antes de realizar este tipo de pruebas.
- La paciente debe informar a su médico si sabe que tiene triglicéridos altos en la sangre. En casos muy raros, se ha observado que el aumento significativo de los triglicéridos en la sangre durante el tratamiento con estrógenos puede causar pancreatitis.
- Divina no previene el embarazo. Por lo tanto, no debe usarse como método anticonceptivo.
Divina y otros medicamentos
Algunos medicamentos pueden interferir con la acción de Divina. Esto puede causar sangrados irregulares. Se aplica a los siguientes medicamentos:
- medicamentos utilizados para tratar la epilepsia(como fenobarbital, fenitoína y carbamazepina),
- medicamentos utilizados para tratar la tuberculosis(como rifampicina, rifabutina),
- medicamentos utilizados para tratar la infección por VIH o hepatitis C
- (inhibidores de proteasa y inhibidores no nucleósidos de la transcriptasa inversa, como nevirapina, efavirenz, ritonavir y nelfinavir),
- medicamentos herbales que contienen Hypericum perforatum(hierba de San Juan).
La terapia hormonal sustitutiva con estrógeno puede afectar la forma en que funcionan otros medicamentos. Se aplica a los siguientes medicamentos:
- medicamento utilizado para tratar la epilepsia- lamotrigina, ya que puede aumentar el riesgo de convulsiones.
- medicamentos utilizados para tratar la hepatitis C(como el esquema de tratamiento combinado con ombitasvir/paritaprevir/ritonavir con dasabuvir o sin dasabuvir, y el esquema de tratamiento combinado con glecaprevir/pibrentasvir), ya que pueden causar un aumento en los resultados de las pruebas de función hepática [aumento de la actividad de la enzima hepática, alanina aminotransferasa (ALAT)] en mujeres que toman productos anticonceptivos hormonales combinados que contienen etinilestradiol. No se sabe si la ingesta simultánea de Divina con estos esquemas de tratamiento para la hepatitis C puede causar un aumento en la actividad de la enzima ALAT.
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando actualmente, recientemente o potencialmente en el futuro, incluyendo los que se venden sin receta, los medicamentos herbales o otros productos naturales. Su médico le dará consejos al respecto.Pruebas de laboratorio
Si es necesario realizar una prueba de sangre, debe informar al personal del laboratorio sobre la ingesta de Divina, ya que puede afectar los resultados de algunas pruebas.
Embarazo y lactancia
Divina está indicada solo para mujeres posmenopáusicas. Si la paciente queda embarazada, debe dejar de tomar Divina y consultar a su médico.
La ingesta de Divina está contraindicada durante la lactancia.Conducción de vehículos y uso de maquinaria
No se ha demostrado que el medicamento afecte la capacidad de conducir vehículos o usar maquinaria.
Divina contiene lactosa.
Si se ha diagnosticado previamente una intolerancia a algunos azúcares, la paciente debe consultar a su médico antes de tomar el medicamento.
Una tableta blanca contiene 86,6 mg de lactosa, y una tableta azul contiene 72,0 mg de lactosa.3. Cómo tomar Divina
Este medicamento debe tomarse siempre según las indicaciones de su médico. En caso de dudas, debe consultar a su médico. El médico tratará de recetar la dosis más baja necesaria para tratar los síntomas, durante el período más corto posible. Si la paciente considera que la dosis es demasiado alta o demasiado baja, debe informar a su médico.
Divina debe tomarse según las instrucciones del paquete de calendario, una tableta al día en ciclos de 21 días sin interrupción, seguido de 7 días de pausa. Durante este período, la mayoría de las mujeres experimentan un sangrado de retirada similar a la menstruación. Se recomienda tomar la tableta por la noche.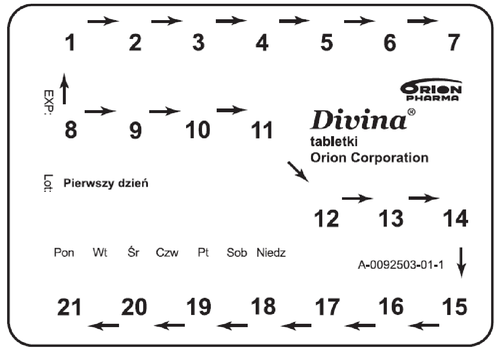
- 1. En cada blíster, hay una inscripción „Primer día” con los días de la semana siguientes marcados. Debe marcar en el blíster (por ejemplo, haciendo un agujero) el día de la semana en que comienza el tratamiento. De esta manera, puede verificar fácilmente si ha tomado las tabletas según el calendario.
- 2. Las mujeres posmenopáusicas pueden comenzar el tratamiento en cualquier momento. Las mujeres que aún menstrúan deben comenzar el tratamiento en el quinto día del ciclo menstrual (en el quinto día después del inicio de la menstruación).
- 3. En mujeres que no toman THS o en mujeres que cambian de otro medicamento de THS a Divina, el tratamiento puede comenzar en cualquier día conveniente.
- 4. En mujeres que cambian de un tratamiento cíclico o secuencial continuo de THS, el tratamiento con Divina debe comenzar al día siguiente de completar el ciclo de tratamiento anterior (de 28 días).
- 5. Las tabletas deben tomarse en el orden indicado en el paquete - primero las blancas, luego las azules. Después de este período, sigue una pausa de 7 días. Durante este tiempo, la mayoría de las mujeres experimentan un sangrado de retirada.
- 6. El siguiente ciclo de tratamiento debe comenzar el mismo día de la semana en que se inició el primer ciclo. Es posible que algunas mujeres no experimenten sangrado durante la pausa de 7 días en el tratamiento o que solo lo experimenten en algunos ciclos.
En caso de sangrado
Durante los primeros meses de tratamiento, pueden ocurrir sangrados y manchados. Debe consultar a su médico si experimenta sangrados prolongados o irregulares. Puede ser útil registrar las fechas de los sangrados, ya que su médico puede preguntar sobre su ocurrencia durante las visitas.
Si la paciente considera que el efecto de Divina es demasiado fuerte o demasiado débil, no debe cambiar la dosis o dejar de tomar el medicamento sin consultar antes a su médico.Si es necesario someterse a una operación
Antes de la operación, debe informar al cirujano sobre la ingesta de Divina. Es posible que sea necesario dejar de tomar Divina durante 4 a 6 semanas antes de la operación para reducir el riesgo de trombosis (véase el punto 2 „Trombosis venosa”). Debe consultar a su médico sobre cuándo puede volver a tomar Divina.
Si se toma una dosis mayor de la recomendada de Divina
No se han observado efectos graves de sobredosis después de la ingesta de dosis altas de medicamentos utilizados en la THS. La sobredosis de estrógeno puede causar náuseas, dolor de cabeza y sangrado vaginal. En caso de tomar una dosis mayor de la recomendada, debe consultar a su médico o farmacéutico de inmediato.
Si se olvida una dosis de Divina
Si no se toma una tableta, debe tomarla al día siguiente por la mañana y tomar la tableta correspondiente a ese día por la noche. Si la paciente olvida tomar una tableta, debe continuar con el tratamiento con la siguiente tableta. Puede ocurrir un sangrado ligero durante el ciclo.
En caso de planificar un viaje largo, la paciente debe asegurarse de tener suficientes tabletas.
No debe tomar una dosis doble para compensar una dosis olvidada.Si se deja de tomar Divina
En caso de dudas adicionales sobre la ingesta de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Divina puede causar efectos adversos, especialmente durante los primeros meses de tratamiento. Por lo general, son leves y desaparecen durante el tratamiento.
Los efectos adversos más comunes durante el tratamiento con Divina son dolor de cabeza y sensibilidad en los senos (en aproximadamente el 10% de las pacientes).
Las siguientes enfermedades se informan con más frecuencia en mujeres que toman THS que en aquellas que no la toman:- cáncer de mama,
- hiperplasia endometrial o cáncer de endometrio,
- cáncer de ovario,
- trombosis venosa en las extremidades inferiores o pulmones (enfermedad tromboembólica venosa),
- enfermedad cardíaca,
- accidente cerebrovascular,
- riesgo de demencia, si se inicia la THS después de los 65 años.
Más información sobre los efectos adversos anteriores se encuentra en el punto 2.
Frecuentes (pueden ocurrir en hasta 1 de cada 10 personas)
- aumento de peso,
- disminución de peso,
- dolor de cabeza, mareo,
- náuseas, vómitos, calambres abdominales, gases intestinales,
- flujo vaginal, infecciones del tracto urinario, trastornos del ciclo menstrual,
- irritación de la piel, picazón en el lugar de aplicación, dolor, aumento de la transpiración,
- sensibilidad o dolor en los senos,
- sangrado o manchado, menstruación irregular,
- depresión, nerviosismo, letargo,
- edema,
- olas de calor.
Poco frecuentes (pueden ocurrir en hasta 1 de cada 100 personas)
- cambios de humor, trastornos del deseo sexual, ansiedad, insomnio, apatía, inestabilidad emocional, trastornos de la concentración, euforia, agitación,
- migraña, entumecimiento, convulsiones,
- trastornos de la visión, sequedad en los ojos,
- hipertensión, trombosis venosa superficial, erupción cutánea,
- disnea, resfriado,
- adenoma mamario o endometrial,
- aumento del apetito, colesterol alto en la sangre,
- palpitaciones,
- estreñimiento, diarrea, enfermedad del ano,
- acné, alopecia, sequedad de la piel, enfermedad de las uñas, queratosis, hipertricosis, eritema nodoso, urticaria,
- dolor en las articulaciones, calambres musculares,
- aumento de la frecuencia urinaria y (o) necesidad de orinar, incontinencia urinaria, cistitis, cambios en el color de la orina, hematuria,
- sensibilidad o edema en los senos, hiperplasia endometrial, enfermedad uterina,
- fatiga, resultados anormales de pruebas de laboratorio, debilidad, fiebre, gripe, malestar general,
- hipersensibilidad.
Raros (pueden ocurrir en hasta 1 de cada 1000 personas)
- trombosis venosa (por ejemplo, trombosis venosa profunda de las extremidades inferiores o trombosis venosa de la pelvis y embolia pulmonar),
- trastornos de la función hepática y del flujo biliar,
- erupción cutánea,
- intolerancia a las lentes de contacto,
- dismenorrea, síndrome premenstrual.
Desconocidos (frecuencia no puede establecerse a partir de los datos disponibles)
- miomas uterinos,
- exacerbación de la angioedema hereditaria o adquirida,
- trastornos de la circulación cerebral (episodios de isquemia cerebral),
- dolor abdominal, distensión abdominal,
- enfermedades hepáticas que causan ictericia (ictericia colestásica),
- erupción cutánea.
Los siguientes efectos adversos se han observado en otros tratamientos con THS:
- infarto de miocardio,
- enfermedades de la vesícula biliar,
- diferentes trastornos de la piel y el tejido subcutáneo:
- manchas en la piel, especialmente en la cara o el cuello, conocidas como „melasma” (cloasma),
- erupción cutánea con manchas rojas en forma de anillo o úlceras (eritema multiforme),
- erupción cutánea con manchas rojas en forma de anillo o úlceras (eritema nodoso).
Notificación de efectos adversos
Si ocurren efectos adversos, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico.
Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad
Calle Alcalá, 56, 28071 Madrid
Teléfono: +34 91 596 44 00
Fax: +34 91 596 44 01
Sitio web: https://www.aemps.gob.es/
Los efectos adversos también pueden notificarse al titular de la autorización de comercialización.
La notificación de efectos adversos permite recopilar más información sobre la seguridad del medicamento.5. Cómo conservar Divina
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
No debe tomar este medicamento después de la fecha de caducidad que se indica en el paquete después de „Caducidad (EXP)”. La fecha de caducidad es el último día del mes indicado.
No debe conservar a temperaturas superiores a 25°C.
No debe tirar los medicamentos por el desagüe ni a los contenedores de basura domésticos. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no necesita. Este comportamiento ayudará a proteger el medio ambiente.6. Contenido del paquete y otra información
Qué contiene Divina
Una tableta blanca contiene:
- El principio activo es: 2 mg de valerato de estradiol.
- Los demás componentes son: lactosa monohidratada, almidón de maíz, gelatina, talco, estearato de magnesio.
Una tableta azul contiene:
- Los principios activos son: 2 mg de valerato de estradiol y 10 mg de acetato de medroxiprogesterona.
- Los demás componentes son: lactosa monohidratada, almidón de maíz, indigotina (E 132), gelatina, polivinilo, talco, estearato de magnesio.
Cómo se presenta Divina y qué contiene el paquete
Tamaño del paquete
El blíster contiene 21 tabletas (11 blancas + 10 azules).
1 o 3 blísteres en una caja de cartón.Título del responsable y fabricante
Responsable
CS 50070
Lys Lez Lannoy 59452
Francia
Para obtener más información sobre este medicamento, debe consultar al representante local del responsable:
Orion Pharma Poland Sp. z o.o.
[email protected]Fecha de la última actualización de la hoja de instrucciones:
- País de registro
- Principio activo
- Requiere recetaSí
- Fabricante
- ImportadorDELPHARM LILLE S.A.S. Orion Corporation
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a DivinaForma farmacéutica: Comprimidos, 2 mg (blancas), 2 mg + 0,5 mg (marrón claro)Principio activo: norgestrel and estrogenFabricante: Bayer AG Bayer Weimar GmbH und Co. KGRequiere recetaForma farmacéutica: Comprimidos, 1 mg (blanca), 1 mg + 10 mg (gris)Principio activo: dydrogesterone and estrogenFabricante: Abbott Biologicals B.V.Requiere recetaForma farmacéutica: Comprimidos, 1 mg (blanco), 1 mg + 10 mg (gris)Principio activo: dydrogesterone and estrogenRequiere receta
Alternativas a Divina en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Divina en Spain
Médicos online para Divina
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Divina – sujeta a valoración médica y normativa local.






