
Anbinex

Consulta con un médico sobre la receta médica de Anbinex

Cómo usar Anbinex
HOJA DE INSTRUCCIONES DEL PAQUETE: INFORMACIÓN PARA EL USUARIO
Anbinex
50 UI/ml; 500 UI y 1000 UI
Polvo y disolvente para la preparación de una solución para infusión. Antitrombina III humana densificada
Es importante leer el folleto antes de tomar el medicamento, ya que contiene información importante para el paciente
- Debe conservar este folleto para poder volver a leerlo si es necesario.
- En caso de dudas, debe consultar a su médico, farmacéutico o enfermera
- Este medicamento ha sido recetado específicamente para usted. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en este folleto, debe informar a su médico, farmacéutico o enfermera. Véase el punto 4.
Índice del folleto:
- 1. Qué es Anbinex y para qué se utiliza
- 2. Información importante antes de tomar Anbinex
- 3. Cómo tomar Anbinex
- 4. Posibles efectos adversos
- 5. Cómo conservar Anbinex
- 6. Contenido del paquete y otra información
1. Qué es Anbinex y para qué se utiliza
Anbinex es
un medicamento
anticoagulante,
pertenece
a la clase
de medicamentos
anticoagulantes
parenterales.
Este medicamento se utiliza para tratar la deficiencia congénita de antitrombina, para prevenir
la formación de trombosis venosas profundas en las extremidades inferiores y
cambios tromboembólicos en otros vasos sanguíneos.
Si hay indicaciones para ello, también se administra durante procedimientos quirúrgicos y
durante el período periparto. En algunos casos, puede administrarse en combinación con heparina.
Anbinex también se utiliza en la deficiencia adquirida de antitrombina.
2. Información importante antes de tomar Anbinex
Cuándo no tomar Anbinex
Si el paciente es alérgico a la antitrombina o a cualquier otro componente de este
medicamento (enumerados en el punto 6).
Debe leer la información importante al final de este punto.
Advertencias y precauciones
Antes de comenzar a tomar Anbinex, debe discutirlo con su médico, farmacéutico o
enfermera.
Al igual que con otros productos administrados por vía intravenosa, es posible que ocurran reacciones
alérgicas. Durante la infusión, el paciente debe ser estrechamente monitorizado debido al riesgo
de efectos adversos. En caso de experimentar síntomas de reacción de hipersensibilidad,
incluyendo erupciones, urticaria generalizada, sensación de opresión en el pecho, respiración
sibilante (dificultad para respirar), hipotensión y síntomas de anafilaxia, debe informar
inmediatamente a su médico.
- selección detallada de donantes de sangre y plasma, cuyo objetivo es excluir a los donantes que puedan ser una fuente de infección;
- análisis de cada donación y lote de plasma recolectado para detectar la presencia de virus / factores infecciosos;
- inclusión de etapas en el proceso de procesamiento del plasma, durante las cuales los virus pueden ser inactivados o eliminados.
A pesar de la implementación de estas medidas de prevención, no se puede excluir completamente la posibilidad de transmisión de infección si se administran medicamentos producidos a partir de sangre o plasma humanos. Esto también se aplica a los virus y patógenos desconocidos o recién descubiertos.
Se considera que las medidas de prevención adoptadas son efectivas contra los virus envueltos,
como el virus de la inmunodeficiencia humana adquirida (VIH), el virus de la hepatitis B, el virus
de la hepatitis C y el virus de la hepatitis A no envuelto. Las medidas anteriores pueden tener
un valor limitado en el caso de los virus no envueltos, como el parvovirus B19.
La infección por parvovirus B19 puede ser particularmente grave en mujeres embarazadas (infección
fetal) y en personas con sistema inmunitario debilitado o que padecen ciertos tipos de anemia
(por ejemplo, anemia falciforme, anemia hemolítica).
En pacientes que reciben regularmente / múltiples dosis de antitrombina humana derivada de plasma,
el médico puede recomendar la vacunación contra el virus de la hepatitis A y B.
Se recomienda encarecidamente que, en cada administración de Anbinex al paciente, se registre el
nombre del paciente y el número de lote del producto, para poder vincular al paciente con el lote
del medicamento.
Anbinex y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté tomando
actualmente o recientemente, así como sobre los medicamentos que planea tomar.
La administración de antitrombina al mismo tiempo que dosis terapéuticas de heparina aumenta
el riesgo de sangrado. El efecto de la antitrombina se potencia significativamente con la heparina.
La administración concomitante de heparina a pacientes con mayor riesgo de sangrado debe
ser monitoreada cuidadosamente desde el punto de vista clínico y biológico.
Embarazo y lactancia
Si la paciente está embarazada o en período de lactancia, sospecha que puede estar embarazada
o planea tener un hijo, debe consultar a su médico o farmacéutico antes de tomar este
medicamento.
Anbinex debe utilizarse durante el embarazo y la lactancia solo si es estrictamente necesario.
La decisión debe tomarse después de considerar que, durante el embarazo, existe un mayor
riesgo de tromboembolismo.
Conducción de vehículos y uso de máquinas
Anbinex no tiene o tiene un efecto mínimo sobre la capacidad para conducir vehículos y
utilizar máquinas.
Anbinex contiene sodio
Anbinex 500 UI contiene 1,45 mmol (33,35 mg) de sodio en 10 ml.
Anbinex 1000 UI contiene 2,90 mmol (66,7 mg) de sodio en 20 ml
Debe llamar la atención de los pacientes que están en dietas con restricción de sal.
3. Cómo tomar Anbinex
El medicamento Anbinex para administración por infusión intravenosa debe ser preparado
por un médico o enfermera.
Uso en niños y adolescentes
Debido a la falta de datos suficientes, no se recomienda el uso de Anbinex en niños menores
de 6 años.
Frecuencia de administración
El médico determinará la frecuencia de administración de Anbinex y los intervalos entre
dosis.
Duración del tratamiento
El médico determinará la duración del tratamiento con Anbinex.
En caso de sobredosis de Anbinex
No se han notificado casos de sobredosis.
4. Posibles efectos adversos
Como cualquier medicamento, este medicamento puede causar efectos adversos, aunque no
todos los pacientes los experimentarán.
En casos raros, se ha observado un aumento de la temperatura corporal y reacciones
alérgicas o anafilácticas, como enrojecimiento de la cara, erupciones, aumento o disminución
de la presión arterial, taquicardia (aceleración del ritmo cardíaco), escalofríos, respiración
sibilante y edema, así como reacciones generalizadas (incluyendo dolor en el pecho, fiebre,
dolor de cabeza, náuseas y / o vómitos), que en algunos casos han llevado al desarrollo de
una reacción anafiláctica grave (incluyendo shock).
En casos raros, se ha observado un aumento de la temperatura corporal.
Lista de efectos adversos en forma de tabla.
La frecuencia de ocurrencia se evaluó utilizando los siguientes criterios:
- muy frecuente (> 1/10),
- frecuente (> 1/100, <1>
- no muy frecuente (> 1/1000, <1>
- raros (> 1/10 000, <1>
- muy raros (<1>
- frecuencia desconocida (frecuencia no puede ser determinada a partir de los datos disponibles)
| Sistema de clasificación MedDRA (SOC) | Reacción adversa | Frecuencia de ocurrencia |
| Trastornos del sistema inmunológico | Reacciones alérgicas, hipersensibilidad | No muy frecuente |
| Trastornos psiquiátricos | Ansiedad | No muy frecuente |
| Trastornos del sistema nervioso | Dolor de cabeza, letargia | No muy frecuente |
| Trastornos del sistema cardiovascular | Taquicardia | No muy frecuente |
| Trastornos vasculares | Enrojecimiento de la cara, disminución de la presión arterial, shock | No muy frecuente |
| Trastornos del sistema respiratorio, torácico y mediastínico | Sensación de opresión en el pecho y sibilancias | No muy frecuente |
| Trastornos gastrointestinales | Náuseas, vómitos, | No muy frecuente |
| Trastornos de la piel y del tejido subcutáneo | Edema angioneurótico, urticaria generalizada, erupciones | No muy frecuente |
| Trastornos generales y condiciones en el lugar de administración | Dolor o sensación de quemazón en el lugar de administración, escalofríos | No muy frecuente |
| Fiebre | Raro |
Debe informar a su médico si experimenta alguno de estos síntomas.
Información sobre las medidas de seguridad para prevenir la transmisión de agentes infecciosos - véase
el punto 2.
Si ocurren efectos adversos, incluidos los efectos adversos no mencionados en este folleto, debe
informar a su médico, farmacéutico o enfermera.
Los efectos adversos
se pueden
notificar
directamente
al
Departamento de Vigilancia de Medicamentos de la Agencia de Registros de Medicamentos,
Dispositivos Médicos y Productos Biocidas:
Al. Jerozolimskie 181C,
02-222 Varsovia,
Tel.: + 48 22 49 21 301,
Fax: + 48 22 49 21 309,
correo electrónico: [email protected]
Los efectos adversos también se pueden notificar al titular de la autorización de comercialización.
Gracias a la notificación de los efectos adversos, se pueden recopilar más información sobre la
seguridad del medicamento.
5. Cómo conservar Anbinex
El medicamento debe conservarse en un lugar no visible y no accesible para los niños.
No debe utilizarse después de la fecha de caducidad (EXP) impresa en la etiqueta. La fecha
de caducidad es el último día del mes indicado
No debe conservarse a una temperatura superior a 30 ° C. No debe congelarse.
Después de la reconstitución:
Los estudios de estabilidad indican un período de validez de hasta 12 horas a 25 ° C. Desde
el punto de vista microbiológico, el producto debe utilizarse de inmediato. Si después de la
reconstitución el producto no se ha utilizado, puede conservarse durante un máximo de 24
horas a una temperatura de 2 ° C - 8 ° C, pero solo si el usuario asume la responsabilidad
y la preparación de la solución se ha realizado de acuerdo con las normas de asepsia.
La solución debe ser transparente y ligeramente opalescente.
No debe utilizarse este medicamento si se observan grumos o sedimentos.
Los medicamentos no deben tirarse por el desagüe ni a los contenedores de basura doméstica.
Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no se utilizan.
Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Anbinex?
El principio activo del medicamento es la antitrombina humana.
El frasco con polvo contiene 500 UI o 1000 UI de antitrombina humana.
Después de la reconstitución, el producto contiene 50 UI / ml (500 UI / 10 ml o 1000 UI / 20
ml) de antitrombina humana.
Los demás componentes son: D-mannitol, cloruro de sodio y citrato de sodio.
La jeringa con aguja contiene 10 ml o 20 ml de agua para inyección.
Para obtener más información sobre los componentes, véase el punto 2.
Cómo se presenta Anbinex y qué contiene el paquete?
El paquete contiene un frasco con una sustancia blanca, higroscópica, quebradiza o polvo y
una jeringa con agua para inyección.
Cada paquete de Anbinex 500 UI contiene un frasco con 500 UI de antitrombina humana
(polvo para la preparación de una solución para infusión)
y
1
jeringa
con
10
ml
de agua
para
inyección (disolvente).
Cada paquete de Anbinex 1000 UI contiene un frasco con 1000 UI de antitrombina humana
(polvo para la preparación de una solución para infusión)
y
1
jeringa
con
20
ml
de agua
para
inyección (disolvente).
Con cada paquete de Anbinex se proporciona un conjunto para la preparación de la solución que
incluye un conector de sujeción para el frasco y un microfiltro.
Título del responsable y fabricante
Instituto Grifols, S.A.
Polígono Levante, c/Can Guasch, 2Parets del Vallès
08150 Barcelona, ESPAÑA.
Para obtener información más detallada, debe dirigirse al representante del titular de la
autorización de comercialización.
Grifols Polska Sp. z o. o.
Ul. Grzybowska 87, 00-844 Varsovia
Tel.: + 48 22 5040641
Fecha de la última actualización del folleto:
----------------------------------------------------------------------------------------------------------------
Información destinada exclusivamente al personal médico especializado:
En la deficiencia congénita, la dosis y la duración del tratamiento deben adaptarse
individualmente para cada paciente en función del resultado de la historia familiar que tenga
en cuenta los casos de cambios tromboembólicos, los factores de riesgo clínico actuales y los
resultados de las pruebas de laboratorio.
La dosis y la duración del tratamiento de la sustitución en la deficiencia adquirida de antitrombina
dependen del nivel de antitrombina en el suero, la presencia de síntomas que indiquen un
consumo acelerado, la enfermedad subyacente y la gravedad de los síntomas clínicos. El
tamaño de las dosis y la frecuencia de administración deben adaptarse siempre individualmente
para cada paciente, en función de los efectos clínicos.
La dosis de antitrombina administrada se expresa en unidades internacionales (UI), de acuerdo
con las normas actuales de la OMS. La actividad de la antitrombina en el suero puede expresarse
en porcentajes (en relación con la actividad en el suero normal) o en unidades internacionales
(de acuerdo con el estándar internacional para la antitrombina del suero).
Una unidad internacional (UI) de actividad de la antitrombina equivale a la cantidad media de
antitrombina en 1 ml de suero humano normal. El cálculo de la dosis necesaria de antitrombina
se basa en la observación empírica de que la administración de 1 UI de antitrombina por kg
de peso corporal aumenta la actividad de la antitrombina en el suero en aproximadamente
1,1 % a 1,6 %.
La dosis inicial se calcula según la siguiente fórmula:
Cantidad de unidades necesarias = peso corporal (kg) x (100 – actividad de antitrombina inicial (en porcentaje) x 0,8
En la fase inicial del tratamiento, debe establecerse el nivel deseado de actividad de la
antitrombina en función de la situación clínica. Después de establecer las indicaciones para
la administración de antitrombina, debe administrarse una dosis para alcanzar el nivel deseado
de actividad de la antitrombina y, a continuación, mantener su nivel para garantizar la
eficacia del tratamiento.
La dosis debe calcularse y monitorearse sobre la base de los resultados de las pruebas
de laboratorio de la actividad de la antitrombina en el suero. Las pruebas deben realizarse
al menos dos veces al día, y cuando el estado del paciente se estabilice, una vez al día;
siempre justo antes de la siguiente administración del medicamento. Debe tenerse en cuenta
que, en el caso de estados clínicos graves, como el síndrome de coagulación intravascular
diseminada, el período de persistencia de la antitrombina puede ser significativamente
más corto. La corrección del tamaño de la dosis debe realizarse teniendo en cuenta tanto la
velocidad de consumo de la antitrombina determinada por los resultados de las pruebas
de laboratorio como el curso clínico. La actividad de la antitrombina debe mantenerse por
encima del 80 % de la norma durante todo el período de tratamiento o adaptarse
adecuadamente cuando los síntomas clínicos indiquen que otro nivel puede ser más eficaz.
En el tratamiento de la deficiencia congénita, la dosis inicial es de 30 a 50 UI / kg de peso
corporal.
A continuación, el tamaño de la dosis, la frecuencia de administración y la duración del
tratamiento dependen de la respuesta biológica en una situación clínica determinada.
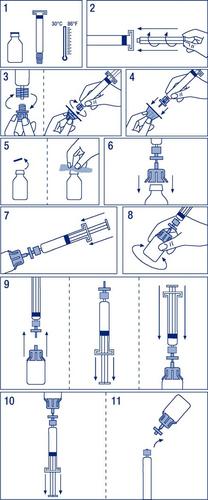
Instrucciones para la preparación del medicamento para su administración
- 1. Calentar los frascos a una temperatura no superior a 30 ° C (dibujo n. ° 1).
- 2. Fijar el émbolo en la jeringa con el disolvente (dibujo n. ° 2).
- 3. Retirar el filtro de su embalaje. Retirar la cubierta de plástico del extremo de la jeringa y
fijar el filtro (dibujo n. ° 3). - 4. Retirar el conector de sujeción del frasco y conectar la jeringa con el filtro (dibujo n. ° 4).
- 5. Retirar la cubierta de plástico del frasco y descubrir el tapón de goma y desinfectarlo con
un desinfectante (dibujo n. ° 5). - 6. Perforar el tapón del frasco con la aguja del conector (dibujo n. ° 6).
- 7. Inyectar todo el disolvente en el frasco (dibujo n. ° 7).
- 8. Agitar suavemente el frasco hasta que el polvo se disuelva (dibujo n. ° 8).
- 9. Desconectar la jeringa con el filtro del frasco con el conector. Tirar del émbolo para
introducir aire en una cantidad igual al volumen del disolvente. Volver a conectar la
jeringa con el filtro fijado al frasco con el conector (dibujo n. ° 9). - 10. Invertir el frasco y aspirar la solución a la jeringa (dibujo n. ° 10).
- 11. Desconectar la jeringa del filtro y del frasco y administrar lentamente por vía
intravenosa a una velocidad no superior a 0,08 ml / kg / min (dibujo n. ° 11).
No debe dejar el producto sin utilizar para su uso posterior.
No debe volver a utilizar el conjunto para la administración.
Al utilizar el conjunto para la infusión, debe comprobar su compatibilidad con la jeringa.
Debe utilizar los adaptadores adecuados para garantizar la administración correcta del
producto.
- País de registro
- Principio activo
- Requiere recetaNo
- Fabricante
- ImportadorInstituto Grifols, S.A.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a AnbinexForma farmacéutica: Polvo, 1000 UIPrincipio activo: Antitrombina iiiFabricante: Instituto Grifols S.A.No requiere recetaForma farmacéutica: Polvo, 50 UI/ml; 500 UIPrincipio activo: Antitrombina iiiFabricante: Takeda Manufacturing Austria AGNo requiere recetaForma farmacéutica: Polvo, 50 UI/mlPrincipio activo: Antitrombina iiiFabricante: Takeda Manufacturing Austria AGNo requiere receta
Alternativas a Anbinex en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Anbinex en Ucrania
Alternativa a Anbinex en España
Médicos online para Anbinex
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Anbinex – sujeta a valoración médica y normativa local.














