
Фібрига

Запитайте лікаря про рецепт на Фібрига

Інструкція із застосування Фібрига
Упаковка з інструкцією: інформація для користувача
Фібрига, 1 г
Порошок і розчинник для приготування розчину для ін'єкцій/інфузій
Людський фібриноген
Перед застосуванням лікарського засобу необхідно ретельно ознайомитися з вмістом інструкції, оскільки вона містить важливу інформацію для пацієнта.
- Зберігайте цю інструкцію, щоб у разі потреби знову її прочитати.
- Якщо у вас виникли додаткові сумніви, зверніться до лікаря або фармацевта.
- Цей лікарський засіб призначений лише для конкретної особи. Не передавайте його іншим. Лікарський засіб може нашкодити іншій особі, навіть якщо симптоми її хвороби такі самі.
- Якщо в пацієнта виникли будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, повідомте про це лікаря або фармацевта. Див. пункт 4.
Зміст інструкції
- 1. Що таке лікарський засіб Фібрига і для чого він використовується
- 2. Інформація, важлива перед застосуванням лікарського засобу Фібрига
- 3. Як застосовувати лікарський засіб Фібрига
- 4. Можливі побічні ефекти
- 5. Як зберігати лікарський засіб Фібрига
- 6. Зміст упаковки і інші відомості
1. Що таке лікарський засіб Фібрига і для чого він використовується
Що таке лікарський засіб Фібрига
Фібрига містить людський фібриноген, який є важливим білком у процесі згортання крові. Недостатність
фібриногену означає, що кров не згортається так добре, як повинно бути, що призводить до підвищеної схильності
до кровотеч.
Для чого використовується лікарський засіб Фібрига
Лікарський засіб Фібрига використовується для:
- лікування епізодів кровотечі та профілактики під час хірургічних операцій у пацієнтів з вродженим дефіцитом фібриногену (гіпо- або афібриногенемією) зі схильністю до кровотеч.
- доповнення фібриногену у пацієнтів з неконтрольованим важким кровотечею, якому супроводжується набутий дефіцит фібриногену під час хірургічних операцій.
2. Інформація, важлива перед застосуванням лікарського засобу Фібрига
Коли не застосовувати лікарський засіб Фібрига:
- якщо пацієнт має алергію на людський фібриноген або будь-який з інших компонентів цього лікарського засобу (перелічених у пункті 6).
- якщо у пацієнта раніше виникла алергічна реакція на лікарський засіб Фібрига.
Необхідно повідомити лікаря, якщо пацієнт має алергію на будь-який лікарський засіб.
Попередження та обережність
Перед початком застосування лікарського засобу Фібрига необхідно обговорити це з лікарем або фармацевтом.
Ризик тромбозу крові в судинах
Лікар повинен оцінити користь від застосування цього лікарського засобу щодо ризику утворення тромбів
у судинах, особливо якщо:
- пацієнт отримав велику дозу або багаторазові дози цього лікарського засобу,
- пацієнт мав раніше інфаркт міокарда (хвороба коронарних судин або інфаркт міокарда в анамнезі),
- пацієнт має захворювання печінки,
- пацієнт знаходиться у післяопераційному періоді (пацієнт післяопераційний),
- пацієнт проходить хірургічну операцію (пацієнт околоопераційний),
- у новонароджених,
- якщо пацієнт має великий ризик утворення тромбів або порушення згортання крові в судинах (пацієнти з ризиком тромбоемболічних подій або дисемінованого внутрішньосудинного згортання). Лікар може призначити проведення додаткових тестів на згортання крові для моніторингу ризику.
Алергічні реакції та анафілактичний шок
Кожен лікарський засіб, такий як Фібрига, який виробляється з людської крові (містить білки) і який вводиться в жили (вводиться внутрішньовенно), може спричинити алергічні реакції. Якщо у пацієнта раніше виникли алергічні реакції на лікарський засіб Фібрига, лікар вирішить, чи необхідно застосування лікарського засобу протиалергійного.
Лікар пояснить пацієнтові, які є попереджувальні ознаки алергічної реакції або анафілактичного шоку.
Необхідно звернути увагу на ранні ознаки алергічної реакції (гіперчутливості), такі як:
- кропив'янка,
- виразка,
- чуття стискання в грудній клітці,
- свистячий дихання,
- низький тиск крові,
- або анафілактичний шок (якщо будь-яка або всі вищеозначені ознаки виникають раптово і з великою інтенсивністю). Якщо виникають такі ознаки, введення/інфузія лікарського засобу Фібрига повинна бути негайно припинена.
Вірусологічна безпека
Коли лікарські засоби виробляються з людської крові або плазми, приймаються певні заходи обережності,
аби запобігти передачі інфекцій пацієнтам. Вони включають:
- уважний відбір донорів крові та плазми, щоб забезпечити виключення донорів, які можуть бути носіями інфекцій,
- перевірку кожної донорської крові та плазми на наявність вірусів/інфекцій,
- включення до процесу обробки крові або плазми етапів, спрямованих на інактивацію або видалення вірусів. Незважаючи на ці заходи обережності, при застосуванні лікарських засобів, приготовлених з людської крові або плазми, не можна повністю виключити можливість передачі інфекції. Це стосується також невідомих або недавно виниклих вірусів або інших типів інфекцій. Прийняті заходи вважаються ефективними щодо вірусів з оболонкою, таких як вірус імунодефіциту людини (ВІЛ), вірус гепатиту типу Б (HBV) та вірус гепатиту типу С (HCV), а також безоболонкового вірусу гепатиту типу А (HAV). Прийняті заходи обережності можуть мати обмежену ефективність щодо безоболонкових вірусів, таких як парвовірус В19. Інфекція парвовірусом В19 може бути серйозною у разі вагітних жінок (інфекція ненародженого дитини) та осіб з імунодефіцитом або з певними типами анемії (наприклад, серпоподібноклітинна анемія або патологічний розклад червоних кров'яних клітин). Безумовно рекомендується, щоб у кожному випадку застосування лікарського засобу Фібрига пацієнтові реєструвалася назва та номер серії продукту для можливості зв'язку пацієнта з певною серією застосованого лікарського засобу. Якщо пацієнт регулярно/багаторазово приймає продукти, що містять фібриноген людського походження, лікар може порекомендувати пацієнтові розглянути питання про щеплення проти вірусного гепатиту типу А та Б.
Діти та підлітки
Не існує жодних спеціальних або додаткових попереджень чи обережностей щодо дітей та підлітків.
Лікарський засіб Фібрига та інші лікарські засоби
Необхідно повідомити лікаря або фармацевта про всі лікарські засоби, які приймає пацієнт зараз або останнім часом, а також про лікарські засоби, які пацієнт планує приймати.
Лікарського засобу Фібрига не можна змішувати з жодними іншими лікарськими засобами, крім тих, що перелічені в пункті „Інформація, призначена лише для фахового медичного персоналу / Реконституція”.
Вагітність, годування грудьми та вплив на фертильність
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітна або планує мати дитину, вона повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цього лікарського засобу. Цей лікарський засіб повинен застосовуватися під час вагітності або годування грудьми лише після консультації з лікарем або фармацевтом.
Водіння транспортних засобів та обслуговування машин
Лікарський засіб Фібрига не впливає на здатність водіння транспортних засобів та обслуговування машин.
Лікарський засіб Фібрига містить натрій
Цей лікарський засіб містить натрій (основний компонент кухонної солі) в кількості до 132 мг у кожній флаконі.
Це відповідає 6,6% рекомендованої максимальної добової норми споживання натрію дорослими. Необхідно враховувати це, якщо пацієнт дотримується дієти з низьким вмістом натрію.
3. Як застосовувати лікарський засіб Фібрига
Цей лікарський засіб завжди повинен застосовуватися згідно з рекомендаціями лікаря. У разі сумнівів необхідно звернутися до лікаря.
Лікарський засіб Фібрига вводиться у вигляді внутрішньовенної інфузії (капельниці) медичним персоналом.
Доза та схема дозування залежать від:
- маси тіла пацієнта,
- тяжкості захворювання,
- місцезнаходження кровотечі,
- характеру хірургічної операції,
- загального стану здоров'я.
Застосування у дітей та підлітків
Спосіб введення лікарського засобу Фібрига дітям та підліткам (внутрішньовенно) не відрізняється від введення дорослим.
Застосування більшої ніж рекомендована дози лікарського засобу Фібрига
Лікар буде регулярно проводити аналізи крові для визначення рівня фібриногену, щоб зменшити ризик передозування.
У разі передозування збільшується ризик утворення патологічних тромбів крові у судинах.
У разі будь-яких додаткових сумнівів, пов'язаних з застосуванням цього лікарського засобу, необхідно звернутися до лікаря або фармацевта.
Спосіб введення
Цей лікарський засіб повинен вводитися у вигляді ін'єкції або інфузії (капельниці) у вену після реконституції
з використанням доданого розчинника. У разі будь-яких додаткових сумнівів, пов'язаних з застосуванням лікарського засобу, необхідно звернутися до лікаря або фармацевта.
4. Можливі побічні ефекти
Як і будь-який лікарський засіб, цей лікарський засіб може спричинити побічні ефекти, хоча вони не виникають у кожного.
Необхідно негайно звернутися до лікаря:
- якщо виникне будь-яка з побічних ефектів,
- якщо виникне будь-який побічний ефект, не перелічений у цій інструкції.Наступні побічні ефекти були повідомлені при застосуванні лікарського засобу Фібрига та інших продуктів, що містять фібриноген (частота виникнення перелічених нижче побічних ефектів невідома):
- алергічні реакції або анафілактичний шок: шкіряні реакції, такі як висипка або червонілення шкіри (див. пункт 2 „Попередження та обережність”).
- відносно судинної системи: запалення судин та утворення тромбів крові (див. пункт 2 „Попередження та обережність”).
- збільшення температури тіла (гарячка).
Якщо у пацієнта виник будь-який з вищеозначених симптомів, необхідно звернутися до лікаря.
Звітність про побічні ефекти
Якщо у пацієнта виникли будь-які симптоми побічних ефектів, включаючи будь-які симптоми побічних ефектів, не перелічені в інструкції, необхідно повідомити про це лікаря або фармацевта. Побічні ефекти можна повідомляти безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я України:
вул. Миколи Амосова, 7
03038 Київ
Телефон: +38 (044) 206-92-44
Факс: +38 (044) 206-92-44
Веб-сайт: https://www.moz.gov.ua/
Побічні ефекти також можна повідомляти подієві, відповідальному за лікарський засіб.
Звітність про побічні ефекти дозволить зібрати більше інформації про безпеку застосування лікарського засобу.
5. Як зберігати лікарський засіб Фібрига
Лікарський засіб повинен зберігатися в місці, недоступному для дітей.
Не застосовувати цей лікарський засіб після закінчення терміну придатності, вказаного на етикетці та на коробці.
Термін придатності означає останній день вказаного місяця.
Не зберігати при температурі вище 25 °C. Не заморожувати. Зберігати флакон у зовнішній упаковці для захисту від світла.
Порошок повинен розчинятися лише безпосередньо перед ін'єкцією/інфузією. Встановлено стабільність реконституованого розчину протягом 24 годин при кімнатній температурі (макс. 25°C). Однак розчин повинен застосовуватися негайно та лише один раз, щоб запобігти забрудненню. Приготованого розчину не можна зберігати в холодильнику чи морозильній камері.
Лікарських засобів не слід викидати в каналізацію чи домашні контейнери для відходів. Необхідно запитати у фармацевта, як видалити лікарські засоби, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки і інші відомості
Що містить лікарський засіб Фібрига
- Активним інгредієнтом є людський фібриноген.
Лікарський засіб Фібрига містить 1 г фібриногену людського походження в флаконі або 20 мг фібриногену людського походження на мл після реконституції у доданому розчиннику (50 мл води для ін'єкцій).
- Інші компоненти: L-аргінін гідрохлорид, гліцин, хлорид натрію та цитрат натрію двогідрат. Розчинник: вода для ін'єкцій
Як виглядає лікарський засіб Фібрига та що містить упаковка
Лікарський засіб Фібрига випускається у вигляді порошку та розчинника для приготування розчину для ін'єкцій/інфузій та доступний у скляних флаконах.
Білий або блідо-жовтий гігроскопічний порошок або крихка, затверділа маса.
Розчинник є безбарвною та прозорою рідиною.
Приготований розчин повинен бути майже безбарвним та легенько опалесцентним.
Лікарський засіб Фібрига випускається у паперовій коробці, яка містить:
- 1 флакон з порошком для приготування розчину для ін'єкцій/інфузій,
- 1 флакон з 50 мл розчинника (вода для ін'єкцій),
- 1 пристрій для реконституції nextaro.
Відповідальна особа
Octapharma (IP) SPRL
Вул. Аллея досліджень, 65
1070 Андерлехт
Бельгія
Виробник
Octapharma Pharmazeutika Produktionsges.m.b.H.
Вул. Оберлааер Штрассе, 235, 1100 Відень, Австрія
Octapharma AB
Вул. Ларса Форсселла, 23, 112 75 Стокгольм, Швеція
Octapharma GmbH
Вул. Елізабет-Сельберт-Штрассе, 11
40764 Лангенфельд, Німеччина
Цей лікарський засіб дозволений до обігу в країнах-членах Європейського економічного простору та у Сполученому Королівстві (Північна Ірландія) під наступними назвами:
Фібрига: Австрія, Бельгія, Болгарія, Хорватія, Кіпр, Чехія, Данія, Естонія, Фінляндія, Франція,
Іспанія, Нідерланди, Ірландія, Ісландія, Литва, Люксембург, Латвія, Мальта, Німеччина, Норвегія,
Польща, Португалія, Румунія, Словаччина, Швеція, Угорщина, Італія, Сполучене Королівство (Північна Ірландія)
Фібрема: Словенія
Дата останньої актуалізації інструкції: 2023-12-22
Інформація, призначена лише для фахового медичного персоналу: Дозування
Дозування та тривалість заміщення терапії залежать від ступеня тяжкості захворювання, місця та інтенсивності кровотечі, а також від клінічного стану пацієнта.
Необхідно визначати рівень (функціональний) фібриногену для розрахунку індивідуального дозування та кількості та частоти введених доз для кожного пацієнта шляхом регулярних вимірювань рівня фібриногену в плазмі та постійного моніторингу клінічного стану пацієнта та інших застосованих заміщення терапій.
У разі важких хірургічних операцій необхідно проводити точний моніторинг заміщення терапії шляхом визначення параметрів згортання крові.
- 1. Профілактика у пацієнтів з вродженим дефіцитом фібриногену або афібриногенемією та відомою схильністю до кровотеч Аби запобігти надмірному кровотечі під час хірургічних операцій рекомендується профілактичне застосування для збільшення рівня фібриногену до 1 г/л та утримання його на цьому рівні до досягнення гемостазу та понад 0,5 г/л до закінчення заживлення ран. У разі хірургічної операції або лікування епізоду кровотечі необхідно розрахувати дозу наступним чином:
Доза (мг/кг маси тіла) = [Цільовий рівень (г/л) - визначений рівень (г/л)]
0,018 (г/л на мг/кг маси тіла)
Дальше дозування (дози та частота ін'єкцій) повинно бути调整роване до клінічного стану пацієнта та результатів лабораторних тестів.
Біологічний період напіврозпаду фібриногену становить 3-4 доби. У зв'язку з цим, при відсутності споживання зазвичай повторне лікування людським фібриногеном не є необхідним. Враховуючи акумуляцію, яка відбувається при повторному введенні з профілактичною метою, дозу та частоту необхідно встановлювати залежно від терапевтичних цілей, встановлених лікарем для конкретного пацієнта.
Діти та підлітки
У разі хірургічної операції або лікування епізоду кровотечі дозу для підлітків необхідно розрахувати на підставі наведеного вище формулу для дорослих, натомість дозу для дітей у віці до 12 років необхідно розрахувати наступним чином:
Доза (мг/кг маси тіла) = [Цільовий рівень (г/л) - визначений рівень (г/л)]
0,014 (г/л на мг/кг маси тіла)
Дальше дозування повинно бути调整роване до клінічного стану пацієнта та результатів лабораторних тестів.
Особи похилого віку
Клінічні дослідження продукту Фібрига не включали пацієнтів у віці 65 років та старших з метою подання переконливих доказів, чи існували у них відмінності у відповіді на лікування порівняно з молодшими пацієнтами.
- 2. Лікування кровотечі
Кровотеча у пацієнтів з вродженим дефіцитом фібриногену або афібриногенемією
Лікування епізодів кровотечі повинно проводитися згідно з наведеними вище формулами відповідно для дорослих/підлітків та дітей з метою досягнення рекомендованого цільового рівня фібриногену в плазмі у розмірі 1 г/л. Цей рівень повинен бути утриманий до досягнення гемостазу.
Кровотеча у пацієнтів з набутим дефіцитом фібриногену Дорослі
Зазвичай спочатку вводиться 1-2 г, а подальші інфузії за необхідності. У разі важкого кровотечі, наприклад, під час важливої хірургічної операції, може бути необхідна більша кількість фібриногену (4-8 г).
Діти та підлітки
Дозування повинно бути встановлено залежно від маси тіла та клінічних показань, але зазвичай становить 20-30 мг/кг.
Інструкція з приготування та введення Загальні інструкції
- Приготований розчин повинен бути майже безбарвним та легенько опалесцентним. Не використовувати розчини, які є мутними або містять осад.
- Лікарський засіб Фібрига призначений лише для одноразового використання. Не застосовувати повторно жодного з компонентів.
- Для забезпечення мікробіологічної безпеки розчин повинен вводитися негайно після реконституції. Встановлено хімічну та фізичну стабільність приготованого розчину протягом 24 годин при кімнатній температурі (до 25°C). Не зберігати в холодильнику чи морозильній камері лікарський засіб Фібрига після реконституції.
Реконституція
- 1. Перевірити, що флакон з порошком (Фібрига) та флакон з розчинником мають кімнатну температуру. Необхідно підтримувати цю температуру протягом усього процесу реконституції. Якщо для нагрівання використовується водяна баня, необхідно бути обережним, щоб не допустити контакту води з гумовими пробками чи відірваними кришками контейнерів. Температура водяної бані не повинна перевищувати +37°C.
- 2. Зняти відірвані кришки з флакону з порошком (Фібрига) та флакону з розчинником, щоб відкрити центральну частину ін'єкційного пробка. Протирання гумовими пробками ватним тампоном, змоченим у спирті, та залишити до висихання.
- 3. Відкрити упаковку пристрою для реконституції (nextaro) шляхом зняття кришки (рис. 1). Для збереження стерильності залишити пристрій для реконституції у прозорому блистерному упаковуванні. Не торкатися голки.
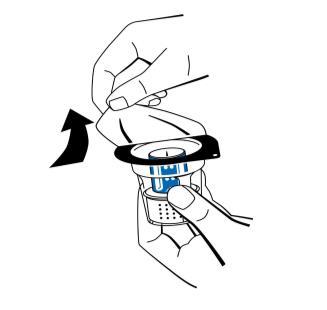
- 4. Помістити флакон з розчинником на пласку, чисту поверхню та міцно утримувати. Без зняття блистерного упаковування помістити синю частину пристрою для реконституції на верх флакону з розчинником. Натиснути прямо та міцно вниз, поки не почується клацання (рис. 2). Не повертати під час підключення.
Увага:
Пристрій для реконституції необхідно спочатку прикріпити до флакону з розчинником, а потім до флакону з ліофілізованим порошком. В іншому разі буде втрачено підтиск та не відбуватиметься переливання розчинника.
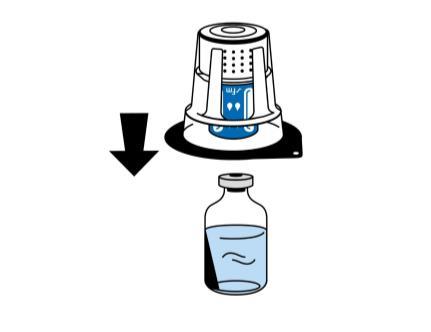
- 5. Тримаючи флакон з розчинником, обережно зняти блистерне упаковування з пристрою для реконституції (nextaro) шляхом потягання вертикально вгору. Необхідно переконатися, що пристрій для реконституції міцно прикріплено до флакону з розчинником (рис. 3).
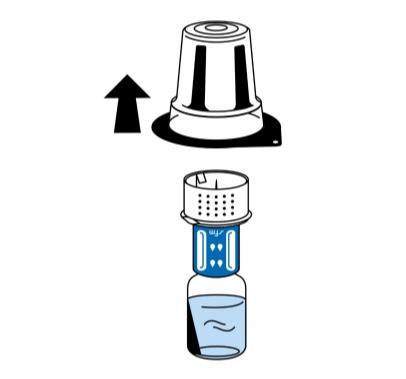
- 6. Помістити флакон з порошком (Фібрига) на пласку, чисту поверхню та міцно утримувати. Взяти флакон з розчинником з підключеним пристроєм для реконституції та повернути догори дном. Помістити білу частину з'єднувача пристрою для реконституції на верх флакону з порошком (Фібрига) та міцно натиснути, поки не почується клацання (рис. 4). Не повертати під час підключення. Розчинник автоматично переливається до флакону з порошком (Фібрига).
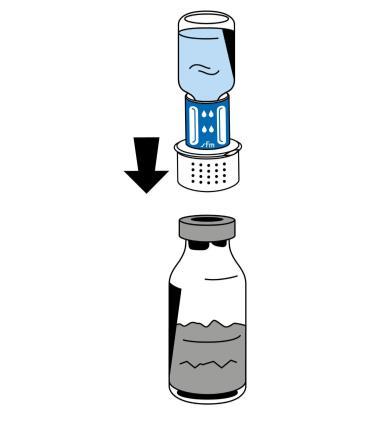
- 7. З підключеним флаконом з розчинником обережно повертати флакон з лікарським засобом Фібрига, поки порошок не розчиниться повністю. Для уникнення утворення піни не слід потрясати флаконом. Порошок повинен розчинитися повністю протягом близько 5 хвилин.
Розчинення порошку не повинно тривати довше 20 хвилин. Якщо порошок не розчиниться протягом 20 хвилин, продукт необхідно видалити.
- 8. У рідкісному випадку, коли під час переливання води для ін'єкцій спостерігається підняття на поверхню незреконституованого продукту або коли час реконституції несподівано збільшується, процес розчинення можна прискорити шляхом більш енергійного перемішування флакону в горизонтальному напрямку.
- 9. Після закінчення реконституції відвернути пристрій для реконституції (синю частину) у напрямку, протилежному до руху годинникової стрілки, на дві частини (рис. 5). Не торкатися з'єднувача луер-лок на білій частині пристрою для реконституції.
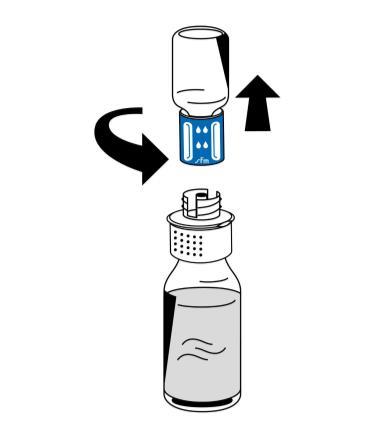
- 10. Видалити пустий флакон з розчинником разом з підключеною синьою частиною пристрою для реконституції.
Введення
- 1. Обережно підключити шприц до з'єднувача луер-лок на білій частині пристрою для реконституції (рис. 6).
- 2. Перевернути флакон з лікарським засобом Фібрига догори дном та витягнути розчин до шприцу (рис. 7).
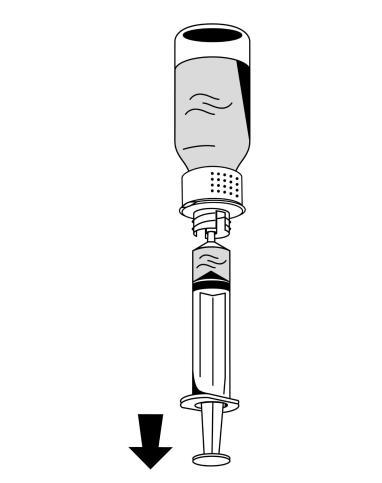
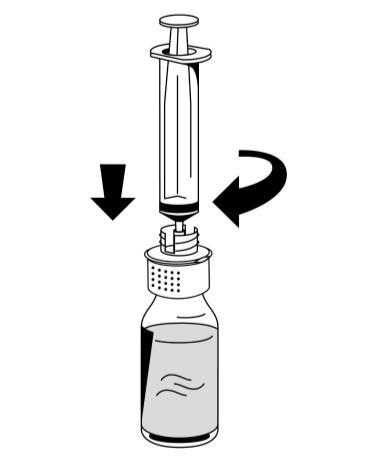
- 3. З підключеним шприцем міцно утримувати поршень шприцу (тримаючи поршень шприцу, спрямований вниз) та витягнути шприц з пристрою для реконституції (рис. 8).

- 4. Видалити білу частину пристрою для реконституції разом з пустим флаконом з лікарським засобом Фібрига.
Рекомендується внутрішньовенне введення приготованого розчину при кімнатній температурі з використанням стандартного набору для інфузії.
Всі невикористані залишки лікарського засобу або його відходи повинні бути видалені згідно з місцевими правилами.
Спосіб введення
Інфузія або внутрішньовенне введення.
Лікарський засіб Фібрига повинен вводитися повільно внутрішньовенно при рекомендованій максимальній швидкості 5 мл на хвилину у пацієнтів з вродженим дефіцитом фібриногену або афібриногенемією та при рекомендованій максимальній швидкості 10 мл на хвилину у пацієнтів з набутим дефіцитом фібриногену.
Несумісність
Не змішувати лікарський засіб з іншими лікарськими засобами.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептНі
- Виробник
- ІмпортерOctapharma AB Octapharma GmbH Octapharma Pharmazeutika Produktionsges.m.g.H.
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до ФібригаФорма випуску: Порошок, 1 гДіючі речовини: fibrinogen, humanВиробник: CSL Behring GmbHНе потрібен рецептФорма випуску: Порошок, 1000 МОДіючі речовини: coagulation factor VIIIВиробник: CSL Behring GmbHПотрібен рецептФорма випуску: Порошок, 2000 МОДіючі речовини: coagulation factor VIIIВиробник: CSL Behring GmbHПотрібен рецепт
Аналоги Фібрига в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Фібрига у Україна
Аналог Фібрига у Іспанія
Лікарі онлайн щодо Фібрига
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Фібрига – за рішенням лікаря та згідно з місцевими правилами.














