
Цлувот 1250 й.м.
Запитайте лікаря про рецепт на Цлувот 1250 й.м.

Інструкція із застосування Цлувот 1250 й.м.
Укладена інструкція до пакування: інформація для пацієнта
Клувот 1250 од.р.
Порошок і розчинник для приготування розчину для ін'єкцій/інфузій
Людський фактор згортання крові XIII
Необхідно уважно ознайомитися з вмістом інструкції перед застосуванням препарату, оскільки вона містить важливу інформацію для пацієнта.
- Необхідно зберегти цю інструкцію, щоб у разі потреби можна було її знову прочитати.
- У разі будь-яких сумнівів необхідно звернутися до лікаря або фармацевта.
- Цей препарат призначений строго для певної особи. Не слід його передавати іншим. Препарат може нашкодити іншій особі, навіть якщо симптоми її хвороби такі самі.
- Якщо в пацієнта з'являються будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, необхідно повідомити про це лікаря або фармацевта. Див. пункт 4.
Зміст інструкції
- 1. Що таке Клувот і для чого він використовується
- 2. Важливі відомості перед застосуванням Клувот
- 3. Як застосовувати Клувот
- 4. Можливі побічні ефекти
- 5. Як зберігати Клувот
- 6. Зміст пакування і інші відомості
1. Що таке Клувот і для чого він використовується
Що таке Клувот
Клувот є препаратом, доступним у вигляді білого порошку і розчинника. Приготовлений розчин повинен
бути введений внутрішньовенно.
Клувот є людським фактором згортання крові XIII (F XIII) виробленим з людської плазми (це
рідка частина крові) і відіграє важливу роль у процесі гемостазу (зупинення кровотечі).
Для чого використовується Клувот
Клувот показаний для застосування у дорослих, дітей і підлітків.
- для профілактичного лікування вродженої недостатності фактору XIII та
- у хірургічному періоді для лікування кровотеч у пацієнтів з вродженою недостатністю фактору XIII.
2. Важливі відомості перед застосуванням Клувот
Ця частина інструкції містить відомості, які необхідно врахувати перед початком застосування препарату
Клувот.
Коли не застосовувати Клувот:
- якщо пацієнт має алергію на активну речовину або будь-який з інших компонентів цього препарату (перелічених у пункті 6).
Необхідно повідомити лікаря, якщо існує підвищена чутливість до будь-якого препарату або харчового продукту.
Попередження і заходи обережності:
- якщо після введення фактору XIII згортання крові раніше спостерігалися алергічні реакції. Профілактично необхідно застосувати антигістамінні препарати і кортикостероїди, якщо так вирішить лікар.
- коли з'являються симптоми алергії або реакції типу анафілаксії (важкі симптоми алергії можуть спричинити значне утруднення дихання або головокружіння). Введення Клувот повинно бути негайно припинено (тобто перервано введення або інфузію). У разі шоку необхідно застосувати лікування згідно з чинними медичними стандартами.
- якщо раніше спостерігалася свіжа тромбоз (тромб). Необхідно уважно спостерігати за пацієнтом через стабілізуючу фібрину дію F XIII.
- утворення інгібіторів (антитіл, що нейтралізують) є відомим ускладненням лікування і означає, що лікування перестає діяти. Якщо кровотеча не була зупинена за допомогою препарату Клувот, необхідно негайно повідомити про це лікаря. Пацієнта необхідно ретельно моніторити щодо розвитку (з'явлення) інгібіторів.
Лікар завжди повинен зважити вигоди від лікування щодо ризику, пов'язаного з ускладненнями.
Безпека щодо вірусів
Коли препарати виробляються з людської крові або плазми, проводяться різні заходи з метою захисту пацієнта від передачі інфекційних агентів. До цих методів належать:
- відповідний відбір донорів крові і плазми для виключення ризику передачі інфекційних агентів
- перевірка кожної донорської крові і плазми на наявність маркерів вірусів/інфекцій.
- введення до процесу виробництва препаратів з крові або плазми етапів, які можуть привести до інактивації або видалення вірусів.
Незважаючи на застосування вище згаданих методів, не можна повністю виключити можливість передачі інфекційних агентів після введення препарату, отриманого з людської крові або плазми
Людської. Це ризик стосується також невідомих або недавно відкритих вірусів і інших інфекційних агентів.
Західні заходи є ефективними щодо оболонкових вірусів, таких як людський вірус імунодефіциту (ВІЛ, вірус, який викликає СНІД), вірус гепатиту типу Б (ВГВ, який викликає гепатит типу Б), вірус гепатиту типу С (ВГС, який викликає гепатит типу С)
та вірусів без оболонки, таких як вірус гепатиту типу А (ВГА, який викликає гепатит типу А) і парвовірус В 19.
У пацієнтів, які багаторазово отримують препарати, отримані з людської плазми, необхідно розглянути можливість застосування вакцин проти вірусного гепатиту типу А і Б.
Рекомендується кожен раз, коли вводиться Клувот, щоб дата введення, номер серії і введена кількість були зареєстровані в медичній документації.
Клувот і інші препарати
- Необхідно повідомити лікаря або фармацевта про прийняття інших препаратів, включаючи ті, які доступні без рецепта.
- Не відомо про існування взаємодії концентрату фактору згортання крові FXIII з іншими лікарськими засобами.
- Клувот не можна змішувати з іншими лікарськими засобами, розчинниками і розбавниками, крім тих, які перелічені в пункті 6, і повинен бути введений за допомогою окремих інфузійних наборів.
Вагітність і годування грудьми
- Якщо пацієнтка вагітна або годує грудьми, припускає, що вона може бути вагітною або планує мати дитину, повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цього препарату.
- Обмежені дані про клінічне застосування Клувот під час вагітності не виявили жодних негативних ефектів, пов'язаних з вагітністю та розвитком ембріона і післяпологовим періодом. У разі необхідності можна розглянути застосування Клувот під час вагітності.
- Не відомо про ступінь проникнення Клувот до людського молока, однак, враховуючи його високу молекулярну масу, імовірність виділення з молоком матері дуже низька, а через його білковий характер абсорбція цілими частинками новонародженим також малоймовірна. У зв'язку з цим Клувот можна застосовувати під час годування грудьми.
- Відсутні дані про вплив Клувот на фертильність.
Проведення транспортних засобів і обслуговування машин
Не проводилися дослідження щодо впливу на здатність керувати транспортними засобами і обслуговувати машини.
Важливі відомості про деякі компоненти Клувот
Клувот містить натрій.
Необхідно враховувати той факт, що Клувот містить натрій. Це важливо для пацієнтів, які перебувають на контрольованій
дієті з низьким вмістом натрію. Клувот містить від 124,4 до 195,4 мг (5,41 до 8,50 ммоль) натрію на дозу (40 од.р. / маса
тіла - при середній масі тіла 70 кг), якщо введено рекомендовану дозу (2800 од.р. = 44,8 мл)
3. Як застосовувати Клувот
- Клувот зазвичай вводиться лікарем.
- Клувот призначений лише для внутрішньовенного введення.
Дозування
Лікар повинен розрахувати відповідну дозу і вирішити, як часто Клувот повинен бути введений
пацієнтові, враховуючи прогрес у лікуванні.
Більш детальні рекомендації див. пункт: „ Інформація, призначена лише для медичного персоналу
або працівників охорони здоров'я”.
Передозування
Не зареєстровано випадків передозування, і не слід їх очікувати у разі введення цього препарату
медичним персоналом.
4. Можливі побічні ефекти
Як і будь-який препарат, цей препарат може викликати побічні ефекти, хоча вони не виникнуть у кожного.
Нижче перелічені побічні ефекти спостерігалися рідко(викликалися у більше ніж 1 на 10 000 пацієнтів
і менше ніж у 1 на 1 000)
- Алергічні реакції, такі як загальна кропивниця (свербіжний набряк на шкірі), висип, зниження артеріального тиску (що може викликати відчуття оmdlіння або головокружіння), труднощі з диханням.
- Збільшення температури тіла
Нижче перелічені побічні ефекти спостерігалися дуже рідко(викликалися у менше ніж 1 на 10 000
пацієнтів):
- Утворення інгібіторів FXIII.
Якщо з'являються алергічні реакції, введення препарату Клувот повинно бути негайно припинено
і повинно бути розпочато відповідне лікування. Повинні бути застосовані чинні медичні стандарти для лікування шоку.
Побічні ефекти у дітей і підлітків
Чекається, що побічні ефекти у дітей такі самі, як і у дорослих.
Звітність про побічні ефекти
Якщо з'являються будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в інструкції, необхідно повідомити про це лікаря або фармацевта. Побічні ефекти можна повідомляти
безпосередньо до Департаменту моніторингу побічних ефектів лікарських засобів Міністерства охорони здоров'я
вул. Єрусалимські, 181С,
02-222 Варшава
Тел.: + 48 22 49 21 301
Факс: + 48 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Побічні ефекти також можна повідомляти відповідальному суб'єкту.
Звітність про побічні ефекти дозволить зібрати більше інформації про безпеку застосування препарату.
5. Як зберігати Клувот
- Зберігати в холодильнику (2 ⁰ С - 8 ⁰ С).
- Не заморожувати.
- Зберігати в зовнішньому пакуванні для захисту від світла.
- Клувот не містить консервантів. Препарат повинен бути використаний негайно після реконституції. Якщо він не буде негайно використаний, зберігання при кімнатній температурі не повинно перевищувати 4 години. Не зберігати в холодильнику і не заморожувати розчин після реконституції.
- Препарат повинен бути збережений у місці, недоступному для дітей.
- Не застосовувати Клувот після закінчення терміну придатності, вказаного на етикетці і зовнішньому пакуванні після скорочення EXP.
- Номер серії лікарського засобу знаходиться на зовнішньому пакуванні і етикетці після скорочення: Lot.
6. Зміст пакування і інші відомості
Що містить Клувот Активна речовина:
Концентрат XIII фактору згортання крові людини (FXIII) містить 1250 од.р. на флакон.
Допоміжні речовини:
Людський альбумін, глюкоза моногідрат, хлорид натрію, гідроксид натрію (у малих кількостях для встановлення
рН).
Розчинник:Вода для ін'єкцій
Як виглядає Клувот і що містить пакування
Клувот випускається у вигляді білого порошку і розчинника, яким є вода для ін'єкцій.
Приготовлений розчин повинен бути безбарвним, прозорим до легкого опалесценції. Триманий під світлом не
повинен бути мутним чи містити залишки (кластери/частинки).
Величини пакування
Одне пакування 1250 од.р. містить:
1 флакон з порошком
1 флакон з 20 мл води для ін'єкцій
1 систему для перекачування 20/20 з фільтром (Mix2Vial)
Набір для введення (внутрішнє пакування);
1 шприц одноразового використання об'ємом 20 мл
1 набір для введення
2 ватні тампони, насичені алкоголем
1 нестерильна пластина
Відповідальний суб'єкт і Виробник
CSL Behring GmbH
Еміль фон Берінг Штрассе 76
35041 Марбург
Німеччина
Дата останньої актуалізації інструкції:серпень 2021
----------------------------------------------------------------------------------------------------------------------
Інформація, призначена лише для фахового медичного персоналу: Дозування
1 мл відповідає приблизно 62,5 од.р., а 100 од.р. дорівнює відповідно 1,6 мл.
Важливо:
Кількість, необхідна для введення, і частота введення повинні бути завжди підібрані згідно з клінічною ефективністю
у окремих пацієнтів .
Дозування
Дозування повинно бути індивідуально підібрано залежно від маси тіла, результатів лабораторних досліджень та клінічного стану пацієнта.
Рутинний схема дозування у профілактиці
Початкова доза
- 40 міжнародних одиниць (од.р.) на кілограм маси тіла.
- Швидкість інфузії не повинна бути більшою ніж 4 мл на хвилину
Наступні дози
- Дозування повинно бути визначено на основі поточного рівня активності FXIII, дози повинні бути введені з інтервалом 28 днів (4 тижні) для підтримання мінімальної активності F XIII на рівні близько 5 до 20%.
- Рекомендується коригування дозування на +/- 5 од.р. на кг маси тіла повинно бути розраховано з урахуванням мінімального рівня активності F XIII як показано в таблиці № 1 та клінічного стану пацієнта .
- Коригування дозування повинно бути проведено на основі специфічного, чутливого тесту для визначення рівня F XIII. Приклади коригування з використанням стандартного тесту активності Berichrom були представлені в нижченаведеній таблиці № 1.
Таблиця 1 : Коригування дозування з використанням тесту активності Berichrom
Активність виражається в одиницях і визначається з використанням тесту активності Berichrom, що відноситься
до чинного Міжнародного стандарту для плазмового XIII фактору згортання крові. У зв'язку
з цим одиниця відповідає Міжнародній одиниці.
| Мінімальний рівень активності фактору XIII(%) | Зміна дозування |
| Один мінімальний рівень <5% | Збільшення на 5 одиниць на кг. |
| Мінімальний рівень 5% до 20% | Без змін |
| Два мінімальні рівні > 20% | Зменшення на 5 одиниць на кг. |
| Один мінімальний рівень > 25% | Зменшення на 5 одиниць на кг. |
Профілактика передопераційна.
Після останньої дози, застосованої в рамках рутинної профілактики, у разі планування хірургічної операції:
- Між 21 і 28 днем після останньої дози - необхідно застосувати пацієнтові повну дозу безпосередньо перед хірургічною операцією, а наступна профілактична доза повинна бути введена через 28 днів.
- Між 8 і 21 днем після останньої дози - додаткова доза (повна або часткова) може бути введена перед хірургічною операцією. Доза повинна бути підібрана залежно від рівня активності FXIII пацієнта , його клінічного стану і повинна бути підібрана з урахуванням періоду напіврозпаду лікарського засобу Клувот.
- У разі застосування протягом 7 днів після останньої дози - додаткове введення може не бути необхідним.
Коригування дозування може бути іншим, ніж рекомендоване дозування, і повинно бути індивідуально підібрано
з урахуванням рівня активності F XIII і клінічного стану пацієнта. Усі пацієнти повинні бути ретельно моніторовані під час і після хірургічної операції.
У зв'язку з цим рекомендується моніторинг зростання рівня активності F XIII на основі тесту
фактору XIII. У разі важких хірургічних операцій та великих кровотеч цією метою повинно бути досягнення значення, близького до нормального (у здорових осіб: 70%-140%).
Діти і підлітки
Дозування і спосіб введення у дітей і підлітків ґрунтується на масі тіла і, таким чином, загалом не відрізняється від рекомендацій для дорослих. Дозування і/або частота введення для кожного пацієнта повинні бути завжди підібрані з урахуванням клінічної ефективності і рівня активності FXIII.
Пацієнти похилого віку
Дозування і спосіб введення у пацієнтів похилого віку (> 65 років) не були задокументовані
у клінічних дослідженнях.
Спосіб введення
Загальні рекомендації
Розчин повинен бути прозорим або легкого опалесценції. Після фільтрації/використання вмісту флакона (див. нижче)
препарат після реконституції перед введенням повинен бути підданий візуальній оцінці; необхідно перевірити, чи не з'явилися будь-які забруднення і чи не відбулися зміни забарвлення.
Не слід застосовувати мутні розчини і ті, які містять хлоп'я або частинки.
Реконституція і використання флакона повинні бути проведені в умовах асептики.
Реконституція
Розчинник повинен бути приведений до кімнатної температури. Зняти з флаконів, що містять порошок
і розчинник, пластикові кришки і промити корки асептичним розчином. Після висихання відкрити
систему, що містить з'єднувач Mix2Vial.
1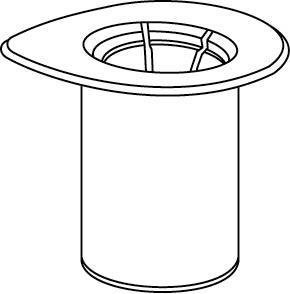 |
|
2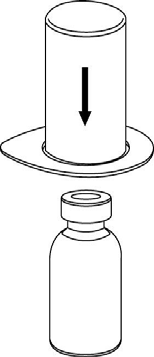 |
|
3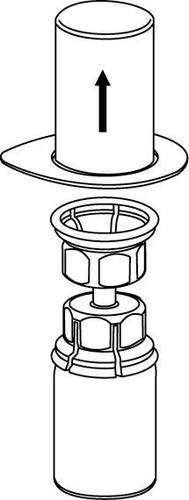 |
|
4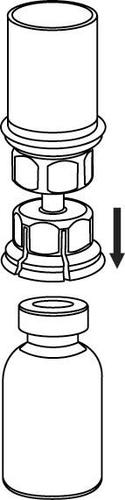 |
|
5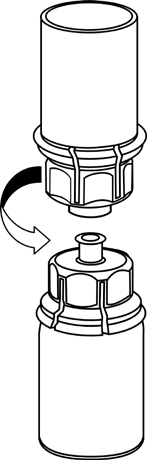 |
|
6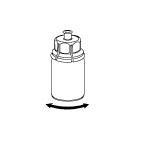 |
|
7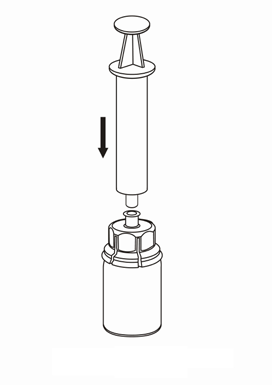 |
|
Використання і спосіб введення
8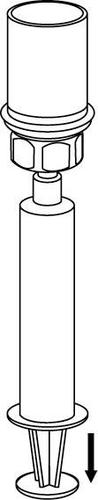 |
|
9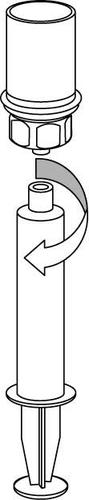 |
|
Необхідно бути обережним, щоб кров не потрапила до шприца, наповненого лікарським засобом, оскільки
існує ризик, що кров може згорнутися у шприці і скреплини фібрину можуть бути введені
пацієнтові.
Розчин після реконституції повинен бути введений до окремих інфузійних наборів (доставлених з препаратом), у повільному внутрішньовенному введенні, зі швидкістю не більшою ніж 4 мл на
хвилину.
Всі не використані лікарські засоби та їх залишки повинні бути видалені згідно з місцевими вимогами.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептТак
- Виробник
- ІмпортерCSL Behring GmbH
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до Цлувот 1250 й.м.Форма випуску: Порошок, 250 МОДіючі речовини: coagulation factor XIIIВиробник: CSL Behring GmbHПотрібен рецептФорма випуску: Порошок, 1000 МОДіючі речовини: coagulation factor VIIIВиробник: CSL Behring GmbHПотрібен рецептФорма випуску: Порошок, 2000 МОДіючі речовини: coagulation factor VIIIВиробник: CSL Behring GmbHПотрібен рецепт
Аналоги Цлувот 1250 й.м. в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Цлувот 1250 й.м. у Іспанія
Лікарі онлайн щодо Цлувот 1250 й.м.
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Цлувот 1250 й.м. – за рішенням лікаря та згідно з місцевими правилами.














