
NUCEIVA 50 units powder for injectable solution


How to use NUCEIVA 50 units powder for injectable solution
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
NUCEIVA 50 Units Powder for Solution for Injection
Botulinum toxin type A
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet, you may need to read it again.
- If you have any further questions, ask your doctor or pharmacist.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their symptoms are the same as yours.
- If you get any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack
- What is NUCEIVA and what is it used for
- What you need to know before you use NUCEIVA
- How to use NUCEIVA
- Possible side effects
- Storage of NUCEIVA
- Contents of the pack and other information
1. What is NUCEIVA and what is it used for
NUCEIVA contains the active substance botulinum toxin type A.
It prevents muscle contraction, which causes temporary paralysis. It works by blocking nerve impulses to the muscles into which it has been injected.
NUCEIVA is used to temporarily improve the appearance of vertical wrinkles between the eyebrows. It is used in adults under 65 years of age in whom facial wrinkles have a significant psychological impact.
2. What you need to know before you use NUCEIVA
Do not use NUCEIVA:
- if you are allergic to botulinum toxin type A or any of the other ingredients of this medicine (listed in section 6);
- if you have severe myasthenia gravis or Lambert-Eaton syndrome (chronic diseases that affect the muscles);
- if you have an infection or inflammation at the proposed injection sites between the eyebrows and above them (as indicated in figure 1).
Warnings and precautions
Very rarely, side effects possibly related to the spread of botulinum toxin from the injection site (e.g., muscle weakness, difficulty swallowing or food or liquids entering the airways) may occur. Patients who receive the recommended doses may experience excessive muscle weakness.
Injection has been associated with localized pain, inflammation/swelling, abnormal sensitivity (paresthesia), decreased sensitivity (hypoesthesia), pain on palpation, skin rash (erythema), localized infection, bleeding, and/or bruising. Pain and/or anxiety related to the needle have led to vasovagal responses, such as pallor, nausea, sweating, blurred vision, rapid heartbeat, dizziness, and/or a temporary drop in blood pressure that causes dizziness or fainting.
See your doctor immediately if you have difficulty swallowing, speaking, or breathing after treatment.
- This medicine is not recommended in patients who have had problems swallowing (dysphagia) and breathing recently or in the past, as it would prevent the safe administration of the medicine in the doctor's opinion.
- Too frequent or excessive administration may cause the formation of antibodies. The formation of antibodies may prevent botulinum toxin type A from working even for other uses.
- Very rarely, an allergic reaction may occur after injection of botulinum toxin.
Among the symptoms are skin reactions, such as hives, itching, and reddened or pale skin, swelling of the eyes, lips, mouth, or throat, weak and rapid pulse, dizziness, and wheezing or shortness of breath.
- It is possible to experience eyelid drooping after treatment.
Tell your doctor if:
- you have had problems with previous botulinum toxin injections;
- you do not observe any significant improvement in wrinkles one month after the first treatment cycle;
- you have certain diseases that affect the nervous system (such as amyotrophic lateral sclerosis or motor neuropathy);
- you have inflammation at the proposed injection site;
- the muscles to be injected are weak or damaged;
- you have a bleeding disorder, as injection may cause bruising.
Children and adolescents
This medicine is not recommended for use in children under 18 years of age.
Other medicines and NUCEIVA
Tell your doctor or pharmacist if you are taking, have recently taken, or might take any other medicines.
The use of botulinum toxin associated with aminoglycoside antibiotics, spectinomycin, or other medicines that affect nerve impulses to the muscle is not recommended.
Tell your doctor if you have recently been injected with a medicine that contains botulinum toxin (the active substance of NUCEIVA), as this may excessively increase the effect of this medicine.
Pregnancy and breastfeeding
If you are pregnant or breastfeeding, think you may be pregnant, or are planning to have a baby, ask your doctor for advice before using this medicine.
This medicine is not recommended during pregnancy or in women who are able to have children and do not use contraceptive methods.
This medicine is not recommended in women who are breastfeeding.
Driving and using machines
Muscle weakness, dizziness, and visual disturbances have been described with this medicine that may make driving or using machines hazardous. Do not drive or use machines until these effects have disappeared.
NUCEIVA contains sodium
This medicine contains less than 1 mmol of sodium (23 mg) per dose, which is essentially "sodium-free".
3. How to use NUCEIVA
The single-dose units of NUCEIVA are not interchangeable with those used for other botulinum toxin preparations.
This medicine should only be injected by doctors with the appropriate qualification and experience in the treatment of frown lines.
The usual dose of NUCEIVA is 20 Units. You will be injected with the recommended volume of 0.1 milliliters (ml) (4 Units) of this medicine at each of the 5 injection sites.
Improvement in the depth of wrinkles between the eyebrows usually occurs within a few days of treatment.
The interval between treatments will be decided by your doctor.
How NUCEIVA is injected
This medicine is injected into the muscles (by intramuscular route), directly into the affected area between the eyebrows and above them.
Once reconstituted, NUCEIVA should only be used to treat a single patient during a single session.
If you have any further questions on the use of this product, ask your doctor or pharmacist.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
In general, side effects appear in the first few days after injection and are transient. Most side effects are mild or moderate in intensity.
If you have difficulty breathing, swallowing, or speaking after receiving this medicine, contact your doctor immediately.
If you experience hives, swelling, including swelling of the face or throat, wheezing, feeling of weakness, and shortness of breath, contact your doctor immediately, as these may be symptoms of an allergic reaction.
The likelihood of experiencing a side effect is described in the following categories:
Frequent (may affect up to 1 in 10) | Headache, muscle imbalance that produces elevated or asymmetrical eyebrows, eyelid drooping, bruising at the injection site |
Uncommon (may affect up to 1 in 100 people) | Sensory disorders, headaches, dry eye, eyelid swelling, eye swelling, muscle contractions, injection site: redness, pain, tingling |
Reporting of side effects
If you experience side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. You can also report side effects directly via the national reporting system listed in Appendix V. By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of NUCEIVA
Store in a refrigerator (between 2°C and 8°C).
Keep out of the sight and reach of children.
Unopened vial
Do not use this medicine after the expiry date which is stated on the vial and carton after EXP.
6. Contents of the pack and other information
Composition of NUCEIVA
- The active substance is: 50 Units of botulinum toxin type A.
- The other ingredients are human albumin and sodium chloride.
Appearance and pack contents
NUCEIVA is presented as a white powder for solution for injection in a transparent glass vial.
Each pack contains 1 vial.
Marketing authorisation holder and manufacturers
Evolus Pharma B.V.
Apollolaan 151
1077 AR Amsterdam
Netherlands
You can request more information about this medicine from the local representative of the marketing authorisation holder.
Date of last revision of this leaflet: May 2024.
THIS INFORMATION IS INTENDED ONLY FOR MEDICAL PROFESSIONALS:
The Units of botulinum toxin are not interchangeable from one product to another. The recommended doses in Units are different from those of other botulinum toxin preparations.
Reconstitution should be performed in accordance with good clinical practices, especially with regard to aseptic technique. NUCEIVA is reconstituted with sodium chloride 9 mg/ml (0.9%) solution for injection. 1.25 ml of sodium chloride 9 mg/ml (0.9%) solution for injection is drawn into a syringe to obtain a reconstituted injectable solution at a concentration of 4 Units/0.1 ml.
Amount of diluent added to the vial of 50 Units (sodium chloride 9 mg/ml (0.9%) solution for injection) | Resulting dose (Units per 0.1 ml) |
1.25 ml | 4.0 U |
The central part of the rubber stopper should be cleaned with alcohol. The diluent should be slowly injected into the vial through the rubber stopper and the vial should be gently swirled, avoiding the formation of bubbles. The vial should be discarded if, when creating a vacuum, the diluent is not introduced into the vial. Once reconstituted, the injectable solution should be visually inspected before use to ensure it is a clear and colorless solution free of particles.
Reconstituted NUCEIVA (50 Units/1.25 ml) is injected with a sterile 30-gauge needle. Four units (4 U/0.1 ml) are administered at each of the 5 injection sites (see figure 1): 2 injections in each corrugator muscle (lower inner face and upper inner face) and 1 injection in the procerus muscle, representing a total dose of 20 Units.
Figure 1 Injection points
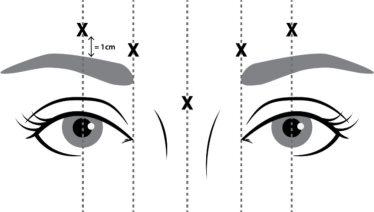
To reduce the complication of eyelid drooping, the following measures should be taken:
- Avoid injection near the levator palpebrae superioris, especially in patients with large eyebrow depressor complexes.
- Injections into the lateral corrugator should be applied at least 1 cm above the supraorbital bony edge.
- Ensure that the volume/dose injected is accurate and, when possible, kept to a minimum.
Procedure for the safe disposal of vials, syringes, and materials used:
Immediately after use, any unused reconstituted injectable solution of NUCEIVA should be inactivated, prior to disposal, with 2 ml of diluted sodium hypochlorite solution (0.5% or 1% available chlorine). After inactivation, dispose of in accordance with local requirements.
Vials, syringes, and used materials should not be emptied and should be disposed of in appropriate containers and eliminated in accordance with local regulations.
Recommendations in case of accident during handling of botulinum toxin:
In case of an accident when handling the product, whether in the dry or reconstituted state, the appropriate measures described below should be applied immediately.
- The toxin is very sensitive to heat and certain chemicals.
- Spills should be cleaned with an absorbent material soaked in a sodium hypochlorite solution (bleach) in the case of the dry product or with a dry absorbent material if the product is already reconstituted.
- Contaminated surfaces should be cleaned with an absorbent material soaked in a sodium hypochlorite solution (bleach) and then dried.
- If a vial is broken, carefully collect the glass fragments and clean the product as indicated above, avoiding cuts to the skin.
- In case of splashes, wash with a sodium hypochlorite solution and rinse thoroughly with plenty of water.
- In case of splashes in the eyes, rinse well with plenty of water or an eye wash solution.
- If the operator is injured (cut, pricked), follow the steps above and take appropriate medical measures depending on the dose injected.
These instructions for use, handling, and disposal should be strictly followed.
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to NUCEIVA 50 units powder for injectable solutionDosage form: INJECTABLE, 200 U/mlActive substance: botulinum toxinManufacturer: Ipsen PharmaPrescription requiredDosage form: INJECTABLE, 125 Speywood UnitsActive substance: botulinum toxinManufacturer: Ipsen Pharma S.A.U.Prescription requiredDosage form: INJECTABLE, 100 unitsActive substance: botulinum toxinManufacturer: Merz Pharmaceuticals GmbhPrescription required
Online doctors for NUCEIVA 50 units powder for injectable solution
Discuss questions about NUCEIVA 50 units powder for injectable solution, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions















