
Рабипур

Спросите врача о рецепте на Рабипур

Инструкция по применению Рабипур
Инструкция, прилагаемая к упаковке: информация для пользователя
Рабипур
Порошок и растворитель для приготовления раствора для инъекций в шприце-ампуле
Вирус бешенства, штамм Flury LEP, (инактивированный)
Необходимо внимательно ознакомиться с содержанием инструкции перед применением вакцины Рабипур, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Эту вакцину назначили конкретному человеку. Не следует передавать ее другим.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. См. пункт 4.
Содержание инструкции
- 1. Что такое вакцина Рабипури для чего она используется
- 2. Важная информация перед применением вакцины Рабипур
- 3. Как применять вакцину Рабипур
- 4. Возможные нежелательные реакции
- 5. Как хранить вакцину Рабипур
- 6. Содержание упаковки и другие сведения
1. Что такое вакцина Рабипур и для чего она используется
Что такое вакцина Рабипур
Рабипур - это вакцина, содержащая убитый вирус бешенства. После введения вакцины иммунная система (естественная защитная система организма) производит антитела против вируса бешенства. Эти антитела защищают от инфекций или заболеваний, вызванных вирусом бешенства. Ни один из компонентов вакцины не может вызвать бешенство.
Для чего используется вакцина Рабипур
Вакцина Рабипур может быть использована у людей любого возраста.
Вакцина Рабипур может быть использована для профилактики заболевания бешенством:
- до возможного контакта с вирусом бешенства (профилактика до контакта) или
- после возможного или подтвержденного контакта с вирусом бешенства (профилактика после контакта). Бешенство - это инфекция, которой можно заразиться, будучи укушенным или поцарапанным, а также просто полизанным зараженным животным, особенно если кожа повреждена. Даже контакт с ловушками для животных, которые были полизаны или погрызены зараженными животными, может быть причиной заражения у людей.
2. Важная информация перед применением вакцины Рабипур
Не следует применять вакцину Рабипур до возможного контакта с вирусом бешенства:
- если у пациента ранее была тяжелая аллергическая реакция на активное вещество или любой из компонентов вакцины, указанных в пункте 6;
- если пациент в настоящее время страдает от острой болезни, требующей лечения. Учитывая, что бешенство - это особенно опасная болезнь, вакцина Рабипур может быть введена любой человеку после контакта с вирусом бешенства, даже беременным женщинам.
Тяжелые аллергические реакции (чувствительность)
Если у пациента есть риск тяжелой аллергической реакции на вакцину или любой из ее компонентов, можно ввести другую вакцину против бешенства, не содержащую этих компонентов. Если другая вакцина недоступна, врач или медсестра оценят риск, связанный с вакцинацией, и риск заражения бешенством.
Предостережения и меры предосторожности
В случае острой болезни, требующей лечения, вакцинация обычно откладывается до как минимум 2 недель после выздоровления. Легкая инфекция не должна быть основанием для отсрочки вакцинации, но необходимо предварительно обсудить это с врачом или медсестрой.
Перед введением вакцины Рабипур в рамках профилактики после контакта необходимо сообщить врачу или медсестре, если:
- пациент имеет тяжелую аллергию на куриные яйца или продукты, содержащие их (симптомы указаны в пункте 4этой инструкции). Вакцина Рабипур содержит следовые количества белка куриных яиц, оставшиеся после производственного процесса.
- пациент имеет тяжелую аллергию на антибиотики, такие как неомицин, хлоротетрациклин или амфотерицин Б. Эти антибиотики могут присутствовать в вакцине в следовых количествах.
- пациент имеет тяжелую аллергию на полигелин. Во время, а также до любого укола может произойти обморок, поэтому необходимо сообщить врачу или медсестре, если у пациента ранее был обморок во время инъекции. После введения вакцины Рабипур были зарегистрированы очень редкие, но тяжелые случаи нарушений, влияющих на нервную систему. См. пункт 4. Противовоспалительные препараты (стероиды), часто используемые для лечения таких нарушений, могут повлиять на эффективность вакцины (см. ниже, Рабипур и другие препараты). О дальнейших действиях в таком случае решит врач или медсестра. Как и в случае со всеми вакцинами, вакцина Рабипур может не защитить полностью всех привитых людей. Вакцины неследует вводить в ягодицы, под кожу или в кровеносный сосуд.
Рабипур и другие препараты
Необходимо сообщить врачу или медсестре о всех препаратах, которые принимает пациент в настоящее время или ранее, а также о препаратах, которые пациент планирует принимать, включая препараты, отпускаемые без рецепта. Если врач не назначил иного, необходимо продолжать принимать все назначенные препараты как обычно.
Если иммунная система пациента ослаблена или пациент принимает препараты, снижающие защитные силы организма, вакцина Рабипур может быть введена, но может не обеспечить такой же высокой защиты, как у других людей. В этом случае врач может назначить анализ крови после вакцинации для проверки уровня антител против вируса бешенства и необходимости возможного введения дополнительных доз вакцины. В случае необходимости необходимо ввести дополнительные дозы вакцины (см. пункт 3этой инструкции).
Вакцина Рабипур может быть введена одновременно с другими инактивированными вакцинами.
Для каждой вакцины необходимо использовать отдельное место инъекции.
Может также потребоваться введение антител против бешенства в инъекции(называемых «иммуноглобулином против бешенства»), если пациент не был полностью привит против бешенства и существует высокий риск заражения вирусом. В этом случае иммуноглобулин против бешенства (который вводится только один раз, обычно с первой дозой вакцины) и вакцина будут введены в разные местана теле.
Беременность и грудное вскармливание
Если пациентка беременна или кормит грудью, предполагает, что может быть беременной, или планирует иметь ребенка, вакцина против бешенства должна быть введена, если произошел или мог произойти контакт с вирусом.
Вакцина Рабипур может также быть введена пациентке, находящейся в состоянии беременности или кормящей грудью, до контакта с вирусом, если риск заражения вирусом считается значительным. В этом случае врач оценит риск, связанный с вакцинацией, и риск заражения бешенством и определит наиболее подходящее время введения вакцины Рабипур.
Вождение транспортных средств и использование машин
Некоторые нежелательные реакции, описанные в пункте 4этой инструкции, могут повлиять на способность вождения транспортных средств и использования машин.
Рабипур содержит:
Менее 23 мг натрия на дозу, что означает, что практически «не содержит натрия».
3. Как применять вакцину Рабипур
Вакцина Рабипур будет введена врачом или медсестрой, прошедшими специальную подготовку по введению вакцин.
Должны быть доступны средства, необходимые для лечения очень тяжелых аллергических реакций, которые могут возникнуть после введения вакцины (см. пункт 4этой инструкции). Вакцина должна быть введена в поликлинике или кабинете, где доступны средства, необходимые для лечения таких реакций.
Инструкция для врачей и медицинского персонала по реконструкции вакцины можно найти в конце этой инструкции.
Рекомендуемая доза для взрослых и детей любого возраста составляет один миллилитр (1 мл) на инъекцию.
Врач решит, сколько доз необходимо ввести. Количество доз зависит от того, вводится ли вакцина Рабипур до возможного контакта с вирусом или после него.
Вакцина вводится в виде инъекции в мышцу (обычно в верхнюю часть руки или, у маленьких детей, в мышцу бедра).
ДОЗИРОВАНИЕ ДО ВОЗМОЖНОГО КОНТАКТА С ВИРУСОМ
В случае людей, никогда не привитыхпротив бешенства:
- первоначально необходимо ввести 3 дозы вакцины. Первую дозу вводят во время первого посещения, вторую дозу - через 7 дней, а третью дозу - через 21 или 28 дней после первой дозы.
- у взрослых в возрасте от 18 до 65 лет, которым необходимо быстрое развитие защиты, вакцина Рабипур может быть введена также в три дозы в течение 7 дней. Первую дозу вводят во время первого посещения, вторую дозу - через 3 дня, а третью дозу - через 4 дня после второй дозы.
- альтернативно, у людей с нормальной иммунной реакцией вакцина Рабипур может быть введена в две дозы в течение 7 дней. Первую дозу вводят во время первого посещения, а вторую дозу - через 7 дней. Если срок вакцинации был пропущен, необходимо обеспечить введение вакцины как можно скорее после рекомендованного срока.
Необходимость введения дополнительных доз зависит от риска контакта с вирусом бешенства.
Врач, ознакомившись с официальными рекомендациями по вакцинации против бешенства, оценит необходимость введения дополнительной дозы.
В случае людей с постоянным высоким рискомзаражения врач может также рекомендовать регулярное проведение тестов на определение уровня антител против вируса бешенства в крови, чтобы в случае необходимости провести дополнительную дозу как можно скорее.
Опыт показывает, что дополнительные дозы обычно необходимы каждые 2-5 лет.
ДОЗИРОВАНИЕ ПОСЛЕ ВОЗМОЖНОГО ИЛИ ПОДТВЕРЖДЕННОГО КОНТАКТА С ВИРУСОМ
Люди, ранее привитые
В случае людей, которые были полностью привиты против бешенства и/или получили дополнительные дозы, после контакта с животным, зараженным бешенством или подозреваемым в бешенстве, обычно вводят 2 дополнительные дозы вакцины (по 1,0 мл каждая). Первую дозу вводят как можно скорее после контакта, а вторую - через 3 дня.
Люди, не привитые
В случае людей, которые не были ранее привиты или получили неполную основную вакцинацию, вводят 4 или 5 доз (по 1,0 мл каждая) в соответствии с одним из следующих схем:
- в случае использования четырехдозовой схемы, первые 2 дозы вакцины вводят как можно скорее после контакта в день 0, а следующие одиночные дозы вводят через 7 и 21 день после первой дозы.
- альтернативная четырехдозовая схема может быть использована у здоровых людей с известной хорошей иммунной реакцией; первую дозу вводят как можно скорее после контакта в день 0, а следующие дозы вводят через 3, 7 и 14 дней после введения первой дозы.
- в случае использования пятидозовой схемы, первую дозу вакцины вводят как можно скорее после контакта в день 0, а следующие дозы вводят через 3, 7, 14 и 28 дней после первой дозы. После возможного контактас вирусом бешенства врач оценит риск заражения в зависимости от типа контакта, который произошел. Например, у людей, которые были укушены или поцарапаны животным, которое может быть заражено вирусом, или которые имели контакт с летучими мышами, риск заражения вирусом бешенства намного выше, чем у людей, которые были полизаны животным, но их кожа не повреждена. Люди с нарушением иммунной системы (с ослабленным иммунитетом)
В случае людей с повышенным риском заражения бешенством из-за нарушения иммунной системы после контакта с животным, зараженным бешенством или подозреваемым в бешенстве, необходимо ввести 5 или 6 доз (по 1,0 мл каждая) вакцины против бешенства. Помимо введения вакцины, необходимо провести местное лечение раны и ввести иммуноглобулин против бешенства. В случае использования шестидозовой схемы, первые 2 дозы вводят как можно скорее после контакта, а следующие одиночные дозы вводят через 3, 7, 14 и 28 дней после первой дозы. В случае использования пятидозовой схемы, первую дозу вводят как можно скорее после контакта, а следующие дозы вводят через 3, 7, 14 и 28 дней после первой дозы. Может также потребоваться анализ крови для оценки уровня антител против вируса бешенства и необходимости возможного введения дополнительных доз вакцины. Врач сообщит пациенту, что необходимо делать и когда обратиться для проведения дополнительных исследований или вакцинации дополнительными дозами.
4. Возможные нежелательные реакции
Как и любой препарат, этот препарат может вызывать нежелательные реакции, хотя они не возникают у каждого человека.
Тяжелые нежелательные реакции, затрагивающие все тело, иногда с сопровождающим шоком (опасно низкое кровяное давление)*, могут возникнуть после введения вакцины Рабипур. Адекватное лечение и наблюдение должны быть всегда легко доступны на случай возникновения редких тяжелых аллергических реакций на вакцину. Если они возникают, необходимо немедленно сообщить об этом врачу.
К наиболее часто зарегистрированным нежелательным реакциям, связанным с использованием вакцины Рабипур, относятся боль в месте инъекции, в основном боль, связанная с выполнением инъекции, или уплотнение кожи в месте инъекции. Эти реакции возникали очень часто (у более чем 1 из 10 человек). Большинство реакций в месте инъекции имели легкий или умеренный характер и проходили в течение 24-48 часов после введения вакцины.
Другие нежелательные реакции включают:
Очень часто(могут возникнуть у более чем 1 из 10 человек)
Головная боль
Головокружение
Сыпь
Общее недомогание
Усталость
Слабость
Лихорадка
Часто(могут возникнуть у не более чем 1 из 10 человек)
Увеличение лимфатических узлов
Понижение аппетита
Тошнота
Рвота
Диарея
Боль в животе/ дискомфорт в желудке
Крапивница
Боль в мышцах
Боль в суставах
Редко(могут возникнуть у не более чем 1 из 1000 человек)
Аллергические реакции
Чувство онемения, покалывания
Потливость
Озноб
Очень редко(могут возникнуть у не более чем 1 из 10 000 человек)
Воспаление мозга, повреждение нерва, которое может вызывать онемение, невозможность двигаться или потерю чувствительности в некоторых частях тела*
Обморок, шаткость с головокружением*
Тяжелые аллергические реакции, которые могут вызывать отек лица или горла*
*Описание нежелательных реакций, зарегистрированных спонтанно
Дополнительные нежелательные реакции, возникающие у детей
Ожидается, что частота, тип и тяжесть нежелательных реакций у детей такие же, как и у взрослых.
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления регистрации лекарственных препаратов, медицинских изделий и биоцидных препаратов, Ал. Ерозолимских 181С, 02-222 Варшава, тел.: +48 22 49 21 301, факс: +48 22 49 21 309. Сайт: https://smz.ezdrowie.gov.pl. Нежелательные реакции можно также сообщать ответственному лицу.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности использования препарата.
5. Как хранить вакцину Рабипур
Вакцину необходимо хранить в месте, недоступном для детей.
Защищать от света. Хранить в холодильнике (2°C – 8°C). Не замораживать.
Хранить флакон и шприц-ампулу в наружной упаковке для защиты от света.
Не использовать эту вакцину после истечения срока годности, указанного на наружной упаковке.
Срок годности указывает последний день указанного месяца.
Вакцин не следует выбрасывать в канализацию. Необходимо спросить у фармацевта, как утилизировать препараты, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит вакцина Рабипур
Активным веществомвакцины является вирус бешенства (инактивированный, штамм Flury LEP) не менее 2,5 ИЕ, выращенный на очищенных эмбриональных клетках курицы (анг. purified chick embryo cells, PCEC).
Другими компонентамиявляются: трометамол, хлорид натрия, эдетат натрия, глутаминат калия, полигелин, сахароза и вода для инъекций. Белки куриных яиц (например, альбумин яиц), человеческий альбумин, неомицин, хлоротетрациклин, амфотерицин Б присутствуют в вакцине как остатки.
Как выглядит вакцина Рабипур и что содержит упаковка
Рабипур - это белый, лиофилизированный порошок, предназначенный для реконструкции с помощью прозрачного, бесцветного растворителя. Вакцина после реконструкции является прозрачной до слегка опалесцирующей и бесцветной до легкого розового цвета.
Вакцина Рабипур поставляется в упаковках, содержащих 1 флакон порошка, 1 шприц-ампулу одноразового использования с стерильным растворителем и 2 идентичными иглами (25 Г, 25 мм) - одну для реконструкции и одну для инъекции.
Ответственное лицо и производитель
Ответственное лицо
Bavarian Nordic A/S
Филип Хейманс Алле 3
2900 Хеллеруп
Дания
Производитель
GSK Vaccines GmbH
Эмиль-фон-Беринг-Штр. 76
35041 Марбург
Германия
Bavarian Nordic A/S
Хейресковвег 10А
3490 Квистгард
Дания
Этот препарат разрешен к обращению в странах-членах Европейского экономического пространства под следующими названиями:
Австрия
Рабипур
Бельгия
Рабипур
Хорватия
Рабипур
Дания
Рабипур
Франция
Рабипур
Испания
Рабипур
Нидерланды
Рабипур
Люксембург
Рабипур
Германия
Рабипур
Норвегия
Рабипур
Польша
Рабипур
Португалия
Рабипур
Швеция
Рабипур
Венгрия
Рабипур
Италия
Рабипур
Дата последнего обновления инструкции:
Другие источники информации
Информация, предназначенная только для медицинского персонала:
Инструкция по использованию шприца-ампулы одноразового использования с вакциной Рабипур
Шприц-ампула
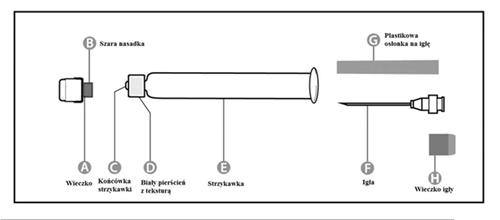
| Шаг 1: Одной рукой держать шприц (Е) так, чтобы крышка была направлена вверх. Необходимо держать шприц за белое кольцо с текстурой (D). | 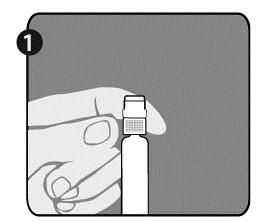 |
| Шаг 2: Другой рукой взять крышку (А) и сильно двигать ею в обе стороны, чтобы оторвать ее от кольца (D). Не поворачивать/откручивать крышку. | 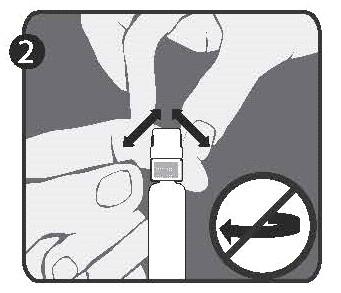 |
| Шаг 3: Поднять крышку, чтобы снять ее (А) и избавиться от серой насадки (Б). Обратите внимание, чтобы не коснуться стерильного кончика шприца (С). | 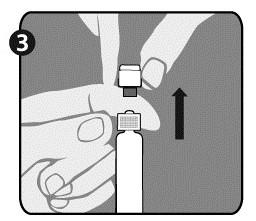 |
Надевание иглы (инструкция относится к обоим поставляемым иглам):
| Шаг 1: Повернуть крышку (Х), чтобы снять ее с одной из двух идентичных игл. Это будет игла, используемая для реконструкции. Не удалять пластиковый защитный чехол (Г). | 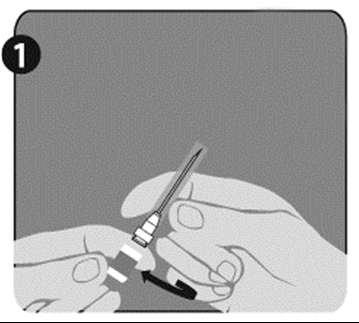 |
| Шаг 2: Одной рукой крепко держать шприц (Е) за белое кольцо с текстурой (D). Другой рукой надеть эту иглу (Ф) и поворачивать ее по часовой стрелке, пока она не заблокируется на месте. После надевания иглы удалить пластиковый защитный чехол (Г). Шприц (Е) готов к использованию. | 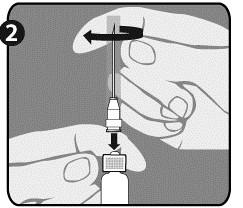 |
Инструкция по реконструкции вакцины Рабипур с помощью шприца-ампулы:
И перед реконструкцией вакцины, и после нее необходимо визуально проверить, не содержит ли она посторонних предметов и не изменился ли вид препарата. Не следует использовать вакцину, если ее вид изменился. Вакцина после реконструкции является прозрачной до слегка опалесцирующей и бесцветной до легкого розового цвета.
Порошок должен быть растворен с помощью прилагаемого растворителя для приготовления раствора. Раствор перед инъекцией необходимо осторожно встряхнуть. Вакцина должна быть введена сразу после реконструкции.
В флаконе присутствует под давлением. После реконструкции вакцины рекомендуется открутить шприц от иглы, чтобы удалить под давлением. После выполнения этой операции можно будет легко оттянуть вакцину из флакона. Не рекомендуется создавать чрезмерное давление, поскольку это может вызвать проблемы с оттягиванием необходимого количества вакцины.
Длина иглы не позволяет достичь до дна флакона, поэтому необходимо перевернуть флакон и оттянуть иглу назад, близко к пробке. Это позволит получить всю необходимую quantity раствора вакцины из флакона.
После реконструкции вакцины удалить крышку с второй иглы (как описано в шаге 1 для игл), а затем заменить иглу, использованную для реконструкции, на вторую иглу, которая будет использована для инъекции.
Не использовать одну и ту же иглу для реконструкции и инъекции.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- ИмпортерBavarian Nordic A/S GSK Vaccines GmbH
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги РабипурФорма выпуска: Порошок, 3,25 МЕ вируса бешенства, штамм Wistar Rabies PM/WI38 1503-3M (инактивированный)/0,5 мл; 1 доза (0,5 мл)Активное вещество: rabies, inactivated, whole virusТребуется рецептФорма выпуска: Суспензия, 160 единиц антигена ELISA вируса гепатита A, штамм GBM/0,5 мл; 1 доза (0,5 мл)Активное вещество: hepatitis A, inactivated, whole virusТребуется рецептФорма выпуска: Суспензия, 60 мкг HA/штамм, 1 доза (0,7 мл)Активное вещество: influenza, inactivated, split virus or surface antigenТребуется рецепт
Аналоги Рабипур в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Рабипур в Испания
Аналог Рабипур в Украина
Врачи онлайн по Рабипур
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Рабипур – по решению врача и с учетом местных правил.














