
Приорикс-тетра

Спросите врача о рецепте на Приорикс-тетра

Инструкция по применению Приорикс-тетра
Инструкция, прилагаемая к упаковке: информация для пользователя
Priorix-Tetra, порошок и растворитель для приготовления раствора для инъекций в ампуло-шприце
шприц
Вакцина против кори, эпидемического паротита, краснухи и ветряной оспы, живая
Необходимо внимательно ознакомиться с содержанием инструкции перед применением вакцины, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу или фармацевту.
- Этот препарат назначен строго определённому лицу. Не следует передавать его другим.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или фармацевту. См. пункт 4.
Содержание этой инструкции сформулировано с учетом того, что она будет читаться лицом, получающим вакцину. Однако, поскольку вакцина может быть введена взрослым и детям, возможно, что содержание инструкции будет ознакомлено родителем или опекуном ребенка.
Содержание инструкции
- 1. Что такое вакцина Priorix-Tetra и для чего она используется
- 2. Информация, важная перед применением вакцины Priorix-Tetra
- 3. Как применять вакцину Priorix-Tetra
- 4. Возможные нежелательные реакции
- 5. Как хранить вакцину Priorix-Tetra
- 6. Содержание упаковки и другие сведения
1. Что такое вакцина Priorix-Tetra и для чего она используется
Priorix-Tetra - это вакцина, применяемая у лиц в возрасте от 11 месяцев для профилактики заболеваний, вызываемых вирусами кори, эпидемического паротита, краснухи и ветряной оспы. В определенных обстоятельствах Priorix-Tetra может быть введена детям после 9-го месяца жизни.
Как действует вакцина Priorix-Tetra
После введения вакцины Priorix-Tetra иммунная система (защитная система организма) вакцинированного человека начинает производить антитела, которые защищают от заражения вирусами кори, эпидемического паротита, краснухи и ветряной оспы.
Хотя Priorix-Tetra содержит живые вирусы, они ослаблены до такой степени, что не могут вызвать корь, эпидемический паротит, краснуху и ветряную оспу у здоровых людей.
Как и в случае с другими вакцинами, Priorix-Tetra может не полностью защитить всех вакцинированных лиц.
2. Информация, важная перед применением вакцины Priorix-Tetra
Когда не применять вакцину Priorix-Tetra
- если у пациента выявлена аллергия на любой компонент этой вакцины (перечисленный в пункте 6). Среди симптомов аллергической реакции следует упомянуть зудящую кожную сыпь, трудности с дыханием, отек лица или языка,
- если у пациента произошла аллергическая реакция после предыдущего введения любой вакцины против кори, эпидемического паротита, краснухи и (или) ветряной оспы,
- если пациент аллергичен на нейомицин (антибиотик). Выявленный контактный дерматит, вызванный нейомицином (кожная сыпь, возникающая в результате прямого контакта кожи с аллергеном, таким как нейомицин), не должен быть проблемой, но сначала необходимо
проконсультироваться с врачом,
- если у пациента есть тяжелая инфекция с лихорадкой. В этом случае вакцинация должна быть отложена до выздоровления. Легкая инфекция, такая как простуда, не должна быть противопоказанием для вакцинации, но сначала необходимо сообщить об этом врачу,
- если у пациента есть любое заболевание (например, инфекция, вызванная вирусом иммунодефицита человека (ВИЧ) или синдром приобретенного иммунодефицита (СПИД)) или если пациент принимает лекарства, которые могут ослабить иммунную систему. То, будет ли пациент получать вакцину, будет зависеть от уровня иммунитета,
- если выявлена беременность. Кроме того, необходимо избегать беременности в течение 1 месяца после вакцинации.
Предостережения и меры предосторожности
Необходимо проконсультироваться с врачом или фармацевтом перед введением вакцины Priorix-Tetra, если:
- в анамнезе или семейном анамнезе выявлено наличие у пациента судорог, включая судороги, вызванные лихорадкой. В этом случае пациент должен быть внимательно наблюдаем после вакцинации, поскольку лихорадка, связанная с вакцинацией, может возникнуть особенно в период с 5-го по 12-й день после введения вакцины (см. пункт 4),
- у пациента ранее произошла тяжелая аллергическая реакция на яичный белок,
- у пациента произошли нежелательные реакции после вакцинации против кори, эпидемического паротита или краснухи, включая легкое образование синяков или более длительное кровотечение (см. пункт 4),
- если у пациента ослаблен иммунитет (например, в случае заражения ВИЧ). Пациента необходимо подвергнуть тщательному наблюдению, поскольку ответ на вакцину может быть недостаточным для обеспечения защиты от заболевания (см. пункт 2 «Когда не применять вакцину Priorix-Tetra»).
Если пациент был вакцинирован в течение 72 часов после контакта с человеком, больным корью или ветряной оспой, вакцина Priorix-Tetra может обеспечить некоторую защиту от заболевания.
После вакцинации пациент должен в течение как минимум 6 недель после вакцинации стараться избегать близкого контакта с:
- лицами с пониженным иммунитетом к инфекциям,
- беременными женщинами, которые ранее не болели ветряной оспой или не были вакцинированы против ветряной оспы,
- новорожденными детьми матерей, которые ранее не болели ветряной оспой или не были вакцинированы против ветряной оспы.
После или даже до введения каждой вакцины в виде инъекции может возникнуть обморок (особенно у подростков). В связи с этим необходимо сообщить врачу или медсестре, если у пациента ранее произошел обморок во время введения инъекции.
Как и в случае с другими вакцинами, вакцина Priorix-Tetra может не полностью защитить всех вакцинированных лиц. Однако у вакцинированных лиц течение заболевания обычно бывает намного легче, чем у невакцинированных.
Вакцина Priorix-Tetra и другие лекарства
Необходимо сообщить врачу о всех лекарствах, которые пациент принимает в настоящее время или принимал недавно, о лекарствах, которые пациент планирует принимать, и о вакцинах, которые пациент получил недавно.
Вакцинация может быть отложена врачом на как минимум 3 месяца, если пациент недавно получил переливание крови или человеческие антитела (иммуноглобулин).
Если у пациента будет проведен тест на туберкулин (кожное исследование на туберкулез), его необходимо провести до или одновременно с введением вакцины или после истечения 6 недель после вакцинации.
Необходимо избегать приема салицилатов (веществ, входящих в состав многих жаропонижающих и обезболивающих препаратов) в течение 6 недель после вакцинации.
Priorix-Tetra может быть введена одновременно с другими вакцинами. Каждая вакцина должна быть введена в другое место на теле.
Беременность и грудное вскармливание
Вакцину Priorix-Tetra не следует вводить беременным женщинам.
В случае беременности или грудного вскармливания или если существует подозрение, что женщина беременна, или если она планирует иметь ребенка, перед применением этой вакцины необходимо проконсультироваться с врачом или фармацевтом. Кроме того, важно, чтобы в течение месяца после вакцинации пациентка не стала беременной. В это время необходимо использовать эффективный метод контрацепции, чтобы избежать беременности.
Вождение транспортных средств и эксплуатация машин
Нет данных, которые бы свидетельствовали о том, что вакцина Priorix-Tetra влияет на способность вождения транспортных средств и эксплуатации машин.
Priorix-Tetra содержит сорбитол, пара-аминобензойную кислоту, фенилаланин, натрий и калий
Эта вакцина содержит 14 мг сорбитола в каждой дозе.
Priorix-Tetra содержит пара-аминобензойную кислоту. Она может вызывать аллергические реакции (возможные реакции замедленного типа) и в редких случаях бронхоспазм.
Вакцина содержит 583 мкг фенилаланина в каждой дозе. Фенилаланин может быть вредным для пациентов с фенилкетонурией (ФКУ), редким генетическим заболеванием, при котором фенилаланин накапливается в организме, поскольку организм не удаляет ее должным образом.
Эта вакцина содержит менее 1 ммоль (23 мг) натрия на дозу, то есть вакцину считают «свободной от натрия».
Эта вакцина содержит калий, менее 1 ммоль (39 мг) калия на дозу, то есть вакцину считают «свободной от калия».
3. Как применять вакцину Priorix-Tetra
Priorix-Tetra вводится подкожно или внутримышечно, в верхнюю часть руки или внешнюю часть бедра.
Priorix-Tetra предназначен для лиц в возрасте от 11 месяцев.
Срок вакцинации и количество доз, которые получит пациент, будут определены врачом на основе официальных рекомендаций.
Вакцины в любом случае не следует вводить внутривенно.
4. Возможные нежелательные реакции
Как и в случае с любым лекарством, нежелательные реакции также могут возникнуть после введения этой вакцины, хотя они не возникают у каждого.
После введения вакцины могут возникнуть следующие нежелательные реакции:
♦
Очень часто (могут возникнуть чаще, чем 1 на 10 доз вакцины):
- боль и покраснение в месте инъекции
- лихорадка 38°C или выше*
- отек в месте инъекции, в случае, когда вакцина вводится молодым людям и взрослым
♦
Часто (могут возникнуть не чаще, чем 1 на 10 доз вакцины):
- отек в месте инъекции, в случае, когда вакцина вводится детям
- лихорадка выше 39,5°C*
- раздражительность
- сыпь (пятна и (или) пузырьки)
♦
Не очень часто (могут возникнуть не чаще, чем 1 на 100 доз вакцины):
- необычный плач, нервозность, бессонница
- общее плохое самочувствие, вялость, усталость
- отек слюнных желез
- диарея, рвота
- потеря аппетита
- инфекция верхних дыхательных путей
- насморк
- отек лимфатических узлов
♦
Редко (могут возникнуть не чаще, чем 1 на 1 000 доз вакцины):
- инфекция среднего уха
- судороги, вызванные лихорадкой
- кашель
- бронхит
* Было обнаружено более частое возникновение лихорадки после введения первой дозы вакцины Priorix-Tetra по сравнению с отдельным введением вакцины против кори, эпидемического паротита, краснухи и вакцины против ветряной оспы во время одного и того же посещения.
Следующие нежелательные реакции были зарегистрированы во время регулярного применения вакцины против кори, эпидемического паротита и краснухи или вакцины против ветряной оспы, производимых компанией GlaxoSmithKline Biologicals:
- боль в суставах и мышцах
- аллергические реакции (аллергия). Такое состояние может проявляться зудящей или пузырчатой сыпью, отеком век и лица, трудностями с дыханием или глотанием, внезапным падением артериального давления и потерей сознания. Указанные реакции могут возникнуть еще до выхода из кабинета врача. Если у пациента возник любой из вышеуказанных симптомов, необходимо немедленно обратиться к врачу
- инфекция или воспаление мозга, спинного мозга и периферических нервов,导致щие временные трудности с ходьбой (неустойчивость) и/или временную потерю координации движений, инсульт, воспаление некоторых нервов с возможным онемением или потерей чувствительности или нарушениями движений (синдром Гийена-Барре)
- сужение или блокировка кровеносных сосудов
- малые местные кровотечения или более легкое, чем обычно, образование синяков из-за снижения количества тромбоцитов
- многоформная эритема (симптомы включают красные, часто зудящие пятна, подобные сыпи, возникающей при ветряной оспе, которые появляются на конечностях, а иногда на лице и других частях тела)
- сыпь, похожая на возникшую при ветряной оспе
- опоясывающий лишай
- симптомы, похожие на корь и эпидемический паротит (в том числе временный, болезненный отек яичек и опухание лимфатических узлов на шее)
Сообщение о нежелательных реакциях
Если возникнут любые нежелательные реакции, включая любые нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу или фармацевту. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных средств Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов:
Ал. Ерозолимские 181С
02-222 Варшава
Тел.: 22 49 21 301
Факс: 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции также можно сообщать в организацию, ответственной за выпуск продукта.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности применения лекарства.
5. Как хранить вакцину Priorix-Tetra
Хранить вакцину в месте, недоступном для детей.
Не применять эту вакцину после истечения срока годности, указанного на этикетке после «EXP». Срок годности указывает последний день указанного месяца.
Аббревиатура «Lot» обозначает номер серии вакцины.
Хранить и перевозить в охлажденном состоянии (2°C - 8°C).
Не замораживать.
Хранить в оригинальной упаковке для защиты от света.
После реconstitution вакцина должна быть введена немедленно или должна быть хранена в холодильнике (2°C - 8°C). Если она не будет использована в течение 24 часов, ее необходимо утилизировать.
Лекарства не следует выбрасывать в канализацию или домашние контейнеры для отходов. Необходимо спросить у фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит вакцина Priorix-Tetra
Активными веществами вакцины являются: живые, аттенуированные вирусы кори, эпидемического паротита, краснухи и ветряной оспы.
Другие компоненты вакцины:
Порошок: аминокислоты (в том числе фенилаланин), лактоза безводная, маннитол (Е 421), сорбитол (Е 420), среда 199 (в том числе фенилаланин, пара-аминобензойная кислота, натрий и калий).
Растворитель: вода для инъекций.
Как выглядит вакцина Priorix-Tetra и что содержит упаковка
Вакцина поставляется в виде порошка и растворителя для приготовления раствора для инъекций (порошок находится в 1-дозовой ампуле, растворитель в ампуло-шприце по 0,5 мл), с отдельными иглами или без игл, в следующих упаковках:
- с 2 отдельными иглами: упаковки по 1 или 10,
- без игл: упаковки по 1 или 10.
Вакцина Priorix-Tetra имеет вид белого или слегка розового порошка, часть которого может быть желтоватой, и прозрачного, бесцветного растворителя (воды для инъекций) для растворения порошка.
Не все размеры упаковок могут находиться в обращении.
Ответственное лицо и производитель
GlaxoSmithKline Biologicals S.A.
Рю де л'Институт 89
Б-1330 Рикенсарт
Бельгия
Дата последней актуализации инструкции:март 2025
Другие источники информации
Подробная информация о этой вакцине доступна на сайте Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов .
-------------------------------------------------------------------------------------------------------------------------
Информация, предназначенная только для медицинского персонала:
Как и в случае со всеми вакцинами, вводимыми в виде инъекций, всегда необходимо обеспечить возможность надлежащего лечения и медицинского наблюдения на случай редко возникающих после вакцинации анафилактических реакций.
Алкоголь, а также другие дезинфицирующие средства должны испариться с кожи перед введением вакцины, поскольку они могут инактивировать аттенуированные вирусы, содержащиеся в вакцине.
Вакцины Priorix-Tetra ни в коем случае не следует вводить внутривенно или внутрикожно.
Поскольку не проводились исследования по совместимости, не следует смешивать лекарственный продукт с другими лекарствами.
Вакцину после реconstitution необходимо подвергнуть визуальной оценке. Из-за небольших изменений pH вакцина после реconstitution может принимать цвет от светло-персикового до розового оттенка фуксии. После реconstitution могут быть видны полупрозрачные частицы продукта. Это явление нормальное и не влияет на действие вакцины.
Если вакцина имеет другую окраску или содержит другие твердые частицы, ее не следует вводить.
Вакцину необходимо реconstituir, добавив весь растворитель из ампуло-шприца в ампулу с порошком.
Чтобы присоединить иглу к ампуло-шприцу, необходимо внимательно ознакомиться с инструкцией, представленной на рисунках 1 и 2. Ампуло-шприц, поставляемый с вакциной Priorix-Tetra, может слегка отличаться от представленного на рисунке (может не иметь резьбы для вкручивания иглы). В этом случае игла должна быть закреплена без вкручивания.
Игла
Ампуло-шприц
Необходимо всегда держать ампуло-шприц за его корпус, а не за поршень или адаптер Luer Lock (Luer Lock Adaptor, LLA), а иглу необходимо держать в оси ампуло-шприца (как показано на рисунке 2). Неисполнение этих рекомендаций может привести к перекосу адаптера LLA и утечке из ампуло-шприца.
Если во время присоединения иглы к ампуло-шприцу происходит отсоединение адаптера LLA, необходимо использовать новую дозу вакцины (новую ампуло-шприц и ампулу).
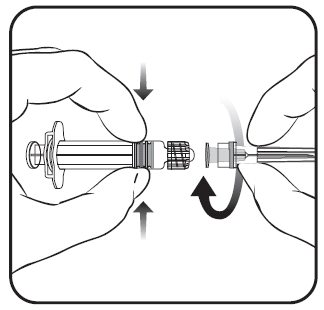
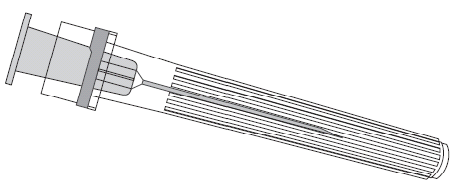
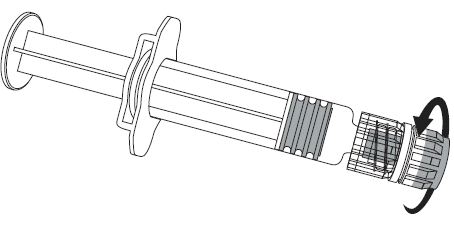
Рисунок 1. Рисунок 2.
- 1. Необходимо открутить крышку ампуло-шприца, повернув ее в направлении, противоположном направлению часовой стрелки (как показано на рисунке 1).
Независимо от того, вращается ли адаптер LLA или нет, необходимо следовать следующим инструкциям:
- 2. Необходимо присоединить иглу к ампуло-шприцу, осторожно присоединив насадку иглы к адаптеру LLA и повернув ее на четверть оборота в направлении, совпадающем с направлением часовой стрелки, до тех пор, пока не будет чувствоваться блокировка иглы (как показано на рисунке 2).
- 3. Необходимо снять защитный чехол иглы, который может оказывать сопротивление.
- 4. Необходимо добавить растворитель к порошку. Затем необходимо энергично встряхнуть до полного растворения порошка.
- 5. Необходимо набрать всю содержимое ампулы.
- 6. Для введения вакцины необходимо использовать новую иглу. Для этого необходимо открутить иглу от ампуло-шприца и присоединить иглу для инъекций, следуя описанию, содержащемуся в пункте 2.
- 7.
После реconstitution вакцина должна быть введена немедленно или должна быть хранена в холодильнике (2°C - 8°C). Если она не будет использована в течение 24 часов, ее необходимо утилизировать.
Все остатки непримененного лекарственного продукта или его отходы необходимо утилизировать в соответствии с местными правилами.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- ИмпортерGlaxoSmithKline Biologicals S.A.
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Приорикс-тетраФорма выпуска: Порошок, -Активное вещество: measles, combinations with mumps, rubella and varicella, live attenuatedПроизводитель: GlaxoSmithKline Biologicals S.A.Требуется рецептФорма выпуска: Порошок, -Активное вещество: measles, combinations with mumps and rubella, live attenuatedПроизводитель: GlaxoSmithKline Biologicals S.A.Требуется рецептФорма выпуска: Суспензия, 160 единиц антигена ELISA вируса гепатита A, штамм GBM/0,5 мл; 1 доза (0,5 мл)Активное вещество: hepatitis A, inactivated, whole virusТребуется рецепт
Аналоги Приорикс-тетра в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Приорикс-тетра в Испания
Аналог Приорикс-тетра в Украина
Врачи онлайн по Приорикс-тетра
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Приорикс-тетра – по решению врача и с учетом местных правил.














