

Пгоксилиум

Спросите врача о рецепте на Пгоксилиум

Инструкция по применению Пгоксилиум
Инструкция, прилагаемая к упаковке: Информация для пользователя
ФОКСИЛИУМ 1,2 ммоль/л фосфатов
Раствор для гемодиализа и гемофильтрации
Хлорид кальция дигидрат, хлорид магния гексагидрат, хлорид натрия, бикарбонат натрия, хлорид калия, безводный дифосфат натрия
Прежде чем использовать препарат, необходимо внимательно ознакомиться с содержанием инструкции, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы иметь возможность повторно прочитать ее при необходимости.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Если у пациента出现ы любые нежелательные явления, включая те, которые не указаны в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. См. пункт 4.
Содержание инструкции:
- 1. Что такое препарат Фоксилиум и для чего он используется
- 2. Важная информация перед использованием препарата Фоксилиум
- 3. Как использовать препарат Фоксилиум
- 4. Возможные нежелательные явления
- 5. Как хранить препарат Фоксилиум
- 6. Содержание упаковки и другие сведения
1. Что такое препарат Фоксилиум и для чего он используется
Препарат Фоксилиум, относящийся к группе растворов для гемофильтрации, содержит хлорид кальция дигидрат, магний хлорид гексагидрат, хлорид натрия, бикарбонат натрия, хлорид калия и безводный дифосфат натрия.
Препарат Фоксилиум используется в больницах в условиях интенсивной медицинской помощи для восстановления химического баланса крови у пациентов с повреждением почек.
Продолжительное лечениезаместительной почечной терапии направлено на удаление накопившихся продуктов обмена из крови в ситуации, когда почки не функционируют.
Раствор Фоксилиумиспользуется для лечения пациентов в критическом состоянии с острым повреждением почек, которые характеризуются:
- нормальным содержанием калия в крови (нормокалиемия)или
- нормальным или низким содержанием фосфатов в крови (нормо- или гипофосфатемия).
Этот препарат также можно использовать в случае отравления лекарствами, содержащими вещества, подвергающиеся диализу или фильтрации.
2. Важная информация перед использованием препарата Фоксилиум
Не использовать препарат Фоксилиум в следующих трех случаях:
- если у пациента наблюдается высокое содержание калия в крови (гиперкалиемия);
- если у пациента наблюдается высокое содержание бикарбоната в крови (метаболический алкалоз);
- если у пациента наблюдается высокое содержание фосфатов в крови (гиперфосфатемия).
1/8
Не использовать гемодиализ или гемофильтрацию в следующих трех случаях:
- если с помощью гемофильтрации невозможно облегчить симптомы, вызванные высоким содержанием мочевины в крови (симптомы уремии),которые являются результатом повреждения почек с выраженным гиперкатаболизмом (неправильный рост процессов распада веществ);
- недостаточное артериальное давление в сосудистом доступе;
- снижение свертываемости крови (общая антикоагуляция)при существующем риске кровотечения.
Предостережения и меры предосторожности
Прежде чем начать использовать препарат Фоксилиум, необходимо обсудить это с врачом, фармацевтом или медсестрой.
Прежде чем начать лечение и во время его проведения будет контролироваться кровь, т.е. будет контролироваться кислотно-щелочной баланс и содержание солей (электролитов), включая объем введенных (внутривенных вливаний) и удаленных (мочи) жидкостей, даже если они не связаны напрямую с лечением.
Препарат Фоксилиум и другие лекарства
Необходимо сообщить врачу или фармацевту о всех лекарствах, которые пациент принимает в настоящее время или принимал недавно, а также о лекарствах, которые пациент планирует принимать. Необходимо сделать это, поскольку содержание других принимаемых лекарств может повлиять на лечение Фоксилиумом. Врач решит, необходимо ли вносить какие-либо изменения в другие принимаемые лекарства.
В частности, необходимо сообщить о приеме:
- фосфатов из дополнительных источников (например, питательных жидкостей), поскольку они могут увеличить риск возникновения высокого содержания фосфатов в крови (гиперфосфатемия);
- витамина D и лекарств, содержащих хлорид кальция или глюконат кальция, из-за возможности увеличения риска возникновения высокого содержания кальция в крови (гиперкальциемия);
- бикарбоната натрия, поскольку это может увеличить риск избытка бикарбоната в крови (метаболический алкалоз);
- цитрата как антикоагулянт, поскольку он может снижать содержание кальция в сыворотке крови.
Беременность, грудное вскармливание и влияние на фертильность
Беременность и грудное вскармливание:
Нет документированных клинических данных о применении этого препарата во время беременности и лактации. Этот препарат должен быть назначен женщинам в период беременности и лактации только в случае явной необходимости.
Фертильность:
Не ожидается влияние препарата на фертильность, поскольку кальций, натрий, калий, магний, хлориды, фосфаты и бикарбонаты являются нормальными компонентами организма.
Вождение транспортных средств и управление механизмами
Фоксилиум не влияет на способность управлять транспортными средствами и механизмами.
3. Как использовать препарат Фоксилиум
Фоксилиум является препаратом, применяемым в больницах и вводимым исключительно медицинским персоналом.
Объем препарата Фоксилиум и, следовательно, доза зависят от состояния пациента. Объем дозы определяет врач, ответственный за лечение.
Препарат Фоксилиум может быть введен непосредственно в кровоток (внутривенно)через аппарат для CRRT или через гемодиализ, когда раствор проходит по одной стороне диализной мембраны, а кровь - по другой стороне.
2/8
Этот препарат всегда должен использоваться точно в соответствии с рекомендациями врача, фармацевта или медсестры. В случае сомнений необходимо обратиться к врачу, фармацевту или медсестре.
Инструкция по применению находится в разделе "Ниже приведенная информация предназначена исключительно для медицинских работников".
Использование большей, чем рекомендуемая, дозы Фоксилиума
Препарат Фоксилиум предназначен для использования в больницах и вводится исключительно врачами в условиях тщательного мониторинга баланса жидкости и химического состава крови.
Следовательно, маловероятно использование большей, чем рекомендуемая, дозы Фоксилиума.
В маловероятном случае передозировки лечащий врач примет все необходимые корректирующие меры и отрегулирует дозу.
Передозировка может привести к перегрузке жидкостью, снижению содержания бикарбоната в сыворотке крови (метаболическому ацидозу) и (или) высокому содержанию фосфатов (гиперфосфатемии) у пациентов с повреждением почек.
Может также привести к серьезным последствиям, таким как застойная сердечная недостаточность и нарушения химического состава крови.
В случае сомнений, связанных с использованием препарата, необходимо обратиться к врачу или фармацевту.
4. Возможные нежелательные явления
Как и любой препарат, этот препарат может вызывать нежелательные явления, хотя они не возникают у каждого пациента.
Могут возникать три нежелательных явления, связанных с использованием препарата Фоксилиум:
- неправильно большое или малое содержание воды в организме (перегидратация или обезвоживание),
- изменения содержания минеральных солей в крови (электролитный дисбаланс, такой какгиперфосфатемия)и
- увеличение содержания бикарбоната в сыворотке крови (метаболический алкалоз)или снижение содержания бикарбоната в сыворотке крови ( метаболический ацидоз) .
Существуют также некоторые нежелательные явления, которые могут быть вызваны диализотерапией:
- тошнота, рвота, судороги и низкое кровяное давление ( гипотония).
Сообщение о нежелательных явлениях
Если возникают любые нежелательные явления, включая те, которые не указаны в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. Нежелательные явления можно сообщать напрямую в Департамент мониторинга нежелательных реакций на лекарственные препараты Управления по регистрации лекарственных препаратов, медицинских изделий и биоцидных продуктов
Аллея Ероzолимские 181С
02-222 Варшава
Тел.: +48 22 4921301
Факс: +48 22 4921309
Сайт: https://smz.ezdrowie.gov.pl
Нежелательные явления можно также сообщать ответственному лицу.
Благодаря сообщению о нежелательных явлениях можно будет собрать больше информации о безопасности применения препарата.
3/8
5. Как хранить препарат Фоксилиум
Препарат должен храниться в месте, недоступном для детей.
Не использовать этот препарат после истечения срока годности, указанного на этикетке и упаковке.
Срок годности указывает последний день месяца.
Хранить при температуре от +4°C до +30°C. Не хранить в холодильнике или замораживать.
Установлена химическая и физическая стабильность восстановленного раствора в течение 24 часов при температуре +22°C. Если раствор не будет использован сразу, пользователь отвечает за время и условия хранения перед использованием, и это время не должно превышать 24 часа, включая время процедуры.
Не использовать этот препарат, если обнаружено, что раствор мутный или внешняя защитная упаковка повреждена. Все швы должны быть целыми.
Лекарства не должны выбрасываться в канализацию или домашние контейнеры для мусора. Необходимо спросить фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит препарат Фоксилиум
Активные вещества до смешивания и после смешивания ( восстановления) приведены ниже.
Активные вещества до смешивания:
1000 мл раствора в малой камере Асодержит:
Хлорид кальция дигидрат
3,68 г
Хлорид магния гексагидрат
2,44 г
1000 мл раствора в большой камере Бсодержит:
Хлорид натрия 6,44 г
Бикарбонат натрия
2,92 г
Хлорид калия
0,314 г
Безводный дифосфат натрия 0,225 г
Активные вещества после смешивания:
Растворы в камерах А (250 мл) и Б (4750 мл) смешиваются для получения одного восстановленного раствора (5000 мл), содержащего:
ммоль/л
кальций, Ca
1,25
магний, Mg
0,6
натрий, Na
140
хлориды, Cl -
115,9
фосфат, HPO
1,2
бикарбонат, HCO
30
калий, K
4
Теоретическая осмолярность: 293 мОсм/л
Другие компоненты:
- диоксид углерода (для установления pH), E290;
- соляная кислота (для установления pH), E507;
- вода для инъекций.
4/8
Как выглядит Фоксилиум и что содержит упаковка
Фоксилиум является раствором для гемодиализа и гемофильтрации, упакованным в двукамерные мешки.
Конечный восстановленный раствор получается после разрыва разрывного шва и смешивания обоих растворов. Восстановленный раствор прозрачный и бесцветный. Каждый мешок (А+Б) содержит 5000 мл раствора для гемофильтрации и гемодиализа. Каждый мешок помещен в прозрачную внешнюю упаковку.
В каждой упаковке находятся два мешка и информационный листок.
Ответственное лицо:
Vantive Belgium SRL
Бульвар д'Англетер 2
1420 Брен-л'Аллюд
Бельгия
Производитель:
Bieffe Medital S.p.A., Виа Стельвио 94, 23035 Сондальо (SO), ИТАЛИЯ
Vantive Manufacturing Limited, Монеен Роуд, Каслбар, Каунти Майо, F23 XR63, ИРЛАНДИЯ
Этот препарат разрешен к обращению в странах-членах Европейского экономического пространства и Великобритании (Северной Ирландии) под следующими названиями:
Австрия, Бельгия, Болгария, Кипр, Дания, Эстония, Финляндия, Франция, Греция, Испания, Нидерланды, Ирландия, Исландия, Литва, Люксембург, Латвия, Мальта, Германия, Норвегия, Польша, Португалия, Румыния, Словакия, Словения, Швеция, Великобритания (Северная Ирландия), Италия: Фоксилиум
Венгрия: Фоксил
Дата последнего обновления инструкции: сентябрь 2024
Ниже приведенная информация предназначена исключительно для медицинских работников:
ФОКСИЛИУМ 1,2 ммоль/л фосфатов
Раствор для гемодиализа и гемофильтрации
Меры предосторожности
Необходимо строго соблюдать инструкцию по применениюпрепарата Фоксилиум.
Растворы из обеих камер должныбыть смешаны перед использованием.
Использование загрязненного раствора может привести к сепсису и шоку.
Чтобы увеличить комфорт пациента, Фоксилиум можно нагреть до температуры +37°C. Нагревание раствора перед использованием должно быть выполнено до восстановления и исключительно с использованием сухого источника тепла. Растворы не должны быть нагреты в водяной бане или микроволновой печи. Перед введением необходимо визуально проверить Фоксилиум, чтобы обнаружить наличие твердых частиц и изменение цвета. Не вводить, если раствор не является прозрачным, и шов поврежден.
Необходимо регулярно измерять содержание неорганических фосфатов. Неорганические фосфаты должны быть补ены в случаях низкого содержания фосфатов в крови.
Дополнительная замена бикарбоната натрия может увеличить риск метаболического алкалоза.
В случае нарушения баланса жидкости необходимо тщательно контролировать клиническое состояние и восстановить баланс жидкости:
- В случае гиперволемии можно увеличить скорость ультрафильтрации (нетто) в аппарате для CRRT и (или) уменьшить скорость введения жидкостей, кроме замещающей жидкости и (или) диализата.
5/8
- В случае гиповолемии можно уменьшить скорость ультрафильтрации (нетто) в аппарате для CRRT и (или) увеличить скорость введения жидкостей, кроме замещающей жидкости и (или) диализата.
Предостережения:
Фоксилиум не должен использоваться у пациентов с гиперкалиемией. Содержание калия в сыворотке крови должно быть контролировано перед началом и во время гемофильтрации и (или) гемодиализа.
Поскольку Фоксилиум является раствором, содержащим калий, после начала лечения может временно возникнуть гиперкалиемия. Необходимо уменьшить скорость введения до достижения нормального содержания калия. Если гиперкалиемия не проходит, необходимо немедленно прекратить введение препарата.
Если во время использования препарата Фоксилиум как диализата возникает гиперкалиемия, может быть необходимо введение диализата, не содержащего калий, для увеличения скорости удаления калия.
Поскольку Фоксилиум является раствором, содержащим фосфаты, после начала лечения может временно возникнуть гиперфосфатемия. Необходимо уменьшить скорость введения до достижения нормального содержания фосфатов. Если гиперфосфатемия не проходит, необходимо немедленно прекратить введение препарата.
У пациентов, которым вводится препарат Фоксилиум, необходимо регулярно контролировать электролиты и кислотно-щелочной баланс крови. Фоксилиум содержит фосфат, слабую кислоту, которая может влиять на кислотно-щелочной баланс пациента. Если во время лечения препаратом Фоксилиум возникает или усиливается метаболический ацидоз, может возникнуть необходимость уменьшить скорость введения или прекратить введение препарата.
Поскольку Фоксилиум не содержит глюкозы, его введение может привести к гипогликемии. Необходимо регулярно контролировать содержание глюкозы в крови у пациентов с диабетом (особенно у пациентов, принимающих инсулин или другие лекарства, снижающие содержание глюкозы); необходимо также учитывать это у пациентов без диабета, например, из-за риска возникновения бессимптомной гипогликемии во время лечения. В случае возникновения гипогликемии необходимо рассмотреть возможность использования раствора, содержащего глюкозу. Может быть также необходимо принять другие меры для поддержания нормального содержания глюкозы в крови.
Дозировка:
Объем и скорость введения препарата Фоксилиум зависят от содержания фосфатов и других электролитов в крови, кислотно-щелочного баланса, баланса жидкости и общего клинического состояния пациента. Объем раствора замены и (или) диализата, который необходимо ввести, будет также зависеть от желаемой интенсивности лечения (дозы). Способ введения (дозу, скорость инфузии и общий объем) препарата Фоксилиум должен устанавливать исключительно врач, имеющий опыт в области интенсивной терапии и непрерывной заместительной почечной терапии (CRRT).
Следовательно, объем дозы зависит от решения и рекомендаций врача.
Диапазоны скоростей потока для раствора замены в гемофильтрации и гемофильтрации составляют:
Взрослые: 500 до 3000 мл/час.
Диапазоны скоростей потока для диализата в непрерывной гемодиализе и непрерывной гемофильтрации составляют:
Взрослые: 500 до 2500 мл/час.
У взрослых обычно используется общая скорость потока в случае CRRT (диализат и растворы замены) в диапазоне от примерно 2000 до 2500 мл/час, что соответствует суточному объему жидкости в диапазоне от примерно 48 до 60 л.
6/8
Дети и подростки:
У детей, от новорожденных до подростков до 18 лет, диапазон скоростей потока при использовании в качестве замещающей жидкости в гемофильтрации и гемофильтрации, а также в качестве диализата в непрерывной гемодиализе и непрерывной гемофильтрации составляет от 1000 до 4000 мл/час/1,73 м2.
В случае, когда у подростков (12–18 лет) рассчитанная доза для детей превышает максимальную дозу для взрослых, необходимо использовать дозу, рекомендуемую для взрослых.
Инструкция по применению/процедуре
Раствор из малой камеры А добавляется к раствору из большой камеры Б после разрыва разрывного шва или разрыва шва непосредственно перед использованием. Восстановленный раствор должен быть прозрачным и бесцветным.
Во время процедуры и введения препарата пациенту необходимо использовать асептическую технику.
Использовать только в том случае, если внешняя защитная упаковка не повреждена, все швы целы, разрывной шов не поврежден, а раствор прозрачный. Необходимо сильно сжать мешок, чтобы проверить его герметичность. Если обнаружен протек, раствор необходимо немедленно выбросить, поскольку нельзя гарантировать стерильность.
Большая камера Б имеет порт для инъекций, позволяющий после восстановления раствора добавить другие необходимые лекарственные препараты. Пользователь отвечает за оценку совместимости добавляемого препарата с препаратом Фоксилиум путем обнаружения возможных изменений цвета и (или) выпадения осадка, присутствия нерастворимых комплексов или кристаллов.
Перед добавлением другого препарата необходимо проверить, растворим ли он и стабилен ли в препарате Фоксилиум, и соответствует ли диапазон pH препарата Фоксилиум (pH раствора после восстановления составляет от 7,0 до 8,5). Дополнительные компоненты могут быть несовместимы с раствором. Необходимо ознакомиться с инструкцией по применению добавляемого препарата.
Удалить жидкость из порта для инъекций, держать перевернутый мешок («вверх ногами»), ввести препарат через порт для инъекций и тщательно перемешать. Введение и смешивание дополнительных компонентов всегда должно выполняться перед подключением мешка с раствором к экстракорпоральной циркуляции. Раствор необходимо ввести немедленно.
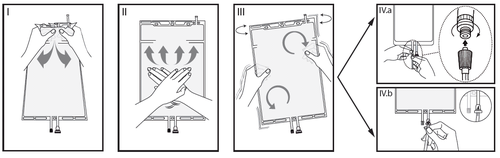
I
Снять внешнюю упаковку непосредственно перед использованием, выбросить все остальные упаковки. Открыть шов, держа малую камеру обеими руками и сжимая до момента образования отверстия в разрывном шве, разделяющем обе камеры (см. рисунок I ниже).
II
Двумя руками нажать на большую камеру до момента полного открытия разрывного шва между двумя камерами (см. рисунок II ниже).
III
Тщательно перемешать, чтобы обеспечить однородность раствора. Теперь раствор готов к использованию, и мешок можно повесить на стойку (см. рисунок III ниже).
IV
К каждому из двух доступных портов можно подключить линию диализа или обмена.
IVaЕсли используется доступ типа Luer, необходимо удалить пробку, повернув ее и потянув, а затем подключить мужской коннектор Luer lock линии диализа или обмена к женскому коннектору типа Luer на мешке, нажимая и поворачивая. Убедиться, что соединение полностью установлено и надежно. Теперь соединение открыто. Проверить, что жидкость течет свободно (см. рисунок IV.a ниже).
Когда линии диализа или обмена отключены от соединения типа Luer, соединение закрывается, и поток жидкости останавливается. Порт типа Luer безигловой и может быть протерт дезинфицирующими средствами.
IVbВ случае использования порта для инъекций необходимо сначала удалить пробку, сломав ее. Порт для инъекций можно протереть дезинфицирующими средствами. Затем необходимо проколоть иглой резиновую пробку. Проверить, что жидкость течет свободно (см. рисунок IV.b ниже).
7/8
Восстановленный раствор должен быть использован немедленно. Если восстановленный раствор не будет использован сразу, он должен быть использован в течение 24 часов после добавления раствора А к раствору Б, включая время процедуры.
Восстановленный раствор предназначен исключительно для одноразового использования. Неиспользованный раствор необходимо выбросить немедленно после использования.
Все неиспользованные остатки препарата или его отходы необходимо утилизировать в соответствии с местными правилами.
8/8
1. Что такое лекарство Phoxilium и для чего оно используется
Лекарство Phoxilium относится к группе растворов для гемофильтрации, содержащих хлорид кальция двузамещенный, магния бикарбонат шестизамещенный, натрия хлорид, натрия бикарбонат, калия хлорид и безводный дифосфат натрия. Лекарство Phoxilium используется в больницах в условиях интенсивной медицинской помощи для восстановления химического баланса крови у пациентов с повреждением почек. Непрерывное заместительное лечение почек направлено на удаление накопившихся продуктов обмена из крови в ситуации, когда почки не функционируют. Раствор Phoxiliumиспользуется для лечения пациентов в критическом состоянии с острым повреждением почек, характеризующихся:
- нормальным содержанием калия в крови (нормокалиемия)или
- нормальным или низким содержанием фосфатов в крови (нормо- или гипофосфатемия).
Это лекарство также может быть использовано в случае отравления лекарствами, содержащими вещества, подвергающиеся диализу или фильтрации.
2. Важные сведения перед использованием лекарства Phoxilium
Не использовать лекарство Phoxilium в следующих трех случаях:
- если у пациента высокое содержание калия в крови (гиперкалиемия);
- если у пациента высокое содержание бикарбоната в крови (метаболический алкалоз);
- если у пациента высокое содержание фосфатов в крови (гиперфосфатемия).
1/8
Не использовать гемодиализ или гемофильтрацию в следующих трех случаях:
- если с помощью гемофильтрации невозможно облегчить симптомы, вызванные высоким содержанием мочевины в крови (симптомы уремии),которые являются результатом повреждения почек с выраженным гиперкATABолизмом (неправильный рост процессов распада веществ);
- недостаточное артериальное давление в сосудистом доступе;
- снижение свертываемости крови (общая антикоагуляция)при существующем риске кровотечения.
Предостережения и меры предосторожности
Прежде чем начать использовать лекарство Phoxilium, необходимо обсудить это с врачом, фармацевтом или медсестрой. Прежде чем начать лечение и в течение его проведения будут проверяться кровь, т.е. контролироваться кислотно-щелочной баланс и содержание солей (электролитов), включая объем введенных (внутривенных вливаний) и удаленных (выделенного мочи) жидкостей, даже тех, которые не связаны напрямую с CRRT.
Лекарство Phoxilium и другие лекарства
Необходимо сообщить врачу или фармацевту о всех лекарствах, которые пациент принимает в настоящее время или принимал ранее, а также о лекарствах, которые пациент планирует принимать. Необходимо сделать это, поскольку концентрация других принимаемых лекарств может повлиять на лечение Phoxilium. Врач решит, следует ли вносить какие-либо изменения в другие принимаемые лекарства. В частности, необходимо сообщить о приеме:
- фосфатов из дополнительных источников (например, питательных жидкостей), поскольку они могут увеличить риск развития высокого содержания фосфатов в крови (гиперфосфатемия);
- витамина D и лекарств, содержащих хлорид кальция или глюконат кальция, поскольку они могут увеличить риск развития высокого содержания кальция в крови (гиперкальциемия);
- бикарбоната натрия, поскольку он может увеличить риск развития метаболического алкалоза;
- цитрата как антикоагулянт, поскольку он может снизить содержание кальция в сыворотке крови.
Беременность, кормление грудью и влияние на фертильность
Беременность и кормление грудью: Нет данных о клиническом использовании этого лекарства во время беременности и лактации. Это лекарство должно быть назначено беременным и кормящим женщинам только в случае необходимости. Фертильность: Не ожидается влияние лекарства на фертильность, поскольку кальций, натрий, калий, магний, хлор, фосфат и бикарбонат являются нормальными компонентами организма.
Вождение транспортных средств и эксплуатация машин
Phoxilium не влияет на способность управлять транспортными средствами и эксплуатировать машины.
3. Как использовать лекарство Phoxilium
Phoxilium является лекарственным продуктом, используемым в больницах и вводимым только медицинским персоналом. Объем лекарства Phoxilium и, следовательно, доза зависят от состояния пациента. Объем дозы определяет врач, ответственный за лечение. Лекарство Phoxilium может быть введено непосредственно в кровоток (внутривенно)через аппарат CRRT или через гемодиализ, когда раствор протекает по одной стороне диализной мембраны, а кровь - по другой стороне. Это лекарство всегда должно использоваться точно в соответствии с рекомендациями врача, фармацевта или медсестры. В случае сомнений следует обратиться к врачу, фармацевту или медсестре. Инструкция по применению находится в разделе "Ниже приведенная информация предназначена только для медицинских работников".
Использование большей, чем рекомендуемой, дозы Phoxilium
Лекарство Phoxilium предназначено для использования в больницах и вводится только врачами в условиях тщательного мониторинга водно-электролитного баланса и химического состава крови.
Следовательно, использование большей, чем рекомендуемой, дозы Phoxilium маловероятно.
В случае передозировки лечащий врач примет все необходимые корректирующие меры и отрегулирует дозу. Передозировка может привести к перегрузке жидкостью, снижению содержания бикарбоната в сыворотке крови (метаболическому ацидозу) и (или) высокому содержанию фосфатов (гиперфосфатемии) у пациентов с повреждением почек. Она также может привести к серьезным последствиям, таким как застойная сердечная недостаточность и нарушения химического состава крови. В случае сомнений, связанных с использованием лекарства, следует обратиться к врачу или фармацевту.
4. Возможные нежелательные реакции
Как и любое лекарство, это лекарство может вызывать нежелательные реакции, хотя они не возникают у каждого. Могут возникнуть три нежелательные реакции связанные с использованием лекарства Phoxilium:
- неправильно большое или малое содержание воды в организме (перегидратация или обезвоживание),
- изменения содержания минеральных солей в крови (расстройство электролитного баланса, такое какгиперфосфатемия)и
- увеличение содержания бикарбоната в сыворотке крови (метаболический алкалоз)или снижение содержания бикарбоната в сыворотке крови ( метаболический ацидоз) .
Также существуют некоторые нежелательные реакции, которые могут быть вызваны диализотерапией:
- тошнота, рвота, судороги и низкое кровяное давление ( гипотония).
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, следует сообщить об этом врачу, фармацевту или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных средств Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов Аллея Ероzолимская 181С 02-222 Варшава Тел.: +48 22 4921301 Факс: +48 22 4921309 Веб-сайт: https://smz.ezdrowie.gov.pl Нежелательные реакции также можно сообщать ответственной организации. Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности использования лекарства. 3/8
5. Как хранить лекарство Phoxilium
Лекарство следует хранить в месте, недоступном для детей. Не использовать это лекарство после истечения срока годности, указанного на этикетке и упаковке. Срок годности указывает последний день месяца. Хранить при температуре от +4°C до +30°C. Не хранить в холодильнике и не замораживать. Была доказана химическая и физическая стабильность восстановленного раствора в течение 24 часов при температуре +22°C. Если раствор не будет использован сразу, пользователь отвечает за время и условия хранения перед использованием, и это время не должно превышать 24 часа, включая время процедуры. Не использовать это лекарство, если раствор мутный или внешняя защитная упаковка повреждена. Все пайки должны быть ненарушенными. Лекарства не следует выбрасывать в канализацию или домашние контейнеры для отходов. Следует спросить фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит лекарство Phoxilium
Активные вещества до смешивания и после смешивания ( реконструкции) приведены ниже.
Активные вещества до смешивания:
1000 мл раствора в малой камере Асодержит: Хлорид кальция двузамещенный 3,68 г Хлорид магния шестизамещенный 2,44 г 1000 мл раствора в большой камере Бсодержит: Хлорид натрия 6,44 г Бикарбонат натрия 2,92 г Хлорид калия 0,314 г Безводный дифосфат натрия 0,225 г
Активные вещества после смешивания:
Растворы в камерах А (250 мл) и Б (4750 мл) смешиваются для получения одного восстановленного раствора (5000 мл) содержащего: ммоль/лкальций, Ca 1,25 магний, Mg 0,6 натрий, Na 140 хлор, Cl 115,9 фосфат, HPO 1,2 бикарбонат, HCO 30 калий, K 4 Теоретическая осмолярность: 293 мОсм/л
Прочие компоненты:
- диоксид углерода (для установления pH), Е290;
- соляная кислота (для установления pH), Е507;
- вода для инъекций.
4/8
Как выглядит Phoxilium и что содержит упаковка
Phoxilium является раствором для гемодиализа и гемофильтрации, упакованным в двукамерные мешки. Окончательный восстановленный раствор получается после разлома разрывной пробки и смешивания обоих растворов. Восстановленный раствор прозрачный и бесцветный. Каждый мешок (А+Б) содержит 5000 мл раствора для гемофильтрации и гемодиализа. Каждый мешок помещен в прозрачную внешнюю упаковку. В каждой упаковке находятся два мешка и информационный листок.
Ответственное лицо:
Vantive Belgium SRL Бульвар д’Англетер 2 1420 Брен-л’Альюд Бельгия
Производитель:
Bieffe Medital S.p.A., Виа Стельвио 94, 23035 Сондальо (SO), ИТАЛИЯ Vantive Manufacturing Limited, Мунин Роуд, Каслбар, Каунти Майо, F23 XR63, ИРЛАНДИЯ
Это лекарство разрешено к обращению в странах-членах Европейского экономического пространства и Великобритании (Северной Ирландии) под следующими названиями:
Австрия, Бельгия, Болгария, Кипр, Дания, Эстония, Финляндия, Франция, Греция, Испания, Нидерланды, Ирландия, Исландия, Литва, Люксембург, Латвия, Мальта, Германия, Норвегия, Польша, Португалия, Румыния, Словакия, Словения, Швеция, Великобритания (Северная Ирландия), Италия: Phoxilium Венгрия: Phoxil
Дата последней актуализации инструкции: сентябрь 2024
Ниже приведенная информация предназначена только для медицинских работников:
Phoxilium 1,2 ммоль/л фосфатов
Раствор для гемодиализа и гемофильтрации
Меры предосторожности Необходимо строго соблюдать инструкцию по применению продукта Phoxilium. Растворы из обеих камер должныбыть смешаны перед использованием. Использование загрязненного раствора может привести к сепсису и шоку. Чтобы увеличить комфорт пациента, Phoxilium можно нагреть до температуры +37°C. Нагрев раствора перед использованием следует выполнять перед восстановлением и только с помощью сухого источника тепла. Растворы не следует нагревать в водяной бане или микроволновой печи. Перед введением необходимо визуально проверить Phoxilium, чтобы обнаружить наличие твердых частиц и изменение цвета. Не вводить, если раствор не прозрачный и пайка повреждена. Необходимо регулярно измерять содержание неорганических фосфатов. Неорганические фосфаты должны быть дополнены в случае низкого содержания фосфатов в крови. Дополнительная замена бикарбоната натрия может увеличить риск метаболического алкалоза. В случае нарушения водно-электролитного баланса необходимо тщательно контролировать клиническое состояние и восстановить водно-электролитный баланс:
- В случае гиперволемии можно увеличить скорость ультрафильтрации (чистую) в аппарате CRRT и (или) уменьшить скорость введения жидкостей, кроме замещающей жидкости и (или) диализата.
5/8
- В случае гиповолемии можно уменьшить скорость ультрафильтрации (чистую) в аппарате CRRT и (или) увеличить скорость введения жидкостей, кроме замещающей жидкости и (или) диализата.
Предостережения:
Phoxilium не должен использоваться у пациентов с гиперкалиемией. Содержание калия в сыворотке крови должно быть контролируемо перед началом и во время гемофильтрации и (или) гемодиализа. Поскольку Phoxilium является раствором, содержащим калий, после начала лечения может временно возникнуть гиперкалиемия. Необходимо уменьшить скорость введения до достижения нормального содержания калия. Если гиперкалиемия не проходит, необходимо немедленно прекратить введение лекарственного продукта. Если во время использования продукта Phoxilium в качестве диализата возникает гиперкалиемия, может быть необходимо введение диализата, не содержащего калия, для увеличения скорости удаления калия. Поскольку Phoxilium является раствором, содержащим фосфаты, после начала лечения может временно возникнуть гиперфосфатемия. Необходимо уменьшить скорость введения до достижения нормального содержания фосфатов. Если гиперфосфатемия не проходит, необходимо немедленно прекратить введение лекарственного продукта. У пациентов, которым вводится продукт Phoxilium, необходимо регулярно контролировать электролиты и кислотно-щелочной баланс крови. Phoxilium содержит фосфат, слабую кислоту, которая может влиять на кислотно-щелочной баланс пациента. Если во время лечения продуктом Phoxilium возникает или усиливается метаболический ацидоз, может возникнуть необходимость уменьшить скорость введения или прекратить введение лекарственного продукта. Поскольку Phoxilium не содержит глюкозы, его введение может привести к гипогликемии. Необходимо регулярно контролировать содержание глюкозы в крови у пациентов с диабетом (особенно у пациентов, принимающих инсулин или другие лекарства, снижающие содержание глюкозы); необходимо также учитывать это у пациентов без диабета, например, из-за риска безсимптомной гипогликемии во время лечения. В случае возникновения гипогликемии необходимо рассмотреть возможность использования раствора, содержащего глюкозу. Может быть необходимо принять другие меры для поддержания нормального содержания глюкозы в крови.
Дозирование:
Объем и скорость введения лекарственного продукта Phoxilium зависят от концентрации фосфатов и других электролитов в крови, кислотно-щелочного баланса, водно-электролитного баланса и общего клинического состояния пациента. Объем раствора замены и (или) диализата, который необходимо ввести, также будет зависеть от желаемой интенсивности лечения (дозы). Способ введения (дозу, скорость инфузии и общий объем) лекарственного продукта Phoxilium должен устанавливать только врач, имеющий опыт в области интенсивной терапии и непрерывного заместительного лечения почек (англ. Continuous Renal Replacement Therapy, CRRT). В связи с этим объем дозы зависит от решения и рекомендаций врача. Диапазоны скоростей потока для раствора замены в гемофильтрации и гемодиафильтрации составляют: Взрослые: 500 до 3000 мл/час. Диапазоны скоростей потока для диализата в непрерывной гемодиализе и непрерывной гемодиафильтрации составляют: Взрослые: 500 до 2500 мл/час. У взрослых обычно используется совокупная скорость потока в случае CRRT (диализат и растворы замены) в размере от примерно 2000 до 2500 мл/час, что соответствует суточному объему жидкости в размере от примерно 48 до 60 л. 6/8
Дети и подростки:
У детей, от новорожденных до подростков до 18 лет, диапазон скоростей потока при использовании в качестве замещающей жидкости в гемофильтрации и гемодиафильтрации, а также в качестве раствора для диализа (диализат) в непрерывной гемодиализе и непрерывной гемодиафильтрации, составляет от 1000 до 4000 мл/час/1,73 м. В случае, когда у подростков (12–18 лет) рассчитанная доза для детей превышает максимальную дозу для взрослых, следует использовать дозу, рекомендуемую для взрослых.
Инструкция по применению/процедуре
Раствор из малой камеры А добавляется к раствору из большой камеры Б после разлома разрывной пробки или разрыва пайки непосредственно перед использованием. Восстановленный раствор должен быть прозрачным и бесцветным. Во время процедуры и введения лекарственного продукта пациенту следует использовать асептическую технику. Применять только в том случае, если внешняя защитная упаковка не повреждена, все пайки не нарушены, разрывная пробка не повреждена, а раствор прозрачный. Сильно сжать мешок, чтобы проверить его герметичность. В случае обнаружения утечки раствор следует немедленно выбросить, поскольку нельзя гарантировать его стерильность. Большая камера Б оснащена портом для инъекций, позволяющим после восстановления раствора добавить другие необходимые лекарственные препараты. Пользователь отвечает за оценку совместимости добавляемого лекарственного препарата с продуктом Phoxilium путем обнаружения возможного изменения цвета и (или) выпадения осадка, наличия нерастворимых комплексов или кристаллов. Перед добавлением другого лекарственного препарата следует проверить, растворим ли он и стабилен в лекарственном продукте Phoxilium, а также соответствует ли диапазон pH продукта Phoxilium для него (pH раствора после реконструкции составляет от 7,0 до 8,5). Дополнительные компоненты могут быть несовместимы с раствором. Следует ознакомиться с инструкцией по применению добавляемого лекарственного препарата. Удалить жидкость из порта для инъекций, удерживать перевернутый мешок (вверх ногами), ввести лекарственный препарат через порт для инъекций и тщательно перемешать. Введение и перемешивание дополнительных компонентов всегда должно осуществляться перед подключением мешка с раствором к экстракорпоральному контуру. Раствор следует вводить немедленно.
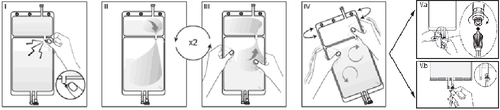
I
Внешнюю упаковку снять непосредственно перед использованием, выбросить все остальные упаковки. Открыть пайку между обеими камерами мешка, разломав разрывную пробку. Разрывная пробка останется в мешке (См. рисунок I ниже).
II
Убедиться, что весь жидкость из малой камеры А был перелит в большую камеру Б (См. рисунок II ниже). IIIПромыть дважды малую камеру А, выжимая смешанный раствор обратно в малую камеру А, а затем снова в большую камеру Б (См. рисунок III ниже).
IV
Если малая камера А пуста: встряхнуть большую камеру Б для полного перемешивания ее содержимого. Теперь раствор готов к использованию, и мешок можно повесить на стойку (См. рисунок IV ниже).
V
К каждому из двух портов доступа можно подключить линию диализа или обмена. V.aЕсли используется доступ типа луэр, следует использовать асептическую технику, удалить пробку и подключить мужской конец луэр-лок линии диализа или обмена к женскому концу типа луэр-рецептор на мешке; затянуть. Используя обе руки, разломать синюю разрывную пробку у основания и переместить ее туда и обратно. Не использовать инструменты. Проверить, что пробка полностью разделена и что жидкость протекает свободно. Во время лечения пробка останется в порте типа луэр (См. рисунок V.a ниже). V.bВ случае использования порта для инъекций сначала удалить пробку, разломав ее. Порт для инъекций можно протирать дезинфицирующими средствами. Затем проколоть иглой gumмовую перегородку. Проверить, что жидкость протекает свободно (См. рисунок V.b ниже). 7/8 Восстановленный раствор следует немедленно использовать. Если восстановленный раствор не будет немедленно использован, его следует использовать в течение 24 часов после добавления раствора А к раствору Б, включая время процедуры. Восстановленный раствор предназначен только для одноразового использования. Неиспользованный раствор следует немедленно выбросить после применения. Все неиспользованные остатки лекарственного препарата или его отходы следует удалить в соответствии с местными правилами.
8/8
- Страна регистрации
- Требуется рецептНет
- ИмпортерBieffe Medital S.p.A. Vantive Manufacturing Limited
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги ПгоксилиумФорма выпуска: Раствор, 9 мг/млАктивное вещество: Хлорид натрияТребуется рецептФорма выпуска: Раствор, 100 мг/млАктивное вещество: декстранаПроизводитель: Fresenius Kabi Italia S.r.L.Не требуется рецептФорма выпуска: Концентрат, -Активное вещество: electrolytes in combination with other drugsПроизводитель: Fresenius Kabi Norge ASНе требуется рецепт
Аналоги Пгоксилиум в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Пгоксилиум в Украина
Аналог Пгоксилиум в Испания
Врачи онлайн по Пгоксилиум
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Пгоксилиум – по решению врача и с учетом местных правил.














