
Цлувот 250 й.м.

Спросите врача о рецепте на Цлувот 250 й.м.

Инструкция по применению Цлувот 250 й.м.
Инструкция, прилагаемая к упаковке: информация для пациента
Клувот 250 МЕ
Порошок и растворитель для приготовления раствора для инъекций/инфузий
Человеческий фактор свертывания крови XIII
Необходимо внимательно ознакомиться с содержанием инструкции перед применением препарата, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу или фармацевту.
- Этот препарат назначен строго определенной personne. Не следует его передавать другим. Препарат может нанести вред другой personne, даже если симптомы ее заболевания такие же.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или фармацевту. См. пункт 4.
Содержание инструкции
- 1. Что такое Клувот и для чего он используется
- 2. Важные сведения перед применением Клувота
- 3. Как применять Клувот
- 4. Возможные нежелательные реакции
- 5. Как хранить Клувот
- 6. Содержание упаковки и другие сведения
1. Что такое Клувот и для чего он используется
Что такое Клувот
Клувот - препарат, выпускаемый в виде белого порошка и растворителя. Приготовленный раствор должен быть введен внутривенно.
Клувот - человеческий фактор свертывания крови XIII (F XIII), произведенный из человеческой плазмы (жидкая часть крови) и играет важную роль в процессе гемостаза (остановки кровотечения).
Для чего используется Клувот
Клувот показан для применения у взрослых, детей и подростков.
- для профилактического лечения врожденного дефицита фактора XIII и
- в послеоперационном периоде для лечения кровотечений во время хирургических операций у пациентов с врожденным дефицитом фактора XIII.
2. Важные сведения перед применением Клувота
Эта часть инструкции содержит сведения, которые необходимо учитывать перед началом применения препарата Клувот.
Когда не применять Клувот:
- если пациент имеет аллергическую реакцию на активное вещество или любой другой компонент этого препарата (перечисленные в пункте 6).
Необходимо сообщить врачу, если существует повышенная чувствительность к любому лекарству или продукту.
Предостережения и меры осторожности:
- если после введения фактора XIII свертывания крови в прошлом наблюдались аллергические реакции. Профилактически необходимо применять антигистаминные препараты и кортикостероиды, если так решит врач.
- если появляются симптомы аллергии или реакции анафилактического типа (тяжелые аллергические симптомы могут вызвать значительное затруднение дыхания или головокружение). Введение Клувота должно быть немедленно прекращено (т.е. прекращено введение или инфузия). В случае анафилактического шока необходимо применить лечение в соответствии с действующими медицинскими стандартами.
- если наблюдалась свежая тромбоз (тромб). Необходимо внимательно наблюдать за пациентом из-за стабилизирующего фибрин действия F XIII.
- образование ингибиторов (антител, нейтрализующих) известно как осложнение лечения и означает, что лечение перестает действовать. Если кровотечение не было устранено с помощью препарата Клувот, необходимо немедленно сообщить об этом врачу. Пациент должен быть тщательно отслежен на предмет развития (появления) ингибиторов.
Врач всегда должен учитывать пользу от лечения по сравнению с риском, связанным с осложнениями.
Безопасность против вирусных инфекций
Когда препараты производятся из человеческой крови или плазмы, принимаются различные меры для защиты пациента от передачи вирусных инфекций. К этим мерам относятся:
- правильный отбор доноров крови и плазмы для исключения риска передачи вирусных инфекций
- исследование каждой донорской крови и плазмы на наличие вирусных маркеров/инфекций.
- введение в процесс производства продуктов из крови или плазмы этапов, которые могут привести к инактивации или удалению вирусов.
Несмотря на применение вышеуказанных мер, нельзя полностью исключить возможность передачи вирусных инфекций после введения препарата, полученного из человеческой крови или плазмы.
Этот риск также относится к неизвестным или недавно открытых вирусам и другим вирусным инфекциям.
Принятые меры безопасности эффективны против вирусов с оболочкой, таких как вирус иммунодефицита человека (ВИЧ, вирус, вызывающий СПИД), вирус гепатита Б (HBV, вызывающий гепатит Б) и вирус гепатита С (HCV, вызывающий гепатит С), а также против вирусов без оболочки, таких как вирус гепатита А (HAV, вызывающий гепатит А) и парвовирус В19.
У пациентов, получающих多кратные дозы препаратов, полученных из человеческой плазмы, следует рассмотреть возможность вакцинации против вирусного гепатита А и В.
Рекомендуется каждый раз, когда вводится Клувот, чтобы дата введения, номер серии и введенный объем были зарегистрированы в медицинской документации.
Клувот и другие препараты
- Необходимо сообщить врачу или фармацевту о приеме других препаратов, включая те, которые доступны без рецепта.
- Не известно о случаях взаимодействия концентрата фактора свертывания крови FXIII с другими лекарственными препаратами.
- Клувот не может быть смешан с другими лекарственными препаратами, растворителями и разбавителями, за исключением тех, которые указаны в пункте 6, и должен быть введен с помощью отдельных инфузионных наборов.
Беременность и грудное вскармливание
- Если пациентка беременна или кормит грудью, предполагает, что может быть беременной, или планирует иметь ребенка, она должна проконсультироваться с врачом или фармацевтом перед применением этого препарата.
- Ограниченные данные о клиническом применении Клувота во время беременности не показали никаких негативных эффектов, связанных с беременностью и эмбриональным развитием. В случае необходимости может быть рассмотрено применение Клувота во время беременности.
- Не известно, проникает ли Клувот в человеческое молоко, однако, учитывая его высокую молекулярную массу, вероятность выделения с молоком матери очень низка, и из-за его белковой природы абсорбция неизмененных частиц новорожденным также маловероятна. Поэтому Клувот может быть применен во время грудного вскармливания.
- Нет данных о влиянии Клувота на фертильность.
Вождение транспортных средств и работа с механизмами
Не проводились исследования о влиянии на способность управлять транспортными средствами и работать с механизмами.
Важные сведения о некоторых компонентах Клувота
Клувот содержит натрий.
Необходимо учитывать, что Клувот содержит натрий. Это важно для пациентов, находящихся на контролируемой диете с низким содержанием натрия. Клувот содержит от 124,4 до 195,4 мг (5,41 до 8,50 ммоль) натрия на дозу (40 МЕ/кг массы тела - при средней массе тела 70 кг), если введена рекомендуемая доза (2800 МЕ = 44,8 мл)
3. Как применять Клувот
- Клувот обычно вводится врачом.
- Клувот предназначен исключительно для внутривенного введения.
Дозирование
Врач должен рассчитать подходящую дозу и решить, как часто Клувот должен быть введен пациенту, учитывая прогресс лечения.
Более подробные рекомендации см. в пункте: "Информация, предназначенная только для медицинского персонала
или работников здравоохранения".
Передозировка
Не зарегистрировано случаев передозировки, и не следует ожидать их в случае введения этого препарата медицинским персоналом.
4. Возможные нежелательные реакции
Как и любой препарат, этот препарат может вызывать нежелательные реакции, хотя они не возникают у каждого пациента.
Ниже перечислены нежелательные реакции, наблюдавшиеся редко(встречающиеся у более чем 1 из 10 000 пациентов и менее чем у 1 из 1 000)
- Аллергические реакции, такие как общая крапивница (зудящий отек на коже), сыпь, снижение артериального давления (которое может вызвать чувство обморока или головокружения), трудности с дыханием.
- Повышение температуры тела
Ниже перечислены нежелательные реакции, наблюдавшиеся очень редко(встречающиеся у менее чем 1 из 10 000 пациентов):
- Образование ингибиторов FXIII.
Если появляются аллергические реакции, введение препарата Клувот должно быть немедленно прекращено и должно быть начато соответствующее лечение. Должны быть применены актуальные медицинские стандарты для лечения шока.
Нежелательные реакции у детей и подростков
Ожидается, что нежелательные реакции у детей такие же, как и у взрослых.
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу или фармацевту. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления регистрации лекарственных препаратов, медицинских изделий и биоцидных продуктов
Ал. Ерозолимских 181С,
02-222 Варшава
Тел.: + 48 22 49 21 301
Факс: + 48 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции также можно сообщать в организацию, ответственной за выпуск препарата.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности применения препарата.
5. Как хранить Клувот
- Хранить в холодильнике (2°C - 8°C).
- Не замораживать.
- Хранить в наружной упаковке для защиты от света.
- Клувот не содержит консервантов. Препарат должен быть использован немедленно после реconstitution. Если он не будет немедленно использован, хранение при комнатной температуре не должно превышать 4 часов. Не хранить в холодильнике и не замораживать раствор после реconstitution.
- Препарат должен храниться в месте, недоступном для детей.
- Не применять Клувот после истечения срока годности, указанного на этикетке и наружной упаковке после аббревиатуры EXP.
- Номер серии препарата указан на наружной упаковке и этикетке после аббревиатуры: Lot.
6. Содержание упаковки и другие сведения
Что содержит Клувот Активное вещество:
Концентрат XIII фактора свертывания человеческой плазмы (FXIII) содержащий 250 МЕ на флакон.
Вспомогательные вещества:
Человеческий альбумин, глюкоза моногидрат, хлорид натрия, гидроксид натрия (в небольших количествах для установления pH).
Растворитель:Вода для инъекций
Как выглядит Клувот и что содержит упаковка
Клувот выпускается в виде белого порошка и прилагаемого растворителя, которым является вода для инъекций.
Приготовленный раствор должен быть бесцветным, прозрачным или слегка опалесцирующим. При освещении он не должен быть мутным или содержать остатки (сгустки/частицы).
Величины упаковок
Одна упаковка 250 МЕ содержит:
1 флакон с порошком
1 флакон с 4 мл воды для инъекций
1 систему для переноса 20/20 с фильтром (Mix2Vial)
Набор для введения (внутренняя упаковка):
1 шприц одноразового использования емкостью 5 мл
1 набор для пункции
2 ватных шарика, смоченных в спирте
1 нестерильный пластырь
Ответственное лицо и Производитель
CSL Behring GmbH
Эмиль-фон-Беринг-Штрассе 76
35041 Марбург
Германия
Дата последней актуализации инструкции:август 2021
----------------------------------------------------------------------------------------------------------------------
Информация, предназначенная только для медицинского персонала: Дозирование
1 мл соответствует примерно 62,5 МЕ, а 100 МЕ эквивалентно соответственно 1,6 мл.
Важно:
Количество, необходимое для введения, и частота введения должны быть всегда адаптированы к клинической эффективности у отдельных пациентов .
Дозирование
Дозирование должно быть индивидуально подобрано в зависимости от массы тела, результатов лабораторных исследований и клинического состояния пациента.
Рутинный режим дозирования в профилактике
Начальная доза
- 40 международных единиц (МЕ) на килограмм массы тела.
- Скорость инфузии не должна превышать 4 мл в минуту
Последующие дозы
- Дозирование должно быть определено на основе текущего уровня активности FXIII, дозы должны быть введены с интервалом 28 дней (4 недели) для поддержания минимальной активности F XIII на уровне около 5 до 20%.
- Рекомендуется корректировка дозирования на +/- 5 МЕ на кг массы тела, которая должна быть рассчитана с учетом минимального уровня активности F XIII, как показано в таблице № 1, и клинического состояния пациента.
- Корректировка дозирования должна быть проведена на основе специфического, чувствительного теста, используемого для определения уровня F XIII. Примеры корректировки с использованием стандартного теста активности Berichrom представлены в таблице № 1.
Таблица 1: Корректировка дозирования с использованием теста активности Berichrom
Активность, выраженная в единицах, определяется с помощью теста активности Berichrom, относящегося к текущему Международному стандарту для плазменного XIII фактора свертывания крови. В связи с этим единица соответствует Международной единице.
Профилактика перед операцией.
| Минимальный уровень активности фактора XIII(%) | Изменение дозирования |
| Один минимальный уровень <5% | Увеличение на 5 единиц на кг. |
| Минимальный уровень 5% до 20% | Без изменений |
| Два минимальных уровня > 20% | Уменьшение на 5 единиц на кг. |
| Один минимальный уровень > 25% | Уменьшение на 5 единиц на кг. |
После последней дозы, примененной в рутинной профилактике, в случае запланированной операции:
- Между 21 и 28 днем после последней дозы - необходимо ввести пациенту полную дозу непосредственно перед операцией, и следующая профилактическая доза должна быть введена через 28 дней.
- Между 8 и 21 днем после последней дозы - дополнительная доза (полная или частичная) может быть введена перед операцией. Доза должна быть выбрана в зависимости от уровня активности FXIII пациента, его клинического состояния и должна быть подобрана с учетом периода полувыведения препарата Клувот.
- В течение 7 дней после последней дозы - дополнительное введение может не быть необходимо.
Корректировка дозирования может быть другой, чем рекомендуемая доза, и должна быть индивидуально подобрана на основе уровня активности F XIII и клинического состояния пациента. Все пациенты должны быть внимательно отслежены во время и после операции.
В связи с этим рекомендуется отслеживать рост уровня активности F XIII на основе теста фактора XIII. В случае серьезных операций и значительных кровотечений целью должно быть достижение близких к нормальным значений (у здоровых людей: 70%-140%).
Дети и подростки
Дозирование и способ введения у детей и подростков основаны на массе тела и, следовательно, в целом не отличаются от рекомендаций для взрослых. Дозирование и/или частота введения для каждого пациента должны быть всегда подобраны на основе клинической эффективности и уровня активности FXIII.
Пациенты пожилого возраста
Дозирование и способ введения у пациентов пожилого возраста (> 65 лет) не были документированы в клинических исследованиях.
Способ введения
Общие рекомендации
Раствор должен быть прозрачным или слегка опалесцирующим. После фильтрации/взятия содержимого флакона (см. ниже) препарат после реconstitution перед введением должен быть подвергнут визуальной оценке; необходимо проверить, не появились ли какие-либо загрязнения и не произошло ли изменение цвета.
Не следует применять мутные растворы и те, которые содержат хлопья или частицы.
Реconstitution и взятие из флакона должны быть проведены в асептических условиях.
Реconstitution
Растворитель должен быть доведен до комнатной температуры. С флаконов, содержащих порошок и растворитель, необходимо снять пластиковые крышки и промыть пробки асептическим раствором. После высыхания необходимо открыть систему, содержащую соединитель Mix2Vial.
1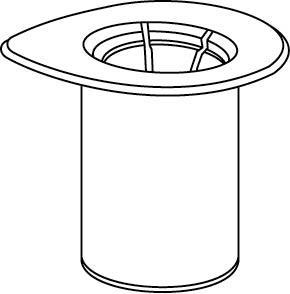 |
|
2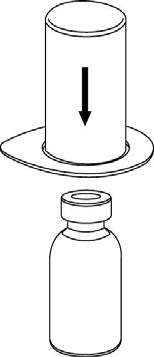 |
|
3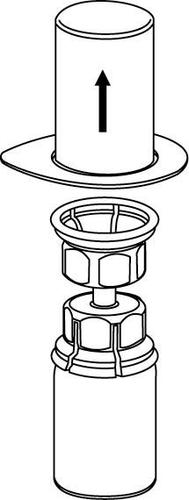 |
|
4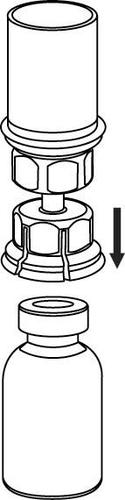 |
|
5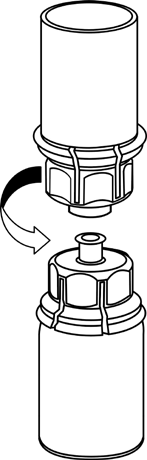 |
|
6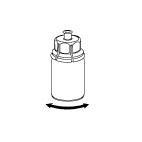 |
|
7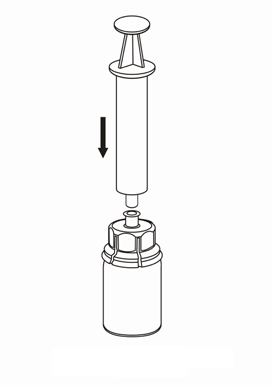 |
|
Взятие и способ введения
8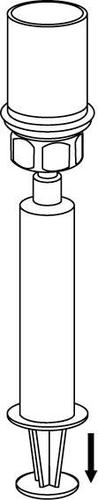 |
|
9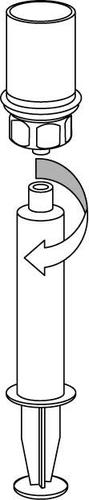 |
|
Необходимо быть осторожным, чтобы кровь не попала в шприц, наполненный препаратом, поскольку существует риск, что кровь может свернуться в шприце и сгустки фибрина могут быть введены пациенту.
Раствор после реconstitution должен быть введен в отдельные инфузионные наборы (поставляемые с препаратом), в медленном внутривенном введении, со скоростью не превышающей 4 мл в минуту.
Все непримененные препараты и их остатки должны быть утилизированы в соответствии с местными требованиями.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- Производитель
- ИмпортерCSL Behring GmbH
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Цлувот 250 й.м.Форма выпуска: Порошок, 1250 МЕАктивное вещество: coagulation factor XIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 1000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецептФорма выпуска: Порошок, 2000 МЕАктивное вещество: фактор свертывания крови VIIIПроизводитель: CSL Behring GmbHТребуется рецепт
Аналоги Цлувот 250 й.м. в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Цлувот 250 й.м. в Испания
Врачи онлайн по Цлувот 250 й.м.
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Цлувот 250 й.м. – по решению врача и с учетом местных правил.














