ZENNUX 10 mg/ml solução injetável em seringa pré-carregada

Pergunte a um médico sobre a prescrição de ZENNUX 10 mg/ml solução injetável em seringa pré-carregada

Como usar ZENNUX 10 mg/ml solução injetável em seringa pré-carregada
Introdução
Prospecto: informação para o utilizador
Zennux 10 mg/ml solução injetável em seringa pré-carregada
cloruro de suxametonio anidro
Leia todo o prospecto detenidamente antes de ser administrado este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, ou farmacêutico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico, ou farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Zennux e para que é utilizado
- O que precisa saber antes de ser administrado Zennux
- Como é administrado Zennux
- Possíveis efeitos adversos
- Conservação de Zennux
- Conteúdo do envase e informação adicional
1. O que é Zennux e para que é utilizado
Zennux pertence a um grupo de medicamentos chamados relaxantes musculares.
O seu efeito é bloquear a ligação entre os nervos e certos músculos, o que relaxa estes músculos paralisando-os de forma temporária.
É utilizado em adultos e em população pediátrica maior de 12 anos em anestesia geral ou casos de urgência.
Zennux é administrado durante a inserção de um tubo na traqueia (intubação endotraqueal), se uma pessoa necessita de assistência para respirar. Durante este procedimento, é necessário que os músculos utilizados para respirar estejam paralisados.
2. O que precisa saber antes de ser administrado Zennux
Não deve ser administradoZennux:
- se é alérgico ao suxametonio ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
- se é um paciente consciente;
- se você ou alguém da sua família teve uma reação negativa a um anestésico previamente como uma temperatura corporal muito alta (hipertermia maligna);
- se apresenta uma deficiência de uma enzima chamada pseudocolinesterase que descompõe o suxametonio no corpo;
- se tem um nível alto de potássio no sangue (hiperpotasemia);
- se teve um acidente grave, cirurgia ou queimaduras graves;
- se sofreu uma lesão da medula espinhal, lesão nervosa ou perda muscular súbita;
- se esteve imobilizado por um longo período de tempo, como para o tratamento de uma fratura de osso ou um longo período de repouso na cama;
- se tem fraqueza muscular ou perda de tecido muscular (p. ex. distrofia muscular de Duchenne);
- se você ou alguém da sua família tem uma doença que causa fraqueza muscular (miotonia congênita, distrofia miotônica);
- se teve lesões recentes nos olhos;
- se padece de um problema causado por uma pressão excessiva no olho (glaucoma), a menos que o benefício potencial seja maior que o risco potencial para o olho.
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro, antes de ser administrado Zennux:
- se já sofreu uma reação alérgica a qualquer relaxante muscular que lhe tenha sido administrado durante uma operação;
- se padece miastenia gravis, uma doença que causa fraqueza muscular grave, ou qualquer outra doença dos nervos ou músculos;
- se está grávida ou deu à luz nas últimas seis semanas;
- se tem tétano, uma infecção que ocorre pela contaminação de feridas;
- se tem tuberculose ou outras infecções bacterianas graves ou de longa duração.
- se tem uma doença de longa duração que o tenha debilitado.
- se padece uma doença do sangue conhecida como anemia.
- se está desnutrido ou é incapaz de absorver nutrientes dos alimentos (desnutrição).
- se padece problemas do fígado ou rins;
- se padece uma doença causada pelo ataque do corpo a si mesmo (doença autoimune) como uma doença da glândula tireoide (mixedema);
- se padece doenças que causam problemas nas articulações (doenças do colágeno);
- se tem ou teve um tratamento do sangue conhecido como plasmaférese terapêutica.
- se teve recentemente um bypass cardiopulmonar.
Crianças
Este medicamento não é recomendado em crianças menores de 12 anos porque a sub-graduação da seringa pré-carregada não permite uma administração exata do produto nesta população.
Deve ter especial cuidado quando este medicamento for administrado a crianças maiores de 12 anos.
Outros medicamentos eZennuxcom
Informa o seu médico, farmacêutico ou enfermeiro se está tomando, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Em particular, informa o seu médico, farmacêutico ou enfermeiro se está tomando ou sendo tratado com qualquer um dos seguintes:
- medicamentos utilizados em psiquiatria (p. ex. fenelzina, promazina);
- medicamentos contra o cancro (p. ex. ciclofosfamida, tiotepa, irinotecano);
- medicamentos anestésicos (p. ex. ketamina, halotano, enflurano, desflurano, propofol);
- medicamentos anestésicos locais (p. ex. lidocaína, procaína, procainamida);
- um medicamento utilizado para tratar ou prevenir as náuseas e os vómitos (metoclopramida);
- medicamentos utilizados para a doença de Alzheimer ou a miastenia gravis (anticolinesterásicos como donepezilo, edrofonio, galantamina, neostigmina, piridostigmina, rivastigmina e tacrina);
- medicamentos para o tratamento do asma ou outros problemas respiratórios (p. ex. bambuterol, terbutalina);
- substâncias orgânicas que contêm fósforo;
- um medicamento utilizado para reduzir o sangramento (aprotinina);
- estrógenos e anticoncepcionais orais que contêm estrógeno;
- um medicamento para contrair o útero (oxitocina);
- medicamentos utilizados para doenças inflamatórias (esteroides como para o reumatismo, etc.);
- medicamentos utilizados no tratamento das alterações do ritmo cardíaco (agentes antiarrítmicos como p. ex. quinidina, verapamilo);
- alguns antibióticos utilizados para tratar infecções bacterianas (p. ex. lincosamidas, polimixinas, e aminoglicosídeos);
- medicamentos antiepilépticos utilizados para deter as crises (p. ex. carbamazepina e fenitoína);
- um medicamento beta bloqueante utilizado para diminuir os batimentos do coração (esmolol);
- um medicamento para suprimir a resposta imunitária (azatioprina);
- um medicamento utilizado para controlar a sobre-excitação e/ou a depressão (lítio);
- sales de magnésio;
- medicamentos que aumentam as contrações do músculo cardíaco (glucósidos cardíacos como a digoxina);
- um medicamento utilizado para tratar a pressão alta nos olhos, ou seja, o glaucoma (ecotiopato).
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de ser administrado este medicamento.
Zennux só deve ser utilizado durante a gravidez se o seu médico decidir que os benefícios para si são superiores a qualquer risco para o bebê por nascer.
Deve ter precaução após a administração de suxametonio a pacientes grávidas ou puérperas.
Desconhece-se se suxametonio é eliminado no leite materno. No entanto, não se prevê nenhum efeito em recém-nascidos/crianças amamentadas, uma vez que suxametonio é rapidamente metabolizado a um metabolito inativo.
Condução e uso de máquinas
Pode ser perigoso conduzir ou usar máquinas demasiado cedo após ter recebido este medicamento. O seu médico dir-lhe-á quanto tempo deve esperar antes de que possa conduzir ou utilizar máquinas.
Zennuxcontém sódio.
Este medicamento contém 27,9 mg de sódio (principal ingrediente do sal de cozinha/mesa). Isto equivale a 1,4% da quantidade diária recomendada de sódio para um adulto.
3. Como é administrado Zennux
Nunca terá que se administrar este medicamento. Sempre lhe será administrado por um profissional de saúde qualificado para isso.
O seu médico decidirá a dose que receberá. Isto depende das suas necessidades pessoais, peso corporal, a quantidade de relaxação muscular requerida.
Zennux será administrado em forma de injeção na sua veia (uso intravenoso). A seringa pré-carregada não é apropriada para uso em uma bomba de seringa.
Se lhe for administrado mais Zennux do que o necessário
Como este medicamento sempre será administrado sob condições cuidadosamente controladas, é pouco provável que lhe seja administrado mais do que o necessário. Em caso de sobredosagem, o músculo se manterá relaxado mais tempo do que o necessário.
Se tiver alguma dúvida sobre o uso deste medicamento, pergunte ao seu médico, ou farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Muito frequentes (podem afetar mais de 1 de cada 10 pessoas):
- contrações musculares visíveis sob a pele
- dores musculares após a operação - o seu médico o vigiará para controlar isto.
Frequentes (podem afetar até 1 de cada 10 pessoas)
- reações alérgicas: picazón, urticária, colapso
- aumento da pressão do líquido no olho que pode causar dor de cabeça ou visão borrosa
- aumento da pressão no estômago
- aumento ou diminuição da sua frequência cardíaca
- pressão arterial baixa
- proteínas no sangue ou na urina devido a lesões musculares
- nível alto de potássio no seu sangue
- vermelhidão da pele
- erupção
Raros (podem afetar até 1 de cada 1.000 pessoas)
- dificuldade respiratória
- temperatura do corpo elevada.
- dificuldade na abertura da boca.
Não conhecido (a frequência não pode ser estimada a partir dos dados disponíveis)
- inchaço (angioedema)
- parada cardíaca
- pressão arterial alta ou baixa
- produção de saliva excessiva
- produção de flema excessiva
- perda de ar temporária
- lesões musculares
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, ou farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Zennux
Mantenha este medicamento fora da vista e do alcance das crianças.
Não deve ser administrado este medicamento após a data de validade que aparece na etiqueta da seringa pré-carregada, o blister e a caixa. A data de validade é o último dia do mês que se indica.
Conservar na geladeira (2°C – 8°C).
Não congelar.
Conservar a seringa pré-carregada no blister fechado até ao seu uso.
O medicamento deve ser utilizado imediatamente após a abertura.
Este medicamento pode ser conservado por um curto período de tempo a temperaturas que não excedam 25 °C. Em qualquer caso, uma vez que tenha sido retirado da geladeira, o medicamento deve ser deitado fora após 30 dias.
Não utilize este medicamento se observar indícios visíveis de deterioração.
Toda a seringa pré-carregada, ainda que parcialmente utilizada, deve ser deitada fora de forma apropriada após o seu uso. Os medicamentos não devem ser deitados fora por os esgotos nem para o lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Zennux
- O princípio ativo é cloruro de suxametonio.
Cada ml de solução injetável contém 10 mg de cloruro de suxametonio anidro (como 11 mg de cloruro de suxametonio dihidrato).
Cada seringa pré-carregada de 10 ml contém 100 mg de cloruro de suxametonio anidro (como 110 mg de cloruro de suxametonio dihidrato).
- Os outros componentes são: cloruro de sódio, ácido succínico, hidróxido de sódio ou ácido clorídrico (para ajuste do pH), água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Zennux é uma solução injetável límpida incolor, em uma seringa pré-carregada de polipropileno de 10 ml, envasada individualmente em um envase blister transparente. Caixas de cartão de 1 ou 10 seringas pré-carregadas.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
Laboratoire Aguettant
1 rue Alexander Fleming
69007 Lyon
França
Responsável pela fabricação
Laboratoire Aguettant
1, rue Alexander Fleming
69007 LYON
França
Laboratoire Aguettant
Lieu Dit Chantecaille
07340 Champagne
França
Representante local:
Aguettant Ibérica S.L.
Parc Científic de Barcelona
Baldiri Reixac, 4-8 (Torre I)
08028 Barcelona
Data da última revisão deste prospecto: Dezembro 2024.
A informação detalhada deste medicamento está disponível na página Web da Agência Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gov.es/)
--------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais do sector sanitário:
Instruções de uso:
A seringa pré-carregada não é apropriada para uso em uma bomba de seringa.
Por favor, prepare a seringa cuidadosamente da seguinte forma
A seringa pré-carregada deve ser utilizada em um só paciente. Deite fora a seringa após o seu uso. Não reutilize a seringa.
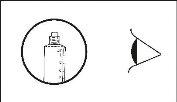
O medicamento deve ser examinado visualmente para detectar partículas e decoloração antes da administração. Só deve ser utilizado uma solução límpida incolor exente de partículas ou precipitados.
O medicamento não deve ser utilizado se o selo de segurança da seringa estiver quebrado.
A superfície externa da seringa é estéril até à abertura do blister. Não se deve abrir o blister até ao momento do seu uso.
Quando se manipula utilizando um método asséptico, este medicamento pode ser colocado sobre um campo estéril uma vez que tenha sido retirado do blister.
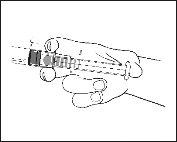
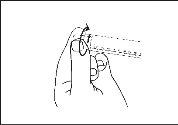
- Retire a seringa pré-carregada estéril do blister.
|
|
|
|
|
|
|
|
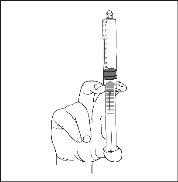
- Conecte a seringa a um dispositivo de acesso ou a uma agulha. Empurre o êmbolo lentamente para injetar o volume requerido.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ZENNUX 10 mg/ml solução injetável em seringa pré-carregadaForma farmacêutica: INJETÁVEL, 50 mg/mlSubstância ativa: suxamethoniumFabricante: EthypharmRequer receita médicaForma farmacêutica: INJETÁVEL, 200 U/mlSubstância ativa: botulinum toxinFabricante: Ipsen PharmaRequer receita médicaForma farmacêutica: INJETÁVEL, 125 Unidades SpeywoodSubstância ativa: botulinum toxinFabricante: Ipsen Pharma S.A.U.Requer receita médica
Alternativas a ZENNUX 10 mg/ml solução injetável em seringa pré-carregada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ZENNUX 10 mg/ml solução injetável em seringa pré-carregada em Polska
Alternativa a ZENNUX 10 mg/ml solução injetável em seringa pré-carregada em Ukraina
Médicos online para ZENNUX 10 mg/ml solução injetável em seringa pré-carregada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ZENNUX 10 mg/ml solução injetável em seringa pré-carregada – sujeita a avaliação médica e regras locais.