OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Como usar OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
Octanine 100 UI/ml, pó e dissolvente para solução injetável
Fator IX de coagulação humana
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi-lhe prescrito somente a si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto:
- O que é Octanine e para que é utilizado
- O que precisa saber antes de começar a usar Octanine
- Como usar Octanine
- Possíveis efeitos adversos
- Conservação de Octanine
- Conteúdo do envase e informações adicionais
1. O que é Octanine e para que é utilizado
Octanine pertence a um grupo de medicamentos denominados factores de coagulação e contém o fator IX de coagulação humana. Trata-se de uma proteína especial, que aumenta a capacidade do sangue para coagular.
Octanine é utilizado para o tratamento e a prevenção do sangramento em doentes com distúrbios sanguíneos (hemofilia B). Trata-se de uma doença que consiste em que a hemorragia pode durar mais do que o esperado. Deve-se a uma deficiência de nascimento na quantidade do fator IX de coagulação no sangue.
Octanine é fornecido sob a forma de pó e dissolvente para preparar uma solução injetável. Depois da reconstituição, é administrado por via intravenosa (injetado dentro de uma veia).
2. O que precisa saber antes de começar a usar Octanine
Não use Octanine:
- se é alérgico ao fator IX de coagulação humana ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
- se sofre de trombocitopenia de tipo II induzida por heparina, que é uma diminuição no número de plaquetas do sangue após a administração de heparina. As plaquetas são células sanguíneas que ajudam a deter o sangramento. A heparina é um medicamento que se utiliza para prevenir os coágulos sanguíneos.
Advertências e precauções
- Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Octanine.
- Assim como todos os medicamentos que contêm proteínas e que se administran por via intravenosa, podem produzir-se reações de hipersensibilidade de tipo alérgico. Octanine contém muito pequenas quantidades de proteínas humanas diferentes do fator IX e da heparina. Os primeiros sinais de reações de hipersensibilidade incluem:
- erupção cutânea
- urticária
- opressão no peito
- dificuldade para respirar
- diminuição da tensão arterial
- reação alérgica aguda e grave (anafilaxia quando algum ou todos os sintomas anteriores se desenvolvem rapidamente e são intensos)
Se aparecerem estes sintomas, interrompa imediatamente a injeção e consulte o seu médico. Em caso de choque anafilático, deve iniciar o tratamento recomendado o mais breve possível.
- O seu médico pode recomendar-lhe que considere a vacinação contra a hepatite A e B se você receber de forma regular ou repetida produtos derivados de plasma humano que contenham fator IX.
- Sabe-se que os indivíduos com hemofilia B podem desenvolver inibidores (anticorpos neutralizantes) do fator IX, produzido pelas células imunitárias. Os inibidores podem aumentar o risco de sofrer um choque anafilático (reações alérgicas graves). Por tanto, se você sofrer uma reação alérgica, têm que analisar a presença de um inibidor. Os doentes com inibidores do fator IX podem ter um risco maior de anafilaxia se forem tratados com fator IX. Por tanto, o seu médico pode decidir administrar-lhe a primeira injeção de fator IX sob supervisão médica, para poder proporcionar-lhe os cuidados adequados em caso de reações alérgicas.
- Os concentrados de proteínas de fator IX podem causar uma obstrução nos vasos sanguíneos por um coágulo. Devido a este risco, que é maior em produtos de baixa pureza, devem controlar os sintomas de formação de coágulos no sangue após a administração de produtos de fator IX se você:
- apresenta sinais de fibrinólise (coágulos sanguíneos que se têm rompido)
- apresenta coagulação intravascular disseminada (a coagulação estendida do sangue dentro dos vasos sanguíneos)
- foi diagnosticado com doença hepática
- apresenta fatores de risco cardiovasculares documentados
- foi operado recentemente
- tem um risco elevado de formação de coágulos ou de coagulação intravascular disseminada.
Se algum dos sintomas anteriores for real em você, o seu médico só lhe administrará Octanine se o benefício superar os riscos.
- Após o tratamento repetido com produtos à base de fator IX de coagulação humana, há que vigiar nos doentes o possível desenvolvimento de anticorpos neutralizantes (inibidores) que devem ser quantificados em Unidades Bethesda (UB) utilizando as provas biológicas adequadas.
Segurança viral dos produtos sanguíneos
- Quando se administram medicamentos derivados de plasma ou sangue humano, há que levar a cabo certas medidas para evitar que as infecções passem aos doentes. Tais medidas incluem uma cuidadosa seleção dos doadores, para excluir aqueles que estão em risco de ser portadores de doenças infecciosas, análise de marcadores específicos de infecções nas doações individuais e nas misturas de plasma, assim como a inclusão de etapas no processo de fabricação para eliminar/inativar vírus. Apesar disto, quando se administram medicamentos derivados do sangue ou plasma humanos, a possibilidade de transmissão de agentes infecciosos não se pode excluir totalmente. Isso também se refere a vírus emergentes ou de natureza desconhecida ou outros tipos de infecções.
- Estas medidas são consideradas eficazes para vírus envoltos como o vírus da imunodeficiência humana (VIH), vírus da hepatite B e vírus da hepatite C e para o vírus não envolto da hepatite A. As medidas tomadas podem ter um valor limitado frente a outros vírus não envoltos como o parvovirus B19. A infecção por parvovirus B19 pode ser grave para uma mulher grávida (infecção fetal) e para pessoas cujo sistema imunológico está deprimido ou em doentes que têm algum tipo de anemia (por exemplo, anemia falciforme ou anemia hemolítica).
- É possível que o seu médico lhe recomende vacinar-se contra a hepatite A e hepatite B, se a você se lhe administrar de forma regular ou repetida medicamentos obtidos de plasma humano.
- Recomenda-se encarecidamente que, cada vez que se administre uma dose de Octanine, se deixe constância do nome do medicamento e número de lote administrado com o fim de manter um registo dos lotes utilizados.
Crianças
Se se administra Octanine a um recém-nascido, há que controlar muito no bebê os sinais de coagulação intravascular disseminada.
Outros medicamentos e Octanine
- Até onde se sabe, os produtos à base de fator IX de coagulação humana não interagem com qualquer outro medicamento.
Informa ao seu médico ou farmacêutico se está utilizando ou utilizou recentemente ou poderia ter que utilizar outros medicamentos, mesmo os adquiridos sem receita.
Gravidez e amamentação
Não se dispõe de dados sobre o uso do fator IX durante a gravidez e a amamentação. Por tanto, o fator IX deve ser usado na gravidez e na amamentação só se estiver claramente indicado.
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
Não se observaram efeitos sobre a capacidade de condução e o uso de máquinas.
Octanine contém sódio
Este medicamento contém até 69 mg de sódio (principal componente do sal para cozinhar/mesa) em 1 frasco de Octanine 500 UI, equivalente a 3,45% do consumo máximo diário recomendado de sódio para um adulto e até 138 mg de sódio em 1 frasco de Octanine 1000 UI, equivalente a 6,9% do consumo máximo diário recomendado de sódio para um adulto.
Deve ter-se em conta no tratamento de doentes com dietas pobres em sódio.
3. Como usar Octanine
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte de novo o seu médico ou farmacêutico.
Octanine deve ser administrado por via intravenosa (injetado em uma veia) após a reconstituição com o dissolvente fornecido.
Utilize somente o equipamento de perfusão que se fornece. O uso de outros equipamentos de injeção/infusão pode causar riscos adicionais e um fracasso do tratamento.
O tratamento deve ser iniciado sob a supervisão de um médico com experiência no tratamento da hemofilia. A quantidade de Octanine que deve utilizar e a duração da terapia de substituição dependem da gravidade da sua deficiência de fator IX. Também depende do local e do grau da hemorragia, além do seu estado clínico.
Cálculo da dose:
O seu médico indicar-lhe-á com que frequência e que quantidade de Octanine precisa que lhe seja injetada.
A dose do fator IX é expressa em Unidades Internacionais (UI). A atividade do Fator IX no plasma refere-se à quantidade de Fator IX presente no plasma. É expressa bem como porcentagem (com respeito ao plasma humano normal) ou em Unidades Internacionais (com respeito a um padrão internacional para o fator IX no plasma).
Uma Unidade Internacional (UI) de atividade de fator IX é equivalente à quantidade de fator IX em um mililitro de plasma humano normal. O cálculo da dose requerida de fator IX baseia-se na observação de que 1 UI de Fator IX por quilograma de peso corporal aumenta a atividade do fator IX no plasma em 1% da atividade normal. Para calcular a dose que você precisa, mede-se o nível de atividade do fator IX no seu plasma sanguíneo. Isso indicará quantia de atividade se precisa aumentar.
A dose requerida é calculada utilizando a fórmula seguinte:
Unidades requeridas = peso corporal (kg) x aumento desejado do fator IX (%) (UI/dl) x 0,8
A quantia da sua dose e a frequência com que deve ser administrada dependem de como você responde ao medicamento e será decidida pelo seu médico. Os produtos do fator IX raramente requerem ser administrados mais de uma vez ao dia.
A sua resposta aos produtos do fator IX pode ser variável. Por tanto, há que medir os seus níveis de fator IX durante o tratamento para calcular a dose correta e a frequência da infusão. Em especial durante as operações quirúrgicas, o seu médico utilizará provas sanguíneas (atividade plasmática do fator IX) para controlar atentamente a terapia de substituição.
Prevenção da hemorragia:
Se você sofre de hemofilia B grave, deve ser injetada 20 a 40 UI de fator IX por quilograma de peso corporal (PC). Deve ser administrada esta dose duas vezes por semana para uma prevenção a longo prazo. A sua dose deve ser ajustada em função da sua resposta. Em alguns casos, especialmente em doentes jovens, podem ser necessários intervalos de administração mais curtos ou doses mais altas.
Uso em crianças:
No estudo realizado em crianças menores de 6 anos, a dose média administrada por dia de exposição foi de 40 UI/kg PC.
Se não pode detener-se a hemorragia devido aos inibidores:
Se não se consegue a atividade esperada do fator IX após uma injeção ou a hemorragia não se interrompe após a administração da dose correta, deve informar o seu médico. O examinará o seu plasma sanguíneo para ver se desenvolveu inibidores (anticorpos) frente à proteína do fator IX. Estes inibidores podem reduzir a atividade do fator IX. Neste caso pode ser necessário escolher um tratamento diferente. O seu médico discutirá isso com você e lhe recomendará outro tratamento se for necessário.
Se usa mais Octanine do que deve
Não se observaram sintomas de sobredose com fator IX de coagulação humana. No entanto, não deve exceder a dose recomendada.
Para as “Instruções para o tratamento em domicílio”, ver o estojo do pacote do equipamento.
4. Possíveis efeitos adversos
Assim como todos os medicamentos, Octanine pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
- De maneira pouco frequente se observaram reações de hipersensibilidade ou alérgicas em doentes tratados com produtos que contenham fator IX. Estas reações podem incluir:
- Contração involuntária dos vasos sanguíneos (espasmos) com inchação na face, boca e garganta
- Ardor e picadas no local da infusão
- arrepios
- rubor
- erupção cutânea
- dor de cabeça
- urticária
- diminuição da tensão arterial
- cansaço
- malestar
- inquietude
- batimentos cardiacos rápidos
- opressão no peito
- formigamento
- vómitos
- dificuldade para respirar
Em alguns casos, estas reações alérgicas podem desembocar em uma reação grave chamada anafilaxia, que pode incluir choque. Geralmente estas reações estão associadas ao desenvolvimento de inibidores do fator IX. Se sofrer um dos sintomas mencionados anteriormente, informe o seu médico.
- Se sofre de hemofilia B pode desenvolver anticorpos neutralizantes (inibidores) do fator IX. Estes anticorpos podem interromper o bom funcionamento do seu medicamento. O seu médico o comentará com você e lhe recomendará outro tratamento se for necessário.
Foi realizado um estudo em 25 crianças com hemofilia B, das quais 6 doentes não foram tratados previamente. Não se observou nenhum inibidor durante o estudo. A tolerabilidade de todas as injeções foi estimada como “muito boa” ou “boa”.
- Alguns doentes com hemofilia B com inibidores do fator IX com terapia de imunotolerância e um histórico de reações alérgicas desenvolveram síndrome nefrótica (uma doença grave dos rins).
- Em raros casos pode produzir febre.
- Os produtos de fator IX de baixa pureza raramente podem fazer com que se forme um coágulo de sangue dentro dos vasos sanguíneos. Isso pode dar lugar a alguma das seguintes complicações:
- ataque cardíaco
- coagulação estendida nos vasos sanguíneos (coagulação intravascular disseminada)
- coágulos de sangue nas veias (trombose venosa)
- coágulos de sangue nos pulmões (embolia pulmonar).
Estes efeitos secundários são mais frequentes se usa produtos de fator IX de baixa pureza e são raros se usa produtos de alta pureza como Octanine.
- A heparina do preparado pode causar uma queda brusca do número de plaquetas no sangue por baixo de 100.000 por microlitro ou menos de 50% do recuento inicial. Isso é uma reação alérgica chamada “trombocitopenia tipo II induzida por heparina”. Em raros casos nos doentes que não são previamente hipersensíveis à heparina, esta queda no número de plaquetas pode ocorrer 6-14 dias após o início do tratamento. Em doentes com hipersensibilidade prévia à heparina, esta alteração pode desenvolver-se às poucas horas do início do tratamento. Esta forma grave de redução plaquetária pode ir acompanhada, ou dar como resultado:
- coágulos sanguíneos nas artérias e nas veias
- obstrução de um vaso sanguíneo por um coágulo procedente de outra área
- um distúrbio grave da coagulação denominado coagulopatia de consumo
- gangrena cutânea na área da injeção
- sangramento com aspecto de picada de mosquito
- hematomas
- fezes cor de alcatrão.
Se observa estas reações alérgicas, interrompa imediatamente as injeções com Octanine e não use no futuro medicamentos que contenham heparina.Devido a este raro efeito sobre as plaquetas sanguíneas, o seu médico controlará muito a quantidade de plaquetas sanguíneas, especialmente ao começar o tratamento.
Para a segurança com respeito a agentes transmissíveis, ver a secção 2.
Comunicação de efeitos adversos
Se experimenta qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es.
Mediante a comunicação de efeitos adversos você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Octanine
Mantenha este medicamento fora da vista e do alcance das crianças.
Conservar o frasco no embalagem exterior para protegê-lo da luz e por baixo de +25ºC. Não congelar.
Não utilize este medicamento após a data de caducidade que aparece na etiqueta e na caixa. A data de caducidade é o último dia do mês que se indica.
Recomenda-se utilizar o produto reconstituído imediatamente, e, de lo contrario, ao menos nas 8 horas posteriores armazenado a temperatura ambiente (25ºC). Use Octanine em uma única ocasião.
Não utilize este medicamento se observar soluções turvas ou que não estejam completamente dissolvidas. Elimine o conteúdo que não foi utilizado. Os medicamentos não devem ser jogados pelos deságues nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma ajudará a proteger o meio ambiente.
6. Conteúdo do frasco e informação adicional
Composição de Octanine
O princípio ativoé o fator IX de coagulação humana.
Os outros componentessão heparina, cloreto de sódio, citrato de sódio, hidrocloruro de arginina e hidrocloruro de lisina.
Aspecto de Octanine e conteúdo do frasco
Octanine apresenta-se em 2 tamanhos de frasco com as seguintes doses:
- Octanine 100 UI/ml apresentação para reconstituir com 5 ml de água para injetáveis, apresenta-se como pó e dissolvente para injeção com um conteúdo nominal de 500 UI de fator IX de coagulação humano por frasco.
- Octanine 100 UI/ml apresentação para reconstituir com 10 ml de água para injetáveis, apresenta-se como pó e dissolvente para injeção com um conteúdo nominal de 1000 UI de fator IX de coagulação humano por frasco.
Octanine é produzido com plasma de doadores humanos.
A potência (UI) é determinada utilizando o teste de coagulação de uma única etapa da Farmacopeia Europeia, comparando-a com o padrão internacional da Organização Mundial da Saúde (OMS). A atividade específica de Octanine é aproximadamente de 100 UI/mg proteína.
Descrição do frasco:
Octanine é fornecido como um pacote combinado que contém dois estuches unidos com um selo de plástico:
Um estuche contém 1 frasco com pó para solução injetável e o prospecto.
O outro estuche contém o frasco com o dissolvente (água para injetáveis, 5 ml para a apresentação de 500 UI e 10 ml para a apresentação de 1000 UI).
Este frasco também contém os seguintes dispositivos médicos:
- 1 estuche do equipamento para injeção intravenosa (1 equipamento de transferência, 1 equipamento de perfusão, 1 seringa descartável)
- 2 compressas com álcool
Título da autorização de comercialização e responsável pela fabricação
Para qualquer informação sobre este medicamento, entre em contato com o titular da autorização de comercialização.
Octapharma S.A.
Parq. Em. S. Fernando,
Avda. Castilla 2 - Edif. Dublin - 2ª Planta,
San Fernando de Henares (Madrid) 28830
Responsável pela fabricação:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Strasse 235
A-1100 Viena
Áustria
ou
Octapharma S.A.S.
70-72 Rue du Maréchal Foch
67380 Lingolsheim
França
Data da última revisão deste prospectoNovembro 2020.
A informação detalhada e atualizada deste medicamento está disponível no site da Agência Espanhola do Medicamento e Produtos Sanitários (AEMPS)
http://www.aemps.gob.es/
Instruções para o tratamento ambulatorial
- Por favor, leia todas as instruções e siga-ascuidadosamente.
- Não utilizeOctanine após a data de validade que aparece na etiqueta e na caixa.
- Durante o procedimento descrito a seguir, deve-se manter a esterilidade.
- Inspeccionar visualmente o medicamento reconstituído para verificar se existem partículas ou mudança de coloração antes da administração
- A solução deve ser límpida ou ligeiramente opalescente. Não use soluções turvas ou que contenham sedimentos.
- Utilize imediatamente a solução preparada, para evitar contaminação microbiana.
- Utilize apenas o equipamento de perfusão que é incluído. O uso de outro equipamento de injeção/perfusão pode ocasionar um risco adicional e o fracasso do tratamento.
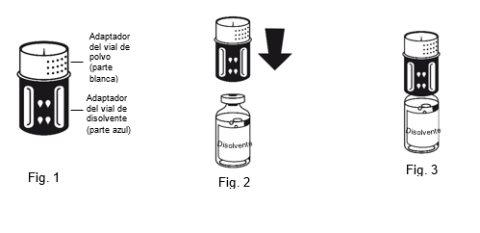
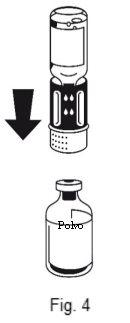
Instruções para preparar a solução:
|
|
|
|
|
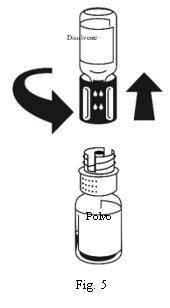
A dissolução é completa em menos de 10 minutos a temperatura ambiente. Pode aparecer uma leve espuma durante a preparação. Desenrosque as duas partes do equipamento de transferência (Fig. 5). A espuma desaparecerá. Descarte o frasco de dissolvente vazio junto com a parte azul do equipamento de transferência. |
|
Instruções para a injeção:
Como precaução, deve-se medir a velocidade do pulso antes e durante a injeção. Se a velocidade do pulso aumentar muito, reduza a velocidade da injeção ou interrompa a administração durante um breve período de tempo.
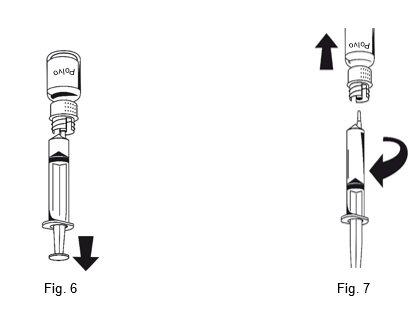
- Acople a seringa à parte branca do equipamento de transferência. Dê a volta ao frasco e extraia a solução para o interior da seringa (Fig.6). A solução deve ser límpida ou ligeiramente opalescente.
Uma vez que a solução foi transferida, segure firmemente o êmbolo da seringa (mantendo-o para baixo) e extraia a seringa do equipamento de transferência (Fig. 7). Descarte o frasco vazio junto com a parte branca do equipamento de transferência.
- Limpe a zona onde se vai aplicar a injeção com uma das compressas com álcool que são incluídas.
- Acople o equipamento de perfusão que é incluído à seringa.
- Insira a agulha de injeção na veia escolhida. Se empregou um torniquete para ver a veia com mais facilidade, este torniquete deve ser liberado antes de começar a injetar Octanine.
Não deve fluir sangue para o interior da seringa devido ao risco de formação de coágulos de fibrina.
- Injete a solução dentro da veia a uma velocidade lenta, não superior a 2-3 ml por minuto.
Se usa mais de um frasco de pó de Octanine para um tratamento, pode empregar a mesma agulha de injeção e a mesma seringa.
O equipamento de transferência é de um só uso.
A eliminação do medicamento não utilizado e de todos os materiais que estiveram em contato com ele será realizada de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 1.000 UISubstância ativa: coagulation factor IXFabricante: Swedish Orphan Biovitrum Ab (Publ)Requer receita médicaForma farmacêutica: INJETÁVEL, 2.000 UISubstância ativa: coagulation factor IXFabricante: Swedish Orphan Biovitrum Ab (Publ)Requer receita médicaForma farmacêutica: INJETÁVEL, 250 UISubstância ativa: coagulation factor IXFabricante: Swedish Orphan Biovitrum Ab (Publ)Requer receita médica
Alternativas a OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Poland
Alternativa a OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de OCTANINE 100 UI/ml PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.