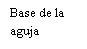
FENDRIX, SUSPENSÃO INJETÁVEL

Pergunte a um médico sobre a prescrição de FENDRIX, SUSPENSÃO INJETÁVEL

Como usar FENDRIX, SUSPENSÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
Fendrix suspensão injetável
Vacina anti-hepatite B (ADN-r) (adjuvada, adsorvida)
Leia todo o prospecto atentamente antes de receber esta vacina, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Esta vacina foi prescrita apenas para si, e não deve dá-la a outras pessoas.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Fendrix e para que é utilizado
- O que precisa saber antes de receber Fendrix
- Como é administrado Fendrix
- Efeitos adversos possíveis
- Conservação de Fendrix
- Conteúdo do envase e informações adicionais
1. O que é Fendrix e para que é utilizado
Fendrix é uma vacina que previne a hepatite B.
É utilizado em doentes com problemas renais:
- doentes submetidos a hemodiálise, nos quais uma máquina de diálise elimina os produtos de resíduo do sangue
- doentes que vão ser submetidos a hemodiálise no futuro.
Fendrix é para adultos e jovens a partir dos 15 anos.
O que é a hepatite B
A hepatite B é causada por um vírus que faz com que o fígado se inflame.
- Pode que não se observem os sinais até ter passado um período de 6 semanas a 6 meses após a infecção.
- Os principais sinais da doença incluem sinais leves de uma gripe, tais como dor de cabeça ou febre, sensação de cansaço extremo, urina de cor escura, fezes de cor pálida, olhos ou pele de cor amarela (icterícia). Estes ou outros sinais podem significar que a pessoa necessita de tratamento no hospital. A maioria das pessoas se recupera completamente da doença.
- Algumas pessoas com hepatite B não parecem doentes ou não se sentem doentes (não têm nenhum sinal da doença).
- O vírus está presente em fluidos corporais, tais como na vagina, sangue, sêmen ou saliva (escarro).
Portadores de hepatite B
- O vírus da hepatite B permanece no organismo de algumas pessoas durante toda a vida.
- Isso significa que podem infectar outras pessoas e são conhecidos como portadores do vírus.
- É provável que os portadores do vírus desenvolvam problemas graves no fígado, tais como cirrose ou cancro do fígado.
Como actua Fendrix
- Fendrix ajuda o seu organismo a desenvolver a sua própria proteção contra o vírus (anticorpos). Estes anticorpos são os que o protegerão contra a doença.
- Fendrix contém duas substâncias denominadas MPL (um derivado gordo purificado não tóxico de origem bacteriana) e fosfato de alumínio. Ambas permitem que a vacina funcione mais rapidamente, melhor e durante mais tempo.
- Como com todas as vacinas, um ciclo de vacinação com Fendrix pode não proteger completamente todas as pessoas vacinadas.
- Pode que Fendrix não o proteja da doença se já foi infectado pelo vírus da hepatite B.
- Fendrix só pode protegê-lo contra a infecção pelo vírus da hepatite B. Não pode protegê-lo contra outras infecções que possam afectar o fígado, mesmo que estas infecções tenham sinais semelhantes aos causados pelo vírus da hepatite B.
2. O que precisa saber antes de receber Fendrix
Não deve ser administrado Fendrix
- se é alérgico ao princípio ativo ou a algum dos outros componentes deste medicamento (incluídos na secção 6). Os sinais de uma reação alérgica podem incluir: erupção cutânea com picazón, dificuldade para respirar e inchação da face ou da língua
- se teve alguma vez uma reação alérgica a qualquer vacina contra a hepatite B
- se tem uma infecção grave com febre. Pode ser administrada a vacina uma vez que se tenha recuperado. Uma infecção de pouca importância, como um resfriado, não deveria ser um problema para a vacinação, mas diga-o primeiro ao seu médico.
Não deve ser administrado Fendrix se alguma das situações acima o afecta. Se não tem a certeza, consulte o seu médico ou farmacêutico antes de receber Fendrix.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de que se lhe administre Fendrix:
- se tem alergias conhecidas
- se teve algum problema de saúde após a administração de uma vacina com anterioridade.
Antes ou depois de qualquer injeção, poderia produzir-se um desmaio (especialmente nos adolescentes), por isso deve informar o seu médico ou enfermeiro se já desmaiou em ocasiões anteriores após a administração de uma injeção.
Se alguma das situações acima o afecta (ou não tem a certeza), consulte com o seu médico ou farmacêutico antes de receber Fendrix.
Outros medicamentose Fendrix
Informa o seu médico se está a utilizar, utilizou recentemente ou poderia ter que utilizar qualquer outro medicamento ou se recebeu recentemente qualquer outra vacina.
- Deveria dispor de um intervalo de, pelo menos, 2 a 3 semanas entre a administração de Fendrix e qualquer outra vacina.
- Pode que Fendrix tenha que ser administrado ao mesmo tempo que uma injeção de imunoglobulinas de hepatite B. O seu médico se certificará de que as vacinas se lhe administram em diferentes partes do corpo.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que poderia estar grávida ou tem intenção de engravidar, consulte o seu médico antes de que se lhe administre esta vacina.
Condução e uso de máquinas
Pode sentir-se cansado ou ter dor de cabeça após receber Fendrix. Se lhe acontecer isso, tenha especial cuidado enquanto conduz ou maneja ferramentas ou máquinas.
Fendrix contém sódio
Esta vacina contém menos de 1 mmol de sódio (23 mg) por dose; isto é, é essencialmente “isento de sódio”.
3. Como é administrado Fendrix
Como é administrada a vacina
O médico ou o enfermeiro lhe injetará Fendrix num músculo, normalmente na parte superior do seu braço.
Quantidade administrada
- Receberá uma série de quatro injeções.
- As injeções serão administradas num período de 6 meses:
- Primeira injeção: na data acordada com o seu médico.
- Segunda injeção: 1 mês após a primeira injeção
- Terceira injeção: 2 meses após a primeira injeção.
- Quarta injeção: 6 meses após a primeira injeção.
- O médico ou o enfermeiro lhe dirá quando deve voltar para as próximas injeções.
- Uma vez que tenha recebido a primeira injeção de Fendrix, é necessário que as próximas injeções sejam também de Fendrix (não outro tipo de vacina para a hepatite B).
O seu médico lhe dirá se precisa de alguma injeção adicional ou de recorde no futuro. Fendrix pode ser utilizado também como dose de recorde após um ciclo de vacinação com um tipo diferente de vacina para a hepatite B.
Se não receber uma dose
- Se não receber uma injeção, consulte o seu médico e concerte outra consulta.
- Certifique-se de que termina o ciclo de vacinação completo de quatro injeções. Caso contrário, pode não estar completamente protegido contra a doença.
4. Efeitos adversos possíveis
Como com todos os medicamentos, esta vacina pode produzir efeitos adversos, embora não todas as pessoas os sofram.
Os seguintes efeitos adversos podem ocorrer com esta vacina. A sua frequência é determinada utilizando a seguinte definição:
Muito frequentes(estes podem ocorrer com mais de 1 de cada 10 doses da vacina): dor de cabeça, sensação de cansaço, dor ou desconforto no local da injeção.
Frequentes(estes podem ocorrer até com 1 de cada 10 doses da vacina): vermelhidão ou inchação no local da injeção, febre, problemas de digestão e de estômago.
Pouco frequentes(estes podem ocorrer até com 1 de cada 100 doses da vacina): arrepios, erupção cutânea com vermelhidão, outras reações no local da injeção.
Raros(estes podem ocorrer até com 1 de cada 1.000 doses da vacina): reações alérgicas, sofocos, sensação de tontura, sensação de sede, sensação de nervosismo, infecção causada por um vírus, dor de costas, inflamação dos tendões.
Além disso, foram notificados os seguintes efeitos adversos com outras vacinas contra a hepatite B:
Muito raros(estes podem ocorrer até com 1 de cada 10.000 doses da vacina): ataques, desmaios, problemas com os nervos do olho (neurite óptica), esclerose múltipla, perda de sensibilidade ou problemas para mover algumas partes do corpo, dor de cabeça grave com rigidez de pescoço, entorpecimento ou fraqueza de braços e pernas (neuropatia), inflamação dos nervos (neurite), fraqueza e paralisia das extremidades progredindo frequentemente para o peito e para a face (síndroma de Guillain-Barré), inchação ou infecção do cérebro (encefalite, encefalopatia).
Reações alérgicas, incluindo reações anafilactoides, também podem ocorrer muito raramente (até com 1 de cada 10.000 doses da vacina). Podem ser erupções cutâneas locais ou disseminadas com picazón ou com bolhas, inchação dos olhos e da face, dificuldade para respirar ou engolir, queda repentina da pressão sanguínea e perda de consciência. Estas reações podem ocorrer antes de abandonar a consulta do médico. No entanto, procure imediatamente tratamento médico em qualquer caso.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilância de Medicamentos de Uso Humano, https://www.notificaram.es. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Fendrix
- Mantenha esta vacina fora da vista e do alcance das crianças.
- Não utilize esta vacina após a data de validade que aparece no envase. A data de validade é o último dia do mês que se indica.
- Conservar em frigorífico (entre 2 ºC e 8 ºC).
- Conservar no embalagem original para protegê-lo da luz.
- Não congelar. O congelamento destrói a vacina.
- Os medicamentos não devem ser jogados fora pelos esgotos nem para o lixo. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Fendrix
- O princípio ativo em 1 dose (0,5 ml) de Fendrix é:
Antígeno de superfície do vírus da Hepatite B 1, 2, 3 20 microgramas
1adjuvado por AS04C que contém:
3-O-desacil-4’- monofosforil lípido A (MPL) 2 50 microgramas
2adsorvido em fosfato de alumínio (0,5 miligramas de Al3+ no total)
3produzido pela tecnologia do ADN recombinante em células de levedura (Saccharomyces cerevisiae)
- Os demais componentes de Fendrix são: cloreto de sódio, água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Fendrix é uma suspensão branca e leitosa.
Fendrix está disponível em seringa pré-carregada de 1 dose com ou sem agulhas separadas, tamanhos de envase de 1 e 10.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação:
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Bélgica GlaxoSmithKline Pharmaceuticals SA/NV Tel: + 32 10 85 52 00 | Lituânia GlaxoSmithKline Biologicals SA Tel: +370 80000334 |
Bulgária GlaxoSmithKline Biologicals SA Tel: + 359 80018205 | Luxemburgo GlaxoSmithKline Pharmaceuticals SA/NV Tel: + 32 10 85 52 00 |
República Checa GlaxoSmithKline s.r.o. Tel: + 420 2 22 00 11 11 | Hungria GlaxoSmithKline Biologicals SA Tel: + 36 80088309 |
Dinamarca GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 | Malta GlaxoSmithKline Biologicals SA Tel: + 356 80065004 |
Alemanha GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0)89 360448701 | Países Baixos GlaxoSmithKline BV Tel: + 31 (0)30 69 38 100 |
Estônia GlaxoSmithKline Biologicals SA Tel: +372 8002640 | Noruega GlaxoSmithKline AS Tlf: + 47 22 70 20 00 |
Grécia GlaxoSmithKline Μονοπρ?σωπη A.E.B.E. Tηλ: + 30 210 68 82 100 | Áustria GlaxoSmithKline Pharma GmbH. Tel: + 43 (0)1 970 75-0 |
Espanha GlaxoSmithKline, S.A. Tel: + 34 900 202 700 | Polônia GSK Services Sp. z o.o. Tel: + 48 (22) 576 9000 |
França Laboratoire GlaxoSmithKline Tél: + 33 (0) 1 39 17 84 44 Croácia GlaxoSmithKline Biologicals SA Tel: + 385 800787089 | Portugal Smith Kline & French Portuguesa - Produtos Farmacêuticos, Lda. Tel: + 351 21 412 95 00 Romênia GlaxoSmithKline Biologicals SA Tel: +40 800672524 |
Irlanda GlaxoSmithKline (Irlanda) Ltd Tel: + 353 (0)1 495 5000 | Eslovênia GlaxoSmithKline Biologicals SA Tel: + 386 80688869 |
Islândia Vistor hf. Sími: +354 535 7000 | Eslováquia GlaxoSmithKline Biologicals SA Tel: + 421 800500589 |
Itália GlaxoSmithKline S.p.A. Tel: + 39 (0)45 774 1111 | Finlândia GlaxoSmithKline Oy Puh/Tel: + 358 10 30 30 30 |
Chipre GlaxoSmithKline Biologicals SA Tηλ: + 357 80070017 | Suécia GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 |
Letônia GlaxoSmithKline Biologicals SA Tel: + 371 80205045 | Reino Unido (Irlanda do Norte) GlaxoSmithKline Biologicals SA Tel: +44 (0)800 221 441 |
Data da última revisão deste prospecto:04/2023
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu, e no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) (http://www.aemps.gob.es/).
--------------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais de saúde:
Durante a conservação da vacina, pode ser observado um depósito branco fino e um sobrenadante transparente.
Antes da administração, a vacina deve ser agitada bem, para obter uma suspensão branca ligeiramente opaca.
A vacina deve ser examinada visualmente antes e após a ressuspensão para observar se existe alguma partícula estranha e/ou mudança do aspecto físico. A vacina não deve ser utilizada se houver ocorrido alguma mudança no aspecto da vacina.
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a normativa local.
Fendrix não deve ser administrado a indivíduos com hipersensibilidade ao princípio ativo ou a qualquer um dos excipientes.
Fendrix não deve ser administrado a indivíduos com hipersensibilidade após uma administração anterior de outras vacinas de hepatite B.
Fendrix não deve ser administrado a indivíduos que padecem de doenças febris agudas graves. A presença de uma infecção de pouca importância, como um resfriado, não é uma contraindicação para a vacinação.
Fendrix deve ser injetado por via intramuscular na região deltóidea.
Deve-se evitar a administração intramuscular no músculo glúteo, pois pode conduzir a uma resposta imunológica subóptima à vacina.
Em nenhuma circunstância deve ser administrado Fendrix por via intradérmica ou intravenosa.
Devido ao fato de que os pacientes pré-hemodiálise e hemodiálise estão particularmente expostos ao VHB e têm um maior risco de estarem infectados de forma crônica, deve-se considerar uma atitude preventiva, ou seja, deve ser administrada uma dose de reforço para assegurar um nível protetor de anticorpos com base nas recomendações e diretrizes locais.
Deve-se dispor em todo momento do tratamento médico adequado, para o caso pouco comum de que se apresente uma reação anafilática após a administração da vacina.
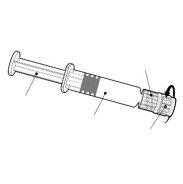
Instruções para a seringa pré-carregada
| Segure a seringa pelo corpo, não pelo êmbolo. Desrosqueie a tampa da seringa girando-a no sentido contrário ao das agulhas do relógio. |
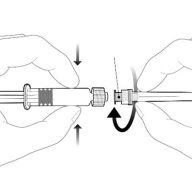
| Para inserir a agulha, conecte a base ao adaptador luer-locke gire-o um quarto de volta no sentido das agulhas do relógio até que sinta que se bloqueia. Não retire o êmbolo da seringa do corpo. Se isso ocorrer, não administre a vacina. |
Eliminação de resíduos
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FENDRIX, SUSPENSÃO INJETÁVELForma farmacêutica: INJETÁVEL, 20 mcg Antígeno de Superfície da Hepatite B/ mlSubstância ativa: hepatitis B, purified antigenFabricante: Glaxosmithkline S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 10 mcg Antígeno de Superfície da Hepatite B / 0,5 mlSubstância ativa: hepatitis B, purified antigenFabricante: Glaxosmithkline S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 20 µgSubstância ativa: hepatitis B, purified antigenFabricante: Glaxosmithkline BiologicalsRequer receita médica
Alternativas a FENDRIX, SUSPENSÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a FENDRIX, SUSPENSÃO INJETÁVEL em Polónia
Alternativa a FENDRIX, SUSPENSÃO INJETÁVEL em Ukraine
Médicos online para FENDRIX, SUSPENSÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de FENDRIX, SUSPENSÃO INJETÁVEL – sujeita a avaliação médica e regras locais.