
EMLA 25 mg/g + 25 mg/g CREME

Pergunte a um médico sobre a prescrição de EMLA 25 mg/g + 25 mg/g CREME

Como usar EMLA 25 mg/g + 25 mg/g CREME
Introdução
Prospecto: Informação para o utilizador
EMLA 25 mg/g + 25 mg/g creme
lidocaína/prilocaína
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contéminformações importantes para si.
- Conserva este prospecto, porque pode ter que o ler novamente.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é EMLA e para que é utilizado
- O que precisa saber antes de começar a usar EMLA
- Como usar EMLA
- Posíveis efeitos adversos
- Conservação de EMLA
- Conteúdo do envase e informações adicionais
1. O que é EMLA e para que é utilizado
EMLA contém dois princípios ativos chamados lidocaína e prilocaína. Pertencem a um grupo de medicamentos chamados anestésicos locais.
EMLA actua insensibilizando a superfície da pele de maneira temporária. É aplicado sobre a pele antes de algumas intervenções médicas. Ajuda a deter a dor na pele; no entanto, si pode continuar a perceber sensações como pressão e contacto.
Adultos, adolescentes e crianças
Pode ser usado para insensibilizar a pele antes de:
- Punção com agulha (p. ex., se lhe vão dar uma injeção ou fazer uma análise de sangue).
- Cirurgia menor na pele.
Adultos e adolescentes
Também pode ser usado:
- Para insensibilizar os genitais antes de:
- Colocar uma injeção.
- Procedimentos médicos como extirpação de verrugas.
O uso de EMLA nos genitais deve ser supervisionado por um médico ou um enfermeiro.
Adultos
Também pode ser utilizado para insensibilizar a pele antes de:
- Limpar ou eliminar pele danificada de úlceras nas pernas.
2. O que precisa saber antes de começar a usar EMLA
Não use EMLA
- se é alérgico à lidocaína ou prilocaína,outros anestésicos locais semelhantes ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a utilizar EMLA
- se si ou seu filho sofrem de uma alteração metabólica rara hereditária que afeta o sangue chamada “deficiência de glucosa-6-fosfato desidrogenase”.
- se si ou seu filho têm uma alteração dos níveis de um pigmento no sangue chamada “metahemoglobinemia”.
- não utilize EMLA sobre áreas com erupção cutânea, cortes, abrasões ou feridas abertas, com a exceção de úlceras nas pernas. Se apresentar algum desses problemas, consulte o seu médico ou farmacêutico antes de utilizar o creme.
- se si ou seu filho têm uma alteração da pele com comichão chamada “dermatite atópica”, pode ser suficiente uma aplicação mais breve. Tempos de aplicação de mais de 30 minutos podem aumentar a incidência de reações locais na pele (ver também a secção 4. “Posíveis efeitos adversos”).
- se está em tratamento com medicamentos para os distúrbios do ritmo cardíaco (antiarrítmicos de classe III, como a amiodarona). Nesse caso, o médico vigiará a sua função cardíaca.
Devido à absorção potencialmente maior sobre a pele recém-raspada, é importante respeitar a dose, a superfície da pele e o tempo de aplicação recomendados.
Evite o contato de EMLA com os olhos, porque pode causar irritação e queimaduras químicas nos olhos. Se acidentalmente penetrar no seu olho, deve lavá-lo imediatamente com água morna ou soro salino (solução de cloreto de sódio). Tenha cuidado de não aplicar nada no olho até que volte a ter sensibilidade.
As crianças devem ser vigiadas cuidadosamente quando se utilizar EMLA em qualquer parte do corpo para evitar que EMLA possa entrar em contato com os olhos.
Não se deve aplicar EMLA sobre o tímpano danificado.
Quando utilizar EMLA antes de ser vacinado com vacinas vivas (p. ex., vacina da tuberculose), volte a visitar o seu médico ou enfermeiro após o período requerido para o seguimento do resultado da vacinação.
Crianças e adolescentes
Em lactentes e recém-nascidos com menos de 3 meses, é frequente observar “metahemoglobinemia”, um aumento transitório e sem importância clínica dos níveis de um pigmento no sangue, até 12 horas após a aplicação de EMLA.
Os estudos clínicos não puderam confirmar a eficácia de EMLA quando se extrai sangue do calcanhar dos recém-nascidos ou para proporcionar a analgesia adequada na circuncisão.
EMLA não deve ser aplicado na mucosa genital (p. ex., na vagina) de crianças (menores de 12 anos) porque não há dados suficientes sobre a absorção dos princípios ativos.
EMLA não deve ser utilizado em crianças menores de 12 meses de idade que estejam recebendo simultaneamente tratamento com outros medicamentos que afetam as concentrações do pigmento sanguíneo “metahemoglobina” (p. ex., sulfonamidas, ver também a secção 2. “Uso de EMLA com outros medicamentos”).
EMLA não deve ser utilizado em recém-nascidos prematuros.
Uso de EMLA com outros medicamentos
Comunique ao seu médico ou farmacêutico se está utilizando ou tomando, tem utilizado ou tomado recentemente ou pode ter que utilizar ou tomar qualquer outro medicamento, incluindo os adquiridos sem receita e os medicamentos à base de plantas. Isso porque EMLA pode afetar o modo de ação de outros medicamentos e outros medicamentos podem ter um efeito sobre EMLA.
Em particular, informe o seu médico ou farmacêutico se si ou seu filho utilizaram recentemente ou receberam tratamento com algum dos seguintes medicamentos:
- Medicamentos utilizados para tratar infecções chamados “sulfonamidas” e nitrofurantoína.
- Medicamentos utilizados para tratar a epilepsia, chamados fenitoína e fenobarbital.
- Outros anestésicos locais.
- Medicamentos para tratar arritmias cardíacas, como a amiodarona.
- Cimetidina ou betabloqueantes, que podem aumentar os níveis de lidocaína no sangue. Esta interação não tem importância clínica no tratamento a curto prazo com EMLA às doses recomendadas.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
O uso ocasional de EMLA durante a gravidez é improvável que tenha algum efeito adverso no feto.
Os princípios ativos de EMLA (lidocaína e prilocaína) são excretados no leite materno. No entanto, a quantidade é tão pequena que geralmente não supõe qualquer risco para a criança.
Estudos em animais mostraram que não existem alterações na fertilidade masculina ou feminina.
Condução e uso de máquinas
EMLA não afeta a capacidade de conduzir e usar máquinas, ou o efeito é insignificante, quando é utilizado às doses recomendadas.
EMLA contém hidroxiestearato de macroglicerol
Este medicamento pode causar reações na pele porque contém hidroxiestearato de macroglicerol.
3. Como usar EMLA
Siga exatamente as instruções de administração deste medicamento, indicadas pelo seu médico, farmacêutico ou enfermeiro. Em caso de dúvida, consulte novamente o seu médico, farmacêutico ou enfermeiro.
Uso de EMLA
- O local de aplicação do creme, a quantidade que deve utilizar e o tempo que deve permanecer aplicado dependem de para que é utilizado.
- Seu médico, farmacêutico ou enfermeiro aplicarão o creme ou lhe ensinarão como fazê-lo si mesmo.
- Quando se utiliza EMLA nos genitais, um médico ou enfermeiro devem supervisionar o seu uso.
Não utilize EMLA nas seguintes zonas:
- Cortes, abrasões ou feridas, exceto úlceras nas pernas.
- Zonas em que exista erupção cutânea ou eczema.
- Nos olhos ou nas proximidades.
- Dentro do nariz, orelha ou boca.
- No ânus.
- Nos genitais das crianças.
As pessoas que frequentemente apliquem ou retirem o creme devem ter cuidado para evitar o contato e prevenir a aparência de hipersensibilidade.
A membrana protetora do tubo é perfurada pressionando a tampa sobre ela.
Uso sobre a pele antes de pequenas intervenções (como punção com agulha ou intervenções cutâneas menores):
- Aplique uma camada grossa de creme sobre a pele. Seu médico, farmacêutico ou enfermeiro lhe indicarão onde aplicá-lo.
- Cubra depois o creme com um penso [plástico transparente]. Este é removido justo antes de começar a intervenção. Se aplicar o creme si mesmo, certifique-se de que seu médico, farmacêutico ou enfermeiro lhe forneçam os penso.
- A dose habitual para adultos e adolescentes de mais de 12 anos é de 2 g (gramas).
- Em adultos e adolescentes de mais de 12 anos, aplique o creme pelo menos 60 minutos antes da intervenção (a menos que o creme vá ser utilizado sobre os genitais). No entanto, não o aplique mais de 5 horas antes.
- Nas crianças, a quantidade de EMLA utilizada e o tempo de utilização dependem da idade. Seu médico, enfermeiro ou farmacêutico lhe indicarão a quantidade que deve utilizar e quando deve aplicá-la.
Quando aplicar o creme si mesmo, é muito importante seguir as seguintes instruções:
- Aperte o tubo para aplicar em um montículo a quantidade necessária de creme sobre a pele onde se vai realizar a intervenção (p. ex., onde se vai inserir a agulha). Uma linha de creme de uns 3,5 cm do tubo de 30 g equivale a 1 g de creme. Não estenda o creme.
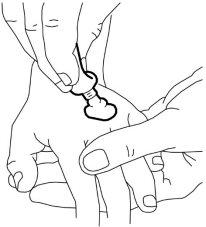
- Despegue a camada de papel do «corte central» do lado não adesivo do penso (deixando um quadro de papel).
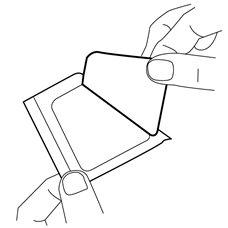
- Retire a cobertura do lado adesivo do penso.
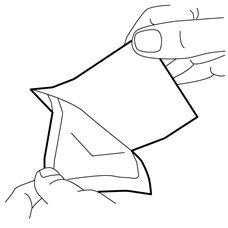
- Coloque o penso cuidadosamente sobre o creme depositado. Não estenda o creme debaixo do penso.
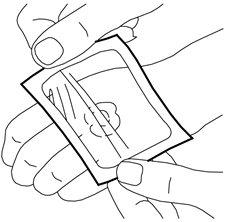
- Retire o suporte de papel. Alise os bordos do penso cuidadosamente. Em seguida, deixe-o colocado durante pelo menos 60 minutos se a pele não estiver danificada. O creme não deve ser deixado colocado durante mais de 60 minutos em crianças menores de 3 meses ou durante mais de 30 minutos em crianças com uma afecção de comichão na pele chamada «dermatite atópica». Se o creme for usado nos genitais ou sobre úlceras, podem ser usados tempos de aplicação mais curtos como descrito a seguir.
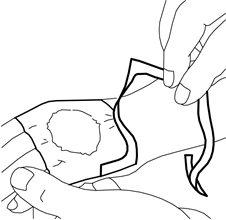
- Seu médico ou enfermeiro removerão o penso e retirarão o creme justo antes de realizar o procedimento médico (por exemplo, justo antes de colocar a agulha).
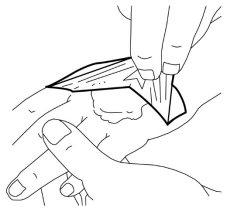
Utilização sobre superfícies extensas de pele recém-raspada antes de intervenções em regime ambulatorial (como técnicas de depilação):
A dose habitual é de 1 g de creme por cada superfície cutânea de 10 cm² (10 centímetros quadrados) de tamanho, aplicada entre 1 e 5 horas sob um penso. EMLA não deve ser utilizado sobre uma superfície de pele recém-raspada maior de 600 cm² (600 centímetros quadrados, p. ex. 30 cm por 20 cm) de tamanho. A dose máxima é de 60 g.
Utilização sobre a pele antes de intervenções hospitalares (como enxertos de pele) que precisam de anestesia cutânea mais profunda:
- EMLA pode ser utilizado desta maneira em adultos e adolescentes de mais de 12 anos.
- A dose habitual é de 1,5 g a 2 g de creme em cada zona de pele de 10 cm² (10 centímetros quadrados) de tamanho.
- O creme é aplicado sob um penso oclusivo durante 2 a 5 horas.
Uso sobre a pele para eliminar lesões verrugosas chamadas “molusco”
- EMLA pode ser utilizado em crianças e adolescentes que sofrem de uma afecção cutânea chamada “dermatite atópica”.
- A dose habitual depende da idade da criança e é utilizada durante 30 a 60 minutos (30 minutos se o paciente tiver dermatite atópica). Seu médico, enfermeiro ou farmacêutico lhe indicarão quanto creme tem que aplicar.
Uso sobre a pele dos genitais antes de colocar injeções de anestesia local
- EMLA pode ser utilizado desta maneira apenas em adultos e adolescentes de mais de 12 anos.
- A dose habitual é de 1 g de creme (1 g a 2 g na pele dos genitais femininos) em cada zona de pele de 10 cm² (10 centímetros quadrados) de tamanho.
- O creme é aplicado sob um penso oclusivo. Este é mantido durante 15 minutos na pele dos genitais masculinos e durante 60 minutos na pele dos genitais femininos.
Uso nos genitais antes de cirurgia cutânea menor (eliminação de verrugas)
- EMLA pode ser utilizado desta maneira apenas em adultos e adolescentes de mais de 12 anos.
- A dose habitual é de 5 g a 10 g de creme durante 10 minutos. Não se utiliza penso oclusivo. O procedimento médico deve ser iniciado imediatamente.
Uso sobre úlceras nas pernas antes de limpar ou eliminar a pele danificada
- A dose habitual é de 1 g a 2 g em cada zona de pele de 10 cm², até 10 g como máximo.
- O creme é aplicado sob um penso oclusivo, p. ex., um plástico transparente. Este é mantido de 30 a 60 minutos antes de limpar a úlcera. Elimine o creme com uma gaze de algodão e comece a limpeza sem demora.
- Pode-se utilizar EMLA antes da limpeza das úlceras nas pernas até 15 vezes em um período de 1-2 meses.
- O tubo de EMLA é para um único uso quando é utilizado sobre úlceras nas pernas: O tubo com qualquer conteúdo restante deve ser descartado cada vez após tratar um paciente.
Se usar mais EMLA do que deve
Se utilizar mais EMLA do que o que lhe foi indicado pelo seu médico, farmacêutico ou enfermeiro, entre em contato imediatamente com um deles, mesmo que não apresente sintomas.
A seguir, são enumerados os sintomas se usar demasiado EMLA. É improvável que apareçam estes sintomas se seguir as recomendações de uso de EMLA.
- Sensação de tontura ou tontura.
- Formigamento na pele do contorno da boca e adormecimento da língua.
- Alteração do gosto.
- Visão borrosa.
- Zumbidos nos ouvidos.
- Existe também risco de “metahemoglobinemia aguda” (um problema nos níveis de um pigmento do sangue). Este risco é maior quando se tomam determinados medicamentos ao mesmo tempo. Se isso acontecer, a pele toma uma coloração azul-acinzentada devido à falta de oxigênio.
Em casos graves de sobredose, os sintomas podem consistir em convulsões, pressão arterial baixa, respiração lenta, parada da respiração e alteração do ritmo cardíaco. Estes efeitos podem ser potencialmente mortais.
Em caso de sobredose ou ingestão acidental, consulte o Serviço de Informação Toxicológica. Telefone 91 562 04 20.
Se tiver alguma dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode provocar efeitos adversos, embora nem todas as pessoas os sofram.
Entre em contacto com o seu médico ou farmacêutico se algum dos seguintes efeitos adversos o incomodar ou não parecer desaparecer. Informe o seu médico de qualquer outra coisa que o faça sentir mal enquanto utilizar EMLA.
Pode aparecer uma ligeira reação (paletez ou rubor da pele, ligeira inchação, ardor ou picada inicial) na zona sobre a qual se aplica EMLA. Trata-se de reações normais à crema e aos anestésicos e desaparecerá em pouco tempo sem necessidade de tomar qualquer medida.
Se experimentar algum efeito desagradável ou incomum enquanto utiliza EMLA, deixe de utilizá-lo e consulte o seu médico ou farmacêutico o mais breve possível.
Frequentes(podem afetar até 1 em cada 10 pessoas)
- Reações na pele locais transitórias (paletez, rubor, inchação) na zona de aplicação durante o tratamento na pele, na mucosa genital ou nas úlceras nas pernas.
- Uma ligeira sensação inicial de ardor, picada ou calor na zona de aplicação durante o tratamento na mucosa genital ou nas úlceras nas pernas.
Pouco frequentes(podem afetar até 1 em cada 100 pessoas)
- Uma ligeira sensação inicial de ardor, picada ou calor na zona tratada durante o tratamento na pele.
- Adormecimento (formigueiro) na zona de aplicação durante o tratamento na mucosa genital.
- Irritação da pele na zona de aplicação durante o tratamento das úlceras nas pernas.
Raros(podem afetar até 1 em cada 1.000 pessoas)
- Reações alérgicas que, em casos raros, podem chegar a ser um choque anafiláctico (erupção cutânea, inchação, febre, dificuldade respiratória e desmaio) durante o tratamento na pele, na mucosa genital ou nas úlceras nas pernas.
- Metahemoglobinemia (distúrbio do sangue) durante o tratamento da pele.
- Pequena hemorragia ponteada na área tratada (particularmente nas crianças com eczema após longos períodos de aplicação), durante o tratamento na pele.
- Irritação dos olhos se EMLA entrar acidentalmente em contacto com os olhos durante o tratamento na pele.
Frequência desconhecida(não pode ser estimada a partir dos dados disponíveis)
- Queimaduras químicas nos olhos se EMLA entrar acidentalmente em contacto com eles durante o tratamento.
Outros efeitos adversos em crianças
Metahemoglobinemia, um distúrbio do sangue que se costuma observar com maior frequência em recém-nascidos e lactentes de 0 a 12 meses, muitas vezes associado a sobredosagem.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es/. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de EMLA
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no estojo e no tubo após “CAD”. A data de validade é o último dia do mês que se indica.
Não congelar.
Conservar o tubo bem fechado.
Os medicamentos não devem ser jogados pelos deságues nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de EMLA
- Os princípios ativos são: lidocaína e prilocaína.
- 1 g de crema contém 25 mg de lidocaína e 25 mg de prilocaína.
- Os demais componentes são carbômeros, hidroxiestearato de macroglicerol, hidróxido de sódio e água purificada.
Aspecto de EMLA e conteúdo do envase
Crema homogênea de cor branca.
Apresenta-se em um tubo de alumínio com tampa de polipropileno provido de um dispositivo de perfuração.
EMLA está disponível em envases de:
1 tubo que contém 5 g de crema.
1 tubo que contém 5 g de crema + 2 aparelhos.
1 tubo que contém 5 g de crema + 3 aparelhos.
3 tubos que contêm 5 g de crema + 8 aparelhos.
5 tubos que contêm 5 g de crema.
5 tubos que contêm 5 g de crema + 10 aparelhos.
5 tubos que contêm 5 g de crema + 12 aparelhos.
1 tubo que contém 30 g de crema.
Pode ser que apenas alguns tamanhos de envase estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização:
Aspen Pharma Trading Limited.
3016 Lake Drive,
Citywest Business Campus,
Dublín 24, Irlanda.
Tel: +34 952 010 137.
Responsável pela fabricação:
Recipharm Karlskoga AB.
Björkbornsvägen 5.
S-69133 – Karlskoga.
Suécia.
Ou.
Aspen Bad Oldesloe GmbH.
32-36 Industriestrasse.
23843 Bad Oldesloe.
Alemanha.
Representante local:
Aspen Pharmacare España S.L.
Avenida Diagonal, 512.
Planta Interior 1, Oficina 4.
Barcelona, 08006, Espanha.
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Áustria. | Emla 5% - Creme. |
Bélgica. | Emla 25mg/25mg creme. |
Chipre. | Emla Cream 5%. |
Finlândia. | EMLA. |
França. | EMLA 5 POUR CENT, crème. |
Grécia. | EMLA. |
Islândia. | Emla. |
Irlanda. | EMLA 5% w/w Cream. |
Itália. | EMLA. |
Luxemburgo. | Emla 25mg/25mg creme. |
Malta. | EMLA 5% w/w Cream. |
Noruega. | Emla. |
Polônia. | EMLA. |
Espanha. | EMLA 25 mg/g + 25 mg/g crema. |
Suécia. | EMLA. |
Países Baixos. | Emla. |
Data da última revisão deste prospecto:Julho 2024.
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/.

Quanto custa o EMLA 25 mg/g + 25 mg/g CREME em Espanha em 2025?
O preço médio do EMLA 25 mg/g + 25 mg/g CREME em dezembro de 2025 é de cerca de 10.02 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia10.02 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a EMLA 25 mg/g + 25 mg/g CREMEForma farmacêutica: CREME, 25 mg/g + 25 mg/gSubstância ativa: combinationsFabricante: Glenmark Arzneimittel GmbhRequer receita médicaForma farmacêutica: CREME, 25 mg/g + 25 mg/gSubstância ativa: combinationsFabricante: Galenicum Derma S.L.U.Requer receita médicaForma farmacêutica: CREME, Lidocaína 25 mg/g + Prilocaína 25 mg/gSubstância ativa: combinationsFabricante: Mesoestetic Pharma Group S.L.Requer receita médica
Alternativas a EMLA 25 mg/g + 25 mg/g CREME noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a EMLA 25 mg/g + 25 mg/g CREME em Poland
Alternativa a EMLA 25 mg/g + 25 mg/g CREME em Ukraine
Médicos online para EMLA 25 mg/g + 25 mg/g CREME
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de EMLA 25 mg/g + 25 mg/g CREME – sujeita a avaliação médica e regras locais.














