BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL
Pergunte a um médico sobre a prescrição de BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL

Como usar BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o paciente adulto
Byooviz 10 mg/ml solução injetável
ranibizumab
Este medicamento está sujeito a acompanhamento adicional, o que agilizará a detecção de nova informação sobre a sua segurança. Pode contribuir comunicando os efeitos adversos que possa ter. A parte final da seção 4 inclui informação sobre como comunicar estes efeitos adversos.
ADULTOS
Leia todo o prospecto atentamente antes de que lhe administrem este medicamento, porque contém informação importante para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico.
- Se experimentar efeitos adversos, consulte o seu médico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Byooviz e para que é utilizado
- O que precisa saber antes de que lhe administrem Byooviz
- Como se administra Byooviz
- Efeitos adversos possíveis
- Conservação de Byooviz
- Conteúdo do envase e informação adicional
1. O que é Byooviz e para que é utilizado
O que é Byooviz
Byooviz é uma solução que se injeta no olho. Byooviz pertence a um grupo de medicamentos denominados agentes anti-angiogénese. Contém o princípio ativo denominado ranibizumab.
Para que é utilizado Byooviz
Byooviz é utilizado em adultos para tratar várias doenças oculares que causam alteração da visão.
Estas doenças são o resultado de uma lesão na retina (camada sensível à luz na parte posterior do olho) provocada por:
- O crescimento de vasos sanguíneos anormais, que perdem líquido. Isto é observado em doenças como a degeneração macular associada à idade (DMAI) e a retinopatia diabética proliferativa (RDP, uma doença provocada pela diabetes). Também pode estar associado à neovascularização coroide (NVC) devida à miopia patológica (MP), estrías angioides, coriorretinopatia serosa central ou NVC inflamatória.
- Edema macular (inchação do centro da retina). A causa desta inchação pode ser a diabetes (uma doença conhecida como edema macular diabético [EMD]) ou um bloqueio das veias retinianas da retina (uma doença conhecida como oclusão da veia da retina [OVR]).
Como actua Byooviz
Byooviz reconhece e une-se de forma específica a uma proteína denominada factor de crescimento endotelial vascular A (VEGF-A) humano presente nos olhos. Em excesso, o VEGF-A causa o crescimento de vasos sanguíneos anormais e inchação no olho que pode ocasionar uma alteração da visão em doenças como DMAI, EMD, RDP, OVR, MP e NVC. Mediante a união ao VEGF-A, Byooviz pode impedir que actue e prevenir dito crescimento e inchação anormais.
Nestas doenças, Byooviz pode ajudar a estabilizar e, em muitos casos, melhorar a sua visão.
2. O que precisa saber antes de que lhe administrem Byooviz
Não lhe devem administrar Byooviz
- Se é alérgico ao ranibizumab ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
- Se tem uma infecção no olho ou à volta do mesmo.
- Se tem dor ou vermelhidão (inflamação intraocular grave) no olho.
Advertências e precauções
Consulte o seu médico antes de que lhe administrem Byooviz.
- Byooviz é administrado mediante uma injeção no olho. Ocasionalmente, após o tratamento com Byooviz pode aparecer uma infecção na parte interna do olho, dor ou vermelhidão (inflamação), desprendimento ou desgarro de uma das camadas situadas na parte posterior do olho (desprendimento ou desgarro da retina e desprendimento ou desgarro do epitélio pigmentar da retina), ou enturbiação do cristalino (catarata). É importante identificar e tratar tal infecção ou desprendimento de retina o mais cedo possível. Informe imediatamente o seu médico se nota sinais como dor no olho ou aumento das molestias no olho, se piora a vermelhidão no olho, visão borrosa ou diminuição da visão, um aumento do número de pequenas manchas na visão ou aumento da sensibilidade à luz.
- Em alguns pacientes, logo após a injeção a pressão no olho pode aumentar durante um curto período de tempo. É possível que não se aperceba disso, por isso pode que o seu médico lhe faça um acompanhamento da pressão ocular após cada injeção.
- Informe o seu médico se teve doenças nos olhos ou recebeu algum tratamento nos olhos anteriormente, ou se sofreu um acidente vascular cerebral ou teve sinais passageiros de acidente vascular cerebral (debilidade ou paralisia de uma extremidade ou face, dificuldade na fala ou na compreensão). Esta informação será tida em consideração para avaliar se Byooviz é o tratamento apropriado para si.
Para consultar informação mais detalhada sobre os efeitos adversos que poderiam ocorrer durante o tratamento com Byooviz, ver seção 4 (“Efeitos adversos possíveis”).
Crianças e adolescentes (menores de 18 anos)
Não foi estabelecido o uso de Byooviz em crianças e adolescentes e, por conseguinte, não é recomendado.
Outros medicamentos e Byooviz
Informe o seu médico se está utilizando, utilizou recentemente ou pudesse ter que utilizar qualquer outro medicamento.
Gravidez e amamentação
- As mulheres que pudessem ficar grávidas devem utilizar um método anticonceptivo eficaz durante o tratamento e durante pelo menos os três meses posteriores à última injeção de Byooviz.
- Não há experiência no uso de Byooviz em mulheres grávidas. Byooviz não deve ser utilizado durante a gravidez salvo que o benefício potencial supere o risco potencial para o feto. Se está grávida, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico antes do tratamento com Byooviz.
- Pequenas quantidades de ranibizumab podem passar para o leite materno, por isso não se recomenda o uso de Byooviz durante a amamentação. Consulte o seu médico ou farmacêutico antes do tratamento com Byooviz.
Condução e uso de máquinas
Após o tratamento com Byooviz pode experimentar visão borrosa temporariamente. Se isso lhe acontecer, não conduza nem use máquinas até que este sintoma desapareça.
3. Como se administra Byooviz
Byooviz é administrado pelo oftalmologista em forma de injeção única no olho sob anestesia local. A dose habitual de uma injeção é 0,05 ml (que contém 0,5 mg de princípio ativo). O intervalo entre duas doses aplicadas no mesmo olho deve ser como mínimo de quatro semanas. Todas as injeções serão administradas por um oftalmologista.
Para prevenir uma infecção, antes da injeção o seu médico lavará o olho cuidadosamente. O seu médico também lhe administrará um anestésico local para reduzir ou prevenir qualquer dor que possa sentir com a injeção.
O tratamento começa com uma injeção de Byooviz cada mês. O seu médico controlará a doença do seu olho e dependendo de como responde ao tratamento, decidirá se precisa ou não receber mais tratamento e quando precisa ser tratado.
No final do prospecto, na parte “Como preparar e administrar Byooviz”, são dadas instruções detalhadas de uso.
Pacientes de idade avançada (65 anos e mais)
Byooviz pode ser utilizado em pessoas de 65 anos de idade ou mais, e não é necessário um ajuste da dose.
Antes de interromper o tratamento com Byooviz
Se está a considerar interromper o tratamento com Byooviz, acuda à próxima consulta e comente antes com o seu médico. O seu médico aconselhará e decidirá durante quanto tempo deve ser tratado com Byooviz.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico.
4. Efeitos adversos possíveis
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os efeitos adversos associados à administração de Byooviz devem-se ou ao próprio medicamento ou ao procedimento de injeção e a maioria afeta o olho.
A seguir são descritos os efeitos adversos mais graves:
Efeitos adversos graves frequentes(podem afetar até 1 de cada 10 pacientes): desprendimento ou desgarro da camada na parte posterior do olho (desprendimento ou desgarro da retina), que dá como resultado destellos de luz com partículas flutuantes que progridem para uma perda de visão transitória ou para um enturbiação do cristalino (catarata).
Efeitos adversos graves pouco frequentes(podem afetar até 1 de cada 100 pacientes): cegueira, infecção do globo ocular (endoftalmite) com inflamação da parte interna do olho.
Os sintomas que poderia experimentar são dor ou aumento das molestias no olho, piora da vermelhidão no olho, visão borrosa ou diminuição da visão, um aumento do número de pequenas manchas na visão ou aumento da sensibilidade à luz. Informe o seu médico imediatamente se apresentar algum destes efeitos adversos.
A seguir são descritos os efeitos adversos comunicados mais frequentemente:
Efeitos adversos muito frequentes(podem afetar mais de 1 de cada 10 pacientes)
Os efeitos adversos oculares incluem: inflamação do olho, sangramento na parte posterior do olho (hemorragia na retina), alterações visuais, dor no olho, pequenas partículas ou manchas na visão (partículas flutuantes), sangue no olho, irritação do olho, sensação de ter algo dentro do olho, aumento da produção de lágrima, inflamação ou infecção no bordo das pálpebras, olho seco, vermelhidão ou picor no olho e aumento da pressão no olho.
Os efeitos adversos não oculares incluem: dor de garganta, congestão nasal, gotejamento nasal, dor de cabeça e dor nas articulações.
A seguir são descritos outros efeitos adversos que podem ocorrer após o tratamento com Byooviz:
Efeitos adversos frequentes
Os efeitos adversos oculares incluem: diminuição da nitidez da visão, inchação de uma seção do olho (úvea, córnea), inflamação da córnea (parte frontal do olho), pequenas marcas na superfície do olho, visão borrosa, sangramento no local de injeção, sangramento no olho, secreção do olho com picor, vermelhidão e inchação (conjuntivite), sensibilidade à luz, molestias no olho, inchação da pálpebra, dor na pálpebra.
Os efeitos adversos não oculares incluem: infecção das vias urinárias, contagem de glóbulos vermelhos baixa (com sintomas tais como cansaço, dificuldade ao respirar, tontura, palidez), ansiedade, tosse, náuseas, reações alérgicas tais como erupção, urticária, picor e vermelhidão da pele.
Efeitos adversos pouco frequentes
Os efeitos adversos oculares incluem: inflamação e sangramento na parte anterior do olho, acúmulo de pus no olho, alterações na parte central da superfície ocular, dor ou irritação no local de injeção, sensação anormal no olho, irritação da pálpebra.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informação sobre a segurança deste medicamento.
5. Conservação de Byooviz
- Mantenha este medicamento fora da vista e do alcance das crianças.
- Não utilize este medicamento após a data de validade que aparece na caixa após CAD e na etiqueta do frasco após EXP. A data de validade é o último dia do mês que se indica.
- Conservar em frigorífico (entre 2 ºC e 8 ºC). Não congelar.
- Antes de usar, o frasco sem abrir pode ser conservado a temperaturas que não excedam os 30 ºC durante um máximo de 2 meses.
- Conservar o frasco no embalagem exterior para protegê-lo da luz.
- Não utilize nenhum envase que esteja danificado.
6. Conteúdo do frasco e informação adicional
Composição de Byooviz
- O princípio ativo é ranibizumab. Cada ml contém 10 mg de ranibizumab. Cada frasco contém 2,3 mg de ranibizumab em 0,23 ml de solução. Isso fornece uma quantidade adequada para fornecer uma dose única de 0,05 ml, que contém 0,5 mg de ranibizumab.
- Os outros componentes são a,a-trealose diidratada; cloridrato de histidina monoidratado; histidina; polissorbato 20; água para preparações injetáveis.
Aspecto do produto e conteúdo do frasco
Byooviz é uma solução injetável contida em um frasco (0,23 ml). A solução é transparente, incolor ou amarelo pálido e aquosa.
Existem dois tipos de embalagens diferentes:
Embalagem apenas com frasco
Embalagem que contém um frasco de vidro com ranibizumab, com uma tampa de borracha de clorobutilo. O frasco é para uso único.
Embalagem com um frasco + agulha com filtro + agulha para injeção
Embalagem que contém um frasco de vidro com ranibizumab, com uma tampa de borracha de clorobutilo, uma agulha romba com filtro (18G x 1½″, 1,2 mm x 40 mm, 5 micrómetros) para extrair o conteúdo do frasco e uma agulha para injeção (30G x ½″, 0,3 mm x 13 mm). Todos os componentes são para uso único.
Pode ser que apenas alguns tipos de embalagens sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
Samsung Bioepis NL B.V.
Olof Palmestraat 10
2616 LR Delft
Países Baixos
Data da última revisão deste prospecto: Julho 2025
Outras fontes de informação
A informação detalhada deste medicamento está disponível no site da Agência Europeia de Medicamentos: http://www.ema.europa.eu
ESTA INFORMAÇÃO É DESTINADA APENAS A PROFISSIONAIS DO SETOR DE SAÚDE:
Ver também a seção 3 “Como administrar Byooviz”.
Como preparar e administrar Byooviz em adultos
Frasco para uso único. Apenas para via intravítrea.
Byooviz deve ser administrado por um oftalmologista que tenha experiência na administração de injeções intravítreas.
Na DMAE exsudativa, na NVC, na RDP e na alteração visual devido à EMD ou ao edema macular secundário à OVR, a dose recomendada de Byooviz é 0,5 mg administrada em forma de injeção intravítrea única. Isso corresponde a um volume de injeção de 0,05 ml. O intervalo entre duas doses injetadas no mesmo olho deve ser de pelo menos quatro semanas.
O tratamento é iniciado com uma injeção por mês até atingir a acuidade visual máxima e/ou não haja sinais de atividade da doença, ou seja, nenhum cambio na acuidade visual nem em outros sinais e sintomas da doença sob tratamento contínuo. Em pacientes com DMAE exsudativa, EMD, RDP e OVR, inicialmente podem ser necessárias três ou mais injeções consecutivas administradas mensalmente.
A partir desse momento, os intervalos de monitorização e tratamento devem ser determinados de acordo com o critério médico e com base na atividade da doença, avaliada mediante a acuidade visual e/ou parâmetros anatômicos.
Deve-se interromper o tratamento com Byooviz se, sob o critério do médico, os parâmetros visuais e anatômicos indicam que o paciente não está se beneficiando do tratamento contínuo.
A monitorização para determinar a atividade da doença pode incluir exame clínico, controle funcional ou técnicas de imagem (p. ex., tomografia de coerência óptica ou angiografia com fluoresceína).
Se os pacientes estiverem sendo tratados de acordo com um regime de tratar e estender, uma vez que a acuidade visual máxima tenha sido atingida e/ou não haja sinais de atividade da doença, os intervalos de tratamento podem ser espaçados gradualmente até que os sinais de atividade da doença ou alteração visual voltem a aparecer. No caso da DMAE exsudativa, o intervalo de tratamento não deve ser espaçado em mais de duas semanas cada vez, e no caso do EMD, pode ser espaçado até um mês cada vez. Para a RDP e a OVR, os intervalos de tratamento também podem ser espaçados gradualmente; no entanto, os dados disponíveis não são suficientes para determinar a duração desses intervalos. Se a atividade da doença voltar a aparecer, o intervalo de tratamento deve ser encurtado de forma consecutiva.
O tratamento da alteração visual devido à NVC deve ser determinado para cada paciente de forma individualizada com base na atividade da doença. Alguns pacientes podem necessitar apenas de uma injeção durante os primeiros 12 meses; outros podem necessitar de tratamento com maior frequência, incluindo uma injeção mensal. No caso da NVC secundária à miopia patológica (MP), muitos pacientes podem necessitar apenas de uma ou duas injeções durante o primeiro ano.
Ranibizumab e fotocoagulação com laser em EMD e edema macular secundário à oclusão da ramo venosa retiniana (ORVR)
Existe alguma experiência com ranibizumab administrado concomitantemente com fotocoagulação com laser. Quando administrados no mesmo dia, ranibizumab deve ser administrado como mínimo 30 minutos após a fotocoagulação com laser. Ranibizumab pode ser administrado em pacientes que receberam fotocoagulação com laser previamente.
Ranibizumab e terapia fotodinâmica com verteporfina na NVC secundária à MP
Não há experiência na administração concomitante de ranibizumab e verteporfina.
Antes da administração de Byooviz, deve-se verificar visualmente a ausência de partículas e decoloração.
O procedimento de injeção deve ser realizado sob condições assépticas, que incluem o lavado quirúrgico das mãos, o uso de luvas estéreis, um campo estéril, um blefarostato estéril para as pálpebras (ou equivalente) e a disponibilidade de uma paracentese estéril (se necessário). Antes de realizar o procedimento de injeção intravítrea, deve-se avaliar detalhadamente a história clínica do paciente em relação a reações de hipersensibilidade. Antes da injeção, deve-se administrar uma anestesia adequada e um microbicida tópico de amplo espectro para desinfetar a pele da zona periocular, pálpebra e superfície ocular, de acordo com a prática local.
Embalagem apenas com frasco
O frasco é para uso único. Após a injeção, deve-se descartar qualquer sobra de produto não utilizado. Não deve ser utilizado nenhum frasco que mostre sinais de deterioração ou manipulação. A esterilidade só pode ser garantida se o selo da embalagem for mantido intacto.
Para a preparação e a injeção intravítrea, são necessários os seguintes produtos sanitários (para uso único):
- uma agulha com filtro de 5 µm (18G)
- uma agulha para injeção (30G x ½″)
- uma seringa estéril de 1 ml (que inclua uma marca em 0,05 ml)
Esses produtos sanitários não estão incluídos na embalagem de Byooviz.
Embalagem com frasco + agulha com filtro + agulha para injeção
Todos os componentes são estéreis e para uso único. Não deve ser utilizado nenhum componente cuja embalagem mostre sinais de deterioração ou manipulação. A esterilidade só pode ser garantida se o selo da embalagem dos componentes for mantido intacto. A reutilização pode dar origem a uma infecção ou outra doença/lesão.
Para a preparação e a injeção intravítrea, são necessários os seguintes produtos sanitários (para uso único):
- uma agulha com filtro de 5 µm (18G x 1½″, 1,2 mm x 40 mm, fornecida)
- uma agulha para injeção (30G x ½″, 0,3 mm x 13 mm, fornecida)
- uma seringa estéril de 1 ml (que inclua uma marca em 0,05 ml, não incluída na embalagem de Byooviz)
Para a preparação de Byooviz para administração intravítrea em pacientes adultos, siga as seguintes instruções:
|
|
|
|
|
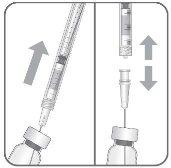
Nota: Segurar a agulha para injeção pelo cone enquanto se retira a cápsula de fechamento.
Nota: Não secar a agulha para injeção. Não puxar o êmbolo para trás. |
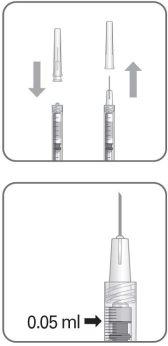
A agulha para injeção deve ser introduzida 3,5-4,0 mm por trás do limbo na cavidade vítrea, evitando o meridiano horizontal e em direção ao centro do globo. Em seguida, deve-se liberar o volume de injeção de 0,05 ml; as injeções subsequentes devem ser aplicadas cada vez em um ponto escleral distinto.
Após a injeção, não tapar a agulha com a cápsula de fechamento nem separá-la da seringa. Eliminar a seringa usada junto com a agulha em um contenedor para objetos pontiagudos ou eliminar de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 10 mg/mLSubstância ativa: ranibizumabFabricante: Novartis Europharm LimitedRequer receita médicaForma farmacêutica: INJETÁVEL, 10 mg/mLSubstância ativa: ranibizumabFabricante: Novartis Europharm LimitedRequer receita médicaForma farmacêutica: INJETÁVEL, 10 mg/mlSubstância ativa: ranibizumabFabricante: Midas Pharma GmbhRequer receita médica
Alternativas a BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL em Ucrania
Médicos online para BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de BYOOVIZ 10 mg/ml SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.