BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA

Pergunte a um médico sobre a prescrição de BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA

Como usar BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA
Introdução
Prospecto: informação para o utilizador
Boostrix, Suspensão injetável em seringa pré-carregada
Vacina antidiftérica, antitetânica e antipertussis (componente acelular) (adsorvida, teor de antígeno reduzido)
Leia todo o prospecto atentamente antes de si ou seu filho receber esta vacina, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Se si ou seu filho experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Boostrix e para que é utilizado
- O que precisa saber antes de si ou seu filho receber Boostrix
- Como usar Boostrix
- Posíveis efeitos adversos
- Conservação de Boostrix
- Conteúdo do envase e informação adicional
1. O que é Boostrix e para que é utilizado
Boostrix é uma vacina indicada para a vacinação de reforço em crianças a partir de 4 anos, adolescentes e adultos para prevenir três doenças: difteria, tétano (rigidez de mandíbula) e tos ferina. A vacina atua ajudando o organismo a produzir sua própria proteção (anticorpos) contra essas doenças.
- Difteria:a difteria afeta principalmente as vias respiratórias e algumas vezes a pele. Geralmente, as vias respiratórias inflamam-se (incham-se) causando dificuldades respiratórias graves e algumas vezes asfixia. A bactéria também libera uma toxina (veneno), que pode causar lesões neurológicas, problemas cardíacos e até a morte.
- Tétano (rigidez de mandíbula):a bactéria do tétano penetra no organismo através de cortes, arranhões ou feridas na pele. As feridas especialmente propensas à infecção são as queimaduras, fraturas, feridas profundas ou feridas contaminadas com sujeira, pó, excrementos de cavalo/estercos ou lascas de madeira. A bactéria libera uma toxina (veneno) que pode causar rigidez muscular, espasmos musculares dolorosos, convulsões, e até a morte. Os espasmos musculares podem ser tão fortes que causem fraturas da espinha dorsal.
- Tos ferina:a tos ferina é uma afecção altamente infecciosa. A doença afeta as vias respiratórias causando ataques de tos graves que podem interferir com a respiração normal. A tos é acompanhada frequentemente de um “uivo” daí o nome comum de tos ferina. A tos pode durar 1-2 meses ou mais tempo. Também pode provocar infecções de ouvido, bronquite que pode durar muito tempo, pneumonia, convulsões, dano cerebral e até a morte.
Nenhum dos componentes da vacina pode causar difteria, tétano ou tos ferina.
O uso de Boostrix durante a gravidez ajudará a proteger seu bebê da tos ferina nos primeiros meses de vida, antes de receber a imunização primária.
2. O que precisa saber antes de si ou seu filho receber Boostrix
Não se deve administrar Boostrix:
- se si ou seu filho teve previamente qualquer reação alérgica a Boostrix ou a algum dos outros componentes desta vacina (incluídos na seção 6) ou ao formaldeído. Os sinais de uma reação alérgica podem incluir erupção cutânea com coceira, dificuldade ao respirar e inflamação da face ou língua.
- se si ou seu filho teve previamente uma reação alérgica a qualquer vacina contra difteria, tétano ou tos ferina.
- se si ou seu filho sofreu problemas no sistema nervoso (encefalopatia) nos 7 dias posteriores a uma vacinação anterior com uma vacina contra tos ferina.
- se si ou seu filho teve uma infecção grave com uma temperatura alta (superior a 38 ºC). Uma infecção menor não deve constituir um problema, mas consulte primeiro o seu médico.
- se si ou seu filho sofreu uma redução temporária de plaquetas no sangue (que aumenta o risco de sangramento ou de aparecimento de hematomas) ou problemas cerebrais ou neurológicos após uma vacinação previa com uma vacina contra difteria e/ou tétano.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de si ou seu filho receber Boostrix:
- se si ou seu filho apresentou algum problema após uma administração previa de Boostrix ou outra vacina antipertussis, especialmente:
- Febre (superior a 40 ºC) nas 48 horas seguintes à vacinação.
- Colapso ou estado semelhante ao “choque” nas 48 horas seguintes à vacinação.
- Choro inconsolável, persistente por mais de 3 horas de duração, produzido nas 48 horas seguintes à vacinação.
- Convulsões, com ou sem febre, produzidas nos 3 dias seguintes à vacinação.
- se seu filho sofre de uma doença cerebral não diagnosticada ou progressiva ou epilepsia não controlada. A vacina deve ser administrada uma vez controlada a doença
- se si ou seu filho tem problemas de hemorragias ou aparecem hematomas com facilidade
- se si ou seu filho tem tendência a convulsões/ataques devidos à febre ou se existe algum antecedente familiar disso
- se si ou seu filho tem problemas do sistema imunológico persistentes devido a qualquer causa (incluindo infecção por VIH). Si ou seu filho pode receber Boostrix, mas a proteção contra infecções após a vacinação não será tão boa quanto a de pacientes com respostas imunológicas adequadas contra infecções.
Antes ou depois de qualquer injeção, pode ocorrer um desmaio (especialmente em adolescentes), por isso deve informar o seu médico ou enfermeira se si ou seu filho desmaiou em ocasiões anteriores após a administração de uma injeção.
Como com todas as vacinas, Boostrix pode não proporcionar uma proteção completa em todos os pacientes vacinados.
Uso de Boostrix com outros medicamentos
Informe o seu médico ou farmacêutico se si ou seu filho está utilizando, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento ou se recebeu recentemente alguma outra vacina.
Boostrix pode ser administrado simultaneamente com outras vacinas. Deve ser usado um local de injeção diferente para cada tipo de vacina. Pode que Boostrix não proporcione uma resposta adequada se si ou seu filho tomar medicamentos que reduzem a eficácia do seu sistema imunológico contra infecções.
Gravidez e lactação
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de receber esta vacina.
Não se dispõe de dados sobre se Boostrix passa para o leite materno. O seu médico informará sobre os possíveis riscos e benefícios da administração de Boostrix durante a lactação.
Condução e uso de máquinas
É pouco provável que Boostrix tenha algum efeito sobre a capacidade de conduzir veículos e utilizar máquinas.
Boostrix contém sódio
Este medicamento contém menos de 23 mg de sódio (1 mmol) por unidade de dose; isto é, essencialmente “isento de sódio”.
3. Como usar Boostrix
- Boostrix será administrado como uma injeção no músculo.
- A vacina nunca deve ser administrada por via intravenosa.
- Si ou seu filho receberá uma única injeção de Boostrix.
- O seu médico verificará se si ou seu filho recebeu previamente vacinas antidiftéricas, antitetânicas e/ou antipertussis.
- Boostrix pode ser usado em caso de suspeita de infecção tetânica, embora também sejam tomadas outras medidas para reduzir o risco de manifestação da doença, como por exemplo curar a ferida e/ou aplicar toxina antitetânica.
- O seu médico recomendará repetir a vacinação.
4. Posíveis efeitos adversos
Como com todos os medicamentos, esta vacina pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Como com todas as vacinas injetáveis, podem aparecer reações alérgicas graves (reações anafiláticas e anafilactoides) em raríssimas ocasiões (até em um máximo de 1 de cada 10.000 doses da vacina). Estas podem ser reconhecidas por:
- Erupções cutâneas como coceira ou bolhas,
- Inchaço dos olhos e da face,
- Dificuldade para respirar ou engolir,
- Diminuição repentina da pressão arterial e perda de consciência.
Estas reações podem ocorrer antes de abandonar a consulta do médico. No entanto, se notar algum desses sintomas em si ou seu filho, deve contactar imediatamente um médico.
Efeitos adversos que ocorreram durante ensaios clínicos em crianças de 4 a 8 anos
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor, vermelhidão e inflamação no local de injeção, irritabilidade, sensação de sono, cansaço.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): perda de apetite, dor de cabeça, febre igual ou superior a 37,5 ºC (incluindo febre de mais de 39 ºC), inchaço extenso da extremidade na qual se aplicou a vacina, vômitos e diarreia.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): infecção do trato respiratório superior, distúrbios da atenção, secreção com coceira dos olhos e pálpebras com crosta (conjuntivite), erupção cutânea, endurecimento no local em que se administrou a injeção, dor.
Efeitos adversos que ocorreram durante ensaios clínicos em adultos, adolescentes e crianças a partir de 10 anos
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor, vermelhidão e inflamação no local de injeção, dor de cabeça, cansaço, mal-estar geral.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): febre igual ou superior a 37,5 ºC, tontura, náuseas, endurecimento e abscesso no local da injeção.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): febre superior a 39 ºC, dor, rigidez muscular e articular, vômitos, diarreia, rigidez nas articulações, dor nas articulações, dor muscular, coceira, excesso de sudorese (hiperhidrose), erupção cutânea, inflamação das glândulas do pescoço, axilas ou virilha (linfadenopatia), dor de garganta e incômodo ao engolir (faringite), infecção do trato respiratório superior, tos, desmaio (síncope), sintomas semelhantes aos da gripe, tais como febre, dor de garganta, corrimento nasal, tos e calafrios.
Os seguintes efeitos adversos ocorreram durante o uso rotineiro de Boostrix e não são específicos para nenhum grupo de idade: inchaço da face, lábios, boca, língua ou garganta que pode causar dificuldade para engolir ou respirar (angioedema), colapso ou perda de consciência, crise ou ataques (com ou sem febre), urticárias, fraqueza incomum (astenia).
Depois da administração de vacinas antitetânicas, em raríssimas ocasiões (até em um máximo de 1 de cada 10.000 doses de vacina) foram notificados casos de inflamação temporária dos nervos, que causam dor, fraqueza e paralisia nos membros e que frequentemente atingem o peito e a face (síndrome de Guillain-Barré).
Comunicação de efeitos adversos
Se si ou seu filho experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano, www.notificaRAM.es. Mediante a comunicação de efeitos adversos, si pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Boostrix
Mantenha esta vacina fora da vista e do alcance das crianças.
Não utilize esta vacina após a data de validade que aparece no envase e na etiqueta da seringa pré-carregada após CAD. A data de validade é o último dia do mês que se indica.
Conservar em refrigerador (entre 2 ºC e 8 ºC).
Não congelar. O congelamento destrói a vacina.
Conservar no embalagem original para protegê-la da luz.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Boostrix
- Os princípios ativos são:
Toxoide diftérico1 não menos de 2 Unidades Internacionais (UI) (2,5 Lf)
Toxoide tetânico1 não menos de 20 Unidades Internacionais (UI) (5 Lf)
Antígenos de Bordetella pertussis
Toxoide pertussis1 8 microgramas
Hemaglutinina filamentosa1 8 microgramas
Pertactina1 2,5 microgramas
1adsorvidos em hidróxido de alumínio hidratado (Al(OH)3) 0,3 miligramas Al3+
e fosfato de alumínio (AlPO4) 0,2 miligramas Al3+
O hidróxido de alumínio e o fosfato de alumínio são incluídos na vacina como adjuvantes.
Os adjuvantes são substâncias incluídas em certas vacinas para acelerar, melhorar e/ou prolongar o efeito protetor da vacina.
- Os demais componentes são: cloreto de sódio e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Suspensão injetável em seringa pré-carregada.
Boostrix é um líquido branco, ligeiramente leitoso que se apresenta em uma seringa pré-carregada (0,5 ml).
Boostrix está disponível em seringa pré-carregada de 1 dose com ou sem agulhas separadas; tamanhos de envase de 1 e 10.
Pode que apenas alguns tamanhos de envases estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
GlaxoSmithKline, S.A.
P.T.M. C/ Severo Ochoa, 2
28760 Tres Cantos
(Madrid)
Tel: 900 202 700
Responsável pela fabricação
GlaxoSmithKline Biologicals S.A.
Rue de l' Institut 89; 1330 Rixensart
Bélgica
Data da última revisão deste prospecto: abril 2023
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) (http://www.aemps.gob.es/).
------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais do setor sanitário:
Antes da administração, a vacina deve estar à temperatura ambiente e agitada bem para obter uma suspensão branca, turva e homogênea e deve ser examinada visualmente para observar se existe alguma partícula estranha e/ou variação do aspecto físico antes da administração. Em caso de apreciar alguma dessas circunstâncias, não administrar a vacina.
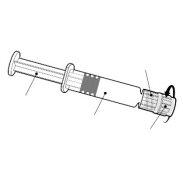
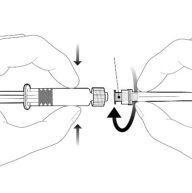
Instruções para a seringa pré-carregada
| Segure a seringa pelo corpo, não pelo êmbolo. Desrosqueie a tampa da seringa girando-a no sentido contrário ao das agulhas do relógio. |
| Para inserir a agulha, conecte a base ao adaptador luer-locke gire um quarto de volta no sentido das agulhas do relógio até que sinta que se bloqueia. Não retire o êmbolo da seringa do corpo. Se isso ocorrer, não administre a vacina. |
Eliminação de resíduos:
A eliminação do medicamento não utilizado e de todos os materiais que estiveram em contato com ele será realizada de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDAForma farmacêutica: INJETÁVEL, 1 doseSubstância ativa: pertussis, purified antigen, combinations with toxoidsFabricante: Sanofi Winthrop IndustrieRequer receita médicaForma farmacêutica: INJETÁVEL, 0,5 ml dose únicaSubstância ativa: meningococcus B, multicomponent vaccineFabricante: Glaxosmithkline Vaccines S.R.L.Requer receita médicaForma farmacêutica: INJETÁVEL, 0,5 ml dose únicaSubstância ativa: meningococcus B, multicomponent vaccineFabricante: Glaxosmithkline Vaccines S.R.L.Requer receita médica
Alternativas a BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA em Polónia
Alternativa a BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA em Ukraine
Médicos online para BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de BOOSTRIX SUSPENSÃO PARA INJEÇÃO EM SERINGA PREENCHIDA – sujeita a avaliação médica e regras locais.