
Adacel
Pergunte a um médico sobre a prescrição de Adacel

Como usar Adacel
Folheto informativo para o utilizador
ADACEL
Suspensão para injeção em seringa pré-cheia
Vacina contra o tétano, a difteria e a tosse convulsa (acelular, combinada), adsorvida, com teor reduzido de antígenos
Deve ler atentamente o conteúdo do folheto antes de administrar a vacina a um adulto ou a uma criança, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico, farmacêutico ou enfermeiro.
- A vacina foi prescrita para uma pessoa específica. Não deve ser transmitida a outros.
- Se um adulto ou uma criança apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é a vacina ADACEL e para que é utilizada
- 2. Informações importantes antes de tomar a vacina ADACEL
- 3. Como a vacina ADACEL é administrada
- 4. Efeitos não desejados
- 5. Como armazenar a vacina ADACEL
- 6. Conteúdo da embalagem e outras informações
1. O que é a vacina ADACEL e para que é utilizada
ADACEL (Tdap) é uma vacina. As vacinas são utilizadas para proteger contra doenças infecciosas. O funcionamento das vacinas consiste em estimular o organismo a produzir sua própria proteção contra as bactérias que causam a doença.
Esta vacina é utilizada para reforçar a proteção contra o tétano, a difteria e a tosse convulsa (coqueluche) em crianças a partir de 4 anos, adolescentes e adultos após um ciclo completo de vacinação de base.
A administração da vacina ADACEL a uma mulher grávida permite a transferência de proteção para o filho ainda durante a gravidez para proteger contra a tosse convulsa durante os primeiros meses de vida da criança.
Limitações da proteção fornecida
A vacina ADACEL previne apenas as doenças causadas pelas bactérias contra as quais a vacina é direcionada. É possível contrair doenças semelhantes se forem causadas por outras bactérias ou vírus.
A vacina ADACEL não contém bactérias ou vírus vivos e não pode causar nenhuma das doenças infecciosas contra as quais protege.
É importante lembrar que nenhuma vacina fornece proteção total e vitalícia em todas as pessoas vacinadas.
2. Informações importantes antes de tomar a vacina ADACEL
Para garantir que a vacina ADACEL seja adequada para um adulto ou uma criança, é importante informar o médico ou enfermeiro se algum dos seguintes pontos se aplica à pessoa ou criança. Se algo não for claro, deve pedir ao médico ou enfermeiro para explicar.
Quando não usar a vacina ADACEL
- se ocorrer reação alérgica:
- às vacinas contra o tétano, a difteria ou a tosse convulsa,
- a qualquer um dos outros componentes (listados no ponto 6), Página 1 de 10
- a qualquer uma das substâncias remanescentes do processo de fabricação (formaldeído, glutaraldeído), que podem estar presentes em quantidades vestigiais.
- se ocorreu reação grave no cérebro dentro de uma semana após a última dose da vacina contra a tosse convulsa
- se ocorrer doença aguda e grave com febre. A vacinação deve ser adiada até a recuperação. Doenças leves sem febre geralmente não são motivo para adiar a vacinação. O médico decidirá se o adulto ou a criança podem receber a vacina ADACEL.
Advertências e precauções
Antes da administração da vacina, deve informar o médico ou enfermeiro:
- sobre a administração de uma dose de reforço da vacina contra o tétano ou a difteria nas últimas 4 semanas. Nesse caso, a pessoa ou a criança não devem receber a vacina ADACEL e o médico decidirá quando é possível receber a próxima dose com base nas recomendações oficiais.
- se ocorreu síndrome de Guillain-Barré (perda temporária da capacidade de se mover ou sentir em todas ou algumas partes do corpo) dentro de 6 semanas após a última dose da vacina contra o tétano. O médico decidirá se a vacina ADACEL deve ser administrada.
- sobre doença progressiva que afeta o cérebro e/ou nervos ou convulsões não controladas. O médico começará o tratamento e administrará a vacina após a estabilização do paciente.
- sobre sistema imunológico fraco ou debilitado devido a
- tratamento (por exemplo, esteroides, quimioterapia ou radioterapia)
- infecção por HIV ou AIDS
- qualquer outra doença.
A vacina pode não proteger tão bem quanto em pessoas com sistema imunológico saudável. Se possível, a vacinação deve ser adiada até o término da doença ou tratamento.
- sobre problemas de sangue que causem hematomas fáceis ou sangramento prolongado após um pequeno corte (por exemplo, devido a uma doença do sangue, como hemofilia ou trombocitopenia, ou ao uso de medicamentos que afetam a coagulação do sangue).
Desmaio pode ocorrer após ou mesmo antes de qualquer injeção. Portanto, deve informar o médico ou enfermeiro se o paciente ou seu filho tiveram desmaios em injeções anteriores.
Antes da administração da vacina ADACEL, deve informar o médico, farmacêutico ou enfermeiro se a pessoa ou a criança têm alergia ao látex. As seringas pré-cheias (1,5 ml) com pontas macias contêm um derivado de látex natural, que pode causar reação alérgica.
Vacina ADACEL e outras vacinas ou medicamentos
Deve informar o médico, enfermeiro ou farmacêutico sobre os medicamentos que o paciente está tomando atualmente ou recentemente, bem como sobre os medicamentos que o paciente planeja tomar.
A vacina ADACEL não contém bactérias vivas, portanto, geralmente pode ser administrada ao mesmo tempo que outras vacinas ou imunoglobulinas, mas em locais diferentes do corpo. Estudos mostraram que a vacina ADACEL pode ser administrada ao mesmo tempo que qualquer uma das seguintes vacinas: vacina contra a hepatite B, vacina contra a poliomielite (inativada ou oral), vacina inativada contra a gripe e vacina recombinante contra o vírus do papiloma humano. A injeção de mais de uma vacina ao mesmo tempo será feita em membros diferentes.
No caso de tratamento que afeta o sistema circulatório ou imunológico (como medicamentos que afetam a coagulação do sangue, esteroides ou quimioterapia), ver "Advertências e precauções" acima.
Página 2 de 10
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, achar que pode estar grávida ou planejar ter um filho, deve consultar um médico ou enfermeiro. O médico ajudará a decidir se a paciente grávida deve receber a vacina ADACEL.
Condução de veículos e operação de máquinas
Não foi estudado o efeito da vacina na capacidade de dirigir veículos ou operar máquinas.
A vacina ADACEL não tem efeito ou tem efeito insignificante na capacidade de dirigir veículos motorizados e operar máquinas.
3. Como a vacina ADACEL é administrada
Quando a vacina deve ser administrada
O médico decidirá se a administração da vacina ADACEL é apropriada com base em:
- tipo de vacinas administradas anteriormente,
- número de doses de vacinas semelhantes administradas anteriormente,
- tempo desde a última dose de vacina semelhante. O médico decidirá o intervalo entre as vacinações. Se a paciente estiver grávida, o médico ajudará a decidir se a paciente deve receber a vacina ADACEL durante a gravidez.
Dosagem e modo de administração
Quem administrará a vacina ADACEL?
A vacina ADACEL deve ser administrada por um profissional de saúde treinado para administrar vacinas, em uma clínica ou centro de saúde equipado com equipamentos para lidar com reações alérgicas graves raras à vacina.
Dosagem
Pessoas de todas as idades para as quais a vacina ADACEL é indicada recebem uma injeção (meio mililitro).
No caso de lesão que exija profilaxia contra o tétano, o médico pode decidir administrar a vacina ADACEL com (ou) sem imunoglobulina antitetânica.
A vacina ADACEL pode ser usada para vacinação de reforço. O médico fornecerá orientação sobre a vacinação de reforço.
Modo de administração
O médico ou enfermeiro administrará a vacina no músculo do braço superior (músculo deltóide).
O médico ou enfermeiro nãoadministrará a vacina em um vaso sanguíneo, na nádega ou sob a pele. No caso de distúrbios de coagulação, o médico ou enfermeiro pode decidir administrar a vacina sob a pele, embora isso possa causar mais efeitos locais não desejados, incluindo um pequeno nódulo sob a pele.
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar um médico, farmacêutico ou enfermeiro.
4. Efeitos não desejados
Como qualquer medicamento, a vacina ADACEL pode causar efeitos não desejados, embora não ocorram em todos.
Página 3 de 10
Reações alérgicas graves
Se ocorrer algum dos seguintes sintomas após deixar o local onde a injeção foi administrada, deve consultar um médico IMEDIATAMENTE:
dificuldade para respirar
azulamento da língua ou lábios
erupção cutânea
inchaço do rosto ou garganta
pressão arterial baixa, causando tontura ou colapso
Os sintomas acima geralmente ocorrem muito rapidamente após a injeção, enquanto a pessoa ainda está na clínica ou centro de saúde. Reações alérgicas graves são muito raras após a administração de qualquer vacina (podem afetar até 1 em 10.000 pessoas).
Outros efeitos não desejados:
Durante os estudos clínicos realizados em grupos de idade específicos, os seguintes efeitos não desejados foram observados:
Crianças de 4 a 6 anos
Muito comuns (podem afetar mais de 1 em 10 pessoas):
- perda de apetite
- dor de cabeça
- diarreia
- fadiga
- dor
- vermelhidão
- inchaço no local da injeção
Comuns (podem afetar até 1 em 10 pessoas):
- náuseas
- vômitos
- erupção cutânea
- dor (em todo o corpo) ou fraqueza muscular
- dor ou inchaço nas articulações
- febre
- calafrios
- aumento ou dor nos gânglios linfáticos axilares
Adolescentes de 11 a 17 anos
Muito comuns (podem afetar mais de 1 em 10 pessoas):
- dor de cabeça
- diarreia
- náuseas
- dor (em todo o corpo) ou fraqueza muscular
- dor ou inchaço nas articulações
- fadiga ou fraqueza
- mal-estar
- calafrios
- dor
- vermelhidão e inchaço no local da injeção.
Comuns (podem afetar até 1 em 10 pessoas):
- vômitos
- erupção cutânea
- febre
- aumento ou dor nos gânglios linfáticos axilares
Página 4 de 10
Adultos de 18 a 64 anos
Muito comuns (podem afetar mais de 1 em 10 pessoas):
- dor de cabeça
- diarreia
- dor (em todo o corpo) ou fraqueza muscular
- fadiga ou fraqueza
- mal-estar
- dor
- vermelhidão e inchaço no local da injeção
Comuns (podem afetar até 1 em 10 pessoas):
- náuseas
- vômitos
- erupção cutânea
- dor ou inchaço nas articulações
- febre
- calafrios
- aumento ou dor nos gânglios linfáticos axilares
Após a comercialização da vacina ADACEL, os seguintes efeitos não desejados adicionais foram observados em diferentes grupos de idade para os quais a vacina é recomendada. A frequência desses efeitos não desejados não pode ser calculada com precisão, pois são relatos voluntários e devem ser relacionados ao número estimado de pessoas vacinadas.
Reações alérgicas / reações alérgicas graves (como reconhecer tal reação, ver início do ponto 4.), sensação de formigamento e dormência ou dormência, fraqueza muscular em parte ou em todo o corpo (síndrome de Guillain-Barré), inflamação dos nervos no braço (inflamação do nervo braquial), distúrbios da função do nervo facial (paralisia de Bell), convulsões, desmaio, inflamação da medula espinhal, inflamação do músculo cardíaco, coceira, urticária, inflamação muscular, inchaço generalizado dos membros, associado à vermelhidão, sensação de calor, sensibilidade ou dor no local da injeção, hematomas, abscesso ou pequeno nódulo no local da injeção.
Notificação de efeitos não desejados
Se ocorrerem algum dos efeitos não desejados, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Saúde Doutor Ricardo Jorge
Rua Alexandre Herculano, 321, 4000-055 Porto, telefone: +351 22 207 66 00, fax: +351 22 207 66 99
Site na internet: https://www.infarmed.pt/
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados permite reunir mais informações sobre a segurança do medicamento.
5. Como armazenar a vacina ADACEL
O medicamento deve ser armazenado em local não visível e inacessível a crianças.
Não deve usar a vacina ADACEL após o término da validade impresso na embalagem após "VAL". A data de validade é o último dia do mês indicado.
Armazenar na geladeira (2°C–8°C). Não congelar. Descartar a vacina se estiver congelada.
As seringas pré-cheias devem ser armazenadas na embalagem exterior para proteger da luz.
Os medicamentos não devem ser jogados na canalização ou lixeiras domésticas. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
Página 5 de 10
6. Conteúdo da embalagem e outras informações
O que a vacina ADACEL contém
Os componentes ativos em cada dose (0,5 ml) da vacina são:
Toxóide diftérico
não menos de 2 unidades internacionais (2 Lf)
Toxóide tetânico
não menos de 20 unidades internacionais (5 Lf)
Antígenos da tosse convulsa:
Toxóide da tosse convulsa
2,5 microgramas
Hemaglutinina filamentosa
5 microgramas
Pertactina
3 microgramas
Fímbrias do tipo 2 e 3
5 microgramas
Adsorvido em fosfato de alumínio
1,5 mg (0,33 mg Al )
O fosfato de alumínio atua como adjuvante nesta vacina. Adjuvantes são substâncias que fazem parte de algumas vacinas e têm a função de acelerar, aumentar e/ou prolongar a ação protetora da vacina.
Outros componentes são: fenoxietanol, água para injeção
Como a vacina ADACEL é apresentada e o que o pacote contém
A vacina ADACEL é uma suspensão para injeção em seringa pré-cheia (0,5 ml):
- sem agulha - embalagem contendo 1 ou 10
- com 1 ou 2 agulhas separadas - embalagem contendo 1 ou 10
- com agulha separada em capa de proteção - embalagem contendo 1 ou 10
Nem todos os tipos de embalagens podem estar disponíveis no mercado.
A aparência correta da vacina é uma suspensão turva e branca. Durante o armazenamento, pode formar um sedimento branco e grumos ou agregados que se desfazem. Após a agitação, torna-se um líquido branco uniforme; no caso de agregados, o produto pode ser agitado novamente até obter uma suspensão uniforme.
Titular da autorização de comercialização e fabricante/importador
Titular da autorização de comercialização
Sanofi-Aventis, S.A.
Edifício Sanofi, Rua Alves Redol, 4 - 8º
1000-029 Lisboa
Portugal
Fabricante
Sanofi Pasteur SA
2, Avenue Pont Pasteur
69007 Lyon
França
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu sob os seguintes nomes:
Alemanha, Áustria
ADACEL
Página 6 de 10
Bélgica, Dinamarca, Espanha, Finlândia, França, Grécia, Irlanda, Itália, Luxemburgo, Noruega, Países Baixos, Portugal, Reino Unido, Suécia:
ADACEL
República Checa, Eslováquia, Eslovênia, Estónia, Hungria, Letónia, Lituânia, Polónia:
ADACEL
Data da última revisão do folheto:janeiro de 2025
Informações destinadas apenas a profissionais de saúde:
Como não foram realizados estudos de compatibilidade, a vacina ADACEL não deve ser misturada com outros medicamentos.
Preparação para administração
A seringa pré-cheia pode ser fornecida com uma ponta Luer Lock com uma capa macia (Figura A) ou com uma capa rígida (Figura B). A seringa com a suspensão para injeção deve ser inspecionada visualmente antes da administração. Se houver partículas estranhas sólidas, vazamento, uso antecipado do êmbolo ou danos ao selo da ponta, a seringa pré-cheia deve ser descartada. A seringa é para uso único e não pode ser reutilizada.
Instruções para o uso da seringa pré-cheia com ponta Luer Lock
Figura A: Seringa com ponta Luer Lock e capa macia
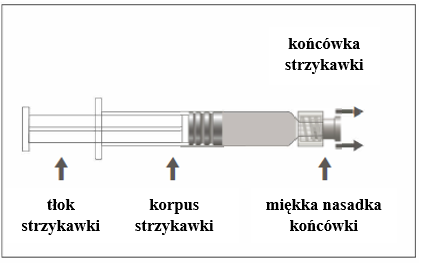 | ||
| Passo 1: Segurando a ponta da seringa com uma mão (evitando segurar o êmbolo ou o corpo da seringa), remover a capa da ponta. | 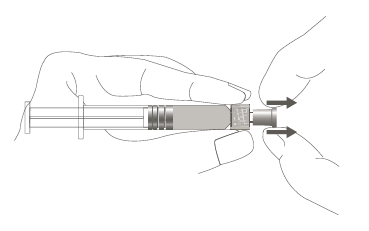 | |
Página 7 de 10
| Passo 2: Para fixar a agulha na seringa, deve-se enroscá-la suavemente na ponta até sentir uma ligeira resistência. | 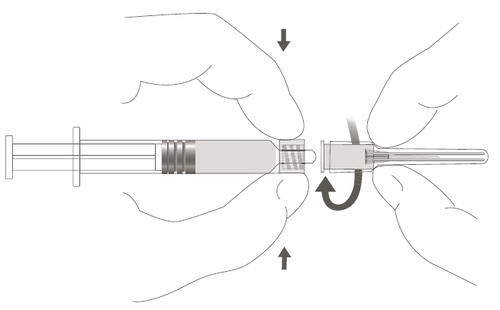 |
Figura B: Seringa com ponta Luer Lock e capa rígida
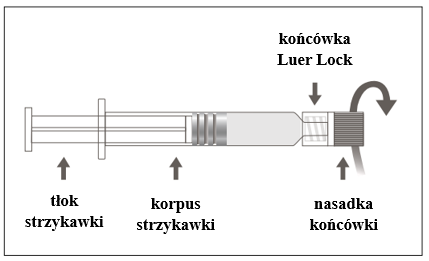
| Passo 1: Segurando a ponta Luer Lock com uma mão (evitando segurar o êmbolo ou o corpo da seringa), desrosquear a capa da ponta. | 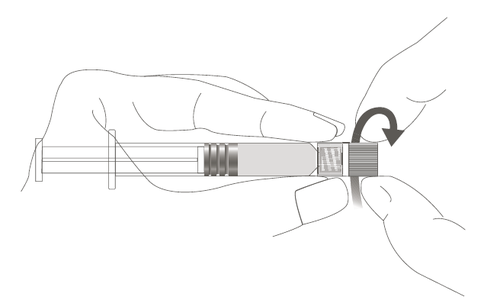 |
| Passo 2: Para fixar a agulha na seringa, deve-se enroscá-la suavemente na ponta Luer Lock até sentir uma ligeira resistência. | 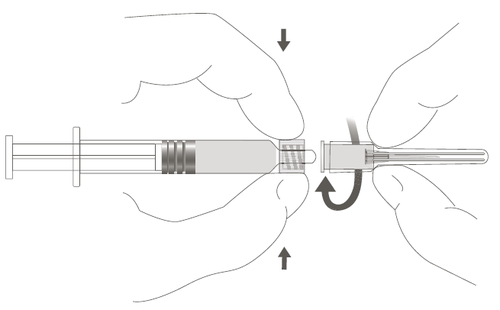 |
Instruções para o uso da agulha com capa de proteção com a seringa pré-cheia com ponta Luer
Lock:
Página 8 de 10
Deve seguir os passos acima 1 e 2 para preparar a seringa com ponta Luer Lock e a agulha para fixação.
| Figura C: Agulha com capa de proteção (na embalagem) | Figura D: Componentes da capa de proteção da agulha (prontos para uso) |
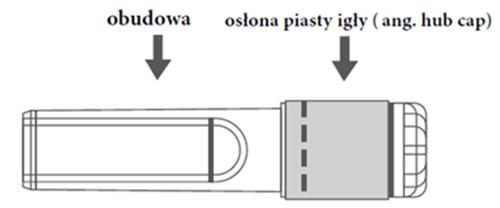 |  |
Passo 3: Remover a embalagem da agulha. A agulha é protegida por uma capa de proteção e uma capa da ponta.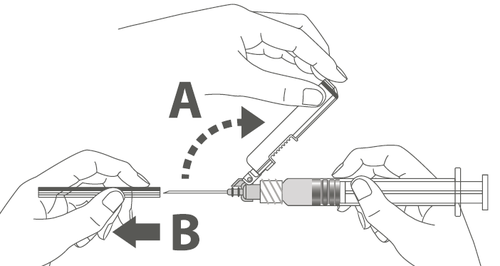 | |
| Passo 4: A: Afastar a capa de proteção da agulha em direção ao corpo da seringa no ângulo mostrado. B: Remover a capa da ponta. | |
| Passo 5: Após a injeção, bloquear (ativar) a capa de proteção usando uma das três técnicas de manipulação com uma mão: ativação em uma superfície plana, com o polegar ou o dedo indicador. Observação: A ativação é confirmada por um "clic" audível e/ou palpável. | 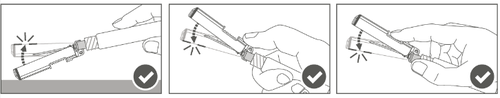 |
| Passo 6: Verificar visualmente o funcionamento da capa de proteção. A capa de proteção deve estar completamente bloqueada (ativada), como mostrado na Figura C. |  |
Página 9 de 10
| A Figura D mostra que a capa de proteção NÃOestá completamente bloqueada (não está ativada). | 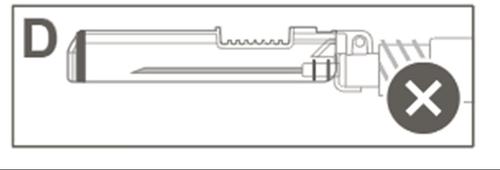 |
| Advertência: Não deve tentar desbloquear (desativar) o dispositivo de proteção empurrando a agulha para fora da capa de proteção. | |
Qualquer resíduo não utilizado do medicamento ou seus resíduos deve ser eliminado de acordo com as regulamentações locais.>
Não deve colocar as capas das agulhas novamente.
Página 10 de 10
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorSanofi Winthrop Industrie Sanofi-Aventis Zrt.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a AdacelForma farmacêutica: Suspensão, 0.5 mlSubstância ativa: pertussis, purified antigen, combinations with toxoidsFabricante: GlaxoSmithKline Biologicals S.A.Requer receita médicaForma farmacêutica: Suspensão, 1 dose (0.5 ml)Substância ativa: pertussis, purified antigen, combinations with toxoidsFabricante: AJ Vaccines A/SRequer receita médicaForma farmacêutica: Suspensão, não menos de 30 UI de toxoide diftérico, não menos de 40 UI de toxoide tetânico e não menos de 4 UI de suspensão da estirpe inativada de Bordetella pertussis/0,5 ml; 1 dia; 1 dose (0,5 ml)Substância ativa: pertussis, inactivated, whole cell, combinations with toxoidsRequer receita médica
Alternativas a Adacel noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Adacel em Ukraine
Alternativa a Adacel em Espanha
Médicos online para Adacel
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Adacel – sujeita a avaliação médica e regras locais.














