

Xancodal

Pergunte a um médico sobre a prescrição de Xancodal

Como usar Xancodal
Folheto informativo para o doente
Xancodal, 5 mg, cápsulas duras
Xancodal, 10 mg, cápsulas duras
Xancodal, 20 mg, cápsulas duras
Hidroclorido de oxycodona
Para administração a adultos e adolescentes a partir dos 12 anos
Deve ler-se atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para poder reler se necessário.
- Em caso de dúvidas adicionais, deve consultar o médico ou farmacêutico.
- O medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é Xancodal e para que é utilizado
- 2. Informações importantes antes de tomar Xancodal
- 3. Como tomar Xancodal
- 4. Efeitos secundários possíveis
- 5. Como conservar Xancodal
- 6. Conteúdo da embalagem e outras informações
1. O que é Xancodal e para que é utilizado
Xancodal contém a substância ativa hidroclorido de oxycodona, que é um medicamento analgésico forte do grupo dos opioides.
Xancodal é utilizado em adultos e adolescentes a partir dos 12 anos para o tratamento da dor intensa, que requer a administração de medicamentos analgésicos opioides.
2. Informações importantes antes de tomar Xancodal
Quando não tomar Xancodal
se o doente tem alergia ao hidroclorido de oxycodona ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6);
se o doente tem distúrbios respiratórios, tais como dificuldades respiratórias graves (depressão respiratória), doença pulmonar obstrutiva crónica grave ou asma brônquica grave. Os sintomas podem incluir, entre outros, falta de ar, tosse ou respiração mais lenta ou mais fraca do que o normal.
se o doente tem níveis elevados de dióxido de carbono no sangue;
se o doente tem alterações cardíacas devido a uma doença pulmonar de longa duração (cor pulmonale);
se o doente tem obstrução intestinal paralítica. Pode ser indicado por um esvaziamento gástrico mais lento do que o normal ou dor abdominal intensa.
Precauções e advertências
Antes de tomar Xancodal, deve discutir com o médico ou farmacêutico se:
- o doente é idoso ou está debilitado
- o doente tem distúrbios respiratórios graves
- o doente tem distúrbios hepáticos ou renais
- o doente tem doença da tiróide, ou se apresenta secura, frio e inchaço da pele do rosto e membros (edema mucinoso)
- o doente tem função tireoidiana reduzida
- o doente tem insuficiência adrenal (doença de Addison), que pode causar sintomas como fraqueza, perda de peso, tonturas, náuseas ou vómitos
- o doente tem hipertrofia da próstata, que pode causar dificuldade em urinar (nos homens)
- a interrupção do álcool ou drogas no passado causou sintomas de abstinência, como agitação, ansiedade, tremores ou suor excessivo
- ou se alguém da sua família já abusou ou foi dependente de álcool, medicamentos de prescrição ou drogas ilegais ("dependência")
- se o doente é fumador
- ou se já teve problemas de humor (depressão, ansiedade ou distúrbios de personalidade) ou foi tratado por um psiquiatra por outras doenças mentais
- o doente tem distúrbios psíquicos devido à intoxicação, por exemplo, álcool (psicose tóxica)
- o doente tem pancreatite, que causa dor abdominal e dor nas costas
- o doente tem distúrbios da vesícula biliar ou vias biliares
- o doente tem doença intestinal relacionada com obstrução ou inflamação
- o doente tem lesão cerebral, dor de cabeça intensa ou apresenta náuseas, pois pode indicar pressão intracraniana aumentada
- o doente tem pressão arterial baixa
- o doente tem volume de sangue reduzido (hipovolemia), por exemplo, devido a uma hemorragia significativa, queimaduras graves, suor excessivo, diarreia grave ou vómitos
- o doente tem epilepsia ou tendência a convulsões
- o doente está a tomar medicamentos conhecidos como inibidores da monoamina oxidase (MAO) (utilizados no tratamento da depressão ou doença de Parkinson) ou os tomou nos últimos 2 semanas
- o doente vai ser submetido a uma operação abdominal.
Se alguma das situações acima se aplica ao doente atualmente ou no passado, deve informar o médico.
Xancodal pode causar dependência. Se for administrado por um longo período, pode ocorrer tolerância ao medicamento, exigindo doses cada vez maiores para manter o controle da dor.
A administração prolongada de Xancodal pode levar à dependência física, e a interrupção súbita do tratamento pode causar sintomas de abstinência (ver ponto 3 "Interrupção do tratamento com Xancodal"). Os sintomas de abstinência podem incluir, por exemplo, bocejos, dilatação das pupilas, lágrimas anormais ou excessivas, corrimento nasal aquoso, tremores, suor excessivo, ansiedade, agitação, convulsões, insónia e dor muscular.
A administração de oxycodona, especialmente em doses elevadas, pode causar aumento da sensibilidade à dor (hiperalgesia), que não responde ao aumento da dose do medicamento. Pode ser necessário reduzir a dose de oxycodona ou mudar para outro medicamento analgésico opioide.
A administração repetida de Xancodal pode levar à dependência e abuso, o que pode resultar em overdose fatal. Se houver preocupação de que o doente possa se tornar dependente de Xancodal, deve consultar o médico.
Xancodal deve ser administrado com especial cuidado em doentes que abusam ou atualmente abusam de álcool ou drogas.
Em caso de injeção não autorizada (intravenosa), os componentes auxiliares do medicamento podem causar destruição (necrose) do tecido no local da injeção, alterações no tecido pulmonar (granulomas pulmonares) ou outros eventos graves, potencialmente fatais.
Distúrbios respiratórios relacionados ao sono
Xancodal pode causar distúrbios respiratórios relacionados ao sono, como apneia do sono (pausas na respiração durante o sono) e hipoxemia relacionada ao sono (baixo nível de oxigênio no sangue).
Os sintomas podem incluir pausas na respiração durante o sono, despertares noturnos devido à falta de ar, dificuldade em manter o sono ou sonolência excessiva durante o dia. Se o doente ou outra pessoa observar esses sintomas, deve consultar o médico. O médico pode considerar reduzir a dose.
Atletas devem ser alertados de que o medicamento pode dar resultado positivo nos testes antidoping. A administração de Xancodal como um meio de doping pode ser perigosa para a saúde.
Crianças
Oxycodona não foi estudada em crianças com menos de 12 anos. Não se recomenda a administração de Xancodal em crianças com menos de 12 anos, pois não foi demonstrada a segurança e eficácia nessa faixa etária.
Xancodal e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, incluindo os que o doente planeia tomar.
Quando administrados juntamente com Xancodal, alguns outros medicamentos que afetam a função cerebral (ver abaixo) podem aumentar o risco de depressão respiratória (especialmente em caso de overdose e em idosos) e (ou) aumentar o efeito sedativo do medicamento Xancodal.
A administração concomitante de Xancodal e medicamentos que afetam a função cerebral (por exemplo, medicamentos sedativos, como benzodiazepinas ou derivados, ver abaixo) aumenta o risco de sonolência, dificuldade respiratória (depressão respiratória) ou coma, que podem ser fatais. Portanto, o tratamento combinado deve ser considerado apenas quando não há outras opções de tratamento disponíveis.
Se Xancodal for administrado juntamente com medicamentos sedativos, o médico deve limitar a dose e o período de administração concomitante. O doente deve informar o médico sobre todos os medicamentos sedativos que está a tomar e seguir estritamente a dose prescrita pelo médico.
Pode ser útil informar um familiar ou amigo próximo sobre a possibilidade de ocorrerem os sintomas acima mencionados. Se ocorrerem os sintomas acima mencionados, deve consultar o médico.
Os medicamentos que afetam a função cerebral incluem:
- outros medicamentos analgésicos fortes (opioides),
- medicamentos para dormir e sedativos (como benzodiazepinas),
- medicamentos utilizados no tratamento da depressão, como paroxetina,
- medicamentos utilizados no tratamento de alergias, doença do movimento ou náuseas (medicamentos antihistamínicos ou antieméticos),
- medicamentos utilizados no tratamento de distúrbios psíquicos ou mentais (medicamentos antipsicóticos),
- medicamentos utilizados no tratamento da doença de Parkinson.
O risco de efeitos secundários aumenta se o doente estiver a tomar medicamentos antidepressivos (como citalopram, duloxetina, escitalopram, fluoxetina, fluvoxamina, paroxetina, sertralina, venlafaxina). Esses medicamentos podem interagir com a oxycodona, causando sintomas como:
- contracções musculares involuntárias, incluindo os músculos que controlam os movimentos oculares,
- agitação,
- suor excessivo,
- tremores,
- aumento dos reflexos,
- aumento da tensão muscular,
- aumento da temperatura corporal acima de 38°C.
Se ocorrerem os sintomas acima mencionados, deve consultar o médico.
Além disso, são possíveis interações com os seguintes medicamentos:
- alguns medicamentos que previnem a formação de coágulos sanguíneos ou ajudam a diluir o sangue (conhecidos como medicamentos anticoagulantes derivados da cumarina, por exemplo, warfarina ou fenprocoumon). Xancodal pode afetar a sua ação.
- medicamentos que relaxam os músculos
- alguns antibióticos (por exemplo, claritromicina, eritromicina, telitromicina ou rifampicina),
- alguns medicamentos utilizados no tratamento de infecções fúngicas (por exemplo, cetoconazol, voriconazol, itraconazol ou posaconazol),
- alguns medicamentos utilizados no tratamento da infecção por HIV (por exemplo, boceprevir, ritonavir, indinavir, nelfinavir ou saquinavir),
- cimetidina (medicamento utilizado no tratamento da azia),
- carbamazepina (medicamento utilizado no tratamento de convulsões ou distúrbios de humor),
- fenitoína (medicamento utilizado no tratamento de convulsões),
- erva-de-são-joão (medicamento utilizado no tratamento da depressão),
- quinidina (medicamento utilizado no tratamento da frequência cardíaca acelerada),
- medicamentos inibidores da monoamina oxidase (MAO) administrados atualmente ou nos últimos 2 semanas (ver subponto "Precauções e advertências").
Xancodal e álcool
O álcool consumido durante a administração de Xancodal pode causar sonolência aumentada ou aumentar o risco de efeitos secundários graves, como depressão respiratória com risco de parada respiratória e perda de consciência. Recomenda-se que o doente não beba álcool durante a administração de Xancodal.
O suco de toranja consumido durante a administração de Xancodal pode aumentar o risco de efeitos secundários. Recomenda-se que o doente não beba suco de toranja durante a administração de Xancodal.
Gravidez e amamentação
Se a paciente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
- GravidezXancodal não deve ser administrado durante a gravidez. Existem dados limitados sobre a administração de oxycodona em mulheres grávidas. A oxycodona atravessa a barreira placentária e entra no sangue do feto. A administração prolongada de oxycodona durante a gravidez pode causar sintomas de abstinência no recém-nascido, e a administração durante o parto pode causar problemas respiratórios (depressão respiratória) no recém-nascido.
- AmamentaçãoXancodal não deve ser administrado durante a amamentação, pois a sua substância ativa (oxycodona) pode passar para o leite materno e causar sonolência (sedação) ou problemas respiratórios (depressão respiratória) no bebê amamentado.
Condução de veículos e operação de máquinas
A oxycodona pode afetar a capacidade de conduzir veículos ou operar máquinas.
As restrições gerais à condução de veículos podem não se aplicar ao tratamento com uma dose estável. O médico responsável avaliará individualmente a situação de cada doente.
Deve discutir com o médico se ou em que condições o doente pode conduzir veículos.
Xancodal contém sódio
Este medicamento contém menos de 1 mmol (23 mg) de sódio por cápsula, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar Xancodal
Este medicamento deve ser sempre administrado de acordo com as recomendações do médico. Em caso de dúvidas, deve consultar o médico ou farmacêutico.
A dose recomendada é
Adultos e adolescentes (a partir dos 12 anos)
A dose inicial recomendada de hidroclorido de oxycodona é de 5 mg a cada 6 horas.
No entanto, o médico determinará a dose do medicamento necessária para controlar a dor e a frequência da administração.
Se o doente continuar a sentir dor apesar de tomar o medicamento, deve informar o médico.
Pacientes com distúrbios renais e (ou) hepáticos
A dose inicial usual é metade da dose recomendada para adultos. O médico prescreverá a dose mais adequada, adaptada ao estado clínico do doente, na forma farmacêutica mais adequada, se possível.
Modo de administração
O medicamento é destinado apenas à administração oral.
As cápsulas devem ser engolidas inteiras, com um grande volume de líquido.
O medicamento pode ser administrado independentemente das refeições.
Durante a administração de Xancodal, não se deve beber bebidas alcoólicas.
Instruções para lidar com o blister perfurado de dose única, protegido contra o acesso de crianças
- 1. Não se deve esmagar a cápsula diretamente através do blister.
- 2. Deve-se separar ao longo da perfuração o fragmento do blister com uma cápsula.
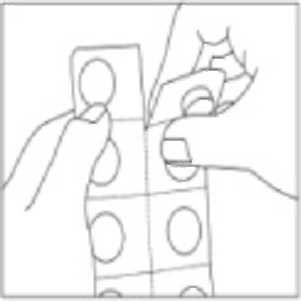
- 3. Deve-se separar cuidadosamente a folha de trás do blister para expor a cápsula.
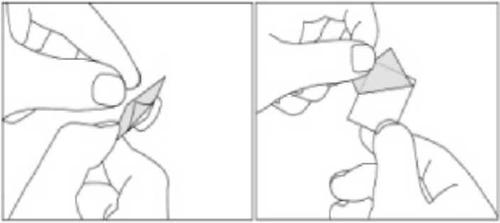
Administração de uma dose maior do que a recomendada de Xancodal
Em caso de administração de uma dose maior do que a recomendada de Xancodal, deve informar imediatamente o médico ou o centro local de controle de envenenamento.
Os sintomas de overdose podem incluir:
- constricção das pupilas
- respiração lenta ou mais fraca do que o normal (depressão respiratória)
- sonolência progressiva até a perda de consciência
- diminuição da tensão muscular
- batimento cardíaco lento
- diminuição súbita da pressão arterial
Em casos graves, pode ocorrer perda de consciência (coma), acúmulo de líquido nos pulmões e colapso circulatório, o que pode levar à morte.
Em nenhum caso se deve realizar atividades que exijam grande concentração, como conduzir veículos.
Omissão da administração de uma dose de Xancodal
Se o doente tomar uma dose menor de Xancodal do que a recomendada ou omitir doses do medicamento, a ação analgésica será inadequada ou não ocorrerá.
Se o doente esquecer uma dose do medicamento, deve proceder de acordo com as instruções abaixo:
- Se faltarem mais de 4 horas para a próxima administração planejada: a dose omitida deve ser administrada imediatamente, e as doses subsequentes devem ser administradas de acordo com a recomendação.
- Se faltarem menos de 4 horas para a próxima administração planejada: a dose omitida deve ser administrada, e a próxima dose deve ser administrada após 4 horas. As doses subsequentes devem ser administradas de acordo com o esquema de dosagem recomendado.
Não se deve administrar mais de uma dose em um período de 4 horas.
Não se deve administrar uma dose dupla para compensar a dose omitida.
Interrupção do tratamento com Xancodal
Não se deve interromper o tratamento sem consultar previamente o médico.
Se a administração de Xancodal não for mais necessária, pode ser recomendável reduzir gradualmente a dose para evitar sintomas de abstinência.
Em caso de dúvidas adicionais relacionadas à administração deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos secundários possíveis
Como qualquer medicamento, Xancodal pode causar efeitos secundários, embora não ocorram em todos.
Os efeitos secundários mais frequentemente relatados são náuseas (especialmente no início do tratamento) e constipação. A constipação pode ser prevenida com métodos como a ingestão de grandes volumes de líquido ou a alimentação com alimentos ricos em fibras. Se o doente sentir náuseas ou tiver vómitos, o médico pode prescrever medicamentos adequados.
Efeitos secundários importantes ou sintomas que devem ser observados e procedimento em caso de ocorrência:
Se o doente apresentar algum dos seguintes sintomas, deve interromper a administração de Xancodal e consultar imediatamente o médico ou procurar atendimento médico de emergência:
- respiração súbita e chiada, dificuldade em respirar, inchaço dos olhos, face ou lábios, erupção cutânea ou coceira (especialmente se afetar todo o corpo). Pode ser um sinal de reações alérgicas graves.
- respiração lenta ou superficial (depressão respiratória). É o efeito secundário mais grave relacionado à overdose de medicamentos analgésicos fortes, como a oxycodona. Ocorre mais frequentemente em doentes idosos e debilitados.
- diminuição súbita e significativa da pressão arterial, que pode causar sintomas como tonturas e desmaio.
Efeitos secundários possíveis
Muito frequentes(podem ocorrer em mais de 1 em 10 doentes)
sonolência, tonturas, dor de cabeça
constipação, náuseas, vómitos
coceira na pele
Frequentes(podem ocorrer em menos de 1 em 10 doentes)
ansiedade, depressão, diminuição da atividade, agitação (principalmente motora), aumento da atividade, nervosismo, distúrbios do sono, pensamento anormal, confusão, tremores
fadiga, fraqueza, cansaço
dificuldade em respirar, respiração chiada
secura na boca, arrotos, dispepsia, dor abdominal, diarreia
diminuição do apetite até a perda de apetite
erupção cutânea, suor excessivo
dor ao urinar, aumento da necessidade de urinar
Pouco frequentes(podem ocorrer em menos de 1 em 100 doentes)
respiração lenta e superficial (depressão respiratória)
reações alérgicas
desidratação
agitação, mudanças de humor, sensação de felicidade
alucinações, percepção alterada da realidade
distúrbios da visão, constricção das pupilas
zumbido no ouvido, sensação de vertigem ou tontura
mudanças no paladar
aumento da tensão muscular, contracções musculares involuntárias, convulsões, tremores
formigamento ou entorpecimento, diminuição da sensação de dor ou toque
distúrbios da coordenação ou equilíbrio
perda de memória, distúrbios da concentração, distúrbios da fala
desmaio
batimento cardíaco acelerado, palpitações (relacionadas à abstinência)
vasodilatação, causando diminuição da pressão arterial
tosse, mudanças na voz
úlceras na boca, dor nos dentes
gases, dificuldade em engolir, arrotos
obstrução intestinal
diminuição da libido, impotência, níveis baixos de hormônios sexuais no sangue detectados em exames de sangue (hipogonadismo)
lesões devido a acidentes
mau-estar geral, dor (por exemplo, no peito)
inchaço nas mãos, tornozelos ou pés
enxaqueca
tolerância ao medicamento
secura na pele
sede
dificuldade em urinar
calafrios
dependência física, incluindo sintomas de abstinência (ver ponto 3 "Interrupção do tratamento com Xancodal")
aumento da atividade das enzimas hepáticas (detectado em exames de sangue)
Raros(podem ocorrer em menos de 1 em 1000 doentes)
pressão arterial baixa, tonturas, desmaio devido à diminuição súbita da pressão arterial ao levantar
hemorragia gengival, aumento do apetite, fezes escuras, alterações nos dentes
formação de bolhas na pele e mucosas (erupção bolhosa), urticária
mudanças no peso (diminuição ou aumento)
Frequência desconhecida(não pode ser estimada com base nos dados disponíveis)
amenorreia
reação alérgica grave, que causa dificuldade em respirar ou tonturas
agressividade
aumento da sensibilidade à dor (hiperalgesia)
cárie dentária
colecistite (causando dor abdominal), icterícia
sintomas de abstinência em recém-nascidos
dependência do medicamento
espasmos musculares
inibição do reflexo da tosse
- apneia do sono (pausas na respiração durante o sono)
Notificação de efeitos secundários
Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos do Instituto de Regulação de Medicamentos, Dispositivos Médicos e Produtos Biocidas: Al. Jerozolimskie 181C, 02-222 Varsóvia
telefone: + 48 22 49 21 301, fax: + 48 22 49 21 309, e-mail: [email protected]
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar Xancodal
O medicamento deve ser conservado em um local não visível e inacessível a crianças.
Não use este medicamento após o prazo de validade impresso na embalagem e na caixa após "EXP". O prazo de validade é o último dia do mês indicado.
Não conserve em temperatura superior a 30°C.
Os medicamentos não devem ser jogados na canalização ou lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais necessários. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém Xancodal
A substância ativa é o hidroclorido de oxycodona.
Xancodal, 5 mg
Cada cápsula dura contém 5 mg de hidroclorido de oxycodona, o que corresponde a 4,48 mg de oxycodona.
Xancodal, 10 mg
Cada cápsula dura contém 10 mg de hidroclorido de oxycodona, o que corresponde a 8,96 mg de oxycodona.
Xancodal, 20 mg
Cada cápsula dura contém 20 mg de hidroclorido de oxycodona, o que corresponde a 17,93 mg de oxycodona.
Os outros componentes são:
Conteúdo da cápsula: celulose microcristalina, estearato de magnésio
Revestimento da cápsula: gelatina, laurilsulfato de sódio, dióxido de titânio (E171), óxido de ferro amarelo (E172), óxido de ferro vermelho (E172), indigotina (E132)
Tinta para impressão: shellac, óxido de ferro preto (E172), hidróxido de potássio (para ajustar o pH).
Como é Xancodal e que conteúdo tem a embalagem
Xancodal, 5 mg
Cápsulas duras com 14,4 mm de comprimento, com corpo de cor rosa escuro e impressão "5" e tampa de cor marrom com impressão "OXY".
Xancodal, 10 mg
Cápsulas duras com 14,4 mm de comprimento, com corpo de cor branca e impressão "10" e tampa de cor marrom com impressão "OXY".
Xancodal, 20 mg
Cápsulas duras com 14,4 mm de comprimento, com corpo de cor rosa clara e impressão "20" e tampa de cor marrom com impressão "OXY".
Tamanhos da embalagem:
Blister perfurado de dose única, protegido contra o acesso de crianças, em caixa de cartão contendo 20x1, 30x1, 50x1 e 100x1 cápsulas duras.
Nem todos os tamanhos da embalagem podem estar disponíveis no mercado.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Sandoz GmbH
Biochemiestrasse 10
6250 Kundl, Áustria
Fabricante
Salutas Pharma GmbH
Otto-von-Guericke-Allee 1
39179 Barleben, Alemanha
Activis ehf.
Reykjavikurvegur 78
220 Hafnarfjordur, Islândia
Balkanpharma Dupnitsa AD
3 Samokovsko Shosse Str.
2600 Dupnitsa, Bulgária
Lek Pharmaceuticals d.d.,
Verovškova ulica 57,
1526 Liubliana, Eslovênia
Para obter mais informações sobre o medicamento e seus nomes em outros países membros do Espaço Econômico Europeu, deve contatar:
Sandoz Polska Sp. z o.o.
ul. Domaniewska 50 C
02-672 Varsóvia
telefone: +48 22 209 70 00
Data da última atualização do folheto:05/2022
Logotipo Sandoz
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorActavis ehf. Balkanpharma - Dupnitsa AD Lek Pharmaceuticals d.d. Salutas Pharma GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Xancodal
Alternativas a Xancodal noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Xancodal em Ukraine
Alternativa a Xancodal em Spain
Médicos online para Xancodal
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Xancodal – sujeita a avaliação médica e regras locais.














