
Sunitinib Krka


Como usar Sunitinib Krka
Folheto informativo: informações para o utilizador
Sunitinib Krka, 12,5 mg, cápsulas duras
Sunitinib Krka, 25 mg, cápsulas duras
Sunitinib Krka, 50 mg, cápsulas duras
sunitinibe
Deve ler atentamente o folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para o poder reler se necessário.
- Se tiver alguma dúvida, deve consultar o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si. Não o deve dar a outros. O medicamento pode ser prejudicial ao outro, mesmo que os sintomas da sua doença sejam os mesmos.
- Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o seu médico. Ver ponto 4.
Índice do folheto
- 1. O que é o Sunitinib Krka e para que é utilizado
- 2. Informações importantes antes de tomar o Sunitinib Krka
- 3. Como tomar o Sunitinib Krka
- 4. Efeitos secundários possíveis
- 5. Como conservar o Sunitinib Krka
- 6. Conteúdo do pacote e outras informações
1 O que é o Sunitinib Krka e para que é utilizado
O Sunitinib Krka contém como substância ativa o sunitinibe, que é um inibidor da quinase proteica.
O Sunitinib Krka é utilizado no tratamento de tumores. Inibe a atividade de um grupo especial de proteínas,
conhecidas por participarem no crescimento e disseminação de células tumorais.
O Sunitinib Krka é utilizado no tratamento dos seguintes tipos de tumores em adultos:
- tumores do estroma gastrointestinal (GIST, tumor estromal gastrointestinal), um tipo de tumor do estômago e intestinos, quando o imatinibe (outro medicamento anticâncer) deixou de ser eficaz ou o doente não pode tomá-lo;
- câncer de células renais metastático (MRCC, carcinoma de células renais metastático), um tipo de tumor renal com metástases para outras partes do corpo;
- tumores neuroendócrinos do pâncreas (pNET, tumores neuroendócrinos do pâncreas) (tumores que se desenvolvem a partir de células que produzem hormônios no pâncreas), que estão em fase de progressão ou não podem ser removidos cirurgicamente.
Se tiver alguma dúvida sobre como o Sunitinib Krka funciona ou por que razão lhe foi prescrito, deve consultar o seu médico.
2 Informações importantes antes de tomar o Sunitinib Krka
Quando não tomar o Sunitinib Krka
- Se o doente for alérgico ao sunitinibe ou a qualquer outro componente deste medicamento (listados no ponto 6).
Precauções e advertências
Antes de começar a tomar o Sunitinib Krka, deve discutir com o seu médico:
- Se o doente tiver hipertensão arterial. O Sunitinib Krka pode aumentar a pressão arterial. O médico pode realizar medições da pressão arterial durante o tratamento com o Sunitinib Krka e, se necessário, o doente pode ser tratado com medicamentos que reduzem a pressão arterial.
- Se o doente tiver ou tiver tido doenças do sangue, sangramentos ou hematomas. O tratamento com o Sunitinib Krka pode aumentar o risco de sangramento ou alterar o número de certos tipos de células sanguíneas, o que pode causar anemia ou afetar a capacidade do sangue de coagular. Se o doente estiver a tomar warfarina ou acenocoumarol, medicamentos que diluem o sangue utilizados para prevenir a formação de coágulos, pode haver um risco maior de sangramento. Deve informar o médico sobre todos os sangramentos durante o tratamento com o Sunitinib Krka.
- Se o doente tiver problemas cardíacos. O Sunitinib Krka pode causar problemas cardíacos. Deve informar o médico se o doente se sentir muito cansado, tiver falta de ar ou inchaço nos pés e tornozelos.
- Se o doente tiver arritmias cardíacas. O Sunitinib Krka pode causar arritmias cardíacas. Durante o tratamento com o Sunitinib Krka, o médico pode realizar um eletrocardiograma para avaliar essas arritmias. Deve informar o médico se o doente tiver tonturas, desmaios ou arritmias cardíacas durante o tratamento com o Sunitinib Krka.
- Se o doente tiver ou tiver tido trombos nas veias e/ou artérias (tipos de vasos sanguíneos), incluindo acidente vascular cerebral, ataque cardíaco, embolia ou trombose. Deve contactar imediatamente o médico se o doente tiver sintomas como dor ou pressão no peito, dor nos braços, nas costas, no pescoço ou queixo, falta de ar, formigamento ou fraqueza de um lado do corpo, fala dificultosa, dor de cabeça ou tonturas.
- Se o doente tiver ou tiver tido aneurisma (dilatação e enfraquecimento da parede de um vaso sanguíneo) ou ruptura da parede de um vaso sanguíneo.
- Se o doente tiver ou tiver tido lesões nos pequenos vasos sanguíneos chamadas de microangiopatia trombótica. Deve informar o médico se o doente tiver febre, cansaço, fadiga, hematomas, sangramento, inchaço, confusão, perda de visão ou convulsões.
- Se o doente tiver problemas da tiróide. O Sunitinib Krka pode causar problemas da tiróide. Deve informar o médico se o doente se sentir muito cansado, tiver frio ou tiver voz baixa durante o tratamento com o Sunitinib Krka. O médico deve verificar a função da tiróide antes de iniciar o tratamento com o Sunitinib Krka e regularmente durante o tratamento. Se a tiróide não produzir hormônios suficientes, o doente pode ser tratado com hormônios da tiróide.
- Se o doente tiver ou tiver tido problemas do pâncreas ou vesícula biliar. Deve informar o médico se o doente tiver algum dos seguintes sintomas: dor na parte superior do abdômen, náuseas, vômitos e febre. Estes podem ser sintomas de pancreatite ou colecistite.
- Se o doente tiver ou tiver tido doenças do fígado. Deve informar o médico se o doente tiver algum dos seguintes sintomas de disfunção hepática: coceira, amarelamento dos olhos ou pele, urina escura e dor ou desconforto no lado direito do abdômen. O médico deve realizar exames de sangue para verificar a função hepática antes de iniciar o tratamento com o Sunitinib Krka, durante o tratamento e se houver sinais clínicos.
- Se o doente tiver ou tiver tido doenças renais. O médico vai controlar a função renal.
- Se o doente for submetido a uma cirurgia ou se recentemente foi submetido a uma cirurgia. O Sunitinib Krka pode afetar a cicatrização das feridas. O medicamento Sunitinib Krka é geralmente interrompido nos doentes antes da cirurgia. O médico decidirá quando reiniciar o Sunitinib Krka.
- Recomenda-se um exame dentário antes de iniciar o tratamento com o Sunitinib Krka:
- se o doente tiver ou tiver tido dor na boca, dor de dente e/ou maxila, inchaço ou ulceração na boca, formigamento ou sensação de peso na maxila, ou mobilidade dentária, deve informar imediatamente o médico oncologista e o dentista.
- se o doente precisar de tratamento dentário invasivo ou for submetido a uma cirurgia dentária, deve informar o dentista sobre o uso do Sunitinib Krka, especialmente se também estiver a tomar bisfosfonatos por via intravenosa. Os bisfosfonatos são medicamentos utilizados para prevenir problemas ósseos, que podem ser tomados devido a outra doença.
- Se o doente tiver ou tiver tido problemas da pele e tecido subcutâneo. Durante o tratamento com este medicamento, pode ocorrer pioderma gangrenosa (ulceração dolorosa da pele) ou fasciite necrotizante (infecção grave da pele e/ou tecidos moles, que pode ser fatal). Deve contactar imediatamente o médico se o doente tiver sintomas de infecção ao redor de uma lesão da pele, incluindo febre, dor, vermelhidão, inchaço ou drenagem de pus ou sangue. Estes problemas geralmente desaparecem após a interrupção do tratamento com o sunitinibe. Durante o tratamento com o sunitinibe, foram observadas reações graves na pele (síndrome de Stevens-Johnson, necrólise epidérmica tóxica, eritema multiforme), que inicialmente parecem manchas vermelhas com forma de alvo ou manchas redondas, frequentemente com bolhas centrais. A erupção pode transformar-se em bolhas extensas ou descamação da pele e pode ser fatal. Se o doente tiver uma erupção ou algum dos sintomas cutâneos mencionados, deve contactar imediatamente o médico.
- Se o doente tiver ou tiver tido convulsões. Deve informar o médico o mais rápido possível se o doente tiver hipertensão arterial, dor de cabeça ou perda de visão.
- Se o doente tiver diabetes. Nos doentes com diabetes, deve ser realizado um controlo regular do nível de açúcar no sangue para avaliar se é necessário ajustar a dose do medicamento anti-diabético, para minimizar o risco de hipoglicemia. Deve informar o médico o mais rápido possível se o doente tiver sintomas de hipoglicemia (cansaço, palpitações, suor excessivo, fome ou perda de consciência).
Crianças e adolescentes
O Sunitinib Krka não é recomendado para pessoas com menos de 18 anos.
Sunitinib Krka e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar
atualmente ou recentemente, incluindo os que são vendidos sem receita médica, e também sobre os medicamentos que o doente planeia tomar.
Alguns medicamentos podem afetar a concentração do Sunitinib Krka no organismo. Deve informar o médico se o doente estiver a tomar medicamentos que contenham as seguintes substâncias ativas:
- ketconazol, itraconazol - utilizados no tratamento de infecções fúngicas
- eritromicina, claritromicina, rifampicina - utilizados no tratamento de infecções
- ritonavir - utilizado no tratamento de infecções por HIV
- desametazona - corticosteroide utilizado em várias doenças (como doenças alérgicas e/ou respiratórias ou doenças da pele)
- fenitoína, carbamazepina, fenobarbital - utilizados no tratamento de epilepsia e outros estados neurológicos,
- produtos fitoterápicos que contenham erva-de-são-joão (Hypericum perforatum) - utilizados no tratamento de depressão e estados de ansiedade.
Uso do Sunitinib Krka com alimentos e bebidas
Durante o tratamento com o Sunitinib Krka, não deve beber suco de toranja.
Gravidez e amamentação
Se a doente estiver grávida ou a amamentar, suspeitar que pode estar grávida ou quando planeia ter
um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
As mulheres que possam engravidar devem utilizar um método anticoncepcional eficaz durante o tratamento com o Sunitinib Krka.
As mulheres que amamentam devem informar o médico. Não deve amamentar durante o tratamento com o Sunitinib Krka.
Condução de veículos e utilização de máquinas
Se ocorrer tontura ou cansaço acentuado, deve ter cuidado ao conduzir veículos e utilizar máquinas.
Sunitinib Krka contém sódio
Este medicamento contém menos de 1 mmol (23 mg) de sódio por cápsula, ou seja, o medicamento é considerado "livre de sódio".
3 Como tomar o Sunitinib Krka
Este medicamento deve ser sempre tomado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
O médico prescreverá a dose adequada para o doente, dependendo do tipo de tumor.
No caso de doentes a serem tratados por:
- GIST ou MRCC: a dose usual é de 50 mg tomados uma vez por dia durante 28 dias (4 semanas), seguidos de uma pausa de 14 dias (2 semanas) (sem medicamento), em ciclos de tratamento de 6 semanas.
- pNET: a dose usual é de 37,5 mg tomados uma vez por dia de forma contínua.
O médico determinará a dose adequada para o doente e o momento de interrupção do tratamento com o Sunitinib Krka.
O Sunitinib Krka pode ser tomado com ou sem alimentos.
Tomada do medicamento
As cápsulas do Sunitinib Krka não devem ser esmagadas, pois isso pode danificá-las. As cápsulas devem ser retiradas da embalagem através da abertura de um quadrado separado da embalagem.
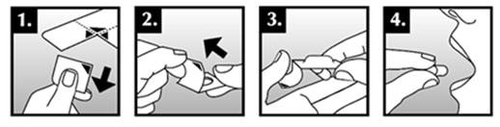
Para retirar a cápsula da embalagem, deve proceder da seguinte forma:
- 1. Segurar a borda da embalagem e separar um quadrado da embalagem, dobrando e arrancando na linha de perfuração.
- 2. Puxar a borda marcada da folha e retirá-la completamente.
- 3. Sacudir a cápsula para a mão.
- 4. Engolir a cápsula inteira.
Tomada de uma dose maior do que a recomendada de Sunitinib Krka
Se o doente tomar mais cápsulas do que o recomendado, deve contactar imediatamente o médico.
Pode ser necessária intervenção médica.
Omissão de uma dose de Sunitinib Krka
Não deve tomar uma dose dupla para compensar a dose omitida.
Se tiver alguma dúvida adicional sobre o uso deste medicamento, deve consultar o médico ou farmacêutico.
4 Efeitos secundários possíveis
Como qualquer medicamento, este medicamento pode causar efeitos secundários, embora não todos os doentes os experimentem.
Deve contactar imediatamente o médico se o doente experimentar algum dos seguintes efeitos secundários (ver também o ponto 2, "Informações importantes antes de tomar o Sunitinib Krka"):
- doenças cardíacas. Deve informar o médico se o doente se sentir muito cansado, tiver falta de ar ou inchaço nos pés e tornozelos. Estes podem ser sintomas de problemas cardíacos, que podem incluir insuficiência cardíaca e problemas com o músculo cardíaco (cardiomiopatia).
- doenças pulmonares ou dificuldades respiratórias. Deve informar o médico se o doente tiver tosse, dor no peito, falta de ar súbita ou tosse com sangue. Estes podem ser sintomas de um estado chamado embolia pulmonar, que ocorre quando coágulos sanguíneos se movem para os pulmões.
- disfunção renal. Deve informar o médico se o doente tiver alterações na frequência ou ausência de micção, que podem ser sintomas de insuficiência renal.
- sangramentos. Deve informar o médico se o doente tiver algum dos seguintes sintomas ou sangramento grave durante o tratamento com o Sunitinib Krka: dor e inchaço no abdômen; vômitos com sangue; fezes pretas e pegajosas; sangue na urina; dor de cabeça ou alterações da consciência; tosse com sangue ou expectoração de sangue dos pulmões ou vias respiratórias.
- destruição do tumor que leva à perfuração intestinal. Deve informar o médico se o doente tiver dor abdominal forte, febre, náuseas, vômitos, sangue nas fezes ou alterações na função intestinal.
Outros efeitos secundários do Sunitinib Krka podem incluir:
Muito frequentes(podem ocorrer em mais de 1 em cada 10 doentes)
- diminuição do número de plaquetas, glóbulos vermelhos e/ou glóbulos brancos (por exemplo, neutrófilos)
- falta de ar
- hipertensão arterial
- cansaço extremo, perda de força
- inchaço devido ao acúmulo de líquido sob a pele e ao redor dos olhos, erupção alérgica profunda
- dor e/ou irritação na boca, ulceração dolorosa e/ou inflamação, e/ou secura na boca, alterações do paladar, distúrbios gástricos, náuseas, vômitos, diarreia, constipação, dores e/ou inchaço abdominal, perda e/ou diminuição do apetite
- diminuição da atividade da tiróide (hipotireoidismo)
- tonturas
- dor de cabeça
- sangramento nasal
- dor nas costas, dores articulares
- dor nos braços e pernas
- amarelamento da pele e/ou pigmentação, excesso de pigmentação da pele, alteração da cor do cabelo, erupção nas palmas das mãos e nas plantas dos pés, erupção, secura da pele
- tosse
- febre
- dificuldades para dormir
Frequentes(podem ocorrer em menos de 1 em cada 10 doentes)
- coágulos sanguíneos nos vasos sanguíneos
- insuficiência cardíaca devido a um coágulo ou estreitamento das artérias coronárias
- dor no peito
- diminuição da quantidade de sangue bombeada pelo coração
- acúmulo de líquido, incluindo na área dos pulmões
- infecções
- complicação após uma infecção grave (sepse), que pode levar a danos nos tecidos, insuficiência de órgãos e morte
- diminuição do nível de açúcar no sangue (ver ponto 2, "Informações importantes antes de tomar o Sunitinib Krka").
- perda de proteína na urina, sometimes causando inchaço
- síndrome gripal
- resultados anormais de exames de sangue, incluindo enzimas pancreáticas e hepáticas
- nível elevado de ácido úrico no sangue
- hemorroidas, dor no ânus, sangramento gengival, dificuldade para engolir ou perda da capacidade de engolir
- sensação de queimadura ou dor na língua, inflamação da mucosa do trato gastrointestinal, excesso de gases no estômago ou intestinos
- perda de peso
- dor muscular-esquelética (dor muscular e óssea), fraqueza muscular, fadiga muscular, dor muscular, cãibras musculares
- secura nasal, sensação de congestão nasal
- lacrimação excessiva
- alterações da sensação na pele, coceira, descamação e inflamação da pele, bolhas, acne, despigmentação das unhas, perda de cabelo
- alterações da sensação nos membros
- alterações relacionadas com o aumento ou diminuição da sensibilidade, especialmente ao toque
- azia
- desidratação
- ondas de calor
- cor da urina anormal
- depressão
- arrepios
Pouco frequentes(podem ocorrer em menos de 1 em cada 100 doentes)
- reação grave na pele e/ou mucosa (síndrome de Stevens-Johnson, necrólise epidérmica tóxica, eritema multiforme)
- síndrome de lise tumorral, que é um grupo de complicações metabólicas que podem ocorrer durante o tratamento de câncer. Estas complicações são causadas pelos produtos da decomposição de células tumorais em decomposição e podem incluir: náuseas, falta de ar, arritmias cardíacas, cãibras musculares, convulsões, alterações na função renal e insuficiência renal aguda, que podem levar a alterações nos rins e insuficiência renal aguda.
- decomposição anormal dos músculos, que pode causar doenças renais (rabdomiólise).
- alterações anormais no cérebro, que podem causar um conjunto de sintomas que incluem dor de cabeça, desorientação, convulsões e perda de visão (síndrome de leucoencefalopatia posterior reversível)
- ulceração dolorosa da pele (piodermia gangrenosa)
- inflamação do fígado
- inflamação da tiróide
- lesões nos pequenos vasos sanguíneos chamadas de microangiopatia trombótica
Frequência desconhecida(frequência não pode ser estimada a partir dos dados disponíveis):
- dilatação e enfraquecimento da parede de um vaso sanguíneo ou ruptura da parede de um vaso sanguíneo (aneurisma e dissecção da artéria)
- falta de energia, confusão, sonolência, perda de consciência ou coma - estes sintomas podem ser sinais de um efeito tóxico do nível elevado de amônia no sangue no cérebro (encefalopatia hipermanmonêmica).
Notificação de efeitos secundários
Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Agência Nacional de Medicamentos e Produtos de Saúde
Al. Jerozolimskie 181C, 02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio da internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários pode ajudar a obter mais informações sobre a segurança do medicamento.
5 Como conservar o Sunitinib Krka
O medicamento deve ser conservado em um local fora do alcance e da vista das crianças.
Não deve tomar este medicamento após o prazo de validade impresso na caixa, frasco e blister após: EXP. O prazo de validade é o último dia do mês indicado.
Conservar na embalagem original para proteger da umidade.
Não há recomendações especiais para a temperatura de conservação do medicamento.
Não deve tomar este medicamento se notar que a embalagem está danificada ou se houver sinais de tentativas de abertura anterior.
Os medicamentos não devem ser jogados na canalização ou nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não são necessários. Este procedimento ajudará a proteger o meio ambiente.
6 Conteúdo do pacote e outras informações
O que contém o Sunitinib Krka
Sunitinib Krka 12,5 mg cápsulas duras
A substância ativa do medicamento é o sunitinibe. Cada cápsula dura contém sunitinibe malato equivalente a 12,5 mg de sunitinibe.
Os outros componentes são:
- Conteúdo da cápsula:povidona K30 LP, celulose microcristalina, croscarmelose sódica (ver ponto 2, "Sunitinib Krka contém sódio"), estearato de magnésio;
- Invólucro da cápsula:gelatina, dióxido de titânio (E 171), óxido de ferro vermelho (E 172), óxido de ferro amarelo (E 172).
- Tinta para impressão:lacas, dióxido de titânio (E 171), propilenoglicol.
Sunitinib Krka 25 mg cápsulas duras
A substância ativa do medicamento é o sunitinibe. Cada cápsula dura contém sunitinibe malato equivalente a 25 mg de sunitinibe.
Os outros componentes são:
- Conteúdo da cápsula: povidona K30 LP, celulose microcristalina, croscarmelose sódica (ver ponto 2, "Sunitinib Krka contém sódio"), estearato de magnésio;
- Invólucro da cápsula:gelatina, dióxido de titânio (E 171), óxido de ferro vermelho (E 172), óxido de ferro amarelo (E 172), óxido de ferro preto (E 172).
- Tinta para impressão:lacas, dióxido de titânio (E 171), propilenoglicol.
Sunitinib Krka 50 mg cápsulas duras
A substância ativa do medicamento é o sunitinibe. Cada cápsula dura contém sunitinibe malato equivalente a 50 mg de sunitinibe.
Os outros componentes são:
- Conteúdo da cápsula: povidona K30 LP, celulose microcristalina, croscarmelose sódica (ver ponto 2, "Sunitinib Krka contém sódio"), estearato de magnésio;
- Invólucro da cápsula:gelatina, dióxido de titânio (E 171), óxido de ferro vermelho (E 172), óxido de ferro amarelo (E 172), óxido de ferro preto (E 172).
- Tinta para impressão:lacas, óxido de ferro preto (E 172), propilenoglicol
Como é o Sunitinib Krka e o que contém o pacote
Sunitinib Krka 12,5 mg cápsulas duras
Sunitinib Krka 12,5 mg: cápsula de gelatina dura com tampa laranja e corpo laranja, com impressão em tinta branca: "SNB" e "12.5" no corpo.
A cápsula é preenchida com pó laranja. Tamanho da cápsula: 4 (comprimento aproximado de 14 mm).
Sunitinib Krka 25 mg cápsulas duras
Sunitinib Krka 25 mg: cápsula de gelatina dura com tampa caramelo (marrom claro) e corpo laranja, com impressão em tinta branca: "SNB" e "25" no corpo.
A cápsula é preenchida com pó laranja. Tamanho da cápsula: 3 (comprimento aproximado de 16 mm).
Sunitinib Krka 50 mg cápsulas duras
Sunitinib Krka 50 mg: cápsula de gelatina dura com tampa caramelo (marrom claro) e corpo caramelo (marrom claro), com impressão em tinta preta "SNB" e "50" no corpo. A cápsula é preenchida com pó laranja. Tamanho da cápsula: 1EL (alongada; comprimento aproximado de 20 mm).
O medicamento é fornecido em frascos de HDPE com fecho de PP protegido contra crianças, com um agente de absorção de umidade, contendo 30 cápsulas duras em uma caixa de cartão, e em blisters unitários com um agente de absorção de umidade, contendo 7 x 1, 10 x 1, 14 x 1, 20 x 1, 21 x 1, 28 x 1 ou 30 x 1 cápsulas duras, em uma caixa de cartão.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização:
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Eslovênia
Fabricante:
Synthon BV, Microweg 22, 6545CM Nijmegen, Holanda
Synthon Hispania S.L., Calle De Castello 1, 08830 Sant Boi de Llobregat, Barcelona, Espanha
Synthon s.r.o., Brnĕnská 32/čp. 597, 678 01 Blansko, República Checa
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Eslovênia
KRKA – FARMA d.o.o., V. Holjevca 20/E, 10450 Jastrebarsko, Croácia
Para obter informações mais detalhadas sobre este medicamento, deve contactar o representante local do titular da autorização de comercialização:
KRKA-POLSKA Sp. z o.o.
ul. Równoległa 5
02-235 Varsóvia
Tel. 22 57 37 500
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu sob os seguintes nomes:
| Bélgica, República Checa, Dinamarca, Estônia, Finlândia, França, Hungria, Croácia, Irlanda, Islândia, Letônia, Lituânia, Noruega, Polônia, Suécia, Eslováquia, Eslovênia, | Sunitinib Krka |
| Bulgária | Сунитиниб Крка |
| Países Baixos | Sunitinib HCS |
Data da última revisão do folheto:13.08.2024
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorKrka, d.d., Novo mesto Krka-Farma d.o.o. Synthon B.V. Synthon Hispania S.L. Synthon s.r.o.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
Consulte um médico online
Tem perguntas sobre este medicamento ou sintomas? Obtenha orientação de um médico qualificado, de forma prática e segura.














