
Spiriva Respimat

Pergunte a um médico sobre a prescrição de Spiriva Respimat

Como usar Spiriva Respimat
Folheto informativo para o doente
Spiriva Respimat, 2,5 microgramas/dose medida, solução para inalação
Tiotrópio
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para poder reler em caso de necessidade.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que tenham os mesmos sintomas que o seu.
- Se ocorrerem efeitos indesejados, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Spiriva Respimat e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Spiriva Respimat
- 3. Como tomar o medicamento Spiriva Respimat
- 4. Efeitos indesejados
- 5. Como conservar o medicamento Spiriva Respimat
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Spiriva Respimat e para que é utilizado
O medicamento Spiriva Respimat facilita a respiração dos doentes com doença pulmonar obstrutiva crónica (DPOC) ou asma. A DPOC é uma doença pulmonar crónica que causa falta de ar e tosse. A DPOC está associada à inflamação crónica dos brônquios e enfisema. A asma é uma doença crónica caracterizada por inflamação das vias respiratórias e sua constrição.
A DPOC e a asma são doenças crónicas, por isso o medicamento Spiriva Respimat deve ser tomado diariamente, e não apenas quando ocorrem problemas respiratórios ou outros sintomas. No tratamento da asma, o medicamento Spiriva Respimat deve ser tomado como medicamento adjuvante com corticosteroides inalatórios e beta-2-agonistas de longa duração.
O Spiriva Respimat é um broncodilatador de longa duração que ajuda a abrir as vias respiratórias e facilita a entrada de ar nos pulmões. A utilização regular do medicamento Spiriva Respimat também pode ajudar a reduzir a falta de ar persistente associada à doença e a melhorar a qualidade de vida diária. A utilização diária do medicamento Spiriva Respimat também ajudará a prevenir o agravamento súbito e temporário dos sintomas da DPOC, que pode durar vários dias.
Para tomar corretamente o medicamento Spiriva Respimat e utilizá-lo, ver ponto 3. Como tomar o medicamento Spiriva Respimat e as instruções para o uso do inhalador Respimat reutilizável no final do folheto.
2. Informações importantes antes de tomar o medicamento Spiriva Respimat
Quando não tomar o medicamento Spiriva Respimat:
- se o doente tiver alergia (hipersensibilidade) ao tiotrópio ou a qualquer outro componente deste medicamento (listados no ponto 6),
- se o doente tiver alergia (hipersensibilidade) à atropina ou seus derivados, como ipratrópio ou oxitrópio.
Precauções e advertências
Antes de tomar o medicamento Spiriva Respimat, deve consultar o médico ou farmacêutico.
Deve consultar o médico se o doente tiver glaucoma de ângulo fechado, problemas da próstata ou dificuldades em urinar.
Se o doente tiver problemas renais, deve consultar o médico.
Ao inalar o medicamento Spiriva Respimat, deve ter cuidado para não deixar que o medicamento entre em contato com os olhos, pois podem ocorrer: dor nos olhos ou desconforto, visão turva, visão de halo colorido em torno de uma fonte de luz ou alterações na visão das cores com vermelhidão dos olhos (glaucoma de ângulo fechado). Os efeitos indesejados nos olhos podem ser acompanhados de dor de cabeça, náuseas ou vómitos. Se o medicamento entrar em contato com os olhos, deve enxaguar os olhos com água morna, interromper a utilização do brometo de tiotrópio e procurar imediatamente um médico para obter orientação adicional.
Se a respiração se tornar difícil ou ocorrer erupção cutânea, inchaço ou coceira logo após a inalação, deve interromper a utilização do medicamento e procurar imediatamente um médico.
A secura da mucosa bucal que ocorre durante a utilização de um medicamento com ação anticolinérgica pode causar cáries dentárias após um longo período, por isso é importante manter a higiene bucal.
O medicamento Spiriva Respimat é indicado para o tratamento de manutenção da doença pulmonar obstrutiva crónica ou asma. Não tome este medicamento para tratar ataques súbitos de falta de ar ou chiado .Para esse fim, o médico prescreverá um outro inhalador (um "medicamento de resgate"). Deve seguir as instruções do médico.
Se o doente foi aconselhado a tomar o medicamento Spiriva Respimat para tratar a asma, deve tomá-lo como medicamento adjuvante para o tratamento que inclui um corticosteroide inalatório e beta-2-agonistas de longa duração. Deve continuar a tomar o corticosteroide inalatório de acordo com as instruções do médico, mesmo que se sinta melhor.
Se o doente teve um ataque cardíaco nos últimos 6 meses, teve problemas cardíacos ou arritmias cardíacas potencialmente fatais nos últimos 12 meses, deve informar o médico. Isso permitirá que o médico decida se o medicamento Spiriva Respimat ainda é adequado para a utilização.
Não tome o medicamento Spiriva Respimat mais de uma vez por dia.
Deve também consultar o médico se ocorrer dificuldade em respirar.
Os doentes com fibrose cística devem informar o médico, pois o medicamento Spiriva Respimat pode agravar os sintomas da fibrose cística.
Crianças e adolescentes
O medicamento Spiriva Respimat não é recomendado para crianças com menos de 6 anos de idade.
Spiriva Respimat e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que está tomando atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar, incluindo os medicamentos sem prescrição médica.
Em particular, deve informar o médico ou farmacêutico sobre a utilização de outros medicamentos com ação anticolinérgica, como ipratrópio ou oxitrópio.
Não foram observados efeitos indesejados durante a utilização do medicamento Spiriva Respimat com outros medicamentos utilizados no tratamento da DPOC e asma, como medicamentos de resgate inalatórios (por exemplo, salbutamol), metilxantinas (por exemplo, teofilina), medicamentos antihistamínicos, medicamentos mucolíticos (por exemplo, ambroxol), medicamentos anti-leucotrienos (por exemplo, montelucaste), cromonas, medicamentos anti-IgE (por exemplo, omalizumabe) e (ou) corticosteroides inalatórios ou orais (por exemplo, budesonida, prednisolona).
Gravidez e amamentação
Se a paciente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico antes de tomar este medicamento.
Não deve tomar este medicamento, a menos que sob orientação médica.
Condução de veículos e utilização de máquinas
Não foram realizados estudos sobre o efeito do medicamento na capacidade de conduzir veículos ou operar máquinas. Se ocorrer tontura ou visão turva, a capacidade de conduzir veículos ou operar máquinas pode estar prejudicada.
Spiriva Respimat contém cloreto de benzalcônio
Este medicamento contém 0,0011 mg de cloreto de benzalcônio em cada dose inalada.
O cloreto de benzalcônio pode causar chiado ou problemas respiratórios (constrição brônquica), especialmente em pacientes com asma.
3. Como tomar o medicamento Spiriva Respimat
Este medicamento deve ser sempre tomado de acordo com as instruções do médico ou farmacêutico. Em caso de dúvidas, deve consultar o médico ou farmacêutico.
O medicamento Spiriva Respimat é destinado apenas à inalação.
A dose recomendada para pacientes com 6 anos de idade ou mais é:
O medicamento Spiriva Respimat atua durante 24 horas, por isso deve ser tomado UMA VEZ POR DIA, sempre que possível no mesmo horário.
Em cada utilização, deve realizar DUAS INALAÇÕES.
Como a DPOC e a asma são doenças crónicas, o medicamento Spiriva Respimat deve ser tomado diariamente, e não apenas quando ocorrem problemas respiratórios. Não deve exceder a dose recomendada.
Deve certificar-se de que está utilizando corretamente o inhalador Respimat reutilizável. As instruções para o uso do inhalador Respimat reutilizável estão no final do folheto, ver ponto "Instruções para o uso do inhalador Respimat reutilizável".
Utilização em crianças e adolescentes
O medicamento Spiriva Respimat não é recomendado para crianças com menos de 6 anos de idade, devido à falta de dados sobre a segurança e eficácia.
Tomada de mais do que a dose recomendada de medicamento Spiriva Respimat
Em caso de tomada de mais do que a dose recomendada de medicamento Spiriva Respimat (mais de duas inalações por dia), deve procurar imediatamente um médico.
O doente pode ter um aumento do risco de efeitos indesejados, como secura da mucosa bucal, constipação, dificuldade em urinar, taquicardia ou visão turva.
Omissão de uma dose de medicamento Spiriva Respimat
Em caso de omissão de uma dose (DUAS INALAÇÕES UMA VEZ POR DIA), deve tomar a dose omissa o mais rápido possível, mas não deve tomar duas doses ao mesmo tempo ou no mesmo dia. A próxima dose deve ser tomada no horário habitual.
Interrupção da utilização do medicamento Spiriva Respimat
Antes de interromper a utilização do medicamento Spiriva Respimat, deve consultar o médico ou farmacêutico.
Após a interrupção da utilização do medicamento Spiriva Respimat, os sintomas da DPOC e asma podem piorar.
Em caso de dúvidas adicionais sobre a utilização deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos indesejados
Como qualquer medicamento, este medicamento pode causar efeitos indesejados, embora não ocorram em todos.
A avaliação dos efeitos indesejados foi realizada com base na seguinte convenção de frequência:
Fremente:
pode ocorrer em menos de 1 em 10 doentes
Não muito frequente:
pode ocorrer em menos de 1 em 100 doentes
Raro:
pode ocorrer em menos de 1 em 1000 doentes
Frequência desconhecida:
a frequência não pode ser estimada com base nos dados disponíveis
Os seguintes efeitos indesejados ocorreram em doentes que tomaram o medicamento e foram classificados por frequência como frequentes, não muito frequentes, raros ou de frequência desconhecida.
| Efeito indesejado | Frequência em DPOC | Frequência em asma |
| Secura da mucosa bucal | Frequente | Não muito frequente |
| Rouquidão (disfonia) | Não muito frequente | Não muito frequente |
| Tosse | Não muito frequente | Não muito frequente |
| Dor de cabeça | Não muito frequente | Não muito frequente |
| Faringite | Não muito frequente | Não muito frequente |
| Dor ao urinar (disúria) | Não muito frequente | Frequência desconhecida |
| Tontura | Não muito frequente | Não muito frequente |
| Infecções fúngicas da boca e garganta (candidíase da boca e garganta) | Não muito frequente | Não muito frequente |
| Dificuldade em urinar (retenção urinária) | Não muito frequente | Frequência desconhecida |
| Constipação | Não muito frequente | Raro |
| Erupção cutânea | Não muito frequente | Não muito frequente |
| Coceira (prurido) | Não muito frequente | Raro |
| Aumento da pressão intraocular | Raro | Frequência desconhecida |
| Reações alérgicas graves que causam inchaço dos lábios e face ou garganta (angioedema) | Raro | Raro |
| Insônia | Raro | Não muito frequente |
| Batimento cardíaco irregular (fibrilação atrial, taquicardia supraventricular) | Raro | Frequência desconhecida |
| Palpitações | Raro | Não muito frequente |
| Sangramento nasal | Raro | Raro |
| Faringite | Raro | Frequência desconhecida |
| Taquicardia | Raro | Frequência desconhecida |
| Aperto no peito, com tosse, chiado ou falta de ar logo após a inalação (constrição brônquica) | Raro | Não muito frequente |
| Dificuldade em engolir (disfagia) | Raro | Frequência desconhecida |
| Efeito indesejado | Frequência em DPOC | Frequência em asma |
| Visão de halo colorido em torno de uma fonte de luz ou alterações na visão das cores com vermelhidão dos olhos (glaucoma) | Raro | Frequência desconhecida |
| Visão turva | Raro | Frequência desconhecida |
| Faringite | Raro | Frequência desconhecida |
| Cáries dentárias | Raro | Frequência desconhecida |
| Gengivite | Raro | Raro |
| Urticária | Raro | Raro |
| Infecção da pele ou úlceras da pele | Raro | Frequência desconhecida |
| Pele seca | Raro | Frequência desconhecida |
| Infecções do trato urinário | Raro | Raro |
| Refluxo gastroesofágico (doença de refluxo gastroesofágico) | Raro | Frequência desconhecida |
| Hipersensibilidade, incluindo reações imediatas | Frequência desconhecida | Raro |
| Estomatite | Frequência desconhecida | Raro |
| Desidratação | Frequência desconhecida | Frequência desconhecida |
| Sinusite | Frequência desconhecida | Frequência desconhecida |
| Obstrução intestinal ou falta de movimento intestinal (obstrução intestinal, incluindo obstrução paralítica) | Frequência desconhecida | Frequência desconhecida |
| Náuseas | Frequência desconhecida | Frequência desconhecida |
| Reações alérgicas graves (reações anafiláticas) | Frequência desconhecida | Frequência desconhecida |
| Artralgia | Frequência desconhecida | Frequência desconhecida |
Após a utilização do medicamento Spiriva Respimat, reações alérgicas imediatas, como erupção cutânea, urticária, inchaço da boca e face ou dificuldade respiratória súbita (angioedema) ou outras reações de hipersensibilidade (como hipotensão súbita ou tontura), podem ocorrer sozinhas ou como parte de uma reação alérgica grave (reação anafilática).
Assim como com outros medicamentos inalatórios, após a inalação do medicamento Spiriva Respimat, podem ocorrer aperto no peito, tosse, chiado ou falta de ar (constrição brônquica) em alguns doentes. Se ocorrer algum desses sintomas, deve procurar imediatamente um médico.
Notificação de efeitos indesejados
Se ocorrerem efeitos indesejados, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Os efeitos indesejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Indesejados de Medicamentos da Agência Nacional de Vigilância Sanitária, Rua São Paulo, 1000, 04001-300 São Paulo, SP, Brasil, telefone: +55 11 3201 1000, fax: +55 11 3201 1001, site: https://www.anvisa.gov.br.
Os efeitos indesejados também podem ser notificados ao titular da autorização de comercialização. A notificação de efeitos indesejados permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Spiriva Respimat
Deve conservar o medicamento em um local seguro e fora do alcance das crianças.
Não utilize o medicamento após o prazo de validade impresso na embalagem e na etiqueta do cartucho de medicamento, após EXP. O prazo de validade é o último dia do mês indicado.
Não congele.
Prazo de validade após a abertura:
Deve substituir o cartucho de medicamento no máximo 3 meses após a colocação no inhalador.
Não utilize o inhalador Respimat reutilizável por mais de 1 ano.
Recomenda-se utilizar 6 cartuchos de medicamento por inhalador.
Observação: A funcionalidade do inhalador Respimat reutilizável foi demonstrada em estudos para 540 inalações (correspondente a 9 cartuchos de medicamento).
Os medicamentos não devem ser jogados na canalização ou lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Spiriva Respimat
O princípio ativo do medicamento é tiotrópio. A dose medida contém 2,5 microgramas de tiotrópio em cada inalação (cada dose terapêutica consiste em duas inalações), o que corresponde a 3,124 microgramas de brometo de tiotrópio monohidratado. A dose medida é a dose que está disponível para o doente após a passagem pelo bocal do inhalador.
Os outros componentes são: cloreto de benzalcônio, edetato dissódico, água purificada e ácido clorídrico 3,6% para ajustar o pH.
Como é o medicamento Spiriva Respimat e que embalagens estão disponíveis
O medicamento Spiriva Respimat 2,5 microgramas/dose medida consiste em um cartucho de solução para inalação e um inhalador Respimat. O cartucho deve ser colocado no inhalador antes da primeira utilização.
Embalagem unitária: 1 inhalador Respimat reutilizável e 1 cartucho de medicamento que fornece 60 inalações (30 doses terapêuticas).
Embalagem tripla: 1 inhalador Respimat reutilizável e 3 cartuchos de medicamento, cada um fornecendo 60 inalações (30 doses terapêuticas).
Embalagem unitária de reposição: 1 cartucho de medicamento que fornece 60 inalações (30 doses terapêuticas).
Embalagem tripla de reposição: 3 cartuchos de medicamento, cada um fornecendo 60 inalações (30 doses terapêuticas).
Nem todos os tamanhos de embalagem podem estar disponíveis.
Responsável e fabricante
Responsável:
Boehringer Ingelheim International GmbH
Binger Strasse 173
55216 Ingelheim am Rhein
Alemanha
Fabricante:
Boehringer Ingelheim Pharma GmbH & Co. KG
Binger Strasse 173
55216 Ingelheim am Rhein
Alemanha
Boehringer Ingelheim España, SA
c/ Prat de la Riba, 50
08174 Sant Cugat del Vallès (Barcelona)
Espanha
Boehringer Ingelheim France
100-104 Avenue de France
75013 Paris
França
Para obter mais informações, deve contatar o representante do responsável:
Portugal
Boehringer Ingelheim Portugal
Tel: +351 21 412 6000
Este medicamento está autorizado para comercialização nos estados membros do Espaço Econômico Europeu e no Reino Unido (Irlanda do Norte) sob as seguintes denominações:
Áustria, Liechtenstein, Bélgica, Luxemburgo, Chipre, República Checa, Dinamarca, Estônia, Finlândia, França, Alemanha, Grécia, Hungria, Islândia, Irlanda, Malta, Reino Unido (Irlanda do Norte), Itália, Letônia, Lituânia, Países Baixos, Noruega, Polônia, Portugal, Romênia, Eslováquia, Eslovênia, Espanha, Suécia: Spiriva Respimat
Bulgária: Спирива Респимат
Data da última atualização do folheto: 12/2024
Instruções para o uso do inhalador Respimat reutilizável
O Respimat é um inhalador que produz um aerossol para inalação. O Respimat é destinado apenas a um doente. Um cartucho de medicamento fornece várias doses. O inhalador Respimat reutilizável permite a substituição do cartucho de medicamento e pode ser utilizado com até 6 cartuchos.
Deve ler as instruções a seguir antes de começar a utilizar o medicamento Spiriva Respimat.
Este inhalador deve ser utilizado apenas UMA VEZ POR DIA. Em cada utilização, deve inalar o medicamento liberado em DUAS INALAÇÕES.
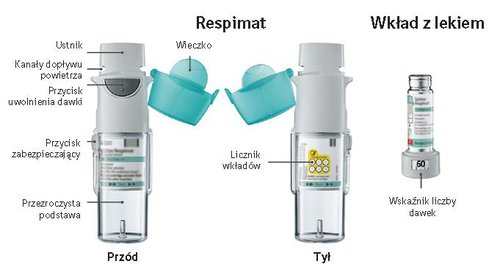
- Se o Spiriva Respimat não foi utilizado por mais de 7 dias, deve realizar uma inalação com o inhalador apontado para baixo.
- Se o Spiriva Respimat não foi utilizado por mais de 21 dias, deve repetir as ações descritas nos pontos 4-6 da seção "Preparação para o uso" até que uma névoa seja visível. Em seguida, repita as ações descritas nos pontos 4-6 mais três vezes.
Como cuidar do inhalador Respimat reutilizável
Deve limpar o bocal, incluindo a parte metálica no interior, com um pano úmido ou lenço pelo menos uma vez por semana.
Uma pequena alteração na cor do bocal não afeta o funcionamento do inhalador Respimat reutilizável.
Se necessário, pode limpar a superfície externa do inhalador Respimat reutilizável com um pano úmido.
Quando substituir o inhalador
Após a utilização do inhalador com 6 cartuchos, deve adquirir um novo conjunto de Spiriva Respimat que inclui um inhalador. O inhalador Respimat reutilizável não deve ser utilizado por mais de 1 ano após a colocação do primeiro cartucho.


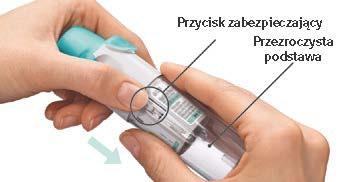
Preparação para o uso
|  |
|  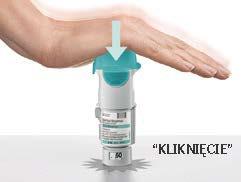 |
|  |
 | |
|  |
|  |
|  |
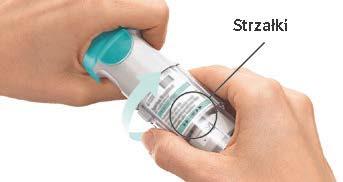
Uso diário
GIRE
| 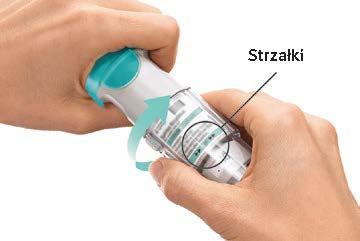 |
ABRA
|  |
PRESSIONE
| 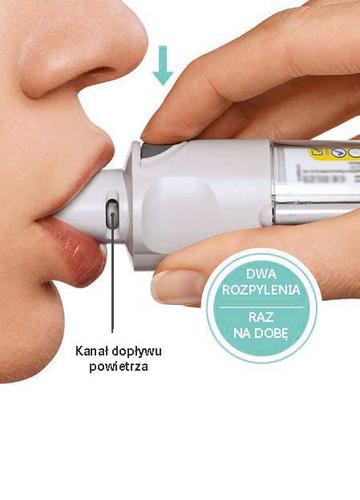 |
Quando substituir o cartucho de medicamento Spiriva Respimat
O indicador de doses mostra o número de inalações restantes no cartucho de medicamento.

Restam 60 inalações

Restam menos de 10 inalações. Deve adquirir um novo cartucho de medicamento.

O cartucho de medicamento está vazio. Gire a base transparente para liberá-lo.
O inhalador agora está bloqueado. Remova o cartucho de medicamento do inhalador Respimat reutilizável.
Coloque um novo cartucho de medicamento no inhalador até ouvir um clique (ver ponto 2).
O novo cartucho colocado será mais proeminente do que o cartucho colocado inicialmente (continue a partir do ponto 3). Lembre-se de colocar a base transparente no lugar para desbloquear o inhalador.
Respostas às perguntas mais frequentes
Está tendo dificuldade em colocar o cartucho de medicamento profundamente o suficiente.
Você girou a base transparente antes de colocar o cartucho de medicamento?
Abra a tampa, pressione o botão de liberação da dose e, em seguida, coloque o cartucho de medicamento.
Você está substituindo o cartucho?
O próximo cartucho novo será mais proeminente do que o primeiro cartucho. Coloque-o até ouvir um clique e, em seguida, coloque a base transparente no lugar.
Não consigo pressionar o botão de liberação da dose.
Você colocou a base transparente no lugar?Se não, coloque a base transparente no lugar. O inhalador Respimat reutilizável funciona apenas com a base transparente no lugar.
Você girou a base transparente?Se não, gire a base transparente com um movimento contínuo até ouvir um clique (meio giro).
O indicador de doses no cartucho de medicamento mostra uma seta branca em um fundo vermelho?
Seu cartucho de medicamento está vazio. Coloque um novo cartucho e coloque a base transparente no lugar.
Após o uso, está tendo dificuldade em remover o cartucho de medicamento.
Puxe e gire o cartucho de medicamento.
Não consigo girar ou colocar a base transparente no lugar.
A base transparente está solta e o indicador de doses no cartucho de medicamento mostra uma seta branca em um fundo vermelho?
Seu cartucho de medicamento está vazio.Coloque um novo cartucho.
Meu inhalador Spiriva Respimat está se esvaziando muito rapidamente.
Você está utilizando o Spiriva Respimat de acordo com as instruções (duas inalações uma vez por dia)?Cada cartucho de medicamento contém medicamento para 30 dias, quando utilizado duas inalações uma vez por dia.
Você está ativando o inhalador Spiriva Respimat com frequência para verificar o funcionamento?Após a preparação do inhalador Spiriva Respimat para o uso, não há necessidade de verificar o funcionamento se for utilizado diariamente.
Você está removendo e colocando a base transparente no lugar com frequência?Não deve remover a base transparente antes de esvaziar o cartucho. A cada remoção da base transparente sem substituir o cartucho, o contador de doses registra uma inalação e a quantidade de doses restantes é reduzida.
Meu inhalador Spiriva Respimat não está funcionando.
Você colocou o cartucho de medicamento?Se não, coloque o cartucho de medicamento. Após a montagem do conjunto Spiriva Respimat, não remova a base transparente ou o cartucho de medicamento até que o cartucho esteja vazio.
Você repetiu as ações descritas nos pontos Girar, Abrir, Pressionar menos de três vezes após a colocação do cartucho de medicamento?
Repetiu as ações descritas nos pontos Girar, Abrir, Pressionar três vezes após a colocação do cartucho de medicamento?Repita as ações descritas nos pontos Girar, Abrir, Pressionar três vezes após a colocação do cartucho de medicamento, como mostrado nos pontos 4-6 da seção "Preparação para o uso".
O indicador de doses no cartucho de medicamento mostra uma seta branca em um fundo vermelho?
Seu cartucho de medicamento está vazio. Coloque um novo cartucho.
Meu inhalador Spiriva Respimat está se ativando sozinho.
A tampa estava aberta enquanto girava a base transparente?Feche a tampa e, em seguida, gire a base transparente.
Você pressionou o botão de liberação da dose enquanto girava a base transparente?Feche a tampa para cobrir o botão de liberação da dose e, em seguida, gire a base transparente.
Você parou de girar a base transparente antes de ouvir o clique?Gire a base transparente com um movimento contínuo até ouvir um clique (meio giro). O contador de doses registra cada giro incompleto e a quantidade de doses restantes é reduzida.
A tampa estava aberta ao substituir o cartucho de medicamento?Feche a tampa e, em seguida, substitua o cartucho.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorBoehringer Ingelheim Espana S.A. Boehringer Ingelheim France Boehringer Ingelheim Pharma GmbH & Co. KG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Spiriva RespimatForma farmacêutica: Pó, 18 mcgSubstância ativa: tiotropium bromideFabricante: Ferrer Internacional, S.A.Requer receita médicaForma farmacêutica: Pó, 10 mcgSubstância ativa: tiotropium bromideFabricante: Actavis Ltd. Laboratorios Liconsa S.A. Teva Operations Poland Sp. z o.o. Teva Pharma B.V.Requer receita médicaForma farmacêutica: Pó, 18 mcg/dose medidaSubstância ativa: tiotropium bromideRequer receita médica
Alternativas a Spiriva Respimat noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Spiriva Respimat em Ucrania
Alternativa a Spiriva Respimat em España
Médicos online para Spiriva Respimat
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Spiriva Respimat – sujeita a avaliação médica e regras locais.














