
Smoflipid

Pergunte a um médico sobre a prescrição de Smoflipid

Como usar Smoflipid
Folheto informativo: informação para o utilizador
SMOFlipid, 200 mg/ml, emulsão para infusão
produto composto
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
Deve guardar este folheto, para que possa relê-lo se necessário.
Em caso de dúvidas, deve consultar um médico ou enfermeiro.
Se o paciente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é SMOFlipid e para que é utilizado
- 2. Informações importantes antes de tomar SMOFlipid
- 3. Como tomar SMOFlipid
- 4. Efeitos não desejados
- 5. Como conservar SMOFlipid
- 6. Conteúdo do pacote e outras informações
1. O que é SMOFlipid e para que é utilizado
SMOFlipid contém quatro diferentes gorduras (lipídios): óleo de soja, triglicerídeos de cadeia média, óleo de oliva e óleo de peixe rico em ácidos graxos ômega-3. O líquido é uma mistura de gorduras e água, ou seja, uma "emulsão lipídica".
- A ação do medicamento consiste em fornecer energia e ácidos graxos ao organismo.
- O medicamento é administrado por via intravenosa, através de uma infusão ou bomba de infusão. O pessoal médico qualificado administra SMOFlipid a pacientes para os quais outras formas de nutrição são inadequadas, impossíveis ou contraindicadas.
2. Informações importantes antes de tomar SMOFlipid
Não tome SMOFlipid se:
- for alérgico ao óleo de soja, triglicerídeos de cadeia média, óleo de oliva, óleo de peixe ou a qualquer outro componente deste medicamento (listados no ponto 6);
- for alérgico a produtos que contenham peixe, ovos, soja ou amendoins;
- tiver excesso de gordura no sangue (hiperlipidemia grave);
- tiver insuficiência renal ou hepática grave;
- tiver distúrbios graves da coagulação do sangue (distúrbios da coagulação);
- estiver em choque;
- tiver líquido nos pulmões (edema pulmonar), excesso de líquido no organismo (sobrecarga hídrica) ou insuficiência cardíaca (causada por excesso de líquido no organismo);
- estiver em estado geral instável, por exemplo, trauma grave, ataque cardíaco, acidente vascular cerebral, embolia, acidose metabólica (distúrbio metabólico que causa alto nível de ácidos no sangue) ou diabetes descontrolada, infecção grave (sepse) e desidratação.
Precauções e advertências
Antes de iniciar o tratamento com SMOFlipid, deve informar o médico ou enfermeiro se tiver níveis elevados de gordura no sangue devido à falta de capacidade do organismo de eliminar a gordura (metabolismo lipídico alterado).
Quando administrado a recém-nascidos e crianças com menos de 2 anos, a solução (no saco e no conjunto de administração) deve ser protegida da luz até o final da administração. A exposição de SMOFlipid à luz, especialmente após a adição de oligoelementos e (ou) vitaminas, pode levar à formação de peróxidos e outros produtos de degradação, o que pode ser minimizado protegendo-o da luz.
Reações alérgicas
Se ocorrer uma reação alérgica durante o tratamento com SMOFlipid, deve interromper imediatamente o tratamento. Deve informar imediatamente o médico ou enfermeiro se ocorrerem os seguintes sintomas durante a infusão:
- febre (temperatura elevada);
- calafrios;
- erupção cutânea;
- dificuldade para respirar.
Crianças
Deve consultar um médico ou enfermeiro se o medicamento for administrado a um recém-nascido que tenha:
- níveis elevados de bilirrubina no sangue (hiperbilirrubinemia);
- hipertensão pulmonar. Durante a administração prolongada de SMOFlipid a recém-nascidos, o médico prescreverá exames de sangue para monitorar a saúde do paciente.
SMOFlipid e outros medicamentos
Deve informar o médico sobre todos os medicamentos que está tomando ou planeia tomar.
Em particular, deve informar o médico se estiver tomando ou tiver tomado recentemente medicamentos que afetam a coagulação do sangue, como a warfarina e a heparina.
- SMOFlipid contém vitamina K, que pode afetar a warfarina. No entanto, a quantidade de vitamina K em SMOFlipid é tão pequena que não deve causar problemas.
- A heparina administrada em doses clínicas pode aumentar temporariamente os níveis de ácidos graxos no sangue, devido à liberação de ácidos graxos dos tecidos para a circulação sanguínea, seguida de uma diminuição na eliminação de ácidos graxos do sangue (diminuição da clearance de triglicerídeos).
Gravidez e amamentação
Não há dados sobre o uso de SMOFlipid em mulheres grávidas ou em período de amamentação. Portanto, SMOFlipid só deve ser administrado a mulheres grávidas ou em período de amamentação se o médico considerar que é necessário.
Se estiver grávida, amamentando, acha que pode estar grávida ou planeia engravidar, deve consultar um médico ou farmacêutico antes de tomar este medicamento.
Condução de veículos e uso de máquinas
Não se aplica, pois o medicamento é utilizado em ambiente hospitalar.
SMOFlipid contém sódio
Este medicamento contém 5 mmol (115 mg) de sódio por 1000 ml. Deve ser considerado em pacientes que controlam a ingestão de sódio na dieta.
3. Como tomar SMOFlipid
SMOFlipid é administrado por via intravenosa, através de uma infusão ou bomba de infusão.
O médico determina a dose individual com base na idade, peso e capacidade do paciente de utilizar a gordura administrada.
Quando administrado a recém-nascidos e crianças com menos de 2 anos, a solução (no saco e no conjunto de administração) deve ser protegida da luz até o final da administração (ver ponto 2).
Informações detalhadas sobre a posologia e administração podem ser encontradas no final do folheto, no ponto "Informações destinadas apenas ao pessoal médico qualificado".
Uso de dose maior do que a recomendada de SMOFlipid
Se o paciente tomar uma dose maior do que a recomendada de SMOFlipid, há risco de absorção excessiva de gordura e problemas de metabolismo lipídico. Isso é conhecido como "síndrome de sobrecarga lipídica". Mais informações podem ser encontradas no ponto 4. Efeitos não desejados.
4. Efeitos não desejados
Como qualquer medicamento, SMOFlipid pode causar efeitos não desejados, embora não todos os pacientes os experimentem.
Síndrome de sobrecarga lipídica
A síndrome de sobrecarga lipídica ocorre quando o organismo tem problemas para metabolizar as gorduras devido à administração excessiva de SMOFlipid. Também pode ocorrer devido a uma mudança repentina no estado de saúde do paciente (por exemplo, problemas renais ou infecção). Os sintomas possíveis incluem níveis elevados de gordura no sangue (hiperlipidemia) e nos tecidos, febre, distúrbios na função de vários órgãos e coma. Todos esses sintomas geralmente desaparecem após a interrupção da infusão.
Efeitos não desejados frequentes(podem ocorrer em até 1 em 10 pacientes):
- aumento leve da temperatura corporal.
Efeitos não desejados menos frequentes(podem ocorrer em até 1 em 100 pacientes):
- calafrios;
- perda de apetite;
- náuseas;
- vômitos.
Efeitos não desejados raros(podem ocorrer em até 1 em 1000 pacientes):
- reações alérgicas (por exemplo, febre, edema, hipotensão, erupção cutânea, rubor, dor de cabeça);
- sensação de frio ou calor;
- palidez;
- coloração azulada da pele e mucosas (devido à baixa oxigenação do sangue);
- dores no pescoço, nas costas, nos ossos, no peito e na região lombar;
- pressão arterial elevada ou reduzida;
- dificuldade para respirar.
Efeitos não desejados muito raros(podem ocorrer em até 1 em 10.000 pacientes):
- ereção prolongada e dolorosa do pênis.
Notificação de efeitos não desejados
Se ocorrerem efeitos não desejados, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas
Al. Jerozolimskie 181C
02-222 Varsóvia
telefone: +48 22 49 21 301
fax: +48 22 49 21 309
e-mail: [email protected]
Efeitos não desejados também podem ser notificados ao responsável pelo produto.
A notificação de efeitos não desejados pode ajudar a coletar mais informações sobre a segurança do medicamento.
5. Como conservar SMOFlipid
Conservar em local fresco e seco, protegido da luz.
Não conservar a uma temperatura superior a 25°C. Não congelar.
Não usar o medicamento após a data de validade impressa no pacote. A data de validade é o último dia do mês indicado.
Não usar o medicamento SMOFlipid se o pacote estiver danificado. Usar apenas se a emulsão estiver branca e homogênea. Para uso único. O medicamento não utilizado deve ser descartado. Não reutilizar.
Quando administrado a recém-nascidos e crianças com menos de 2 anos, a solução (no saco e no conjunto de administração) deve ser protegida da luz até o final da administração (ver ponto 2).
6. Conteúdo do pacote e outras informações
O que contém SMOFlipid
- Os princípios ativos do medicamento são: óleo de soja, triglicerídeos de cadeia média, óleo de oliva e óleo de peixe rico em ácidos graxos ômega-3.
- Os outros componentes são: lecitina de ovo, glicerol, oleato de sódio, alfa-tocoferol, hidróxido de sódio e água para injeção.
Como é SMOFlipid e o que o pacote contém
SMOFlipid é uma emulsão branca e homogênea disponível em frascos de vidro ou sacos do tipo Biofine.
Tamanhos do pacote:
- frasco de vidro: 1 x 100 ml, 10 x 100 ml, 1 x 250 ml, 10 x 250 ml, 1 x 500 ml e 10 x 500 ml;
- saco do tipo Biofine: 1 x 100 ml, 10 x 100 ml, 20 x 100 ml, 1 x 250 ml, 10 x 250 ml, 1 x 500 ml, 12 x 500 ml, 1 x 1000 ml e 6 x 1000 ml.
Nem todos os tamanhos do pacote podem estar disponíveis.
Responsável pelo produto e fabricante
Responsável pelo produto
Fresenius Kabi AB
SE-75174 Uppsala
Suécia
Fabricante
Fresenius Kabi AB
Rapsgatan 7
SE-75174 Uppsala
Suécia
Fresenius Kabi Áustria GmbH
Hafnerstrasse 36
A-8055 Graz
Áustria
Para obter informações mais detalhadas, deve contatar um representante do responsável pelo produto:
Fresenius Kabi Portugal
Rua do Centro Empresarial do Aeroporto, n.º 29, 3.º andar, sala 2
4470-177 Maia
telefone: +351 229 405 010
Este medicamento está autorizado para comercialização nos países membros da Área Económica Europeia sob os seguintes nomes:
Alemanha, Áustria, Bélgica, Chipre, Dinamarca, Eslováquia, Eslovénia, Espanha, Estónia, Finlândia, França, Grécia, Hungria, Irlanda, Islândia, Itália, Letónia, Lituânia, Luxemburgo, Noruega, Países Baixos, Polónia, Portugal, Reino Unido, República Checa, Suécia: SMOFlipid 200 mg/ml
Data da última revisão do folheto:06.03.2020
-----------------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico qualificado:
Precauções e advertências
Durante a infusão, a concentração de triglicerídeos no soro não deve exceder 3 mmol/l.
A sobredosagem pode causar a síndrome de sobrecarga lipídica. Deve haver especial cuidado em pacientes com risco elevado de hiperlipidemia (por exemplo, pacientes que tomam grandes doses de gordura, pacientes com sepse grave e recém-nascidos com peso muito baixo ao nascer).
A administração de ácidos graxos de cadeia média pode causar acidose metabólica. A administração concomitante de ácidos graxos de cadeia longa contidos em SMOFlipid reduz significativamente esse risco. A administração concomitante de carboidratos pode reduzir ainda mais esse risco. Portanto, é recomendada a administração concomitante de soluções de carboidratos ou aminoácidos com carboidratos na infusão.
Deve realizar exames laboratoriais regulares relacionados ao controle da nutrição parenteral. Isso inclui a determinação da glicemia, testes de função hepática, equilíbrio ácido-básico, equilíbrio de líquidos, hemograma completo e níveis de eletrólitos.
Este medicamento contém óleo de soja, óleo de peixe e fosfolipídios de ovo, que podem causar reações alérgicas. Foram observadas reações alérgicas cruzadas entre soja e amendoins.
Se ocorrerem sintomas de reação anafilática (como febre, calafrios, erupção cutânea ou dificuldade para respirar), deve interromper imediatamente a infusão.
SMOFlipid deve ser administrado com cuidado em recém-nascidos e prematuros com hiperbilirrubinemia e em casos de hipertensão pulmonar. Em recém-nascidos, especialmente prematuros, em casos de nutrição parenteral prolongada, deve monitorar a contagem de plaquetas, a atividade de enzimas hepáticos e os níveis de triglicerídeos no soro sanguíneo.
SMOFlipid contém até 5 mmol de sódio por 1000 ml. Deve ser considerado em pacientes que controlam a ingestão de sódio na dieta.
Não deve adicionar outros medicamentos ou substâncias ao SMOFlipid, a menos que sua compatibilidade tenha sido estabelecida.
Método de administração
Infusão em veia central ou periférica.
Quando administrado a recém-nascidos e crianças com menos de 2 anos, a solução (no saco e no conjunto de administração) deve ser protegida da luz até o final da administração.
Instruções de uso e procedimentos especiais Precauções e advertências especiais para o uso
Usar apenas se a emulsão estiver homogênea.
A exposição à luz de soluções para nutrição parenteral, especialmente após a adição de oligoelementos e (ou) vitaminas, pode ter efeitos não desejados na resposta clínica em recém-nascidos, devido à formação de peróxidos e outros produtos de degradação. Quando administrado a recém-nascidos e crianças com menos de 2 anos, SMOFlipid deve ser protegido da luz até o final da administração.
Para o saco do tipo Biofine: antes de remover o saco externo protetor, deve verificar o indicador de estanqueidade do pacote (Oxalert). Se o indicador estiver preto, o oxigênio penetrou no saco externo e o medicamento deve ser descartado.
Antes da administração, deve verificar se a emulsão está homogênea. Deve garantir que a emulsão pronta para a infusão não apresente sinais de separação de fases.
Para uso único. O medicamento não utilizado deve ser descartado. Não reutilizar.
Após a mistura com substâncias adicionais, SMOFlipid pode ser misturado, sob condições assépticas, com soluções de aminoácidos, glicose e eletrólitos, para obter uma mistura para nutrição parenteral total do tipo "tudo em um".
Se necessário, pode obter informações do responsável pelo produto sobre a compatibilidade do medicamento com substâncias adicionais e sobre os períodos de armazenamento de misturas preparadas. Qualquer substância adicional deve ser adicionada ao medicamento em condições assépticas. Qualquer resíduo não utilizado do medicamento ou seus resíduos deve ser descartado de acordo com as regulamentações locais.
Não armazenar a uma temperatura superior a 25°C. Não congelar.
Armazenamento após a mistura
Se SMOFlipid for misturado com substâncias adicionais, a mistura resultante deve ser usada imediatamente. Caso contrário, o período de armazenamento durante o uso e as condições de armazenamento antes da administração são de responsabilidade do usuário. Esse período não deve exceder 24 horas a 2-8°C, a menos que a adição tenha ocorrido em condições assépticas controladas e validadas.
Precauções especiais para a eliminação e preparação do medicamento para uso
Quando administrado a recém-nascidos e crianças com menos de 2 anos, proteger da luz até o final da administração. A exposição de SMOFlipid à luz, especialmente após a adição de oligoelementos e (ou) vitaminas, pode levar à formação de peróxidos e outros produtos de degradação, o que pode ser minimizado protegendo-o da luz.
SMOFlipid - Instruções para a preparação do saco Biofine para uso
- 1.
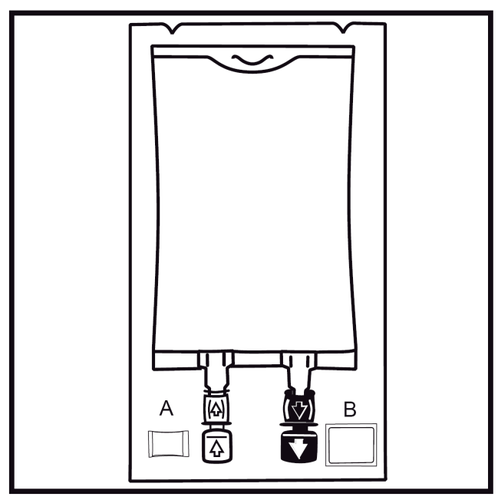
Deve verificar o indicador de estanqueidade do pacote (Oxalert) Aantes de remover o saco externo.
Se o indicador estiver preto, o saco externo está danificado e o medicamento deve ser descartado.
- 2.
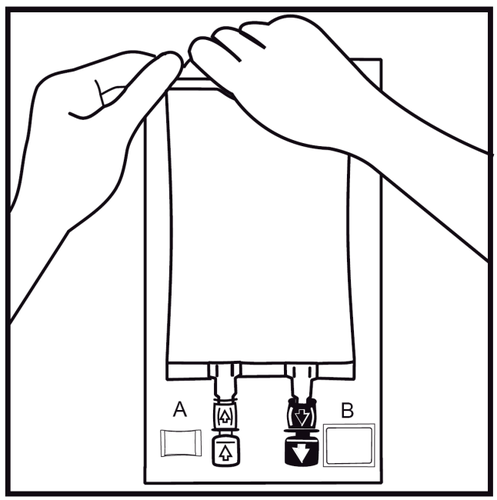
Remover o saco externo rasgando a solda na parte superior e puxando ao longo do pacote.
O indicador de estanqueidade do pacote (Oxalert) Ae o absorvedor de oxigênio Bdevem ser removidos.
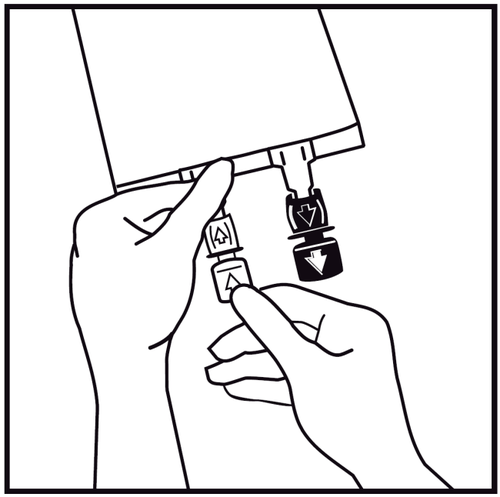
- 3.
Se estiver adicionando substâncias adicionais, deve remover a tampa de uso único marcada com uma seta que protege a porta branca para adicionar essas substâncias.
Se não estiver adicionando substâncias adicionais, deve prosseguir para o ponto 5.
- 4.
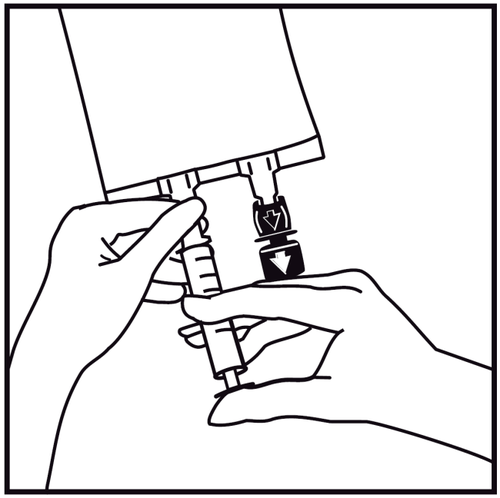
Inserir a agulha horizontalmente através do centro do local de injeção e injetar as substâncias adicionais (com compatibilidade estabelecida). Usar seringas com agulhas de diâmetro de 18 a 23 G e comprimento máximo de 40 mm.
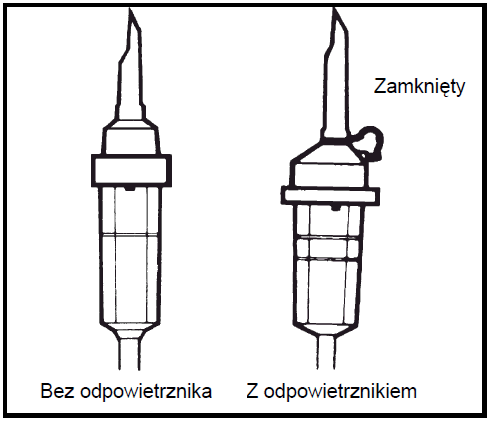
- 5.
Deve usar um conjunto de infusão sem vedação ou fechar a entrada de ar no caso de um conjunto com vedação. Seguir as instruções de uso do conjunto de infusão. Usar um conjunto de infusão com diâmetro especificado na norma ISO 8536-4: 5,6 ± 0,1 mm.
- 6.
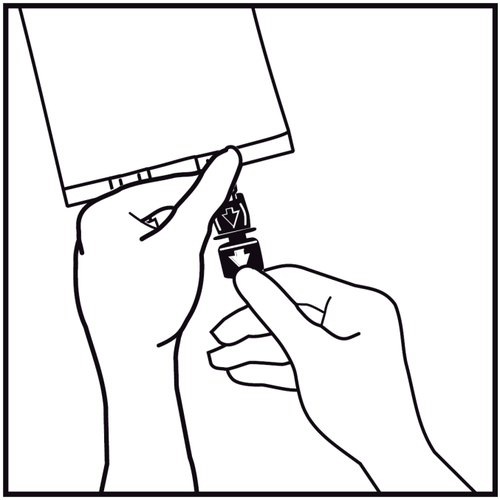
Remover a tampa de uso único que protege a porta de infusão azul.
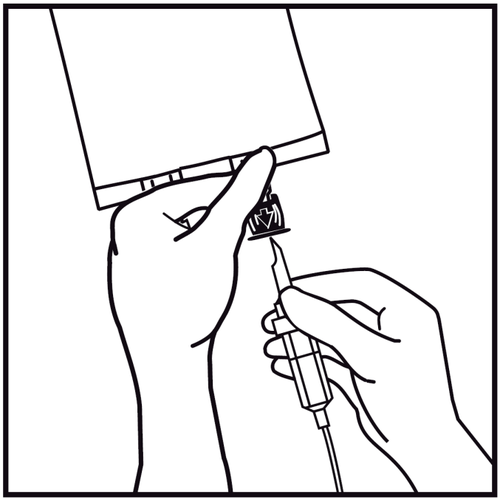
- 7.
Segurar a base da porta de infusão. Inserir a ponta do conjunto de infusão na porta de infusão e girar suavemente até que esteja completamente inserido.
- 8.
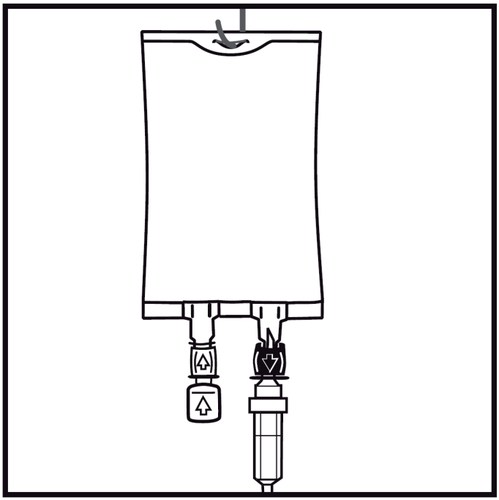
Suspender o saco usando o orifício preparado para esse fim e iniciar a infusão.
- País de registo
- Requer receita médicaNão
- Fabricante
- ImportadorFresenius Kabi AB Fresenius Kabi Austria GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SmoflipidForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Smoflipid noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Smoflipid em Espanha
Médicos online para Smoflipid
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Smoflipid – sujeita a avaliação médica e regras locais.














