
Mirtor
Pergunte a um médico sobre a prescrição de Mirtor

Como usar Mirtor
Folheto informativo para o doente:
Mirtor, 15 mg, comprimidos de desintegração oral
Mirtor, 30 mg, comprimidos de desintegração oral
Mirtor, 45 mg, comprimidos de desintegração oral
Mirtazapina
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Mirtor e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Mirtor
- 3. Como tomar o medicamento Mirtor
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Mirtor
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento Mirtor e para que é utilizado
O medicamento Mirtor pertence a um grupo de medicamentos conhecidos como medicamentos antidepressivos .
O Mirtor é utilizado no tratamento da depressão em adultos.
O Mirtor começa a fazer efeito após 1-2 semanas de tratamento, e após 2-4 semanas, ocorre uma melhoria
do bem-estar. Se após 2-4 semanas de tratamento não ocorrer melhoria ou o doente se sentir pior, deve consultar o médico. Mais informações estão disponíveis no ponto 3 da seção "Quando posso esperar melhoria do meu bem-estar".
2. Informações importantes antes de tomar o medicamento Mirtor
Quando não tomar o medicamento Mirtor:
- se o doente for alérgico à mirtazapina ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6). Nesse caso, antes de tomar o medicamento Mirtor, deve contactar o médico o mais rápido possível.
- se atualmente ou recentemente (nos últimos 2 semanas) estiver a tomar medicamentos do grupo dos inibidores da monoamina oxidase (IMAO).
Precauções e advertências
Antes de começar a tomar o medicamento Mirtor, deve discutir com o médico ou farmacêutico.
Antes de começar a tomar o medicamento Mirtor, deve dizer ao médico:
Se o doente já teve alguma vez uma erupção cutânea grave ou descamação da pele, bolhas e (ou)
ulcerações na boca após a ingestão do medicamento Mirtor.
Crianças e adolescentes
Geralmente, o medicamento Mirtor não deve ser utilizado em crianças e adolescentes abaixo de 18 anos,
pois não foi demonstrada a sua eficácia nesse grupo etário. Além disso, deve estar ciente de que em doentes
abaixo de 18 anos, há um risco mais elevado de efeitos não desejados, tais como tentativas de suicídio,
pensamentos suicidas e hostilidade (principalmente agressividade, comportamento rebelde e ira), quando
tomam medicamentos desta classe. No entanto, o médico pode prescrever o medicamento Mirtor a doentes
desta faixa etária, se considerar que está no melhor interesse deles. Se o médico prescrever o medicamento
Mirtor a um doente abaixo de 18 anos, e surgirem alguma dúvida, deve consultar o médico. No caso de
doentes abaixo de 18 anos que tomam o medicamento Mirtor, deve informar o médico se algum dos sintomas
acima mencionados se desenvolver ou agravar. Além disso, o efeito a longo prazo do medicamento Mirtor
sobre a segurança relacionada ao crescimento, amadurecimento e desenvolvimento cognitivo neste grupo
etário ainda não foi demonstrado. Além disso, nesta faixa etária, após a administração de mirtazapina,
foi observado um aumento significativo de peso.
Pensamentos suicidas e agravamento da depressão
Doentes com depressão podem ter, por vezes, pensamentos de autolesão ou de suicídio. Tais sintomas ou
comportamentos podem agravar-se no início do tratamento com medicamentos antidepressivos, pois
estes medicamentos geralmente começam a fazer efeito apenas após cerca de 2 semanas, por vezes mais
tarde.
Os sintomas acima mencionados são mais prováveis em:
- doentes que já tiveram anteriormente pensamentos de autolesão ou suicídio;
- jovens adultos. Os dados dos estudos clínicos mostram um risco aumentado de comportamentos
suicidas em pessoas com menos de 25 anos com distúrbios psiquiátricos que estavam a tomar
medicamentos antidepressivos. Deve contactar imediatamente o médico ou ir ao hospital, se
ocorrerem pensamentos de autolesão ou suicídio.
Pode ser útil informar familiares ou amigos sobre a depressão e pedir-lhes para lerem este
folheto. O doente pode pedir para ser informado se eles notarem que a depressão ou ansiedade
se agravaram ou ocorreram mudanças preocupantes no comportamento.
Além disso, deve ter especial cuidado ao tomar o medicamento Mirtor
- Se ocorrerem ou tiverem ocorrido: (Deve informar o médico sobre a ocorrência das doenças abaixo
mencionadas antes de iniciar o tratamento com o medicamento Mirtor, se o doente não o fez anteriormente.) - convulsões . Se ocorrerem convulsões ou aumento da frequência das convulsões durante o
tratamento, deve interromper o medicamento e contactar imediatamente o médico; - doenças do fígado , incluindo icterícia. Se ocorrer icterícia, deve interromper o medicamento e
contactar imediatamente o médico; - doenças renais;
- doenças cardíacas ou baixa pressão arterial ;
- esquizofrenia . Deve contactar imediatamente o médico, se os distúrbios psicóticos, como
sintomas paranoides, se agravarem ou aumentarem de frequência; - depressão maníaca (períodos alternados de humor elevado/estimulação e depressão). Se
ocorrer um sentimento de estimulação excessiva, deve interromper o medicamento e contactar
imediatamente o médico; - diabetes (pode ser necessário ajustar a dose de insulina ou outros medicamentos
hipoglicemiantes); - doenças oculares , como pressão intraocular aumentada (glaucoma);
- dificuldades para urinar, que podem resultar de um aumento da próstata;
- certos distúrbios cardíacos, que podem causar alterações no ritmo cardíaco, infarto do
miocárdio recente, insuficiência cardíaca ou uso de certos medicamentos que podem causar
alterações no ritmo cardíaco. - Se ocorrerem sintomas de infecção, como febre de origem desconhecida, dor de garganta,
ulcerações na boca, deve interromper o medicamento, contactar imediatamente o médico e realizar
um exame de sangue. Em casos raros, esses sintomas podem ser um sinal de distúrbios da produção de
glóbulos vermelhos pela medula óssea. Esses sintomas são raros e geralmente ocorrem após 4-6
semanas de tratamento. - Doentes idosos são frequentemente mais sensíveis, especialmente aos efeitos não desejados dos
medicamentos antidepressivos. - Foram relatados reações cutâneas graves, incluindo síndrome de Stevens-Johnson (SSJ), necrólise
epidérmica tóxica (NET) e reação a medicamentos com eosinofilia e sintomas sistémicos (DRESS),
durante o tratamento com mirtazapina. Se o doente notar algum dos sintomas descritos no ponto 4
relacionados a essas reações cutâneas graves, deve interromper imediatamente o medicamento e
consultar o médico. Se o doente já teve alguma vez reações cutâneas graves no passado, não deve
reiniciar o tratamento com mirtazapina.
Deve interromper o medicamento e consultar o médico se ocorrerem sintomas de reações
cutâneas graves.
Mirtor com alimentos e álcool
O consumo de álcool durante o tratamento com o medicamento Mirtor pode causar sonolência.
É recomendável evitar o consumo de álcool durante o tratamento com o medicamento Mirtor.
O medicamento Mirtor pode ser tomado com ou sem alimentos.
Gravidez e amamentação
Se a paciente estiver grávida, amamentando, suspeitar que possa estar grávida ou planejar ter um
filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
As experiências limitadas com o uso do medicamento Mirtor em mulheres grávidas não mostram um
risco aumentado. No entanto, deve ter cuidado ao tomar o medicamento durante a gravidez.
Se o medicamento Mirtor for tomado durante a gravidez ou pouco antes do parto, é recomendável
monitorizar o recém-nascido devido ao risco de efeitos não desejados.
Medicamentos semelhantes (do grupo dos inibidores da recaptação de serotonina - ISRS) tomados
por mulheres grávidas podem aumentar o risco de ocorrência de uma doença grave, conhecida como
hipertensão pulmonar persistente do recém-nascido (HPPRN), que causa respiração acelerada e
cianose no recém-nascido. Esses sintomas geralmente ocorrem no primeiro dia de vida do recém-
nascido. Se ocorrerem, deve contactar imediatamente a parteira e/ou o médico.
Condução de veículos e operação de máquinas
O medicamento Mirtor pode diminuir a vigilância e a capacidade de concentração. Durante o
tratamento com o medicamento Mirtor, deve evitar realizar tarefas potencialmente perigosas que
requeiram atenção constante, como conduzir veículos ou operar máquinas. Se o médico prescrever o
medicamento Mirtor a um doente abaixo de 18 anos, deve ter certeza de que o medicamento não
interfere na concentração e vigilância do doente antes de participar no tráfego rodoviário (por
exemplo, andar de bicicleta).
O medicamento Mirtor contém aspartamo, uma fonte de fenilalanina
Este medicamento contém aspartamo, que é uma fonte de fenilalanina. Cada comprimido de
desintegração oral de 15 mg contém 3 mg de aspartamo. Cada comprimido de desintegração oral
de 30 mg contém 6 mg de aspartamo. Cada comprimido de desintegração oral de 45 mg contém
9 mg de aspartamo.
O aspartamo pode ser prejudicial para doentes com fenilcetonúria. É uma doença genética rara,
na qual a fenilalanina se acumula no organismo devido à sua eliminação anormal.
3. Como tomar o medicamento Mirtor
Este medicamento deve ser sempre tomado de acordo com as recomendações do médico ou
farmacêutico. Em caso de dúvida, deve consultar o médico ou farmacêutico.
Posologia
A dose recomendada inicial é de 15 ou 30 mg por dia. Após alguns dias de tratamento,
o médico pode recomendar aumentar a dose para a mais adequada para o doente (de 15 a 45 mg
por dia). Geralmente, a mesma dose do medicamento é utilizada em doentes de diferentes idades.
No entanto, para doentes idosos ou com doenças renais e hepáticas, o médico pode recomendar uma
dose diferente do medicamento Mirtor.
Quando tomar o medicamento Mirtor
O medicamento Mirtor deve ser tomado diariamente no mesmo horário, preferencialmente em uma
única dose à noite, antes de deitar. O médico pode recomendar, no entanto, tomar duas doses
divididas ao longo do dia
- uma de manhã, outra à noite, antes de deitar. A dose maior deve ser tomada à noite, antes de
deitar.
Informações sobre a administração dos comprimidos de desintegração oral:
Os comprimidos do medicamento Mirtor devem ser tomados por via oral.
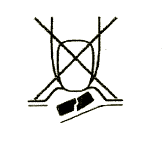
1. Não deve partir o comprimido de desintegração oral
Para evitar partir o comprimido de desintegração oral, não deve pressionar o blister que contém
o comprimido (Figura A).
Figura A
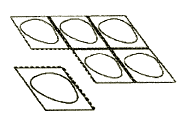
2. Deve separar o blister com o comprimido
Cada blister contém 6 compartimentos com comprimidos, separados por linhas de perfuração.
Deve dobrar o blister e separar um compartimento ao longo da linha de perfuração (Figura 1).
Figura 1
3. Deve remover a folha de cobertura
Deve remover cuidadosamente a folha de cobertura, começando pelo canto marcado com uma seta
(Figuras 2 e 3).
Figura 2
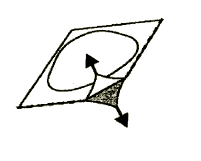
Figura 3
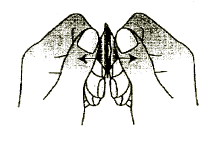
4. Deve remover o comprimido de desintegração oral
Deve remover o comprimido de desintegração oral com a mão seca do blister e colocá-lo na
língua. (Figura 4).
Figura 4
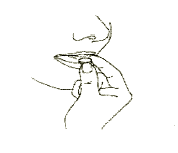
O comprimido se desintegra rapidamente e pode ser engolido sem água.
Quando posso esperar melhoria do meu bem-estar
Os primeiros sinais de efeito do medicamento podem ser esperados após 1-2 semanas de
tratamento. A melhoria do bem-estar pode ocorrer após 2-4 semanas.
É importante discutir com o médico os efeitos do medicamento Mirtor durante as primeiras
semanas de tratamento:
- Após 2 a 4 semanas após o início do tratamento com o medicamento Mirtor, deve discutir com
o médico os efeitos do tratamento até o momento. Se não houver resposta clínica adequada, o
médico pode aumentar a dose. Após mais 2 a 4 semanas, deve discutir novamente com o médico os
efeitos do tratamento. O tratamento deve ser continuado até que os sintomas desapareçam
completamente, o que geralmente leva 4 a 6 meses.
Uso de dose maior do que a recomendada do medicamento Mirtor
Se o doente ou alguém tomar uma dose maior do que a recomendada do medicamento Mirtor,
deve contactar imediatamente o médico.
Os sinais esperados de superdose do medicamento Mirtor (sem outros medicamentos e sem álcool)
são sonolência,
desorientação e aumento da frequência cardíaca. Os sintomas de superdose do medicamento
podem incluir alterações no ritmo cardíaco (aumento da frequência cardíaca, ritmo cardíaco
irregular) e (ou) desmaio. Esses podem ser sintomas de distúrbios cardíacos graves, conhecidos
como "torsades de pointes".
Esquecimento de uma dose do medicamento Mirtor
Se esquecer de tomar uma dose do medicamento que deve ser tomado uma vez por dia
- não deve tomar uma dose dupla para compensar a dose esquecida. Deve tomar a próxima dose
no horário habitual.
Se o medicamento deve ser tomado duas vezes por dia
- se esquecer de tomar a dose da manhã, deve tomá-la com a dose da noite;
- se esquecer de tomar a dose da noite, não deve tomá-la com a dose da manhã; deve omiti-la e
continuar o tratamento tomando as doses habituais da manhã e da noite; - se esquecer de tomar as duas doses, não deve tentar compensá-las. Deve omiti-las e continuar
o tratamento tomando as doses habituais da manhã e da noite no dia seguinte.
Interrupção do tratamento com o medicamento Mirtor
Deve interromper o tratamento com o medicamento Mirtor apenas de acordo com as instruções do
médico.
Não deve interromper o tratamento com o medicamento cedo demais, pois isso pode causar uma
recaída da doença.
Se ocorrer melhoria, deve discutir com o médico. O médico informará quando pode interromper o
tratamento.
A interrupção abrupta do tratamento com o medicamento Mirtor, mesmo que os sintomas da
depressão tenham desaparecido, pode causar náuseas, tonturas, agitação ou ansiedade e dor de
cabeça. Esses sintomas não ocorrerão durante a interrupção gradual do medicamento. O médico
informará como reduzir gradualmente as doses do medicamento.
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar o médico ou
farmacêutico.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não
ocorram em todos.
Em caso de ocorrência de algum dos seguintes efeitos não desejados graves, deve interromper o
tratamento com a mirtazapina e contactar imediatamente o médico.
Não muito frequentes (podem ocorrer em até 1 pessoa em 100):
- humor elevado e atividade psíquica aumentada (mania)
Raros (podem ocorrer em até 1 pessoa em 1.000):
- icterícia; o que pode indicar distúrbios da função hepática (icterícia)
Frequência desconhecida (frequência não pode ser estimada com base nos dados
disponíveis):
- sinais de infecção, como febre súbita e inexplicável, dor de garganta e ulcerações na boca
(agranulocitose). Em casos raros, a mirtazapina pode causar distúrbios da produção de glóbulos
vermelhos (supressão da medula óssea). Em alguns doentes, pode ocorrer uma diminuição temporária
do número de glóbulos brancos (granulocitopenia). Em casos raros, a mirtazapina pode causar
diminuição do número de glóbulos vermelhos e brancos e plaquetas (anemia aplástica), diminuição
do número de plaquetas (trombocitopenia) ou aumento do número de glóbulos brancos (eosinofilia) - convulsões (convulsões)
- combinação de sintomas, como febre inexplicável, suor, aumento da frequência cardíaca,
diarreia, (movimentos musculares não controlados) calafrios, aumento dos reflexos, ansiedade,
mudanças de humor, perda de consciência e aumento da salivação. Em casos muito raros, esses
sintomas podem indicar o desenvolvimento de uma síndrome serotoninérgica - pensamentos de autolesão ou suicídio
- reações cutâneas graves:
- manchas vermelhas semelhantes a um alvo ou manchas redondas, frequentemente com bolhas
centrais no tronco, descamação da pele, ulcerações na boca, garganta, nariz, genitálias e olhos.
A ocorrência dessas reações cutâneas graves é frequentemente precedida por febre e sintomas
semelhantes aos da gripe (síndrome de Stevens-Johnson, necrólise epidérmica tóxica). - erupção cutânea generalizada, febre alta e linfonodos aumentados (síndrome DRESS ou
síndrome de hipersensibilidade a medicamentos)
Outros efeitos não desejados possíveis incluem:
Muito frequentes (podem ocorrer em mais de 1 pessoa em 10):
- aumento do apetite e ganho de peso
- sedação ou sonolência
- dor de cabeça
- secura na boca
Frequentes (podem ocorrer em até 1 pessoa em 10):
- letargia
- tonturas
- convulsões ou tremores
- náuseas
- diarreia
- vômitos
- constipação
- erupções cutâneas ou rash
- dores nas articulações, dores musculares
- dores nas costas
- tonturas ou desmaio ao mudar de posição rapidamente (hipotensão ortostática)
- inchaço (geralmente nos tornozelos ou pés) devido à retenção de líquidos (edema)
- fadiga
- sonhos vívidos
- desorientação
- ansiedade
- distúrbios do sono
- distúrbios da memória, que geralmente desaparecem após a interrupção do tratamento
Não muito frequentes (podem ocorrer em até 1 pessoa em 100):
- sensações anormais na pele, como ardor, formigamento, picadas ou coceira (parestesias)
- síndrome das pernas inquietas
- desmaio
- sensação de entorpecimento na boca (anestesia bucal)
- pressão arterial baixa
- pesadelos
- agitação
- alucinações
- necessidade urgente de se mover
Raros (podem ocorrer em até 1 pessoa em 1.000):
- tremores musculares ou convulsões (convulsões clônicas musculares)
- comportamento agressivo
- dores abdominais e náuseas, que podem indicar pancreatite
Frequência desconhecida (frequência não pode ser estimada com base nos dados
disponíveis):
- sensações anormais na boca (parestesias bucais)
- inchaço na boca
- inchaço generalizado (edema generalizado)
- inchaço localizado
- baixo nível de sódio no sangue
- síndrome da secreção inadequada de hormônio antidiurético
- reações cutâneas graves (pênfigo, eritema multiforme)
- sonambulismo (caminar enquanto dorme)
- distúrbios da fala
- nível elevado de creatina quinase no sangue
- dificuldades para urinar (retenção urinária)
- dores musculares, rigidez e (ou) fraqueza
- escurecimento ou descoloração da urina (rabdomiólise)
- nível elevado de prolactina no sangue (hiperprolactinemia, incluindo sintomas de aumento
das mamas e/ou secreção de leite nos mamilos) - ereção prolongada ou dolorosa
Efeitos não desejados adicionais em crianças e adolescentes
Os seguintes efeitos não desejados foram frequentemente observados nos estudos clínicos com
crianças abaixo de 18 anos: ganho de peso significativo, urticária e aumento do nível de triglicérides
no sangue.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados
neste folheto, deve informar o médico ou farmacêutico. Os efeitos não desejados podem ser
notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Produtos
Farmacêuticos, Dispositivos Médicos e Produtos Biocidas,
Al. Jerozolimskie 181C
02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Site: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao responsável pelo produto.
A notificação de efeitos não desejados permitirá reunir mais informações sobre a segurança do
medicamento.
5. Como conservar o medicamento Mirtor
O medicamento deve ser conservado em local não visível e inacessível a crianças.
Não use este medicamento após o prazo de validade impresso na caixa de cartão.
O prazo de validade é o último dia do mês indicado.
Sem requisitos especiais de conservação.
Não use este medicamento se notar qualquer descoloração ou outros sinais de deterioração.
Os medicamentos não devem ser jogados na rede de esgotos ou em lixeiras domésticas. Deve
perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Esse
procedimento ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Mirtor
- O princípio ativo do medicamento é a mirtazapina. Cada comprimido de desintegração oral
contém 15 mg, 30 mg ou 45 mg de mirtazapina. - Os outros componentes do medicamento são crospovidona, manitol, celulose microcristalina,
aspartamo, aroma de morango e guaraná, aroma de hortelã, dióxido de silício coloidal anidro,
estearato de magnésio.
Como é o medicamento Mirtor e que conteúdo tem o pacote
Comprimido de desintegração oral de 15 mg:
branco, redondo, marcado com "36" em um lado e
"A" no outro lado.
Comprimido de desintegração oral de 30 mg:
branco, redondo, marcado com "37" em um lado e
"A" no outro lado.
Comprimido de desintegração oral de 45 mg:
branco, redondo, marcado com "38" em um lado e
"A" no outro lado.
30 (5x6) ou 90 (15x6) comprimidos em um pacote. Nem todos os tamanhos de pacotes
precisam estar disponíveis.
Responsável pelo produto
Orion Corporation
Orionintie 1
FI-02200 Espoo
Finlândia
Fabricante
Orion Corporation, Orion Pharma
Orionintie 1
FI-02200 Espoo
Finlândia
Para obter informações mais detalhadas, deve contactar o representante local do responsável
pelo produto:
Orion Pharma Poland Sp. z o. o.
[email protected]
Data da última atualização do folheto: 07.10.2021
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorOrion Corporation Orion Pharma
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MirtorForma farmacêutica: Comprimidos, 15 mgSubstância ativa: mirtazapineRequer receita médicaForma farmacêutica: Comprimidos, 30 mgSubstância ativa: mirtazapineRequer receita médicaForma farmacêutica: Comprimidos, 45 mgSubstância ativa: mirtazapineRequer receita médica
Alternativas a Mirtor noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Mirtor em Espanha
Alternativa a Mirtor em Ukraine
Médicos online para Mirtor
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Mirtor – sujeita a avaliação médica e regras locais.









