
Curosurf

Pergunte a um médico sobre a prescrição de Curosurf

Como usar Curosurf
Folheto incluído na embalagem: informação para pais e tutores
Curosurf, 80 mg/ml, suspensão para administração intratraqueal e intra-bronquial
(Poractant alfa)
Fracao de fosfolipídeos de pulmão de porco
Deve ler-se atentamente o conteúdo do folheto antes de administrar o medicamento, pois contém informações importantes para o doente.
- Deve guardar-se este folheto, para que possa ser relido se necessário.
- Em caso de dúvidas, deve consultar-se um médico.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico ou enfermeiro. Ver ponto 3.
Índice do folheto:
- 1. O que é o medicamento Curosurf e para que é utilizado
- 2. Como administrar o medicamento Curosurf
- 3. Efeitos não desejados possíveis
- 4. Como conservar o medicamento Curosurf
- 5. Conteúdo da embalagem e outras informações
1. O QUE É O MEDICAMENTO CUROSURF E PARA QUE É UTILIZADO
O Curosurf é utilizado no tratamento e prevenção da síndrome de dificuldade respiratória (em inglês, Respiratory
Distress Syndrome: RDS) em recém-nascidos. Na maioria dos recém-nascidos, os pulmões contêm
uma substância chamada surfactante (fator de superfície). Esta substância reveste os alvéolos
pulmonares, evita que eles adiram e permite a respiração normal. No entanto, alguns recém-nascidos,
especialmente os prematuros, nascem com deficiência de surfactante, o que leva ao desenvolvimento da RDS. O Curosurf
é um surfactante natural que atua da mesma forma que o surfactante produzido pelos
recém-nascidos e, portanto, ajuda os recém-nascidos a respirar normalmente até que comecem a produzir seu
próprio surfactante natural.
No recém-nascido podem ocorrer outras doenças que podem exigir tratamento diferente.
2. COMO É ADMINISTRADO O MEDICAMENTO CUROSURF
Posologia:
O médico escolhe a dose adequada do medicamento, dependendo do peso do bebê. Se o bebê receber Curosurf
para prevenir a ocorrência de RDS, o medicamento deve ser administrado dentro de 15 minutos após o nascimento. Se o
bebê receber Curosurf para tratar a RDS, o medicamento deve ser administrado o mais rápido possível após o diagnóstico
da doença. Se o bebê precisar de uma dose adicional de Curosurf, ela deve ser administrada 12 horas após a administração
da primeira dose. Se necessário, após mais 12 horas, pode ser administrada uma terceira dose.
A administração de Curosurf em prematuros com insuficiência hepática ou renal não foi estudada.
1
Modo de administração do medicamento:
O Curosurf é administrado ao bebê em incubadora por um médico ou enfermeiro. O medicamento será aquecido
à temperatura ambiente e, em seguida, administrado com a ajuda de uma seringa através de um tubo de intubação para a
traqueia do bebê. Para isso, pode ser necessário desconectar o bebê do respirador por alguns minutos.
Também pode ser utilizada a técnica de administração menos invasiva de surfactante por um cateter fino (LISA – em inglês, Less Invasive Surfactant Administration).
Curosurf contém sódio
O medicamento contém menos de 1 mmol (23 mg) de sódio em uma ampola, ou seja, o medicamento é considerado
"livre de sódio".
3. EFEITOS NÃO DESEJADOS POSSÍVEIS
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não todos eles
ocorram em todas as pessoas. Os efeitos não desejados possíveis estão listados abaixo, de acordo com a frequência
de ocorrência:
Em caso de dúvidas sobre efeitos não desejados, deve consultar-se um médico.
Não muito frequentes(ocorrem em menos de 1 em 100
pacientes):
Raros(ocorrem em menos de 1 em 1000
pacientes):
- infecção
- sangramento no cérebro
- ar no tórax causado
- desaceleração da atividade cardíaca
- baixa pressão arterial
- doença pulmonar crônica
- redução da quantidade de oxigênio no organismo
Além disso, foram relatados os seguintes efeitos não desejados:
- aumento da quantidade de oxigênio no organismo
- coloração azulada da pele ou gengivas devido à falta de oxigênio
- parada respiratória
- complicações decorrentes da colocação de tubos nos pulmões
- redução da atividade cerebral
Durante a administração do medicamento Curosurf por um cateter fino, foram relatados alguns efeitos não desejados
leves e temporários: bradicardia, apneia, redução da saturação de oxigênio no sangue, espuma na boca,
tosse, engasgo e espirros.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado no folheto,
deve informar o médico, farmacêutico ou enfermeiro.
Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos da Agência Reguladora de Medicamentos, Produtos Médicos e Produtos Biocidas, Al. Jerozolimskie 181C, 02-222 Varsóvia,
telefone: + 48 22 49 21 301, fax: + 48 22 49 21 309, e-mail: [email protected] .
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados permitirá a coleta de mais informações sobre a segurança do medicamento.
lesão pulmonar
2
4. COMO CONSERVAR O MEDICAMENTO CUROSURF
- O medicamento deve ser conservado em local não acessível e invisível para as crianças.
- Conservar em refrigerador a uma temperatura entre 2°C e 8°C, conservar no embalagem original para proteger da luz. Antes da administração ao bebê, deve ser aquecido à temperatura ambiente.
- As ampolas não abertas e não utilizadas do produto Curosurf, que foram aquecidas à temperatura ambiente, podem ser colocadas de volta no refrigerador dentro de 24 horas para uso posterior. O medicamento não deve ser aquecido à temperatura ambiente e colocado no refrigerador mais de uma vez.
- Não utilizar o medicamento após a data de validade indicada na caixa e na ampola. A data de validade corresponde ao último dia do mês indicado.
- Um recipiente deve ser utilizado uma vez, e os resíduos devem ser descartados. O hospital deve garantir a eliminação segura dos resíduos não utilizados de Curosurf.
- Os medicamentos não devem ser descartados no sistema de esgotos. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais utilizados. Este procedimento ajudará a proteger o meio ambiente
5. CONTEÚDO DA EMBALAGEM E OUTRAS INFORMAÇÕES
O que contém o medicamento Curosurf
- -A substância ativa é uma mistura de lipídios e proteínas obtidas de alvéolos pulmonares de porco.
- Os outros componentes são: cloreto de sódio, água para injeção, bicarbonato de sódio (para regular o pH).
Como é o medicamento Curosurf e o que contém a embalagem
O Curosurf é uma suspensão estéril. Está disponível em ampolas de vidro de uso único com capacidade de 5 ml, contendo 1,5 ml (120 mg) ou 3 ml (240 mg) de fração de fosfolipídeos de alvéolos pulmonares de porco. Cada ml de suspensão estéril contém 80 mg de fração de fosfolipídeos de alvéolos pulmonares de porco. Em uma embalagem, há 2 ampolas de 1,5 ml de suspensão ou 1 ampola de 3 ml de suspensão do medicamento Curosurf.
Nem todos os tamanhos de embalagem podem estar disponíveis no mercado.
Titular da autorização de comercialização:
Chiesi Farmaceutici S.p.A, Via Palermo 26/A, 43 122 Parma, Itália.
Fabricante:
Chiesi Farmaceutici S.p.A, Via San Leonardo 96 - Via Palermo 26/A, 43 122 Parma, Itália.
Chiesi Pharmaceuticals GmbH, Gonzagagasse 16/16, A-1010 Viena, Áustria.
Para obter informações mais detalhadas, deve contatar o representante do titular da autorização de comercialização em Portugal:
Chiesi Portugal, Lda., Av. da República, 37 - 5º, 1050-187 Lisboa
telefone: (21) 319 74 00, fax: (21) 319 74 09, e-mail: [email protected]
Data da última atualização do folheto:
Pede-se que leia a informação no verso do folheto
-------------------------------------------------------------------------------------------------------------------------
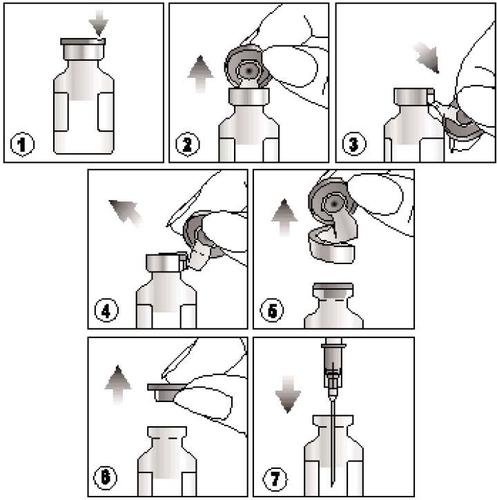
Como retirar o produto?

3
- 1) Encontrar a incisão localizada na tampa de plástico colorida,
- 2) Levantar a tampa na incisão e puxá-la para cima,
- 3) Puxar a parte plástica da tampa para baixo junto com a parte de alumínio,
- 4) e 5) Remover toda a tampa puxando o anel de alumínio
- 6) e 7) Retirar a tampa de borracha antes de retirar o conteúdo da ampola.
Para uso único. A suspensão não utilizada que reste na ampola deve ser descartada.
Não conservar a suspensão não utilizada para uso posterior.
Os resíduos do produto não utilizado ou seus dejetos devem ser eliminados de acordo com as regulamentações.
4
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- ImportadorChiesi Farmaceutici S.p.A. Chiesi Pharmaceuticals GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a CurosurfForma farmacêutica: Suspensão, 80 mg/mlSubstância ativa: natural phospholipidsNão requer receita médicaForma farmacêutica: Suspensão, 80 mg/mlSubstância ativa: natural phospholipidsNão requer receita médicaForma farmacêutica: Pastilhas, 1500 mg + 125 mgSubstância ativa: nikethamideFabricante: Przedsiębiorstwo Produkcyjno-Handlowe EWA S.A.Não requer receita médica
Alternativas a Curosurf noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Curosurf em Ukraine
Alternativa a Curosurf em Espanha
Médicos online para Curosurf
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Curosurf – sujeita a avaliação médica e regras locais.














