
Biotrakson
Pergunte a um médico sobre a prescrição de Biotrakson

Como usar Biotrakson
Folheto informativo para o paciente
Biotrakson, 1 g pó de ceftriaksona para solução injetável ou infusão
Biotrakson, 2 g, pó de ceftriaksona para solução injetável ou infusão
Ceftriaksona
Deve ler atentamente o folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
- Deve conservar este folheto para poder relê-lo se necessário.
- Se tiver alguma dúvida, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o paciente apresentar algum efeito indesejado, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Biotrakson e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Biotrakson
- 3. Como tomar o medicamento Biotrakson
- 4. Efeitos indesejados
- 5. Como conservar o medicamento Biotrakson
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Biotrakson e para que é utilizado
O Biotrakson é um antibiótico utilizado em adultos e crianças (inclusive recém-nascidos). O seu efeito consiste em matar as bactérias que causam infecções. Pertence a um grupo de medicamentos chamados cefalosporinas.
O Biotrakson é utilizado no tratamento de infecções:
- do cérebro (meningite),
- dos pulmões,
- da orelha média,
- da barriga e da parede da cavidade abdominal (peritonite),
- do trato urinário e dos rins,
- dos ossos e das articulações,
- da pele e dos tecidos moles,
- do sangue,
- do coração.
Este medicamento pode ser utilizado:
- no tratamento de certas infecções transmitidas por via sexual (gonorreia e sífilis),
- no tratamento de pacientes com baixo número de glóbulos brancos (neutropenia) que têm febre causada por infecção bacteriana,
- no tratamento de infecções no peito em adultos com bronquite crónica,
- no tratamento da doença de Lyme (doença transmitida por carrapatos) em adultos e crianças, incluindo recém-nascidos a partir do 15º dia de vida,
- para prevenir infecções durante operações.
2. Informações importantes antes de tomar o medicamento Biotrakson
Quando não tomar o medicamento Biotrakson:
- se o paciente for alérgico à ceftriaksona;
- se o paciente tiver tido uma reação alérgica súbita ou grave a penicilina ou antibióticos semelhantes (como cefalosporinas, carbapenêmicos, monobactâmicos); os sintomas de tal reação podem incluir inchaço súbito da garganta ou face, que pode dificultar a respiração ou a deglutição, inchaço súbito das mãos, pés e tornozelos, dor no peito e erupção cutânea grave que aparece rapidamente;
- se o paciente for alérgico à lidocaína e for receber Biotrakson por injeção intramuscular.
Não deve ser utilizado em crianças pequenas, se:
- a criança for prematura,
- a criança for recém-nascida (com até 28 dias) e tiver certos problemas de sangue ou icterícia [amarelamento da pele e (ou) brancos dos olhos], ou for receber intravenosamente um medicamento que contenha cálcio.
Precauções e advertências
Antes de iniciar o tratamento com o medicamento Biotrakson, deve discutir com o médico, farmacêutico ou enfermeiro, se:
- o paciente recebeu ou vai receber recentemente produtos que contenham cálcio,
- o paciente teve recentemente diarreia após tratamento com antibiótico,
- o paciente já teve problemas intestinais, particularmente colite (inflamação do intestino grosso),
- o paciente tem problemas de fígado ou rins (ver ponto 4),
- o paciente tem cálculos biliares ou cálculos renais,
- o paciente tem outras doenças, como anemia hemolítica (diminuição do número de glóbulos vermelhos, que causa palidez e fraqueza ou falta de ar),
- o paciente está seguindo uma dieta com baixo teor de sódio,
- o paciente apresenta ou já apresentou algum dos seguintes sintomas: erupção cutânea, vermelhidão da pele, bolhas na área dos lábios, olhos ou boca, descamação da pele, febre alta, sintomas semelhantes aos da gripe, aumento da atividade de enzimas hepáticos nos resultados dos exames de sangue e aumento do número de um tipo de glóbulos brancos (eosinofilia) e linfonodos aumentados (sintomas de reações graves na pele, ver também ponto 4 "Efeitos indesejados").
Em caso de necessidade de exames de sangue ou urina
Se o paciente estiver recebendo Biotrakson por um período prolongado, podem ser necessários exames de sangue regulares.
O Biotrakson pode afetar os resultados da detecção de açúcar na urina e do exame de sangue chamado teste de Coombs. Se o paciente estiver fazendo exames:
- deve informar a pessoa que está coletando a amostra de que o paciente está recebendo Biotrakson.
Se o paciente tem diabetes ou precisa controlar o nível de glicose no sangue, não deve usar alguns testes que possam detectar incorretamente a glicose no sangue enquanto o paciente estiver recebendo ceftriaksona. Se o paciente está controlando o nível de glicose no sangue, deve verificar as instruções do teste e informar o médico, farmacêutico ou enfermeiro.
Deve usar métodos alternativos de teste, se necessário.
Crianças
Antes de administrar o medicamento Biotrakson a uma criança, deve discutir com o médico, farmacêutico ou enfermeiro, se:
- a criança recebeu ou vai receber recentemente um produto que contenha cálcio por via intravenosa.
Medicamento Biotrakson e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o paciente está atualmente tomando ou planeja tomar.
Em particular, deve informar o médico ou farmacêutico se o paciente estiver tomando algum dos seguintes medicamentos:
- um antibiótico da classe das aminoglicosídeos,
- um antibiótico chamado clorafenicol, utilizado no tratamento de infecções, especialmente infecções oculares.
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, achar que pode estar grávida ou planejar ter um filho, deve consultar o médico antes de tomar este medicamento.
O médico avaliará os benefícios do tratamento com o medicamento Biotrakson para a mãe e os riscos para o feto.
Condução de veículos e uso de máquinas
O Biotrakson pode causar tontura. Se o paciente sentir tontura, não deve conduzir veículos ou operar máquinas. Deve informar o médico se apresentar tais sintomas.
Medicamento Biotrakson contém sódio
O medicamento contém 83 mg de sódio (3,6 mmol) (principal componente do sal de cozinha) em 1 g. Isso corresponde a 4,15% da dose diária máxima recomendada de sódio na dieta para adultos.
Preparação do medicamento para administração - ver ponto: "Informações destinadas apenas ao pessoal médico" no final do folheto. Ao calcular o conteúdo total de sódio na solução diluída preparada do medicamento, deve-se considerar o sódio proveniente do diluente. Para obter informações precisas sobre o conteúdo de sódio na solução utilizada para diluir o medicamento, deve-se consultar o folheto do paciente do diluente utilizado.
3. Como tomar o medicamento Biotrakson
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
O Biotrakson é geralmente administrado por um médico ou enfermeiro. Pode ser administrado por infusão intravenosa (gotejamento) ou por injeção direta na veia ou no músculo. O Biotrakson é preparado por um médico, farmacêutico ou enfermeiro e não será misturado ou administrado simultaneamente com soluções que contenham cálcio.
Dose usualmente administrada
O médico decidirá qual dose do medicamento Biotrakson é apropriada para o paciente. A dose depende da gravidade e do tipo de infecção; se o paciente está tomando outros antibióticos; da idade e peso do paciente; da função hepática e renal do paciente. O número de dias ou semanas durante os quais o paciente receberá Biotrakson depende do tipo de infecção.
Adultos, idosos e crianças com 12 anos ou mais e peso corporal de pelo menos
50 quilogramas (kg):
- 1 a 2 g uma vez ao dia, dependendo da gravidade e do tipo de infecção. No caso de infecção grave, o médico pode prescrever uma dose maior (até 4 g uma vez ao dia). Se a dose diária for maior que 2 g, o medicamento pode ser administrado em uma dose ou em duas doses separadas.
Recém-nascidos, lactentes e crianças com idade entre 15 dias e 12 anos e peso corporal abaixo de 50 kg:
- 50 a 80 mg do medicamento Biotrakson por quilograma de peso corporal da criança, uma vez ao dia, dependendo da gravidade e do tipo de infecção. No caso de infecção grave, o médico pode prescrever uma dose maior, até 100 mg por quilograma de peso corporal da criança, com um máximo de 4 g uma vez ao dia. Se a dose diária for maior que 2 g, o medicamento pode ser administrado em uma dose por dia ou em duas doses separadas.
- Crianças com peso corporal de 50 kg ou mais devem receber a dose usual para adultos.
Recém-nascidos com idade entre 0 e 14 dias
- 20 a 50 mg do medicamento Biotrakson por quilograma de peso corporal da criança, uma vez ao dia, dependendo da gravidade e do tipo de infecção.
- A dose diária máxima não deve exceder 50 mg por quilograma de peso corporal da criança.
Pacientes com disfunção hepática ou renal
O paciente pode receber uma dose diferente da usualmente administrada. O médico determinará qual dose do medicamento Biotrakson é apropriada para o paciente e monitorará cuidadosamente o seu estado, dependendo da gravidade da doença hepática e renal.
Administração de dose maior do que a recomendada do medicamento Biotrakson
Em caso de administração acidental de dose maior do que a prescrita pelo médico, deve-se entrar em contato imediatamente com o médico ou o hospital mais próximo.
Omissão da administração do medicamento Biotrakson
Se o paciente esquecer uma injeção, deve recebê-la o mais breve possível. No entanto, se estiver próximo ao horário da próxima injeção, não deve tomar a injeção esquecida. Não deve tomar uma dose dupla (duas injeções ao mesmo tempo) para compensar a injeção esquecida.
Interrupção do tratamento com o medicamento Biotrakson
Não deve interromper o tratamento com o medicamento Biotrakson, a menos que o médico o aconselhe. Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar o médico ou enfermeiro.
4. Efeitos indesejados
Como qualquer medicamento, este medicamento pode causar efeitos indesejados, embora não todos os pacientes os apresentem.
Durante o tratamento com este medicamento, podem ocorrer os seguintes efeitos indesejados:
Reações alérgicas graves (frequência desconhecida - não pode ser determinada com base nos dados disponíveis)
Em caso de ocorrência de reação alérgica grave, deve informar imediatamente o médico.
Os sintomas podem incluir:
- inchaço súbito da face, garganta, lábios ou boca; pode dificultar a respiração ou a deglutição;
- inchaço súbito das mãos, pés e tornozelos;
- dor no peito relacionada à reação alérgica, que pode ser um sinal de ataque cardíaco causado por alergia (síndrome de Kounis).
Reações cutâneas graves (frequência desconhecida - não pode ser determinada com base nos dados disponíveis)
Em caso de ocorrência de reação cutânea grave, deve informar imediatamente o médico.
Os sintomas podem incluir:
- erupção cutânea grave que se desenvolve rapidamente, com bolhas ou descamação da pele e possíveis bolhas na boca (síndrome de Stevens-Johnson [eritema multiforme bolhoso] e síndrome de Lyell [necrólise tóxica epidérmica], também conhecidas como SJS e TEN);
- qualquer um dos seguintes sintomas: erupção cutânea que se espalha, febre alta, aumento da atividade de enzimas hepáticos, anormalidades nos resultados dos exames de sangue (eosinofilia), linfonodos aumentados e acometimento de outros órgãos (reação medicamentosa com eosinofilia e sintomas sistêmicos, também conhecida como síndrome DRESS ou síndrome de hipersensibilidade a medicamentos);
- reação de Jarisch-Herxheimer, que causa febre, calafrios, dor de cabeça, dor muscular e erupção cutânea, geralmente autolimitada; essa reação ocorre logo após o início do tratamento com o medicamento Biotrakson para infecções causadas por espiroquetas, como a doença de Lyme.
Outros efeitos indesejados possíveis
Comuns (até 1 em cada 10 pacientes)
- anormalidades relacionadas a glóbulos brancos (como diminuição do número de leucócitos e aumento do número de eosinófilos) e plaquetas (diminuição do número de plaquetas),
- fezes soltas ou diarreia,
- alterações nos resultados dos exames de sangue que avaliam a função hepática,
- erupção cutânea.
Menos comuns (até 1 em cada 100 pacientes)
- infecções fúngicas (como candidíase),
- diminuição do número de glóbulos brancos (granulocitopenia),
- diminuição do número de glóbulos vermelhos (anemia),
- problemas de coagulação do sangue; os sintomas podem incluir facilidade para formar hematomas e dor e inchaço nas articulações,
- dor de cabeça,
- tontura,
- náuseas e (ou) vômitos,
- coceira (prurido),
- dor ou ardor ao longo da veia na qual o Biotrakson foi administrado; dor no local da injeção do medicamento,
- febre alta,
- resultado anormal do exame de função renal (aumento da creatinina no sangue).
Raros (até 1 em cada 1.000 pacientes)
- inflamação do intestino grosso (colite); os sintomas podem incluir diarreia, geralmente com presença de sangue e muco, dor abdominal e febre,
- dificuldade para respirar (broncoespasmo),
- erupção cutânea elevada (urticária), que pode afetar uma grande parte do corpo, coceira e inchaço,
- sangue ou açúcar na urina,
- inchaço (retenção de líquidos no organismo),
- calafrios. O tratamento com ceftriaksona - especialmente em pacientes idosos com disfunção renal ou neurológica grave - pode causar raramente diminuição do nível de consciência, movimentos anormais, agitação e convulsões.
Com frequência desconhecida (frequência não pode ser determinada com base nos dados disponíveis)
- infecção secundária, que não pode ser tratada com antibióticos prescritos anteriormente,
- um tipo de anemia em que os glóbulos vermelhos são destruídos (anemia hemolítica),
- diminuição significativa do número de glóbulos brancos (agranulocitose),
- convulsões,
- tontura forte (sensação de vertigem),
- inflamação do pâncreas; os sintomas podem incluir dor abdominal forte que irradia para as costas,
- inflamação da mucosa que reveste a boca,
- inflamação da língua; os sintomas podem incluir inchaço, vermelhidão e dor na língua,
- problemas relacionados à vesícula biliar e (ou) fígado, que podem causar dor, náuseas, vômitos, amarelamento da pele, coceira, urina muito escura e fezes de cor de argila,
- condição neurológica que pode ocorrer em recém-nascidos com icterícia grave (icterícia nuclear do cérebro),
- problemas renais causados pelo depósito de sal de ceftriaksona de cálcio; podem
apresentar-se como dor ao urinar ou produção de pequena quantidade de urina,
- resultado falso positivo do teste de Coombs (teste que detecta certos distúrbios do sangue),
- resultado falso positivo do teste de galactosemia (acúmulo anormal de açúcar no organismo),
- O Biotrakson pode afetar os resultados de alguns testes que detectam glicose no sangue - deve consultar o médico sobre isso.
Notificação de efeitos indesejados
Se ocorrerem efeitos indesejados, incluindo quaisquer efeitos indesejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos indesejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Indesejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas
Al. Jerozolimskie 181C
02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio na internet: https://smz.ezdrowie.gov.pl
Os efeitos indesejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos indesejados permitirá reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Biotrakson
O medicamento deve ser conservado em local não visível e inacessível a crianças.
Conservar a uma temperatura de até 25°C. Proteger da luz.
De acordo com as normas de boas práticas, recomenda-se a preparação de soluções logo antes da administração.
A solução preparada pode ser conservada por 24 horas na geladeira, a uma temperatura entre 2°C e 8°C.
Não deve ser utilizado após o prazo de validade impresso na embalagem.
A indicação na embalagem após a abreviatura EXP significa prazo de validade, e após a abreviatura Lot significa número do lote.
Os medicamentos não devem ser jogados na canalização ou lixeiras domésticas. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais utilizados. Esse procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Biotrakson
- A substância ativa do medicamento é ceftriaksona. Cada frasco contém 1 g ou 2 g de ceftriaksona na forma de ceftriaksona sódica.
- O medicamento não contém substâncias auxiliares.
Como é o medicamento Biotrakson e o que a embalagem contém
O medicamento tem a forma de pó cristalino branco ou amarelado.
Biotrakson, 1 g: frasco de vidro com capacidade de 26 ml, fechado com uma rolha de borracha e protegido por uma cápsula de alumínio ou uma cápsula de alumínio com capa, em uma caixa de papelão.
Biotrakson, 2 g: frasco de vidro incolor com capacidade de 26 ml, fechado com uma rolha de borracha bromobutilada e protegido por uma cápsula de alumínio ou uma cápsula de alumínio com capa, em uma caixa de papelão.
A caixa de papelão contém 1 ou 10 frascos.
Nem todos os tamanhos de embalagem podem estar disponíveis no mercado.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Zakłady Farmaceutyczne POLPHARMA S.A.
ul. Pelplińska 19, 83-200 Starogard Gdański
tel. + 48 22 364 61 01
Fabricante
Zakłady Farmaceutyczne POLPHARMA S.A.
Divisão de Produção em Duchnice
ul. Ożarowska 28/30, 05-850 Ożarów Mazowiecki
Data da última atualização do folheto:maio de 2024.
INFORMAÇÕES DESTINADAS APENAS AO PESSOAL MÉDICO ESPECIALIZADO
Método de perfuração do frasco
| Zakłady Farmaceutyczne POLPHARMA S.A. | |
| ul. Pelplińska 19, 83-200 Starogard Gdański |
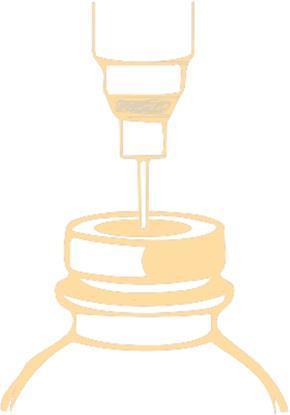
Para perfurar a rolha, deve-se usar uma agulha com diâmetro não maior que 0,8 mm (21 G na escala Gauge [G]).
A agulha deve ser inserida no campo centralmente marcado com um ângulo de 90°.
Método de administração
O medicamento Biotrakson pode ser administrado por infusão intravenosa que dura pelo menos 30 minutos (método de administração recomendado) ou por injeção intravenosa lenta que dura 5 minutos ou por injeção intramuscular profunda. A injeção intravenosa intermitente deve ser administrada em 5 minutos, preferencialmente em uma veia grande. Em lactentes e crianças com menos de 12 anos, as doses intravenosas de 50 mg/kg ou mais devem ser administradas por infusão. Em recém-nascidos, as doses intravenosas devem ser administradas em um período mais longo que 60 minutos para reduzir o risco de encefalopatia bilirubinêmica.
As injeções intramusculares devem ser feitas na profundidade adequada em um músculo relativamente grande; não deve ser administrado mais de 1 g em um único local. A administração intramuscular deve ser considerada quando a administração intravenosa não for possível ou for menos apropriada para o paciente.
Doses maiores que 2 g devem ser administradas por via intravenosa.
Para a reconstituição do medicamento Biotrakson ou para a diluição adicional da solução preparada para administração intravenosa, não deve ser usado um diluente que contenha cálcio (por exemplo, solução de Ringer ou solução de Hartmann) devido ao risco de formação de um precipitado. O sal de ceftriaksona de cálcio também pode se precipitar se o ceftriaksona for misturado com uma solução que contenha cálcio na mesma linha de administração intravenosa. Portanto, o ceftriaksona não deve ser misturado ou administrado simultaneamente com soluções que contenham cálcio.
O volume de substituição do medicamento Biotrakson de 1 g é de 0,68 ml, tanto em água para injeção quanto em solução de lidocaína a 1%.
Após a adição de 10 ml de água para injeção, a concentração final da solução resultante é de 93,63 mg/ml. Após a adição de 3,5 ml de solução de lidocaína a 1%, a concentração final da solução resultante é de 239,23 mg/ml.
O volume de substituição do medicamento Biotrakson de 2 g é de 1,36 ml em água para injeção.
Para evitar a formação de um precipitado em pacientes com mais de 28 dias, o ceftriaksona e as soluções que contenham cálcio podem ser administrados sequencialmente, um após o outro, se as linhas de infusão forem inseridas em locais diferentes ou forem trocadas, ou se as linhas de infusão forem cuidadosamente lavadas com solução fisiológica de cloreto de sódio. Se for necessário administrar soluções de nutrição parenteral total (NPT) que contenham cálcio a pacientes, um profissional de saúde pode considerar o uso de métodos alternativos de tratamento antibacteriano que não estejam associados a esse risco de formação de um precipitado. Se o uso do ceftriaksona em pacientes que necessitam de NPT for considerado necessário, o ceftriaksona e as soluções de NPT podem ser administrados simultaneamente, mas por linhas de infusão diferentes inseridas em locais diferentes. Outra possibilidade é interromper a administração de NPT durante a infusão de ceftriaksona e lavar a linha de infusão entre as administrações das soluções.
Para a reconstituição de soluções para injeção e infusão, não deve ser usado um diluente que contenha cálcio (por exemplo, solução de Ringer ou solução de Hartmann) devido ao risco de formação de um precipitado.
Preparação de soluções para injeção e infusão
| Conteúdo de antibiótico no frasco | Volume do diluente | ||
| Injeção intramuscular | Injeção intravenosa | Infusão intravenosa | |
| 1 g | 3,5 ml | 10 ml | 40-50 ml |
| 2 g | 7,0 ml | 20 ml | 40-50 ml |
Antes da administração, deve-se verificar se a solução é transparente e não contém partículas insolúveis.
Injeção intramuscular
O medicamento deve ser administrado por injeção intramuscular profunda após a reconstituição em um volume adequado de água para injeção ou solução de lidocaína a 1%.
O medicamento não deve ser misturado na mesma seringa com nenhum outro medicamento, exceto a solução de lidocaína a 1%.
Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
Doses maiores que 1 g devem ser divididas e injetadas em mais de um local.
Doses maiores que 2 g devem ser administradas por via intravenosa.
Injeção intravenosa (5 minutos)
O conteúdo do frasco é reconstituído em água para injeção em um volume dependente da dose, como mostrado na tabela acima. Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
Infusão intravenosa (pelo menos 30 minutos)
Para a preparação de soluções para infusão intravenosa com concentração de ceftriaksona entre 10 mg/ml e 40 mg/ml, o pó é reconstituído em água para injeção. A solução resultante deve ser então diluída em um dos seguintes diluentes:
solução de cloreto de sódio a 0,9%;
solução de glicose a 5%;
solução de glicose a 10%;
solução de dextrana a 6% em solução de glicose a 5%;
solução de cloreto de sódio a 0,45% em solução de glicose a 2,5%.
Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
A solução do medicamento Biotrakson pode ser incolor ou amarelo-clara, a intensidade da coloração depende do tipo de diluente e da concentração de ceftriaksona.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorZakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w Duchnicach
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BiotraksonForma farmacêutica: Pó, 1 gSubstância ativa: ceftriaxoneFabricante: Zakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w DuchnicachRequer receita médicaForma farmacêutica: Pó, 1 gSubstância ativa: ceftriaxoneFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requer receita médicaForma farmacêutica: Pó, 2 gSubstância ativa: ceftriaxoneFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requer receita médica
Alternativas a Biotrakson noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Biotrakson em Espanha
Alternativa a Biotrakson em Ukraine
Médicos online para Biotrakson
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Biotrakson – sujeita a avaliação médica e regras locais.















