

Biotrakson

Pergunte a um médico sobre a prescrição de Biotrakson

Como usar Biotrakson
Folheto informativo para o doente: informação para o doente
Biotrakson, 1 g pó de reconstituição para solução injectável ou perfusão
Biotrakson, 2 g, pó de reconstituição para solução injectável ou perfusão
Ceftriaxona
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Biotrakson e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Biotrakson
- 3. Como tomar o medicamento Biotrakson
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Biotrakson
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Biotrakson e para que é utilizado
O Biotrakson é um antibiótico utilizado em adultos e crianças (incluindo recém-nascidos). O seu efeito consiste em matar as bactérias que causam infecções. Pertence a um grupo de medicamentos chamados cefalosporinas.
O Biotrakson é utilizado no tratamento de infecções:
- do cérebro (meningite),
- dos pulmões,
- do ouvido médio,
- da barriga e da parede da cavidade abdominal (peritonite),
- do trato urinário e dos rins,
- dos ossos e das articulações,
- da pele e dos tecidos moles,
- do sangue,
- do coração.
Este medicamento pode ser utilizado:
- no tratamento de certas infecções transmitidas por via sexual (gonorreia e sífilis),
- no tratamento de doentes com baixo número de glóbulos brancos (neutropenia) que têm febre causada por infecção bacteriana,
- no tratamento de infecções no peito em adultos com bronquite crónica,
- no tratamento da doença de Lyme (doença transmitida por carrapatos) em adultos e crianças, incluindo recém-nascidos a partir do 15º dia de vida,
- para prevenir infecções durante operações.
2. Informações importantes antes de tomar o medicamento Biotrakson
Quando não tomar o medicamento Biotrakson:
- se o doente tiver alergia à ceftriaxona;
- se o doente tiver tido uma reação alérgica súbita ou grave a penicilina ou antibióticos semelhantes (como cefalosporinas, carbapenémicos, monobactâmicos); os sintomas de tal reação podem incluir inchaço súbito da garganta ou face, que pode dificultar a respiração ou a deglutição, inchaço súbito das mãos, pés e tornozelos, dor no peito e erupção cutânea grave que aparece rapidamente;
- se o doente tiver alergia à lidocaína e for receber Biotrakson por injeção intramuscular.
Não deve ser utilizado em crianças pequenas, se:
- a criança for prematura,
- a criança for recém-nascida (com até 28 dias) e tiver certos problemas de sangue ou icterícia [amarelamento da pele e (ou) brancos dos olhos], ou for receber intravenosamente um medicamento que contenha cálcio.
Precauções e advertências
Antes de começar a tomar o medicamento Biotrakson, deve discutir com o médico, farmacêutico ou enfermeiro, se:
- o doente recebeu ou vai receber recentemente produtos que contenham cálcio,
- o doente teve recentemente diarreia após tratamento com antibiótico,
- o doente teve problemas intestinais, particularmente colite (inflamação do intestino grosso),
- o doente tem problemas de fígado ou rins (ver ponto 4),
- o doente tem cálculos biliares ou cálculos renais,
- o doente tem outras doenças, como anemia hemolítica (diminuição do número de glóbulos vermelhos, que causa palidez e fraqueza ou falta de ar),
- o doente está a seguir uma dieta com baixo teor de sódio,
- o doente tem ou teve anteriormente algum dos seguintes sintomas: erupção cutânea, vermelhidão da pele, bolhas na área dos lábios, olhos ou boca, descamação da pele, febre alta, sintomas semelhantes aos da gripe, aumento da atividade de enzimas hepáticos nos resultados dos exames de sangue e aumento do número de um certo tipo de glóbulos brancos (eosinofilia) e linfonodos aumentados (sintomas de reações graves na pele, ver também ponto 4 "Efeitos não desejados").
Em caso de necessidade de realizar exames de sangue ou urina
Se o doente estiver a tomar Biotrakson durante um período prolongado, podem ser necessários exames de sangue regulares.
O Biotrakson pode afetar os resultados da detecção de açúcar na urina e do exame de sangue chamado teste de Coombs. Se o doente estiver a realizar exames:
- deve informar a pessoa que está a recolher a amostra de que está a tomar Biotrakson.
Se o doente tem diabetes ou precisa controlar o nível de glicose no sangue, não deve utilizar para esse fim alguns testes que possam detectar incorrectamente a glicose no sangue enquanto estiver a tomar ceftriaxona. Se o doente estiver a controlar o nível de glicose no sangue, deve verificar as instruções do teste e informar o médico, farmacêutico ou enfermeiro.
Deve utilizar métodos alternativos de teste, se necessário.
Crianças
Antes de administrar o medicamento Biotrakson a uma criança, deve discutir com o médico, farmacêutico ou enfermeiro, se:
- a criança recebeu ou vai receber recentemente um produto que contenha cálcio por via intravenosa.
Medicamento Biotrakson e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, e sobre os medicamentos que planeia tomar.
Em particular, deve informar o médico ou farmacêutico se estiver a tomar algum dos seguintes medicamentos:
- um antibiótico pertencente ao grupo das aminoglicosídeos,
- um antibiótico chamado clorafenicol, utilizado no tratamento de infecções, particularmente infecções oculares.
Gravidez, amamentação e fertilidade
Se a doente estiver grávida ou a amamentar, suspeitar que pode estar grávida ou planeiar ter um filho, deve consultar o médico antes de tomar este medicamento.
O médico avaliará os benefícios do tratamento com o medicamento Biotrakson para a mãe e os riscos para o feto.
Condução de veículos e utilização de máquinas
O Biotrakson pode causar tonturas. Se o doente sentir tonturas, não deve conduzir veículos ou operar máquinas. Deve informar o médico se apresentar tais sintomas.
Medicamento Biotrakson contém sódio
O medicamento contém 83 mg de sódio (3,6 mmol) (principal componente do sal de cozinha) em 1 g. Isto corresponde a 4,15% da dose diária máxima recomendada de sódio na dieta para adultos.
Preparação do medicamento para administração - ver ponto: "Informações destinadas apenas ao pessoal médico" no final do folheto. Ao calcular o teor total de sódio na solução reconstituída do medicamento, deve ter em conta o sódio proveniente do diluente. Para obter informações precisas sobre o teor de sódio na solução utilizada para diluir o medicamento, deve consultar o folheto do paciente do diluente utilizado.
3. Como tomar o medicamento Biotrakson
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
O Biotrakson é geralmente administrado por um médico ou enfermeiro. Pode ser administrado por infusão intravenosa (gotejamento) ou por injeção directa na veia ou no músculo. O Biotrakson é preparado por um médico, farmacêutico ou enfermeiro e não deve ser misturado ou administrado simultaneamente com soluções que contenham cálcio.
Dose normalmente utilizada
O médico decidirá qual a dose de Biotrakson adequada para o doente. A dose depende da gravidade e do tipo de infecção; do facto de o doente estar a tomar outros antibióticos; da idade e do peso do doente; da função hepática e renal do doente. O número de dias ou semanas durante os quais o doente irá receber Biotrakson depende do tipo de infecção.
Adultos, pessoas idosas e crianças com 12 anos ou mais e com um peso corporal de pelo menos
50 quilogramas (kg):
- 1 a 2 g uma vez por dia, dependendo da gravidade e do tipo de infecção. No caso de infecção grave, o médico pode prescrever uma dose maior (até 4 g uma vez por dia). Se a dose diária for maior que 2 g, o medicamento pode ser administrado em uma dose ou em duas doses separadas.
Recém-nascidos, lactentes e crianças com idade entre 15 dias e 12 anos e com um peso corporal inferior a 50 kg:
- 50 a 80 mg de Biotrakson por quilograma de peso corporal da criança uma vez por dia, dependendo da gravidade e do tipo de infecção. No caso de infecção grave, o médico pode prescrever uma dose maior, até 100 mg por quilograma de peso corporal da criança, máximo 4 g uma vez por dia. Se a dose diária for maior que 2 g, o medicamento pode ser administrado em uma dose por dia ou em duas doses separadas.
- Crianças com um peso corporal de 50 kg ou mais devem receber a dose normal para adultos.
Recém-nascidos com até 14 dias
- 20 a 50 mg de Biotrakson por quilograma de peso corporal da criança uma vez por dia, dependendo da gravidade e do tipo de infecção.
- A dose diária máxima não deve exceder 50 mg por quilograma de peso corporal da criança.
Doentes com disfunção hepática ou renal
O doente pode receber uma dose diferente da normalmente utilizada. O médico decidirá qual a dose de Biotrakson adequada para o doente e irá controlar cuidadosamente o seu estado, dependendo da gravidade da doença hepática e renal.
Administração de uma dose maior do que a recomendada de Biotrakson
Em caso de administração acidental de uma dose maior do que a prescrita pelo médico, deve contactar imediatamente o médico ou o hospital mais próximo.
Omissão da administração de Biotrakson
Se o doente esquecer uma injeção, deve recebê-la o mais breve possível. No entanto, se estiver próximo o momento da próxima injeção, não deve tomar a injeção esquecida. Não deve tomar uma dose dupla (duas injeções ao mesmo tempo) para compensar a injeção esquecida.
Interrupção da administração de Biotrakson
Não deve interromper a administração de Biotrakson, a não ser que o médico o aconselhe. Em caso de dúvidas adicionais sobre a administração deste medicamento, deve consultar o médico ou enfermeiro.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Durante a administração deste medicamento, podem ocorrer os seguintes efeitos não desejados:
Reações alérgicas graves (frequência desconhecida - não pode ser estimada com base nos dados disponíveis)
Em caso de ocorrência de uma reação alérgica grave, deve informar imediatamente o médico.
Os sintomas podem incluir:
- inchaço súbito da face, garganta, lábios ou boca; pode dificultar a respiração ou a deglutição;
- inchaço súbito das mãos, pés e tornozelos;
- dor no peito associada a uma reação alérgica, que pode ser um sintoma de um ataque cardíaco causado por alergia (síndrome de Kounis).
Reações cutâneas graves (frequência desconhecida - não pode ser estimada com base nos dados disponíveis)
Em caso de ocorrência de uma reação cutânea grave, deve informar imediatamente o médico.
Os sintomas de tal reação podem incluir:
- erupção cutânea grave que se desenvolve rapidamente, com bolhas ou descamação da pele e possíveis bolhas na boca (síndrome de Stevens-Johnson [eritema multiforme bolhoso] e síndrome de Lyell [necrólise tóxica epidérmica], também conhecidas como SJS e TEN);
- qualquer um dos seguintes sintomas: erupção cutânea que se espalha, febre alta, aumento da atividade de enzimas hepáticos, anormalidades nos resultados dos exames de sangue (eosinofilia), linfonodos aumentados e envolvimento de outros órgãos (reação medicamentosa com eosinofilia e sintomas sistémicos, também conhecida como síndrome DRESS ou síndrome de hipersensibilidade a medicamentos);
- reação de Jarisch-Herxheimer, que causa febre, calafrios, dor de cabeça, dor muscular e erupção cutânea, geralmente autolimitada; esta reação ocorre pouco após o início do tratamento com Biotrakson para infecções causadas por espiroquetas, como a doença de Lyme.
Outros possíveis efeitos não desejados
Comuns (até 1 em 10 doentes)
- anormalidades relacionadas com glóbulos brancos (como diminuição do número de leucócitos e aumento do número de eosinófilos) e plaquetas (diminuição do número de plaquetas),
- fezes soltas ou diarreia,
- alterações nos resultados dos exames de sangue que avaliam a função hepática,
- erupção cutânea.
Menos comuns (até 1 em 100 doentes)
- infecções fúngicas (como candidíase),
- diminuição do número de glóbulos brancos (granulocitopenia),
- diminuição do número de glóbulos vermelhos (anemia),
- problemas de coagulação do sangue; os sintomas podem incluir hematomas fáceis e dor e inchaço nas articulações,
- dor de cabeça,
- tonturas,
- náuseas e (ou) vómitos,
- coceira (prurido),
- dor ou ardor ao longo da veia onde foi administrado o Biotrakson; dor no local da injeção do medicamento,
- febre alta,
- resultado anormal do exame de função renal (aumento da creatinina no sangue).
Raros (até 1 em 1 000 doentes)
- inflamação do intestino grosso (colite); os sintomas incluem diarreia, geralmente com sangue e muco, dor abdominal e febre,
- dificuldade em respirar (broncoespasmo),
- erupção cutânea elevada (urticária), que pode afetar uma grande parte do corpo, coceira e inchaço,
- sangue ou açúcar na urina,
- inchaço (retenção de água no organismo),
- calafrios. O tratamento com ceftriaxona - especialmente em doentes idosos com disfunção renal ou neurológica grave - pode causar raramente diminuição do nível de consciência, movimentos anormais, agitação e convulsões.
Com frequência desconhecida (frequência não pode ser estimada com base nos dados disponíveis)
- infecção secundária, que não pode ser tratada com antibióticos prescritos anteriormente,
- um tipo de anemia em que os glóbulos vermelhos são destruídos (anemia hemolítica),
- diminuição significativa do número de glóbulos brancos (agranulocitose),
- convulsões,
- tonturas fortes (sensação de rodopio),
- inflamação do pâncreas; os sintomas incluem dor abdominal forte, que irradia para as costas,
- inflamação da mucosa que reveste a boca,
- inflamação da língua; os sintomas incluem inchaço, vermelhidão e dor na língua,
- problemas relacionados com a vesícula biliar e (ou) fígado, que podem causar dor, náuseas, vómitos, amarelamento da pele, coceira, urina muito escura e fezes com cor de argila,
- um estado neurológico que pode ocorrer em recém-nascidos com icterícia grave (icterícia nuclear do cérebro),
- problemas renais causados pelo depósito de sal de cálcio da ceftriaxona; podem
apresentar-se como dor ao urinar ou produção de uma pequena quantidade de urina,
- resultado falso positivo do teste de Coombs (teste que detecta certos distúrbios do sangue),
- resultado falso positivo do teste de galactosemia (acúmulo anormal de açúcar no organismo),
- O Biotrakson pode afetar os resultados de alguns testes de detecção de glicose no sangue - deve consultar o médico sobre isso.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados directamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Farmácia e Medicamentos
Av. do Brasil, 53
1749-004 Lisboa
Telefone: +351 21 798 7000
Fax: +351 21 798 7020
Sítio da Internet: https://www.infarmed.pt/
Os efeitos não desejados também podem ser notificados ao titular da autorização de introdução no mercado.
A notificação de efeitos não desejados permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Biotrakson
O medicamento deve ser conservado num local fora do alcance e da vista das crianças.
Conservar a uma temperatura não superior a 25°C. Proteger da luz.
De acordo com as boas práticas de manipulação, recomenda-se a preparação de soluções para administração imediatamente antes da administração.
A solução reconstituída pode ser conservada durante 24 horas no frigorífico, a uma temperatura entre 2°C e 8°C.
As soluções para perfusão intravenosa preparadas com cloreto de sódio e glicose não devem ser conservadas no frigorífico (2-8°C) devido à incompatibilidade física dos componentes em temperaturas baixas.
Não utilizar este medicamento após o prazo de validade impresso na embalagem.
A indicação na embalagem após a abreviatura EXP significa prazo de validade, e após a abreviatura Lote significa número do lote.
Os medicamentos não devem ser eliminados na canalização ou nos contentores de resíduos domésticos. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não necessita. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Biotrakson
- A substância ativa do medicamento é a ceftriaxona. Cada frasco contém 1 g ou 2 g de ceftriaxona na forma de ceftriaxona sódica.
- O medicamento não contém substâncias auxiliares.
Como é o medicamento Biotrakson e que conteúdo tem a embalagem
O medicamento tem a forma de pó cristalino branco ou amarelado.
Biotrakson, 1 g: frasco de vidro com capacidade de 26 ml, fechado com um rolha de borracha e protegido por uma tampa de alumínio ou uma tampa de alumínio com capuchão, num estojo de cartão.
Biotrakson, 2 g: frasco de vidro incolor com capacidade de 26 ml, fechado com um rolha de borracha bromobutilada e protegido por uma tampa de alumínio ou uma tampa de alumínio com capuchão, num estojo de cartão.
O estojo de cartão contém 1 ou 10 frascos.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Titular da autorização de introdução no mercado e fabricante
Titular da autorização de introdução no mercado
LABORATÓRIO EDOL - PRODUTOS FARMACÊUTICOS, S.A.
Rua João de Deus, 21
1200-470 Lisboa
Telefone: +351 213 155 700
Fax: +351 213 155 709
Fabricante
LABORATÓRIO EDOL - PRODUTOS FARMACÊUTICOS, S.A.
Unidade Fabril de Alverca
Estrada Nacional 10, km 28,3 - Apartado 26
2615-127 Alverca do Ribatejo
Data da última revisão do folheto:maio de 2024
INFORMAÇÕES DESTINADAS APENAS AO PESSOAL MÉDICO ESPECIALIZADO
Método de perfuração do frasco
| LABORATÓRIO EDOL - PRODUTOS FARMACÊUTICOS, S.A. | |
| Rua João de Deus, 21, 1200-470 Lisboa | |
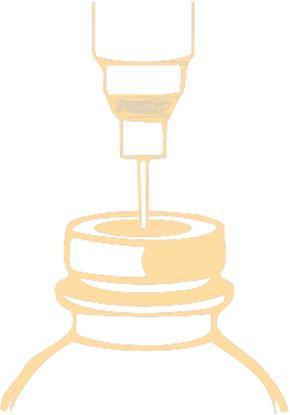
Para perfurar o rolha, deve utilizar uma agulha com diâmetro não superior a 0,8 mm (21 G na escala Gauge [G]).
A agulha deve ser inserida no campo centralmente marcado a um ângulo de 90°.
Método de administração
O medicamento Biotrakson pode ser administrado por perfusão intravenosa com duração mínima de 30 minutos (método de administração recomendado) ou por injeção intravenosa lenta com duração de 5 minutos ou por injeção intramuscular profunda. Na injeção intravenosa intermitente, o medicamento deve ser administrado durante 5 minutos, preferencialmente numa veia grande. Em lactentes e crianças com menos de 12 anos, as doses intravenosas de 50 mg/kg ou mais devem ser administradas por perfusão. Em recém-nascidos, as doses intravenosas devem ser administradas durante um período mais longo do que 60 minutos, para diminuir o risco de encefalopatia bilirubinica.
As injeções intramusculares devem ser realizadas na profundidade adequada num músculo relativamente grande; não deve ser administrada mais de 1 g num único local. A administração intramuscular deve ser considerada quando a administração intravenosa não for possível ou for menos apropriada para o doente.
As doses superiores a 2 g devem ser administradas por via intravenosa.
Preparação de soluções para injeção e perfusão
| Conteúdo de antibiótico no frasco | Volume do diluente | ||
| Injeção intramuscular | Injeção intravenosa | Perfusão intravenosa | |
| 1 g | 3,5 ml | 10 ml | 40-50 ml |
| 2 g | 7,0 ml | 20 ml | 40-50 ml |
Antes da administração, deve verificar se a solução é transparente e não contém partículas insolúveis.
Injeção intramuscular
O medicamento deve ser administrado por injeção intramuscular profunda após reconstituição com a quantidade adequada de água para injeção ou solução a 1% de cloridrato de lidocaína.
O medicamento não deve ser misturado na mesma seringa com qualquer outro medicamento além da solução a 1% de cloridrato de lidocaína.
Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
As doses superiores a 1 g devem ser divididas e injetadas em mais de um local.
As doses superiores a 2 g devem ser administradas por via intravenosa.
Injeção intravenosa (5 minutos)
O conteúdo do frasco é reconstituído com água para injeção, num volume dependente da dose, como apresentado na tabela acima. Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
Perfusão intravenosa (pelo menos 30 minutos)
Para preparar soluções para perfusão intravenosa com uma concentração de ceftriaxona entre 10 mg/ml e 40 mg/ml, o pó é reconstituído com água para injeção. A solução resultante deve ser posteriormente diluída com um dos seguintes soluções:
solução a 0,9% de cloreto de sódio;
solução a 5% de glicose;
solução a 10% de glicose;
solução a 6% de dextrano em solução a 5% de glicose;
solução a 0,45% de cloreto de sódio em solução a 2,5% de glicose.
Não deve ser administrado por via intravenosa a solução do medicamento com lidocaína.
A solução do medicamento Biotrakson pode ser incolor ou ligeiramente amarelada, a intensidade da cor dependendo do tipo de diluente e da concentração de ceftriaxona.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorZakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w Duchnicach
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BiotraksonForma farmacêutica: Pó, 2 gSubstância ativa: ceftriaxoneFabricante: Zakłady Farmaceutyczne POLPHARMA S.A. Zakłady Farmaceutyczne POLPHARMA S.A. Oddział Produkcyjny w DuchnicachRequer receita médicaForma farmacêutica: Pó, 1 gSubstância ativa: ceftriaxoneFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requer receita médicaForma farmacêutica: Pó, 2 gSubstância ativa: ceftriaxoneFabricante: ACS Dobfar S.p.A ACS Dobfar S.p.A.Requer receita médica
Alternativas a Biotrakson noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Biotrakson em Espanha
Alternativa a Biotrakson em Ukraine
Médicos online para Biotrakson
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Biotrakson – sujeita a avaliação médica e regras locais.















