
BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/mL + 2 mg/mL EYE DROPS, SUSPENSION

How to use BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/mL + 2 mg/mL EYE DROPS, SUSPENSION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
- Introduction
- What is Brinzolamida/Brimonidina Zentiva and what is it used for
- What you need to know before you use Brinzolamida/Brimonidina Zentiva
- How to use Brinzolamida/Brimonidina Zentiva
- Possible side effects
- Storage of Brinzolamida/Brimonidina Zentiva
- Container Content and Additional Information
Introduction
Package Leaflet: Information for the User
Brinzolamida/Brimonidina Zentiva 10 mg/ml + 2mg/ml eye drops, suspension
Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
- Keep this leaflet, you may need to read it again.
- If you have any further questions, ask your doctor or pharmacist.
- This medicine has been prescribed for you only. Do not pass it on to others. It may harm them, even if their signs of illness are the same as yours.
- If you get any side effects, talk to your doctor or pharmacist. This includes any possible side effects not listed in this leaflet. See section 4.
Contents of the pack
- What is Brinzolamida/Brimonidina Zentiva and what is it used for
- What you need to know before you use Brinzolamida/Brimonidina Zentiva
- How to use Brinzolamida/Brimonidina Zentiva
- Possible side effects
- Storage of Brinzolamida/Brimonidina Zentiva
- Contents of the pack and other information
1. What is Brinzolamida/Brimonidina Zentiva and what is it used for
Brinzolamida/Brimonidina Zentiva contains two active substances, brinzolamide and brimonidine tartrate. Brinzolamide belongs to a group of medicines called carbonic anhydrase inhibitors and brimonidine tartrate belongs to a group of medicines called alpha-2 adrenergic receptor agonists. Both substances work together to reduce the pressure inside the eye.
Brinzolamida/Brimonidina Zentiva is used to reduce pressure in the eyes in adult patients (18 years or older) who have eye diseases known as glaucoma or ocular hypertension and whose high pressure in the eyes cannot be controlled effectively with a single medicine.
2. What you need to know before you use Brinzolamida/Brimonidina Zentiva
Do not takeBrinzolamida/Brimonidina Zentiva
- if you are allergic to brinzolamide or brimonidine tartrate or any of the other ingredients of this medicine (listed in section 6)
- if you are allergic to sulfonamides (e.g. medicines used to treat diabetes and infections and also diuretics)
- if you are taking monoamine oxidase inhibitors (MAOIs) (e.g. medicines for treating depression or Parkinson's disease) or certain antidepressants. You should tell your doctor if you are taking any antidepressant medicine.
- if you have severe kidney problems
- if you have too much acid in the blood (a condition called hyperchloremic acidosis)
- in infants and toddlers under 2 years
Warnings and precautions
Talk to your doctor, ophthalmologist (eye specialist) or pharmacist before using Brinzolamida/Brimonidina Zentiva if you have now or have had in the past:
- liver problems
- a type of high pressure in the eyes called narrow-angle glaucoma
- dry eyes or cornea problems
- heart disease (symptoms may include chest pain or shortness of breath), heart failure, high or low blood pressure
- depression
- altered or poor blood circulation (such as Raynaud's disease, Raynaud's syndrome or cerebral insufficiency).
- if you have ever developed a severe skin rash, blistering or peeling of the skin after using Brinzolamida/Brimonidina Zentiva or other related medicines.
Be careful with Brinzolamida/Brimonidina Zentiva:
Severe skin reactions, including Stevens-Johnson syndrome and toxic epidermal necrolysis, have been reported in association with brinzolamide treatment. Stop using Brinzolamida/Brimonidina Zentiva and seek immediate medical attention if you notice any of the symptoms related to these severe skin reactions described in section 4.
If you wear soft contact lenses, do not use the eye drops with the lenses in place. See the section "Use of contact lenses: Brinzolamida/Brimonidina Zentiva contains benzalkonium chloride" below).
Children and adolescents
Brinzolamida/Brimonidina Zentiva is not indicated in children and adolescents under 18 years because it has not been studied in this age group. It is particularly important that the medicine is not used in children under 2 years (see section "Do not use Brinzolamida/Brimonidina Zentiva" above) because it is unlikely to be safe.
Using Brinzolamida/Brimonidina Zentiva with other medicines
Tell your doctor, ophthalmologist (eye specialist) or pharmacist if you are using, have recently used or might use any other medicines.
Brinzolamida/Brimonidina Zentiva may affect or be affected by other medicines you are using, including other eye drops for glaucoma treatment.
Tell your doctor if you are taking or plan to take any of the following medicines:
- medicines to lower blood pressure
- heart medicines, including digoxin (used to treat heart conditions)
- other glaucoma medicines that also treat high altitude sickness known as acetazolamide, methazolamide and dorzolamide
- medicines that may affect metabolism, such as chlorpromazine, methylphenidate and reserpine
- antiviral, antiretroviral (used to treat human immunodeficiency virus (HIV)) or antibiotic medicines
- anti-fungal or antimycotic medicines
- monoamine oxidase inhibitors (MAOIs) or antidepressants, including amitriptyline, nortriptyline, clomipramine, mianserin, venlafaxine and duloxetine.
- anesthetics
- sedatives, opioids or barbiturates
You should also tell your doctor if you change the dose of any of your current medicines.
Taking Brinzolamida/Brimonidina Zentiva with alcohol
If you regularly drink alcohol, talk to your doctor, ophthalmologist (eye specialist) or pharmacist before taking this medicine. Brinzolamida/Brimonidina Zentiva may be affected by alcohol.
Pregnancy and breastfeeding
If you are pregnant, think you may be pregnant or are planning to have a baby, ask your doctor or pharmacist for advice before using this medicine. Women who may become pregnant are recommended to use effective contraceptive methods during treatment with Brinzolamida/Brimonidina Zentiva. The use of Brinzolamida/Brimonidina Zentiva is not recommended during pregnancy. Do not use Brinzolamida/Brimonidina Zentiva unless your doctor tells you to.
If you are breastfeeding, Brinzolamida/Brimonidina Zentiva may pass into breast milk. The use of Brinzolamida/Brimonidina Zentiva is not recommended during breastfeeding.
Driving and using machines
You may notice that your vision is blurry or abnormal for a time just after using Brinzolamida/Brimonidina Zentiva. Brinzolamida/Brimonidina Zentiva may also cause dizziness, drowsiness or fatigue in some patients.
Do not drive or use machines until the symptoms go away.
Brinzolamida/Brimonidina Zentiva contains benzalkonium chloride
This medicine contains 0.15 mg of benzalkonium chloride per 5 ml, which is equivalent to 0.03 mg/ml.
Benzalkonium chloride can be absorbed by soft contact lenses and may alter the color of the contact lenses. Remove the contact lenses before using this medicine and wait 15 minutes before putting them back.
Benzalkonium chloride may cause eye irritation, especially if you have dry eyes or other corneal diseases (the transparent layer of the front of the eye). Talk to your doctor if you feel any unusual sensation, itching or pain in the eye after using this medicine.
3. How to use Brinzolamida/Brimonidina Zentiva
Follow exactly the administration instructions of this medicine given by your doctor, ophthalmologist (eye specialist) or pharmacist. If you are not sure, talk to your doctor, ophthalmologist (eye specialist) or pharmacist again.
Use Brinzolamida/Brimonidina Zentiva only for the eyes. Do not swallow or inject.
The recommended doseis one drop in the affected eye(s) twice a day. Use it at the same time every day.
How to use
- Wash your hands before starting.
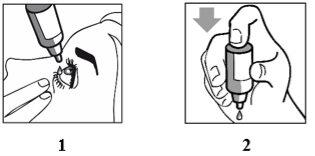
- Shake well before use.
- Remove the cap from the bottle. After removing the cap, if the tamper-evident ring is loose, remove it before using the medicine.
- Do not touch the dropper with your fingers when opening or closing the bottle. You could infect the drops.
- Hold the bottle, upside down, between your thumb and fingers. Tilt your head back.
- Lower the lower eyelid with a clean finger, until a "pocket" is formed between the eyelid and the eye. The drop will fall here (image 1).
- Bring the tip of the bottle close to the eye. Do this in front of a mirror if it helps.
- Do not touch your eye or eyelid, nearby areas or other surfaces with the dropper. You could infect the drops.
- Gently press the base of the bottle to release one drop of Brinzolamida/Brimonidina Zentiva.
- Do not squeeze the bottle: it is designed for a gentle pressure on the base to be enough (image 2).
To reduce the amount of medicine that could pass into the rest of the body after applying the eye drops, close your eye and apply gentle pressure on the corner of your eye near your nose with your finger for at least 2 minutes.
If you use drops in both eyes, repeat the steps in the other eye. You do not need to close and shake the bottle before applying the drop in the other eye. Close the bottle cap firmly immediately after use.
If you are using other eye drops in addition to Brinzolamida/Brimonidina Zentiva, wait at least 5 minutes between using Brinzolamida/Brimonidina Zentiva and the other drops.
If a drop falls outside the eye, try again.
If you use more Brinzolamida/Brimonidina Zentiva than you should
Rinse your eye with warm water. Do not apply more drops until it is time for your next dose.
Adults who had accidentally ingested medicines containing brimonidine experienced a decrease in heart rate, decrease in blood pressure, which may be followed by an increase in blood pressure, heart failure, difficulty breathing and effects on the nervous system. If this happens, contact your doctor immediately.
Severe side effects have been reported in children who had accidentally ingested medicines containing brimonidine. The signs included drowsiness, floppiness, low body temperature, paleness and breathing difficulties. If this happens, contact your doctor immediately.
If you have accidentally ingested Brinzolamida/Brimonidina Zentiva, you should contact your doctor immediately.
If you forget to use Brinzolamida/Brimonidina Zentiva
Continue with the next dose as planned. Do not use a double dose to make up for a forgotten dose. Do not use more than one drop twice a day in the affected eye(s).
If you stop using Brinzolamida/Brimonidina Zentiva
Do not stop using Brinzolamida/Brimonidina Zentiva without talking to your doctor first. If you stop using Brinzolamida/Brimonidina Zentiva, the pressure in your eye will not be controlled, which could lead to loss of vision.
If you have any further questions on the use of this product, ask your doctor, ophthalmologist (eye specialist) or pharmacist.
4. Possible side effects
Like all medicines, this medicine can cause side effects, although not everybody gets them.
If you experience any of the following side effects, stop using this medicine and seek immediate medical attention, as they may be signs of an allergic reaction to the medicine. The frequency of an allergic reaction to this medicine is not known (the frequency cannot be estimated from the available data).
- Severe skin reactions, such as rash, redness or itching on the body or eyes.
- Difficulty breathing
- Chest pain, irregular heartbeat
Talk to your doctor immediately if you experience extreme tiredness or dizziness.
The following side effects have been observed with Brinzolamida/Brimonidina Zentiva and other medicines that contain brinzolamide or brimonidine alone.
Stop using Brinzolamida/Brimonidina Zentiva and seek immediate medical attention if you notice any of the following symptoms:
- red patches, target-like or circular patches on the trunk, often with central blisters, skin peeling, ulcers in the mouth, throat, nose, genitals and eyes. These severe skin rashes may be preceded by fever and flu-like symptoms (Stevens-Johnson syndrome, toxic epidermal necrolysis).
Common(may affect up to 1 in 10 people)
- Eye effects: allergic conjunctivitis (eye allergy), inflammation of the eye surface, eye pain, eye discomfort, blurred or abnormal vision, eye redness.
- Other side effects: drowsiness, dizziness, bad taste, dry mouth.
Uncommon(may affect up to 1 in 100 people)
- Eye effects: damage to the eye surface with loss of cells, eyelid inflammation, deposits on the eye surface, sensitivity to light, eye swelling (affecting the cornea or eyelid), dry eye, eye discharge, watery eye, eyelid redness, abnormal or decreased sensation in the eye, tired eye, reduced vision, double vision, product particles in the eyes.
- Other side effects: low blood pressure, chest pain, irregular heartbeat, slow or fast heart rate, palpitations, difficulty sleeping (insomnia), nightmares, depression, general weakness, headache, dizziness, nervousness, irritability, general feeling of discomfort, memory loss, difficulty breathing, asthma, nosebleeds, cold symptoms, dryness of the nose or throat, sore throat, throat irritation, cough, nasal discharge, nasal congestion, sneezing, sinus infection, chest congestion, ringing in the ears, indigestion, intestinal gas or stomach pain, nausea, diarrhea, vomiting, abnormal sensation in the mouth, increased allergic symptoms on the skin, skin rash, abnormal sensation on the skin, hair loss, generalized itching, increased levels of chloride in the blood or decreased red blood cell count observed in blood tests, pain, back pain, muscle pain or cramp, kidney pain like lower back pain, decreased libido, male sexual dysfunction.
Rare(may affect up to 1 in 10,000 people)
- Eye effects: decreased pupil size
- Other side effects: fainting, high blood pressure.
Frequency not known(cannot be estimated from the available data)
- Eye effects: decreased eyelash growth
- Other side effects: tremor, decreased sensitivity, loss of taste, abnormal liver function values observed in blood tests, facial swelling, joint pain, frequent urination, chest pain, swelling of the limbs, red patches, target-like or circular patches on the trunk, often with central blisters, skin peeling, ulcers in the mouth, throat, nose, genitals and eyes, which may be preceded by fever and flu-like symptoms. These severe skin rashes can be life-threatening (Stevens-Johnson syndrome, toxic epidermal necrolysis).
Reporting of side effects
If you experience any side effects, talk to your doctor, ophthalmologist (eye specialist) or pharmacist, even if it is possible side effects not listed in this leaflet. You can also report side effects directly through the Spanish Pharmacovigilance System for Human Use Medicines: https://www.notificaram.es. By reporting side effects, you can help provide more information on the safety of this medicine.
5. Storage of Brinzolamida/Brimonidina Zentiva
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the carton after “EXP”. The expiry date is the last day of the month shown.
This medicine does not require any special storage conditions.
Discard the bottle 4 weeks after first opening to prevent infections and use a new bottle. Write the date of opening on the space provided on the carton.
Medicines should not be disposed of via wastewater or household waste. Ask your pharmacist how to dispose of medicines no longer required. These measures will help protect the environment.
6. Container Content and Additional Information
Composition of Brinzolamida/Brimonidina Zentiva
- The active ingredients are brinzolamide and brimonidine tartrate. One ml of suspension contains 10 mg of brinzolamide and 2 mg of brimonidine tartrate equivalent to 1.3 mg of brimonidine.
- The other ingredients are benzalkonium chloride (50% solution) (see section 2 "Use of contact lenses - Brinzolamida/Brimonidina Zentiva contains benzalkonium chloride"), propylene glycol (E1520), carbomer 974P, boric acid (E284), sodium chloride, tyloxapol, hydrochloric acid and/or sodium hydroxide, and water for injection.
Small amounts of hydrochloric acid and/or sodium hydroxide are added to maintain normal acidity levels (pH levels).
Product Appearance and Container Content
10 ml white LDPE bottle with a sealed white LDPE dropper tip and a white HDPE/LDPE cap with a tamper-evident closure, containing 5 ml of a homogeneous white suspension.
The following pack sizes are available: boxes containing 1 x 5 ml, 3 x 5 ml.
Only some pack sizes may be marketed.
Marketing Authorization Holder and Manufacturer
Marketing Authorization Holder
Zentiva k.s.
U kabelovny 130
Dolní Mecholupy
102 37 Prague 10
Czech Republic
Manufacturer
Pharmathen S.A.
Dervenakion 6
Pallini 153 51,
Attica, Greece
Balkanpharma-Razgrad AD
68 Aprilsko Vastanie Blvd
Razgrad 7200, Bulgaria
For further information about this medicinal product, please contact the local representative of the marketing authorization holder:
Zentiva Spain S.L.U.
Avenida de Europa, 19, Edificio 3, Planta 1.
28224 Pozuelo de Alarcón, Madrid
Spain
This medicinal product is authorized in the Member States of the European Economic Area under the following names:
Germany | Brinzolamid/Brimonidin Zentiva 10 mg/ml + 2 mg/ml eye drop suspension |
Spain | Brinzolamida/Brimonidina Zentiva 10 mg/ml + 2mg/ml eye drops in suspension |
France | BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/2 mg per mL, eye drops in suspension |
Sweden | Brimonidin/brinzolamide Zentiva |
Date of the last revision of this leaflet: October 2023
Other sources of information:
Detailed information on this medicinal product is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es/
- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/mL + 2 mg/mL EYE DROPS, SUSPENSIONDosage form: EYEDROP, 10 mg/ml + 2 mg/mlActive substance: brinzolamide, combinationsManufacturer: Laboratorio Stada S.L.Prescription requiredDosage form: EYE DROP, 10 mg/ml + 2 mg/mlActive substance: brinzolamide, combinationsManufacturer: Novartis Europharm LimitedPrescription requiredDosage form: EYE DROP, 20 mg/mlActive substance: dorzolamideManufacturer: Tiedra Farmaceutica S.L.Prescription required
Online doctors for BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/mL + 2 mg/mL EYE DROPS, SUSPENSION
Discuss questions about BRINZOLAMIDE/BRIMONIDINE ZENTIVA 10 mg/mL + 2 mg/mL EYE DROPS, SUSPENSION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions















