
BRAMITOB 300 mg/4 ml SOLUTION FOR NEBULIZER INHALATION

How to use BRAMITOB 300 mg/4 ml SOLUTION FOR NEBULIZER INHALATION
Translated with AI
This page provides general information and does not replace a doctor’s consultation. Always consult a doctor before taking any medication. Seek urgent medical care if symptoms are severe.
Show originalContents of the leaflet
Introduction
Package Leaflet: Information for the User
Bramitob 300mg/4ml solution for inhalation by nebulizer
tobramycin
Read the entire package leaflet carefully before starting to use this medication because it contains important information for you.
- Keep this package leaflet, as you may need to read it again.
- If you have any questions, ask your doctor or pharmacist.
- This medication has been prescribed to you only, and you should not give it to others, even if they have the same symptoms as you, as it may harm them.
- If you experience side effects, consult your doctor or pharmacist, even if they are not listed in this package leaflet. See section 4.
Contents of the Package Leaflet
- What is Bramitob and what is it used for
- What you need to know before taking Bramitob
- How to take Bramitob
- Possible side effects
- Storage of Bramitob
- Package Contents and Additional Information
1. What is BRAMITOB and what is it used for
Bramitob contains tobramycin, an antibiotic from the aminoglycoside family, useful for combating infections caused by Pseudomonas aeruginosa.
Antibiotics are used to treat bacterial infections and are not effective against viral infections such as the flu or the common cold.
It is essential to follow the instructions regarding dosage, administration interval, and treatment duration indicated by your doctor.
Do not store or reuse this medication. If you have any leftover antibiotic after finishing treatment, return it to the pharmacy for proper disposal. Do not throw away medications down the drain or in the trash.
Bramitob is used to treat chronic respiratory infections in patients with cystic fibrosis caused by a type of bacteria called Pseudomonas. This medication destroys bacteria and helps improve breathing. Pseudomonasis a very common bacteria that infects almost all patients with cystic fibrosis at some point in their lives. Some people do not contract this infection until they are older, while others contract it at a very young age. If left untreated, the infection will continue to damage the lungs and cause additional problems. Bramitob is administered by inhalation, allowing tobramycin to reach the lungs directly to combat the bacteria that cause the infection.
Bramitob is indicated only for patients over 6 years of age.
In order to achieve optimal results, you must use this medication exactly as indicated.
2. What you need to know before taking Bramitob
Do not use Bramitob:
- If you are allergic to tobramycin or any of the other components of this medication (listed in section 6) or to any other aminoglycoside antibiotic.
- If you are taking any medication mentioned in the section "Other medications and Bramitob".
Warnings and precautions
Consult your doctor or pharmacist before starting to use Bramitob.
Bramitob contains tobramycin, which belongs to a group of medications that can occasionally cause loss of hearing, dizziness, and kidney damage (see section 4 "Possible side effects"). Inform your doctor if you experience any of the following disorders:
- If you feel chest tightness after using Bramitob. Your doctor will supervise the administration of the first dose of Bramitob and check lung function before and after administration. If you are not already using a bronchodilator (such as salbutamol), your doctor may indicate that you use it before administering Bramitob.
- If you have ever experienced any type of neuromuscular disorders such as parkinsonism or other conditions characterized by muscle weakness, including myasthenia gravis.
- If you have ever had kidney problems. Before using Bramitob, your doctor may check if your renal function is adequate through a urine or blood test. Your doctor may regularly check this function throughout treatment.
- If you have ever experienced ringing in the ears, any other hearing condition, or dizziness, your doctor may check your hearing before administering Bramitob or at any time during treatment.
- If you detect blood in your sputum. Inhalation of medications can cause coughing, and your doctor may indicate that you need to interrupt treatment with Bramitob until almost no blood is present in your sputum or until it disappears completely.
- If you are concerned that Bramitob is not as effective as it should be. Bacteria can sometimes develop resistance to antibiotic treatment.
Other medications and Bramitob
Before starting treatment, inform your doctor or pharmacist if you are taking, have recently taken, or may need to take any other medication.
- Do not use Bramitob if you are taking diuretics (medications that increase urine volume) containing furosemide or ethacrynic acid without consulting your doctor.
- Do not use Bramitob if you are taking intravenous or oral urea or mannitol (medications used to treat severe diseases in hospitalized patients).
- Some medications can cause kidney or ear damage that may be worsened by treatment with Bramitob.
It is possible that while receiving treatment with inhaled Bramitob, you may also receive injections of tobramycin or other aminoglycosides. Administration of these injections should be avoided while taking any of the medications listed below, as they can cause an increase in the low body levels of aminoglycosides caused by inhalation of Bramitob:
- amphotericin B, cephalothin, polymyxins (medications for the treatment of bacterial and fungal infections)
- cyclosporine, tacrolimus (medications for controlling the immune response in transplant patients)
- platinum compounds used for cancer treatment (e.g., carboplatin and cisplatin)
- medications with anticholinesterase activity used to relax muscles (e.g., neostigmine and pyridostigmine), botulinum toxin
If this is the case, you must inform your doctor.
Pregnancy and breastfeeding
If you are pregnant or breastfeeding, think you may be pregnant, or plan to become pregnant, consult your doctor or pharmacist before using this medication.
It is not known if inhalation of this medication during pregnancy causes side effects. When administered by injection, tobramycin and other aminoglycoside antibiotics can cause harm to the fetus, such as deafness and kidney problems.
If you are breastfeeding, you must consult your doctor before using this medication.
Driving and using machines
Bramitob has a minimal influence on the ability to drive and use machines.
On rare occasions, Bramitob can cause dizziness. Consequently, Bramitob may affect your ability to drive or operate machines.
3. How to take Bramitob
Follow your doctor's instructions for administering this medication exactly. If in doubt, consult your doctor or pharmacist again. The instructions for using Bramitob are included after the Dosage section.
Do notmix or dilute Bramitob with other medications in the nebulizer.
If you are receiving different treatments for cystic fibrosis, use them in the following order:
- bronchodilator (e.g., salbutamol), followed by
- respiratory physiotherapy, followed by
- other inhaled medications, and finally
- Bramitob
Consult the indicated order with your doctor.
Bramitob must be used with a reusable PARI LC PLUS or PARI LC SPRINT nebulizer (for personal use only), clean and dry, along with a suitable compressor. Ask your doctor or physiotherapist for information on which compressor is best for you.
The single-dose Bramitob package should be opened just before use. Any solution not used must be discarded immediately.
Dosage
- The dose (one 4 ml package) is the same for all individuals from 6 years of age.
- Use twopackages per day for 28 days. Inhale the contents of one package in the morning and the other in the evening. You must leave a 12-hour interval between each dose.
- Then, rest for 28 days without taking the medication before starting a new 28-day treatment cycle.
- It is essential that you use the medication twice a day for 28 days and respect the cycles of 28 days with treatment followed by 28 days without treatmentwith Bramitob. Continue using Bramitob in this way until your doctor tells you to stop.
If you use more Bramitob than you should
If you inhale too much Bramitob, your voice may become hoarse. Inform your doctor as soon as possible.
In case of overdose or accidental ingestion, consult your doctor or pharmacist immediately or call the Toxicology Information Service, phone 91 562 04 20, indicating the medication and the amount ingested.
If you forget to use Bramitob
- If there are more than 6 hours until the next dose (package), use Bramitob now.
- If there are less than 6 hours until the next dose (package), skip this dose (package).
Continue with the next dose normally.
Instructions for use
Bramitob must be used only in a nebulizer; do not use it in any other way.
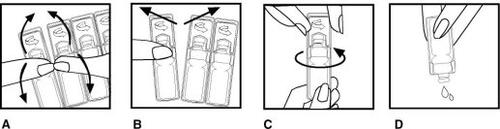
- Wash your hands well with water and soap before opening the single-dose package according to the following instructions.
- Fold the single-dose package forward and backward (figure A).
- Carefully separate a new package from the strip, first from the top and then from the middle (figure B), leaving the rest in the aluminum wrapper.
- Open the single-dose package by turning the top in the direction indicated by the arrow (figure C).
- Gently squeeze the package to transfer its contents to the nebulizer chamber (figure D).
- Connect the compressor.
- Check that the mist coming out of the mouthpiece is uniform.
- Stand or sit to breathe normally.
- Place the mouthpiece between your teeth and the top of your tongue. Breathe normally, only through your mouth (you can use nose clips for help). Try not to block the airflow with your tongue.
- Continue until you have consumed all of Bramitob, which occurs after approximately 15 minutes.
- If someone interrupts you, or you need to cough or rest during medication administration, turn off the compressor to save medication. Reconnect the compressor when you are ready to start treatment again.
If you still have doubts about how to use this medication, consult your doctor or pharmacist.
Maintenance of the nebulizer and compressor:
Follow the manufacturer's instructions for maintaining and using the nebulizer and compressor.
4. Possible side effects
Like all medications, this medication can cause side effects, although not everyone experiences them.
If you are unsure about any of the side effects mentioned below, ask your doctor to explain them to you.
The most frequentside effects of Bramitob that may affect up to 1 in 10 people are: cough and hoarseness.
The uncommonside effects of Bramitob that may affect up to 1 in 100 people are: mouth ulcers (due to candida infection), dizziness, deafness, increased saliva, tongue inflammation, rash, sore throat, and altered liver function analysis (increase in liver enzymes in blood), wheezing, nausea, dry mucous membranes, presence of blood in sputum, oropharyngitis (throat inflammation), chest pain, hearing loss, headache, difficulty breathing, weakness, increased sputum production (substance expelled when coughing), stomach pain, and fungal infections.
The rareside effects that may affect up to 1 in 1,000 people are: loss of appetite, ringing in the ears, chest tightness or difficulty breathing, loss of voice, nasal bleeding, nasal discharge, mouth ulcers, vomiting, taste alterations, asthma, dizziness, loss of strength, fever, and pain and laryngitis (voice alteration with sore throat and difficulty swallowing).
The very rareside effects that may affect up to 1 in 10,000 people are: swelling of the lymph nodes, drowsiness, hearing problems, ear pain, rapid and deep breathing (hyperventilation), sinusitis (inflammation of the nasal sinuses), diarrhea, allergic reactions including hives and itching, lack of oxygen available in the blood and body tissues (hypoxia), back pain, pain, abdominal discomfort, and general feeling of discomfort.
Reporting side effects
If you experience any side effects, consult your doctor or pharmacist, even if they are not listed in this package leaflet. You can also report them directly through the national reporting system included in the Spanish Medicines Agency's Pharmacovigilance System for Human Use Website: www.notificaram.es.
By reporting side effects, you can contribute to providing more information on the safety of this medication.
5. Storage of Bramitob
- Keep this medication out of sight and reach of children.
- For individual use only. Do not use this medication after the expiration date shown on the label and on the outer packaging next to EXP. The expiration date is the last day of the month indicated. You can also use Bramitob even if the color of the solution has changed.
Expiry date after first opening: The Bramitob bags (intact or opened) can be stored for up to 3 months at a temperature not exceeding 25°C.
- Store the packages in the refrigerator (between 2°C and 8°C). If you do not have a refrigerator and for transportation, you can store the packages for 3 months at a temperature below 25°C.
- Keep the packages in the original packaging to protect them from light.
- Use the single-dose package immediately after opening.
- Discard the used single-dose package immediately after the first administration.
- Medications should not be thrown away down the drain or in the trash. Deposit the packages and medications you no longer need at the SIGRE collection point in the pharmacy. If in doubt, ask your pharmacist how to dispose of the packages and medications you no longer need. This way, you will help protect the environment.
6. Package Contents and Additional Information
Composition of Bramitob
The active ingredient is tobramycin. Each 4 ml single-dose package contains 300 mg of tobramycin.
The other components (excipients) are: sodium chloride, sulfuric acid, and sodium hydroxide (to adjust the pH), water for injectable preparations.
Appearance of the product and package contents
Bramitob is presented as a clear yellowish solution.
Bramitob solution for nebulization is presented in single-dose packages of 4 ml. Each sealed bag contains 4 packages, in package sizes of 4, 16, 28, or 56 units.
Only some package sizes may be marketed.
Marketing Authorization Holder and Manufacturer
Marketing Authorization Holder:
Chiesi Spain, S.A.U., Plaça d’Europa, 41-43, Planta 10 – 08908 L’Hospitalet de Llobregat - Barcelona (Spain)
Manufacturer:
Chiesi Farmaceutici S.p.A., 96 Via San Leonardo, 43122 Parma (Italy).
or
Genetic S.p.A., Contrada Canfora, 84084 Fisciano (Italy).
This medication has been authorized in the following European Economic Area member states with the following names:
Austria: Bramitob
Czech Republic: Bramitob
Denmark: Bramitob
Finland: Bramitob
Germany: Bramitob
Greece: Bramitob
Hungary: Bramitob
Ireland: Bramitob
Italy: Tobrineb
Netherlands: Bramitob
Norway: Bramitob
Poland: Bramitob
Portugal: Bramitob
Slovakia: Bramitob
Spain: Bramitob
Sweden: Bramitob
United Kingdom (Northern Ireland): Bramitob
Date of the last revision of this package leaflet:January 2022.
Detailed information about this medication is available on the website of the Spanish Agency for Medicines and Health Products (AEMPS) http://www.aemps.gob.es.
You can access detailed and updated information about this medication by scanning the QR code included in the package leaflet and packaging with your smartphone. You can also access this information at the following internet address:
https://www.aemps.gob.es/cima/especialidad.do?metodo=verPresentaciones&codigo=68621

- Country of registration
- Active substance
- Prescription requiredYes
- Manufacturer
- This information is for reference only and does not constitute medical advice. Always consult a doctor before taking any medication. Oladoctor is not responsible for medical decisions based on this content.
- Alternatives to BRAMITOB 300 mg/4 ml SOLUTION FOR NEBULIZER INHALATIONDosage form: PULMONARY INHALATION, 28 mg tobramycinActive substance: tobramycinManufacturer: Viatris Healthcare LimitedPrescription requiredDosage form: PULMONARY INHALATION, 300 mg/5 mlActive substance: tobramycinManufacturer: Accord Healthcare S.L.U.Prescription requiredDosage form: PULMONARY INHALATION, 300 MG/5 MLActive substance: tobramycinManufacturer: Altan Pharmaceuticals SaPrescription required
Online doctors for BRAMITOB 300 mg/4 ml SOLUTION FOR NEBULIZER INHALATION
Discuss questions about BRAMITOB 300 mg/4 ml SOLUTION FOR NEBULIZER INHALATION, including use, safety considerations and prescription review, subject to medical assessment and local regulations.
Frequently Asked Questions















