
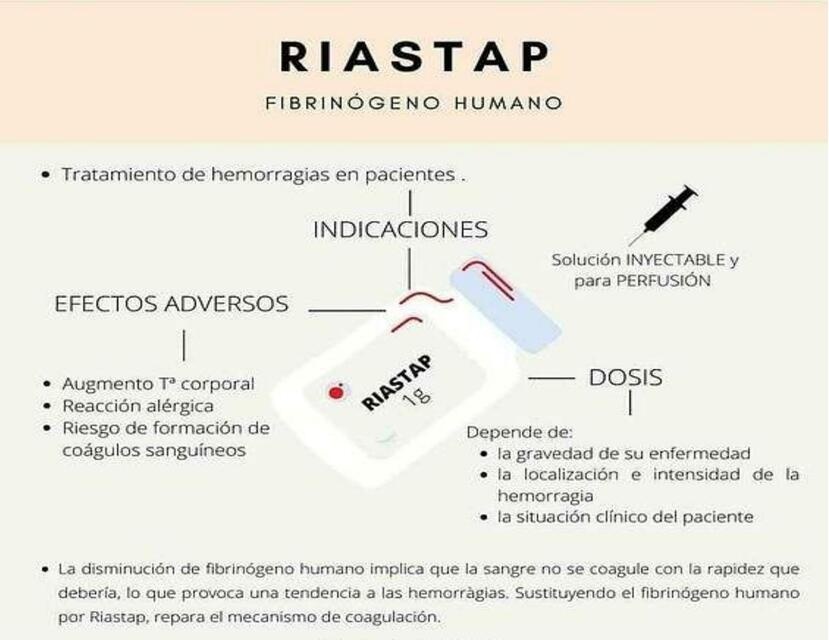
Riastap

Zapytaj lekarza o receptę na Riastap

Jak stosować Riastap
ULOTKA INFORMACYJNA: INFORMACJE DLA PACJENTA
Riastap, 1 g
Proszek do sporządzania roztworu do wstrzykiwań / do infuzji.
Fibrynogen ludzki
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten został przepisany ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest Riastap i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem Riastap
- 3. Jak stosować Riastap
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Riastap
- 6. Zawartość opakowania i inne informacje
1. Co to jest Riastap i w jakim celu się go stosuje
Co to jest Riastap?
Riastap zawiera ludzki fibrynogen, który jest ważnym białkiem dla krzepnięcia krwi
(koagulacji). Brak fibrynogenu oznacza, że krew nie krzepnie tak szybko, jak powinna, co
powoduje zwiększoną skłonność do krwawienia. Zastąpienie ludzkiego fibrynogenu lekiem
Riastap powoduje naprawę mechanizmów krzepnięcia.
W jakim celu stosuje się Riastap?
Riastap jest stosowany w terapii krwawienia u pacjentów z wrodzonym brakiem fibrynogenu
(hypo- lub afibrynogenemią) ze skłonnością do krwawienia.
2. Informacje ważne przed zastosowaniem Riastap
Informacje podane w tej części powinny zostać uwzględnione przez lekarza przed podaniem
leku Riastap.
Kiedy nie stosować leku Riastap:
- jeżeli u pacjenta występuje alergia na ludzki fibrynogen lub na którykolwiek z innych składników tego leku (wymienionych w punkcie 6.).
W przypadku alergii na jakikolwiek lek lub żywność należy poinformować lekarza.
Ostrzeżenia i środki ostrożności:
- jeśli w przeszłości wystąpiły reakcje alergiczne na Riastap. Należy wówczas profilaktycznie przyjąć leki przeciwhistaminowe i kortykosteroidy, jeśli zostaną zalecone przez lekarza.
- gdy wystąpią reakcje alergiczne lub reakcje typu anafilaktycznego (poważna reakcja alergiczna, która powoduje ciężkie zaburzenia oddychania lub zawroty głowy). Podawanie
Riastap należy natychmiast przerwać (np. zaprzestając wykonywania wstrzyknięcia).
- z powodu zwiększonego ryzyka tworzenia skrzepów krwi w naczyniu krwionośnym (zakrzepica), w szczególności:
- w przypadku podania dużej dawki lub powtórnego dawkowania
- gdy wystąpiła choroba serca (choroba wieńcowa serca lub zawał mięśnia sercowego w wywiadzie)
- w przypadku choroby wątroby
- bezpośrednio po zabiegu chirurgicznym (pacjenci pooperacyjni)
- wkrótce przed zabiegiem chirurgicznym (pacjenci przedoperacyjni)
- u nowonarodzonych dzieci (noworodków)
- jeśli istnieje większa niż normalna skłonność do tworzenia skrzepów krwi (pacjenci z ryzykiem zaburzeń zakrzepowo-zatorowych lub rozsianego wykrzepiania wewnątrznaczyniowego)
Lekarz rozważy stosunek korzyści z terapii lekiem Riastap do ryzyka związanego
z powyższymi powikłaniami.
Bezpieczeństwo wirusowe
W przypadku produktów leczniczych otrzymywanych z ludzkiej krwi lub osocza,
podejmowane są środki mające na celu zapobieganie zakażeniom przenoszonym na pacjentów.
Należy do nich:
- dokładna selekcja dawców krwi i osocza w celu wykluczenia osób zakażonych oraz
- badania poszczególnych donacji i pul osocza w kierunku obecności wirusów / zakażeń.
Wytwórcy tych produktów również włączają do procesu obróbki krwi lub osocza etapy
mogące inaktywować lub eliminować wirusy. Pomimo tego, nie można całkowicie wykluczyć
możliwości przeniesienia czynników zakaźnych podczas podawania produktów leczniczych
otrzymanych z ludzkiej krwi lub osocza. Dotyczy to także wirusów nieznanych
i nowoodkrytych oraz innych rodzajów zakażeń.
Procedury te są uważane za skuteczne wobec wirusów otoczkowych, takich jak ludzki wirus
niedoboru odporności (HIV, wirus powodujący AIDS), wirus zapalenia wątroby typu B i C
(stan zapalny w wątrobie) oraz wobec bezotoczkowych wirusów zapalenia wątroby typu A
(stan zapalany w wątrobie) oraz parwowirusa B19.
Lekarz może zalecić rozważenie szczepienia przeciw wirusowemu zapaleniu wątroby typu A i
B w przypadku regularnego/powtarzanego przyjmowania produktów pochodzących
z ludzkiego osocza.
Zaleca się odnotowanie przez lekarza daty podania preparatu, numeru serii i wstrzykniętą
objętość.
Riastap a inne leki
- Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio, a także o lekach które pacjent planuje przyjmować.
- Leku Riastap nie wolno mieszać z innymi produktami leczniczymi, z wyjątkami opisanymi w części „Informacje przeznaczone wyłącznie dla fachowego personelu medycznego /Rekonstytucja”.
Ciąża i karmienie piersią
- Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
- Podczas ciąży lub karmienia piersią, preparat Riastap powinien być podany jedynie w wyraźnej potrzebie.
Prowadzenie pojazdów i obsługiwanie maszyn
Riastap nie wywiera wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia
pojazdów mechanicznych i obsługiwania maszyn.
Ważne informacje o niektórych składnikach Riastap
Riastap zawiera do 164 mg (7,1 mmol) sodu na fiolkę. Odpowiada to 11,5 mg (0,5 mmol) sodu
na kg masy ciała pacjenta, jeśli została podana zalecana początkowa dawka 70 mg/kg masy
ciała. Należy wziąć to pod uwagę podczas stosowania u pacjentów na diecie z kontrolowaną
zawartością sodu.
3. Jak stosować Riastap
Terapia powinna być rozpoczęta i nadzorowana przez lekarza doświadczonego w leczeniu tego
typu schorzenia.
Dawkowanie
Potrzebna ilość ludzkiego fibrynogenu oraz czas trwania terapii zależy od:
- zaawansowania choroby
- umiejscowienia i intensywności krwawienia
- stanu klinicznego pacjenta. Zastosowanie większej niż zalecana dawki leku RiastapLekarz powinien regularnie sprawdzać status krzepnięcia krwi podczas terapii. W przypadku przedawkowania, ryzyko wystąpienia powikłań zakrzepowo-zatorowych jest zwiększone.
Sposób podawania
W przypadku pytań dotyczących stosowania tego produktu, należy skonsultować się
z lekarzem lub farmaceutą (patrz część „ Informacje przeznaczone wyłącznie dla fachowego
personelu medycznego”).
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one
wystąpią.
Należy natychmiast skontaktować się z lekarzem:
- w przypadku wystąpienia jakichkolwiek działań niepożądanych
- w przypadku wystąpienia działań niepożądanych niewymienionych w tej ulotce.
Następujące reakcje niepożądane obserwowano bardzo często(mogą wystąpić u więcej niż 1
na 10 osób):
- Podwyższenie temperatury ciała
Następujące reakcje niepożądane obserwowano niezbyt często(u mniej niż 1 na 100 osób):
- Nagła reakcja alergiczna (taka jak zaczerwienienie skóry, wysypka skórna na całej powierzchni ciała, spadek ciśnienia krwi, trudności w oddychaniu).
Następujące reakcje niepożądane obserwowano często(u mniej niż 1 na 10 osób, jakkolwiek
incydenty te występują częściej u pacjentów nie otrzymujących fibrynogenu):
- Ryzyko zwiększonego powstawania skrzepów krwi (patrz część 2. ”Ostrzeżenia i środkiostrożności”).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane
niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania
niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych
Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów
Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
tel.: +48 22 49 21 301
fax.: +48 22 49 21 309
Strona internetowa: ://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Riastap
- Lek przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować leku Riastap po upływie terminu ważności zamieszczonego na etykiecie i kartonie.
- Nie przechowywać w temperaturze powyżej 25°C. Nie zamrażać.
- W celu ochrony przed światłem fiolkę należy przechowywać w opakowaniu zewnętrznym.
- Rekonstytuowany roztwór najlepiej zużyć natychmiast.
- Jeśli przygotowany roztwór nie jest podany natychmiast, okres jego przechowywania nie powinien przekraczać 8 godzin w temperaturze pokojowej (maks. 25 ºC).
- Rekonstytuowanego roztworu nie należy przechowywać w lodówce.
6. Zawartość opakowania i inne informacje
Co zawiera Riastap Substancją czynną jest:
Fibrynogen ludzki (1 g/fiolkę; po rekonstytucji w 50 ml wody do wstrzykiwań około
20 mg/ml).
W celu uzyskania bardziej szczegółowych informacji, patrz część „ Informacje przeznaczone
wyłącznie dla personelu medycznego”.
Inne składniki to:
Albumina ludzka, sodu chlorek, L-argininy chlorowodorek, sodu cytrynian, sodu wodorotlenek
(do ustalenia pH),
Patrz ostatni rozdział części 2. „ Ważne informacje o niektórych składnikach Riastap”.
Jak wygląda Riastap i co zawiera opakowanie
Riastap ma postać białego proszku.
Po rekonstytucji w wodzie do wstrzykiwań uzyskany roztwór powinien być przezroczysty lub
lekko opalizujący, tj. może się mienić oglądany pod światło lecz nie może zawierać żadnych
widocznych cząsteczek.
Opakowania
Opakowanie zawierające 1 g (Ryc. 1)
Jedna fiolka po 1 g fibrynogenu ludzkiego
Filtr: filtr strzykawkowy Pall
Nakłuwacz dozujący: nakłuwacz dozujący Mini-Spike

Ryc.1
Podmiot Odpowiedzialny i Wytwórca:
CSL Behring GmbH
Emil-von-Behring-Str. 76
35041 Marburg
Niemcy
Ten produkt leczniczy jest zarejestrowany w Państwach Członkowskich EEA pod następującymi nazwami:
Riastap 1g, powder for solution for injection/infusion
Wielka Brytania
Riastap 1g, poudre pour solution injectable/perfusion
Francja
Riastap 1g, prašek za raztopino za injiciranje ali infundiranje
Słowenia
Riastap 1g
Niemcy, Irlandia
Riastap
Belgia, Cypr, Dania, Finlandia, Grecja, Islandia, Włochy, Luksemburg,
Malta, Norwegia, Polska, Słowacja, Hiszpania, Szwecja
Data zatwierdzenia ulotki: Wrzesień 2024
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego Dawkowanie:
Poziom fibrynogenu (funkcjonalny) powinien być oznaczany w celu wyliczenia
indywidualnego dawkowania oraz ilości i częstości podawanych dawek u każdego pacjenta
poprzez regularne pomiary poziomu fibrynogenu w osoczu i ciągły monitoring stanu
klinicznego pacjenta przy uwzględnieniu innych zastosowanych terapii zastępczych.
Normalny poziom fibrynogenu w osoczu mieści się w zakresie 1,5 – 4,5 g/l. Krytyczny poziom
fibrynogenu w osoczu, poniżej którego może dochodzić do krwotoków wynosi około 0,5 - 1
g/l. W przypadku poważnych zabiegów chirurgicznych konieczne jest dokładne monitorowanie
terapii zastępczej badaniami krzepnięcia.
Dawka początkowa
Jeśli poziom fibrynogenu u pacjenta nie jest znany, zalecana dawka podawana dożylnie wynosi
70 mg na kg masy ciała.
Kolejna dawka
Poziom docelowy (1 g/l) w przypadkach nieznacznych krwawień (np. krwawienie z nosa,
krwawienie śródmięśniowe lub menstruacyjne) powinien być utrzymywany przez co najmniej
trzy dni. Poziom docelowy (1,5 g/l) w przypadkach znacznych krwawień (np. uraz głowy lub
krwawienie wewnątrzczaszkowe) należy utrzymywać przez siedem dni.
Dawka fibrynogenu =
[Poziom docelowy (g/l) – poziom zmierzony (g/l)]
(mg/kg masy ciała)
0,017 (g/l na mg/kg masy ciała)
Dawkowanie u noworodków, niemowląt i dzieci
Dostępne są ograniczone dane z badań klinicznych dotyczących dawkowania Riastap u dzieci.
Zalecenia względem dawkowania w terapii dzieci są takie same jak u dorosłych, co wynika
zarówno z tych badań, jak i z długotrwałego doświadczenia klinicznego stosowania preparatów
fibrynogenu.
Sposób podawania
Informacje ogólne
- Proces rekonstytucji oraz pobierania produktu powinien odbywać się w warunkach aseptycznych.
- Rekonstytuowane produkty przed podaniem powinny zostać ocenione wzrokowo w celu wykluczenia obecności cząstek i przebarwień.
- Roztwór powinien być niemal bezbarwny do żółtawego, przeźroczysty do lekko opalizującego z obojętnym pH. Nie stosować roztworów, które są mętne lub zawierają osad.
Rekonstytucja
- Ogrzać zarówno rozpuszczalnik, jak i proszek do temperatury pokojowej lub temperatury ciała (nie wyższej niż 37 ), nie otwierając fiolek.
- Preparat Riastap należy rekonstytuować wodą do wstrzykiwań (50 ml, nie załączona).
- Przed rekonstytucją produktu należy umyć ręce lub założyć rękawiczki.
- Usunąć wieczko z fiolki zawierającej Riastap, tak aby odsłonić centralną część korków infuzyjnych.
- Przetrzeć powierzchnię korka infuzyjnego antyseptycznym roztworem i zostawić do wyschnięcia.
- Wprowadzić rozcieńczalnik do fiolki używając odpowiedniego sprzętu. Upewnić się, że proszek został całkowicie zwilżony.
- Po delikatnym zmieszaniu ruchem obrotowym zawartości fiolki aż do rekonstytucji proszku, roztwór jest gotowy do podania. Unikać silnego wstrząsania, które powoduje powstawanie piany. Ogólnie przyjmuje się, że proszek rozpuszcza się w ciągu około 5 minut. Całkowite rozpuszczenie nie powinno trwać dłużej niż 15 minut.
- Otworzyć plastikowy blister zawierający nakłuwacz dozujący (Mini-Spike ) dostarczony z produktem leczniczym Riastap (Ryc. 2).

Ryc. 2
- Należy wprowadzić załączony nakłuwacz dozujący do korka fiolki z produktem po rekonstytuacji (Ryc. 3)

Ryc. 3
- Po wprowadzeniu nakłuwacza dozującego, usunąć wieczko. Po usunięciu wieczka nie wolno dotykać odkrytej powierzchni.
- Należy otworzyć blister z filtrem (filtr strzykawkowy Pall ) dostarczony z produktem leczniczym Riastap (Ryc.4)

Ryc. 4
Nakręcić strzykawkę na filtr (Ryc.5)
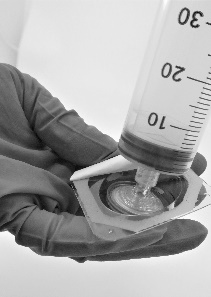
Ryc. 5
- Nakręcić strzykawkę zamocowanym filtrem na końcówkę dozującą (Ryc. 6)

Ryc. 6
- Pobrać produkt po rekonstytucji do strzykawki (Ryc.7)
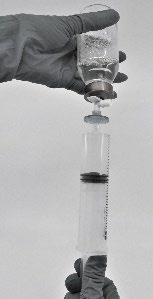
Ryc.7
- Po zakończeniu, należy odłączyć filtr, nakłuwacz dozujący i pustą fiolkę od strzykawki i usunąć zgodnie z obowiązującymi zasadami następnie rozpocząć podawanie leku zgodnie z zaleceniami. Zrekonstytuowany roztwór powinien być podany natychmiast przy użyciu osobnego zestawu do wstrzyknięcia / infuzji.
- Należy uważać, aby nie spowodować aspiracji krwi do strzykawek wypełnionych produktem.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć
zgodnie z lokalnymi przepisami.
Sposób podawania
Do podawania dożylnego roztworu po rekonstytucji w temperaturze pokojowej zalecane jest
stosowanie standardowego zestawu do infuzji. Zrekonstytuowany roztwór powinien być
wstrzyknięty lub podany w infuzji powoli, z szybkością odpowiednią dla komfortu pacjenta.
Szybkość wstrzyknięcia lub infuzji nie powinna przekraczać ok. 5 ml na minutę.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyNie
- Producent
- ImporterCSL Behring GmbH
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki RiastapPostać farmaceutyczna: Proszek, 1 gSubstancja czynna: fibrinogen, humanBez receptyPostać farmaceutyczna: Proszek, 1000 j.m.Substancja czynna: coagulation factor VIIIProducent: CSL Behring GmbHWymaga receptyPostać farmaceutyczna: Proszek, 2000 j.m.Substancja czynna: coagulation factor VIIIProducent: CSL Behring GmbHWymaga recepty
Odpowiedniki Riastap w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Riastap – Ukraine
Odpowiednik Riastap – Spain
Lekarze online w sprawie Riastap
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Riastap – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














