
Olimel N12E

Zapytaj lekarza o receptę na Olimel N12E

Jak stosować Olimel N12E
Ulotka dla pacjenta: Informacja dla użytkownika
OLIMEL N12E, emulsja do infuzji
Należy uważnie zapoznać się z treścią ulotki przed podaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub pielęgniarki.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek OLIMEL N12E, emulsja do infuzji i w jakim celu się go stosuje
- 2. Informacje ważne przed podaniem leku OLIMEL N12E, emulsja do infuzji
- 3. Jak stosować lek OLIMEL N12E, emulsja do infuzji
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek OLIMEL N12E, emulsja do infuzji
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek OLIMEL N12E, emulsja do infuzji i w jakim celu się go stosuje
OLIMEL N12E to emulsja do infuzji. Lek jest dostarczany w trójkomorowym worku.
W pierwszej komorze znajduje się roztwór glukozy z wapniem, w drugiej — emulsja tłuszczowa, zaś w
trzeciej — roztwór aminokwasów z innymi elektrolitami.
OLIMEL N12E jest stosowany do dożylnego odżywiania przez rurkę dorosłych oraz dzieci w wieku
powyżej 2 lat, gdy odżywianie doustne nie jest odpowiednie.
OLIMEL N12E może być stosowany jedynie pod kontrolą lekarza.
2. Informacje ważne przed podaniem leku OLIMEL N12E, emulsja do infuzji
Kiedy nie stosować leku OLIMEL N12E, emulsja do infuzji:
- u wcześniaków, noworodków i dzieci w wieku poniżej 2 lat;
- jeśli pacjent ma uczulenie na jaja, soję, białka orzeszków ziemnych, kukurydzę/produkty zawierające kukurydzę (patrz również punkt „Ostrzeżenia i środki ostrożności” poniżej) lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli stosowanie niektórych aminokwasów wywołuje nieprawidłową reakcję organizmu pacjenta;
- jeśli u pacjenta występuje szczególnie duże stężenie tłuszczów we krwi;
- jeśli u pacjenta występuje hiperglikemia (zbyt duże stężenie cukru we krwi);
- jeśli we krwi pacjenta występuje nieprawidłowo wysoka zawartość któregokolwiek z elektrolitów (sodu, potasu, magnezu, wapnia i (lub) fosforu).
W każdym przypadku lekarz podejmie decyzję o podaniu leku na podstawie czynników takich jak wiek,
masa ciała pacjenta i jego stan zdrowia, włączając wyniki przeprowadzonych badań.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem podawania leku OLIMEL N12E należy omówić to z lekarzem lub pielęgniarką.
Zbyt szybkie podawanie roztworów do całkowitego żywienia pozajelitowego może skutkować urazem
lub zgonem pacjenta.
Jeśli wystąpią nietypowe oznaki lub objawy reakcji alergicznej (takie jak pocenie się, gorączka, dreszcze,
ból głowy, wysypka skórna lub problemy z oddychaniem), należy natychmiast przerwać infuzję. Lek
zawiera olej sojowy oraz fosfolipidy z jaja kurzego. Białka soi oraz jaja mogą wywoływać reakcje
nadwrażliwości. Obserwowano krzyżowe reakcje alergiczne pomiędzy białkami soi i orzeszków
ziemnych.
Lek OLIMEL N12E zawiera glukozę uzyskaną z kukurydzy, która może powodować reakcje
nadwrażliwości, jeśli pacjent ma uczulenie na kukurydzę lub produkty zawierające kukurydzę (patrz
punkt „Kiedy nie stosować leku OLIMEL N12E, emulsja do infuzji” powyżej).
Trudności z oddychaniem mogą być również oznaką, że powstały małe cząstki blokujące naczynia
krwionośne w płucach (osady w naczyniach płucnych). Jeśli wystąpią jakiekolwiek trudności z
oddychaniem, należy powiedzieć o tym lekarzowi lub pielęgniarce. Zdecydują oni o podjęciu
odpowiedniego działania.
Antybiotyku o nazwie ceftriakson nie wolno mieszać ani podawać jednocześnie z jakimikolwiek
roztworami zawierającymi wapń (w tym z lekiem OLIMEL N12E) podawanymi drogą kroplówki
dożylnej.
Nie wolno podawać tych leków jednocześnie nawet przez różne linie do infuzji ani inne miejsca infuzji.
Lek OLIMEL N12E i ceftriakson można jednak podawać kolejno jeden po drugim, jeśli linie do infuzji są
wkłute w różne miejsca lub są wymieniane albo dokładnie płukane roztworem fizjologicznym soli
między infuzjami, aby uniknąć wytrącania osadów (powstawania cząstek soli wapniowej ceftriaksonu).
Niektóre leki oraz choroby mogą zwiększyć ryzyko rozwoju zakażenia lub posocznicy (obecność bakterii
we krwi). Szczególne ryzyko wystąpienia zakażenia lub posocznicy istnieje po umieszczeniu rurki
(cewnika dożylnego) w żyle pacjenta. Lekarz będzie uważnie obserwował pacjenta celem wykrycia
jakichkolwiek objawów zakażenia. Pacjenci wymagający żywienia pozajelitowego (podawania substancji
odżywczych za pomocą rurki umieszczonej w żyle) są, ze względu na swój stan zdrowia, bardziej
narażeni na rozwój zakażenia. Stosowanie postępowania zapewniającego jałowość (z nieobecnością
drobnoustrojów) podczas umieszczania, obsługi cewnika oraz podczas przygotowywania leku do
żywienia (kompletne żywienie pozajelitowe) może zmniejszyć ryzyko rozwoju zakażenia.
Jeśli pacjent jest ciężko niedożywiony, tak że musi otrzymywać pokarm do żyły, lekarz powinien
rozpocząć leczenie powoli. Jednocześnie, lekarz powinien uważnie obserwować pacjenta, aby zapobiec
nagłym zmianom ilości płynów, stężenia witamin, elektrolitów i składników mineralnych.
Przed rozpoczęciem infuzji należy skorygować zaburzenia równowagi wodno-elektrolitowej oraz
zaburzenia metaboliczne pacjenta. Lekarz będzie monitorował pacjenta w czasie terapii i może zmienić
dawkowanie lub jeśli uzna to za stosowne przepisać dodatkowe preparaty odżywcze, takie jak witaminy,
elektrolity i pierwiastki śladowe.
U pacjentów, którzy przyjmują dożylną terapię żywieniową zgłaszano występowanie zaburzeń czynności
wątroby, w tym trudności z usuwaniem żółci (cholestaza), gromadzenie tłuszczu (stłuszczenie wątroby),
zwłóknienie, prawdopodobnie prowadzące do niewydolności wątroby, a także zapalenie pęcherzyka
żółciowego i kamicę żółciową. Uważa się, że przyczyny tych zaburzeń moga być różne u różnych
pacjentów. Jeśli u pacjenta występują takie objawy, jak: nudności, wymioty, ból brzucha, zażółcenie
skóry lub oczu, należy porozumieć się z lekarzem, w celu umożliwienia identyfikacji możliwych
przyczyn i czynników, a także możliwych środków terapeutycznych i zapobiegawczych.
Lekarza należy poinformować:
- o ciężkich chorobach nerek. Należy także poinformować lekarza, jeśli pacjent jest poddawany dializie (sztuczna nerka) lub innym metodom oczyszczania krwi;
- o ciężkich chorobach wątroby;
- o zaburzeniach krzepliwości krwi;
- o nieprawidłowej pracy nadnerczy (niewydolność nadnerczy). Nadnercza to gruczoły o trójkątnym kształcie, znajdujące się na szczycie nerek;
- o niewydolności serca;
- o chorobie płuc;
- o gromadzeniu się wody w organizmie (przewodnienie);
- o niewystarczającej ilości wody w organizmie (odwodnienie);
- o nieleczonym wysokim stężeniu glukozy we krwi (cukrzyca);
- o zawale mięśnia sercowego lub wstrząsie spowodowanym nagłą niewydolnością serca;
- o ciężkiej kwasicy metabolicznej (zbyt kwaśny odczyn krwi);
- o uogólnionym zakażeniu (posocznica);
- o śpiączce.
Aby sprawdzić skuteczność oraz bezpieczeństwo stosowania leku, w trakcie podawania leku pacjent
zostanie poddany testom klinicznym i laboratoryjnym zleconym przez lekarza. W przypadku, gdy lek
podawany jest przez kilka tygodni, krew pacjenta będzie regularnie badana.
Zmniejszona zdolność organizmu do usuwania lipidów zawartych w podawanym leku może skutkować
tzw. zespołem przeciążenia tłuszczami (patrz punkt 4 - „Możliwe działania niepożądane”).
W przypadku wystąpienia w trakcie infuzji bólu, pieczenia lub obrzęku w miejscu infuzji lub w
przypadku wycieku podawanego w infuzji płynu, należy powiadomić o tym lekarza lub pielęgniarkę.
Podawanie leku zostanie niezwłocznie przerwane, a następnie wznowione do innej żyły.
Jeśli stężenie glukozy we krwi zwiększy się nadmiernie, lekarz powinien dostosować szybkość
podawania leku OLIMEL N12E lub podać pacjentowi lek wyrównujący poziom cukru we krwi (insulinę).
OLIMEL N12E może być podawany przez rurkę (cewnik) wkłutą do dużej żyły w klatce piersiowej
pacjenta (żyły centralnej).
Dzieci i młodzież
W przypadku stosowania u dzieci w wieku poniżej 18 lat życia należy zachować szczególną ostrożność w
celu podania właściwej dawki leku. Z powodu zwiększonej wrażliwości dzieci na ryzyko infekcji, trzeba
podjąć również wzmożone środki ostrożności. Zawsze wymagane jest wzbogacenie w witaminy i
pierwiastki śladowe. Dla dzieci muszą być stosowane składy i ilości pediatryczne.
OLIMEL N12E a inne leki
Należy powiedzieć lekarzowi o wszystkich lekach przyjmowanych lub stosowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować lub stosować.
Jednoczesne stosowanie innych leków zazwyczaj nie jest przeciwwskazane. Należy jednak wcześniej
poinformować lekarza o wszystkich przyjmowanych w ostatnim czasie lekach, również wydawanych bez
recepty, w celu sprawdzenia ich zgodności.
Należy poinformować lekarza o przyjmowaniu lub otrzymywaniu:
- insuliny,
- heparyny.
Nie wolno podawać leku OLIMEL N12E jednocześnie z krwią przez ten sam zestaw do infuzji.
OLIMEL N12E zawiera wapń. Nie należy go podawać łącznie z antybiotykiem o nazwie ceftriakson ani
przez tę samą rurkę, gdyż mogą powstać cząstki. Jeśli te leki są podawane kolejno za pomocą tego
samego urządzenia, powinno ono zostać dokładnie przepłukane.
Ze względu na ryzyko wytrącenia się osadu, leku OLIMEL N12E nie należy podawać przez tę samą linię
do infuzji ani dodawać do antybiotyku ampicyliny lub leku przeciwpadaczkowego fosfenytoiny.
Oliwa oraz olej sojowy obecne w leku OLIMEL N12E zawierają witaminę K. Zazwyczaj nie ma to
wpływu na działanie leków rozrzedzających krew (przeciwzakrzepowych), takich jak kumaryna. Jeśli
jednak pacjent przyjmuje leki przeciwzakrzepowe, powinien poinformować o tym lekarza.
Tłuszcze zawarte w emulsji mogą zaburzać wyniki niektórych badań laboratoryjnych, jeśli próbka krwi
do badania zostanie pobrana zanim dojdzie do usunięcia tłuszczów z krwiobiegu pacjenta (są one
usuwane z krwi po czasie od 5 do 6 godzin od podania tłuszczów).
OLIMEL N12E zawiera potas. Należy zachować szczególną ostrożność w przypadku pacjentów
przyjmujących leki moczopędne, inhibitory konwertazy angiotensyny ACE, antagonistów receptora
angiotensyny II (leki stosowane w nadciśnieniu) lub leki immunosupresyjne. Leki tego rodzaju mogą
spowodować wzrost stężenia potasu we krwi.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed podaniem tego leku.
Brak odpowiedniego doświadczenia dotyczącego stosowania leku OLIMEL N12E u kobiet w ciąży lub
karmiących piersią. Jeśli to konieczne, można rozważyć podanie leku OLIMEL N12E w okresie ciąży i
karmienia piersią. Lek OLIMEL N12E należy podawać kobietom w ciąży lub karmiącym piersią tylko po
dokładnym rozważeniu.
Płodność
Brak odpowiednich danych.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie dotyczy.
3. Jak stosować lek OLIMEL N12E, emulsja do infuzji
Dawkowanie
OLIMEL N12E należy stosować wyłącznie u dorosłych oraz u dzieci w wieku powyżej 2 lat.
Lek ma postać emulsji do infuzji podawanej przez rurkę (cewnik) do dużej żyły w klatce piersiowej
pacjenta.
Przed zastosowaniem, OLIMEL N12E powinien znajdować się w temperaturze pokojowej.
OLIMEL N12E jest przeznaczony wyłącznie do jednorazowego użycia.
Infuzja 1 worka trwa zazwyczaj od 12 do 24 godzin.
Dawkowanie – Dorośli
Szybkość podawania, zgodnie z potrzebami i stanem klinicznym pacjenta, zostanie ustalona przez lekarza.
Lek można stosować tak długo jak potrzeba, w zależności od stanu klinicznego pacjenta.
Dawkowanie – Dzieci w wieku powyżej dwóch lat oraz młodzież
Dawka leku oraz okres jego podawania są ustalane przez lekarza. Zależy to od wieku, masy ciała,
wzrostu, stanu zdrowia oraz zdolności organizmu do rozkładania i wykorzystywania składników leku
OLIMEL N12E.
Zastosowanie większej niż zalecana dawki leku OLIMEL N12E, emulsja do infuzji
W przypadku podania pacjentowi zbyt dużej dawki leku lub zbyt szybkiej infuzji, zawarte aminokwasy
mogą przyczynić się do zwiększenia kwasowości krwi i wystąpienia objawów hiperwolemii (zwiększenie
objętości krwi krążącej). Może zwiększyć się stężenie glukozy we krwi i w moczu, może dojść do
powstania zespołu hiperosmolarności (nadmiernej lepkości krwi), a zawarte w emulsji tłuszcze mogą
zwiększyć stężenie triglicerydów we krwi. Przyjęcie podanej z nadmierną szybkością infuzji lub zbyt
dużej objętości leku OLIMEL N12E może wywołać nudności, wymioty, dreszcze, ból głowy, uderzenia
gorąca, nadmierną potliwość (hiperhydrozę) oraz zaburzenia elektrolitowe. W takiej sytuacji należy
natychmiast przerwać infuzję.
Niekiedy, w ciężkich przypadkach, aby wspomóc nerki w wydaleniu nadmiaru leku, lekarz będzie musiał
przez pewien czas poddawać pacjenta dializie nerek.
Aby zapobiec takim sytuacjom, lekarz regularnie monitoruje stan pacjenta oraz sprawdza parametry krwi.
W razie wątpliwości związanych ze stosowaniem leku należy zwrócić się do lekarza.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
W przypadku zaobserwowania jakichkolwiek zmian samopoczucia podczas leczenia lub po jego
zakończeniu, należy od razu powiadomić o tym lekarza lub pielęgniarkę.
Badania wykonywane przez lekarza podczas podawania leku pacjentowi powinny zminimalizować
ryzyko działań niepożądanych.
Jeśli wystąpią jakiekolwiek nietypowe oznaki lub objawy świadczące o rozwoju reakcji alergicznej, takie
jak nadmierne pocenie się, gorączka, dreszcze, ból głowy, wysypka skórna lub trudności z oddychaniem,
należy natychmiast przerwać infuzję.
Podczas stosowania leku OLIMEL opisywano występowanie następujących działań niepożądanych:
Częstość — Często: mogą dotyczyć do 1 na 10 osób
- przyspieszona praca serca (częstoskurcz);
- zmniejszony apetyt;
- zwiększone stężenie tłuszczów we krwi (hipertriglicerydemia);
- ból brzucha;
- biegunka;
- nudności;
- zwiększone ciśnienie tętnicze krwi (nadciśnienie).
Częstość — Nieznana: częstość nie może być określona na podstawie dostępnych danych
- reakcje nadwrażliwości, w tym pocenie się, gorączka, dreszcze, ból głowy, wysypka skórna (rumieniowa, grudkowa, krostkowa, plamkowa, uogólniona wysypka), swędzenie, uderzenia gorąca, trudności w oddychaniu;
- wyciek infuzji do otaczającej tkanki (wynaczynienie) może prowadzić do bólu, podrażnienia, opuchlizny/obrzęku, zaczerwienienia (rumienia)/rozgrzania, obumarcia komórek tkanki (martwicy skóry) lub pęcherzy/pęcherzyków, zapalenia, pogrubienia lub napięcia skóry w miejscu podania wlewu;
- wymioty.
Podczas stosowania podobnych leków do żywienia pozajelitowego opisywano występowanie
następujących działań niepożądanych:
Częstość — Bardzo rzadko: mogą dotyczyć do 1 na 10 000 osób
- zmniejszona zdolność do usuwania lipidów (zespół przeciążenia tłuszczami) związana z nagłym pogorszeniem się stanu zdrowia pacjenta. Wymienione poniżej objawy zespołu przeciążenia tłuszczami zazwyczaj ustępują po przerwaniu infuzji emulsji tłuszczowej:
- gorączka;
- zmniejszenie liczby czerwonych krwinek, które może spowodować bladość skóry i być przyczyną osłabienia lub duszności (niedokrwistość);
- mała liczba krwinek białych, mogąca zwiększać ryzyko zakażeń (leukopenia);
- mała liczba płytek krwi, mogąca zwiększać ryzyko powstawania sińców i (lub) krwotoków (małopłytkowość);
- zaburzenia krzepnięcia, które wpływają na zdolność do krzepnięcia krwi;
- wysokie stężenie tłuszczu we krwi (hiperlipidemia);
- tłuszczowe nacieki w wątrobie (hepatomegalia);
- pogorszenie czynności wątroby;
- objawy ze strony ośrodkowego układu nerwowego (np. śpiączka).
Częstość — Nieznana:częstość nie może być określona na podstawie dostępnych danych
- reakcje alergiczne;
- nieprawidłowe wyniki badania krwi pod kątem czynności wątroby;
- utrudnione wydalanie żółci (cholestaza);
- powiększenie wątroby (hepatomegalia);
- choroby wątroby związane z żywieniem pozajelitowym (patrz „Ostrzeżenia i środki ostrożności” w punkcie 2);
- żółtaczka;
- zmniejszenie liczby płytek krwi (małopłytkowość);
- zwiększone stężenie azotu we krwi (azotemia);
- podwyższona aktywność enzymów wątrobowych;
- powstawanie małych cząstek, które mogą spowodować zablokowanie naczyń krwionośnych w płucach (osady w naczyniach płucnych), prowadzące do zatoru naczyń płucnych i trudności z oddychaniem (niewydolności oddechowej).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w
ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu
Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek OLIMEL N12E, emulsja do infuzji
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności, zamieszczonego na pojemniku oraz opakowaniu
zewnętrznym po (MM/RRRR). Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie zamrażać.
Przechowywać w opakowaniu ochronnym.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek OLIMEL N12E, emulsja do infuzji
Substancjami czynnymi w każdym z worków gotowej emulsji są: 14,2% (co odpowiada 14,2 g/100 ml)
roztwór L-aminokwasów (alanina, arginina, glicyna, histydyna, izoleucyna, leucyna, lizyna (w postaci
lizyny octanu), metionina, fenyloalanina, prolina, seryna, treonina, tryptofan, tyrozyna, walina, kwas
asparaginowy, kwas glutaminowy) z elektrolitami (sód, potas, magnez, fosforany, octany, chlorki),
17,5% (co odpowiada 17,5 g/100 ml) emulsja tłuszczowa (olej z oliwek oczyszczony oraz olej sojowy
oczyszczony) i 27,5% (co odpowiada 27,5 g/100 ml) roztwór glukozy (w postaci glukozy jednowodnej) z
wapniem.
Pozostałe składniki to:
| Komora zawierająca emulsję tłuszczową | Komora zawierająca roztwór aminokwasów | Komora zawierająca roztwór glukozy |
| Oczyszczone fosfolipidy z jaja kurzego, glicerol, sodu oleinian, sodu wodorotlenek (do ustalenia pH), woda do wstrzykiwań | Kwas octowy lodowaty (do ustalenia pH), woda do wstrzykiwań | Kwas solny (do ustalenia pH), woda do wstrzykiwań |
Jak wygląda lek OLIMEL N12E emulsja do infuzji i co zawiera opakowanie
OLIMEL N12E jest emulsją do infuzji dostarczaną w trójkomorowym worku. Pierwsza komora zawiera
emulsję tłuszczową, druga komora zawiera roztwór aminokwasów z elektrolitami, a trzecia komora
zawiera roztwór glukozy z wapniem. Komory są oddzielone od siebie za pomocą nieprzepuszczalnych
spawów. Przed podaniem, zawartość poszczególnych komór należy zmieszać poprzez zwijanie worka w
kierunku do siebie, zaczynając od górnej części worka, aż do otwarcia spawów.
Wygląd przed zmieszaniem:
- Roztwory aminokwasów i glukozy są przezroczyste, bezbarwne lub lekko żółte.
- Emulsja tłuszczowa jest jednorodna o mlecznym wyglądzie.
Wygląd po zmieszaniu: jednorodna emulsja o mlecznym wyglądzie.
Trójkomorowy worek jest wielowarstwowym workiem plastikowym. Wewnętrzna (kontaktowa) warstwa
worka wykazuje zgodność ze składnikami i dozwolonymi dodatkami.
Aby zapobiec kontaktowi z tlenem zawartym w powietrzu, worek zapakowany jest w opakowanie
ochronne, chroniące przed dostępem tlenu, z saszetką pochłaniającą tlen.
Wielkości opakowań
worek 650 ml: 1 tekturowe pudełko z 10 workami
worek 1000 ml: 1 tekturowe pudełko z 6 workami
worek 1500 ml: 1 tekturowe pudełko z 4 workami; 1 tekturowe pudełko z 5 workami
worek 2000 ml: 1 tekturowe pudełko z 4 workami; 1 tekturowe pudełko z 5 workami
1 worek o pojemności 650 ml, 1000 ml, 1500 ml i 2000 ml.
Nie wszystkie rodzaje opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Baxter Polska Sp. z o. o.
ul. Kruczkowskiego 8
00-380 Warszawa
Wytwórca
BAXTER S.A.
Boulevard René Branquart 80
7860 Lessines
Belgia
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Belgia, Bułgaria, Chorwacja, Cypr, Czechy, Estonia, Francja, Grecja, Węgry, Włochy, Łotwa, Litwa,
Luksemburg, Holandia, Rumunia, Słowenia, Słowacja, Hiszpania: OLIMEL N12E
Austria: ZentroOLIMEL 7,6 % mit Elektrolyten
Niemcy: Olimel 7,6 % E
Dania, Islandia, Szwecja, Norwegia, Finlandia, Polska, Portugalia: Olimel N12E
Irlandia, Malta, Wielka Brytania: TRIOMEL 12 g/l nitrogen 950 kcal/l with electrolytes
Data ostatniej aktualizacji ulotki kwiecień 2025
-------------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
A. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
OLIMEL N12E ma postać trójkomorowego worka.
Każdy worek zawiera roztwór glukozy z wapniem, emulsję tłuszczową oraz roztwór aminokwasów z
innymi elektrolitami.
| Zawartości na worek | ||||
| 650 ml | 1000 ml | 1500 ml | 2000 ml | |
| 27,5% roztwór glukozy (co odpowiada 27,5 g/100 ml) | 173 ml | 267 ml | 400 ml | 533 ml |
| 14,2% roztwór aminokwasów (co odpowiada 14,2 g/100 ml) | 347 ml | 533 ml | 800 ml | 1067 ml |
| 17,5% emulsja tłuszczowa (co odpowiada 17,5 g/100 ml) | 130 ml | 200 ml | 300 ml | 400 ml |
Skład gotowej emulsji po wymieszaniu zawartości trzech komór:
| Substancje czynne | 650 ml | 1000 ml | 1500 ml | 2000 ml |
| Olej z oliwek oczyszczony + olej sojowy oczyszczonya | 22,75 g | 35,00 g | 52,50 g | 70,00 g |
| Alanina | 7,14 g | 10,99 g | 16,48 g | 21,97 g |
| Arginina | 4,84 g | 7,44 g | 11,16 g | 14,88 g |
| Kwas asparaginowy | 1,43 g | 2,20 g | 3,30 g | 4,39 g |
| Kwas glutaminowy | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Glicyna | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Histydyna | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| Izoleucyna | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Leucyna | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Lizyna (co odpowiada octanowi lizyny) | 3,88 g (5,48 g) | 5,97 g (8,43 g) | 8,96 g (12,64 g) | 11,95 g (16,85 g) |
| Metionina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Fenyloalanina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Prolina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| Seryna | 1,95 g | 3,00 g | 4,50 g | 5,99 g |
| Treonina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Tryptofan | 0,82 g | 1,26 g | 1,90 g | 2,53 g |
| Tyrozyna | 0,13 g | 0,20 g | 0,30 g | 0,39 g |
| Walina | 3,16 g | 4,86 g | 7,29 g | 9,72 g |
| Sodu octan trójwodny | 0,97 g | 1,5 g | 2,24 g | 2,99 g |
| Sodu glicerofosforan uwodniony | 2,39 g | 3,67 g | 5,51 g | 7,34 g |
| Potasu chlorek | 1,45 g | 2,24 g | 3,35 g | 4,47 g |
| Magnezu chlorek sześciowodny | 0,53 g | 0,81 g | 1,22 g | 1,62 g |
| Wapnia chlorek dwuwodny | 0,34 g | 0,52 g | 0,77 g | 1,03 g |
| Glukoza (co odpowiada glukozie jednowodnej) | 47,67 g (52,43 g) | 73,33 g (80,67 g) | 110,00 g (121,00 g) | 146,67 g (161,33 g) |
Substancjami pomocniczymi są:
| Komora zawierająca emulsję tłuszczową | Komora zawierająca roztwór aminokwasów z elektrolitami | Komora zawierająca roztwór glukozy z wapniem |
| Oczyszczone fosfolipidy z jaja kurzego, glicerol, sodu oleinian, sodu wodorotlenek (do ustalenia pH), woda do wstrzykiwań | Kwas octowy lodowaty (do ustalenia pH), woda do wstrzykiwań | Kwas solny (do ustalenia pH), woda do wstrzykiwań |
Wartości odżywcze gotowej emulsji, odpowiednio do wielkości worków:
| 650 ml | 1000 ml | 1500 ml | 2000 ml | |
| Tłuszcze | 22,8 g | 35,0 g | 52,5 g | 70,0 g |
| Aminokwasy | 49,4 g | 75,9 g | 113,9 g | 151,9 g |
| Azot | 7,8 g | 12,0 g | 18,0 g | 24,0 g |
| Glukoza | 47,7 g | 73,3 g | 110,0 g | 146,7 g |
| Wartość energetyczna: | ||||
| Całkowita wartość energetyczna w przybliżeniu | 620 kcal | 950 kcal | 1420 kcal | 1900 kcal |
| Wartość energetyczna niebiałkowa | 420 kcal | 640 kcal | 960 kcal | 1280 kcal |
| Wartość energetyczna glukozy | 190 kcal | 290 kcal | 430 kcal | 580 kcal |
| Wartość energetyczna tłuszczówb | 230 kcal | 350 kcal | 520 kcal | 700 kcal |
| Stosunek: wartość energetyczna niebiałkowa/azot | 53 kcal/g | 53 kcal/g | 53 kcal/g | 53 kcal/g |
| Stosunek: wartość energetyczna glukoza/tłuszcze | 45/55 | 45/55 | 45/55 | 45/55 |
| Tłuszcze/całkowita ilość kalorii | 37% | 37% | 37% | 37% |
| Elektrolity: | ||||
| Sód | 22,8 mmol | 35,0 mmol | 52,5 mmol | 70,0 mmol |
| Potas | 19,5 mmol | 30,0 mmol | 45,0 mmol | 60,0 mmol |
| Magnez | 2,6 mmol | 4,0 mmol | 6,0 mmol | 8,0 mmol |
| Wapń | 2,3 mmol | 3,5 mmol | 5,3 mmol | 7,0 mmol |
| Fosforanyc | 9,5 mmol | 15,0 mmol | 21,9 mmol | 29,2 mmol |
| Octany | 46 mmol | 70 mmol | 105 mmol | 140 mmol |
| Chlorki | 30 mmol | 45 mmol | 68 mmol | 90 mmol |
| pH | 6,4 | 6,4 | 6,4 | 6,4 |
| Osmolarność w przybliżeniu | 1270 mOsm/l | 1270 mOsm/l | 1270 mOsm/l | 1270 mOsm/l |
B. DAWKOWANIE I SPOSÓB PODAWANIA
Dawkowanie
OLIMEL N12E nie jest zalecany do stosowania u dzieci w wieku poniżej 2 lat, ze względu na
nieodpowiedni skład oraz objętość (patrz punkty 4.4; 5.1 i 5.2 ChPL).
Nie należy przekraczać podanej niżej maksymalnej dawki dobowej. Ze względu na stały skład worka
wielokomorowego, zaspokojenie jednocześnie wszystkich potrzeb żywieniowych pacjenta może nie być
możliwe. Mogą występować sytuacje kliniczne, w których pacjenci potrzebują innych ilości substancji
odżywczych niż znajdujące się w worku o stałym składzie. W takiej sytuacji każda zmiana objętości
(dawki) powinna uwzględniać wpływ, jaki będzie to miało na dawkowanie wszystkich pozostałych
substancji odżywczych produktu leczniczego OLIMEL N12E. W takich przypadkach fachowy personel
medyczny może rozważyć dostosowanie objętości (dawki) produktu leczniczego OLIMEL N12E w celu
zaspokojenia zwiększonego zapotrzebowania.
Dorośli
Dawkowanie zależy od wydatku energetycznego pacjenta, stanu klinicznego, masy ciała oraz możliwości
metabolizowania składników produktu OLIMEL N12E, jak również od składników energetycznych lub
białek, dodatkowo dostarczanych doustnie/dojelitowo, dlatego należy odpowiednio dobrać wielkość
worka.
Średnie dobowe zapotrzebowanie to:
- 0,16 do 0,35 g azotu/kg masy ciała (1 - 2 g aminokwasów/kg), w zależności od stanu odżywienia pacjenta oraz stopnia katabolizmu. Szczególne populacje mogą wymagać do 0,4 g azotu/kg masy ciała (2,5 g aminokwasów/kg).
- 20 do 40 kcal/kg,
- 20 do 40 ml płynu/kg lub 1 do 1,5 ml na zużywaną kcal.
Dla produktu OLIMEL N12E, maksymalną dawkę dobową określono wg przyjęcia aminokwasów,
26 ml/kg odpowiada 2,0 g aminokwasów/kg, 1,9 g glukozy/kg, 0,9 g tłuszczów/kg. Dla pacjenta o masie
ciała 70 kg odpowiadałoby to 1820 ml produktu OLIMEL N12E na dobę, co oznacza przyjęcie
138 g aminokwasów, 133 g glukozy oraz 64 g tłuszczów (tj. 1171 kcal niebiałkowych oraz całkowitej
ilości 1723 kcal).
W ciągłej terapii nerkozastępczej (CRRT):Dla produktu OLIMEL N12E, maksymalną dawkę dobową
określono wg przyjęcia aminokwasów, 33 ml/kg odpowiada 2,5 g aminokwasów/kg, 2,4 g glukozy/kg,
1,2 g lipidów/kg. Dla pacjenta o masie ciała 70 kg odpowiadałoby to 2310 ml produktu OLIMEL N12E
na dobę, co oznacza przyjęcie 175 g aminokwasów, 169 g glukozy i 81 g tłuszczów (tj. 1486 kcal
niebiałkowych oraz całkowitej ilości 2187 kcal).
U pacjentów z chorobliwą otyłością: Dawkę należy obliczyć na podstawie idealnej masy ciała (z ang.
ideal body weight - IBW). Dla produktu OLIMEL N12E, maksymalną dawkę dobową określono wg
przyjęcia aminokwasów, 33 ml/kg IBW odpowiada 2,5 g aminokwasów/kg, 2,4 g glukozy/kg,
1,2 g lipidów/kg. Dla pacjenta o masie ciała 70 kg odpowiadałoby to 2310 ml produktu OLIMEL N12E
na dobę, co oznacza przyjęcie 175 g aminokwasów, 169 g glukozy i 81 g tłuszczów (tj. 1486 kcal
niebiałkowych oraz całkowitej ilości 2187 kcal).
Zazwyczaj, szybkość podawania musi zwiększać się stopniowo podczas pierwszej godziny, a następnie,
szybkość infuzji musi być odpowiednio dostosowana pod względem dawki, dobowej objętości
przyjmowanego produktu leczniczego oraz czasu trwania infuzji.
Dla produktu OLIMEL N12E, maksymalna szybkość infuzji wynosi 1,3 ml/kg/godz., co odpowiada
0,10 g aminokwasów/kg/godz., 0,10 g glukozy/kg/godz. oraz 0,05 g tłuszczów/kg/godz.
Dzieci w wieku powyżej 2 lat i młodzież
Nie przeprowadzono badań w populacji pediatrycznej.
Dawkowanie zależy od wydatku energetycznego pacjenta, stanu klinicznego, masy ciała oraz możliwości
metabolizowania składników produktu OLIMEL N12E, jak również od składników energetycznych lub
białek dodatkowo podawanych doustnie/dojelitowo; dlatego należy odpowiednio dobrać wielkość worka.
Ponadto, dobowe zapotrzebowanie na płyny, azot oraz energię stale maleje wraz z wiekiem. Wzięto pod
uwagę dwie grupy, w wieku od 2 do 11 lat i od 12 do 18 lat.
Dla produktu OLIMEL N12E, w grupie wiekowej 2 do 11 lat, czynnikami ograniczającymi dla dawki
dobowej są stężenia aminokwasów i magnezu. W tej grupie wiekowej, czynnikiem ograniczającym dla
szybkości podania na godzinę jest stężenie aminokwasów. W grupie wiekowej 12 do 18 lat, czynnikami
ograniczającymi dla dawki dobowej są stężenia aminokwasów i magnezu. W tej grupie wiekowej,
czynnikiem ograniczającym dla szybkości podania na godzinę jest stężenie aminokwasów. Wynikające z
tego pobory przedstawiono poniżej:
| Składnik | 2 do 11 lat | 12 do 18 lat | ||
| Zalecanea | Maksymalna objętość OLIMEL N12E | Zalecanea | Maksymalna objętość OLIMEL N12E | |
| Maksymalna dawka dobowa | ||||
| Płyny (ml/kg/doba) |
| 33 |
| 26 |
| Aminokwasy (g/kg/doba) |
| 2,5 |
| 2 |
| Glukoza (g/kg/doba) | 1,4 – 8,6 | 2,4 | 0,7 - 5,8 | 1,9 |
| Tłuszcze (g/kg/doba) | 0,5 - 3 | 1,2 | 0,5 - 2 (do 3) | 0,9 |
| Całkowita wartość energetyczna (kcal/kg/doba) |
| 31,4 |
| 24,7 |
| Maksymalna szybkość podania na godzinę | ||||
| OLIMEL N12E (ml/kg/godz.) | 2,6 | 1,6 | ||
| Aminokwasy (g/kg/godz.) | 0,20 | 0,20 | 0,12 | 0,12 |
| Glukoza (g/kg/godz.) | 0,36 | 0,19 | 0,24 | 0,12 |
| Tłuszcze (g/kg/godz.) | 0,13 | 0,09 | 0,13 | 0,06 |
Zazwyczaj szybkość podawania musi zwiększać się stopniowo podczas pierwszej godziny, a następnie
należy ją dostosować uwzględniając podawaną dawkę, dobową objętość przyjmowanego produktu
leczniczego oraz czas trwania infuzji.
Na ogół, u małych dzieci zaleca się rozpoczynać infuzję od małej dawki dobowej i zwiększać ją
stopniowo do maksymalnego dawkowania (patrz powyżej).
Maksymalna szybkość podania u dzieci w wieku 2 do 11 lat wynosi 2,6 ml/kg/godzinę, a u dzieci w
wieku 12 do 18 lat wynosi 1,6 ml/kg/godzinę.
Sposób i czas podawania
Wyłącznie do jednorazowego użycia.
Zaleca się, aby po otwarciu niezwłocznie zużyć zawartość worka i nie przechowywać do następnej
infuzji.
Po zmieszaniu otrzymuje się jednorodną mieszaninę o mlecznym wyglądzie.
Instrukcje dotyczące przygotowania i stosowania emulsji do infuzji, patrz punkt 6.6 ChPL.
Z powodu wysokiej osmolarności OLIMEL N12E, musi być podawany wyłącznie do żyły centralnej.
Zalecany czas trwania infuzji w przypadku worka do odżywiania pozajelitowego wynosi od 12
do 24 godzin.
Leczenie za pomocą odżywiania pozajelitowego można kontynuować tak długo, jak tego wymaga stan
kliniczny pacjenta.
C. NIEZGODNOŚCI FARMACEUTYCZNE
Nie należy dodawać żadnych produktów leczniczych ani substancji do któregokolwiek ze składników
worka albo do gotowej emulsji, bez uprzedniego potwierdzenia ich zgodności oraz stabilności
otrzymanego produktu (zwłaszcza stabilności emulsji tłuszczowej).
Niezgodności mogą wynikać np. z powodu nadmiernej kwasowości (niskie pH) lub nieodpowiedniej
zawartości kationów dwuwartościowych (Ca oraz Mg ), mogących destabilizować emulsję tłuszczową.
Tak jak w przypadku tworzenia innych mieszanin do żywienia pozajelitowego, należy wziąć pod uwagę
stosunek zawartości wapnia i fosforanów. Nadmierny dodatek wapnia i fosforanu, szczególnie w postaci
soli nieorganicznych, może spowodować powstanie osadów wapnia fosforanu.
OLIMEL N12E zawiera jony wapnia stwarzające dodatkowe ryzyko wytrącania skrzepów w preparatach
krwi lub składników krwi z dodatkiem cytrynianu jako środka przeciwzakrzepowego/konserwującego.
Nie wolno mieszać ani podawać ceftriaksonu jednocześnie z roztworami dożylnymi zawierającymi wapń,
w tym z produktem OLIMEL N12E, przez tę samą linię do infuzji (np. przez łącznik typu Y) ze względu
na ryzyko wytrącenia się soli wapniowych ceftriaksonu (patrz punkty 4.4 i 4.5 ChPL). Ceftriakson
i roztwory zawierające wapń można podawać kolejno jeden po drugim, jeśli linie do infuzji są wkłute
w różne miejsca lub są wymieniane albo dokładnie płukane roztworem fizjologicznym soli między
infuzjami, aby uniknąć wytrącania osadów.
Ze względu na ryzyko wytrącenia się osadu, produktu leczniczego OLIMEL N12E nie należy podawać
przez tę samą linię do infuzji ani dodawać do ampicyliny lub fosfenytoiny.
Należy sprawdzić zgodność z roztworami podawanymi jednocześnie przez ten sam zestaw do infuzji,
cewnik lub kaniulę.
Z powodu ryzyka wystąpienia pseudoaglutynacji, nie należy podawać tego produktu przed, w trakcie lub
po podaniu krwi przez ten sam zestaw do infuzji.
D. SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA I PRZYGOTOWANIA
PRODUKTU LECZNICZEGO DO STOSOWANIA
Przegląd etapów przygotowania do podania OLIMEL N12E przedstawiono na Rysunku 1.
Otwieranie
Usunąć worek ochronny.
Wyrzucić saszetkę zawierającą pochłaniacz tlenu.
Upewnić się, że worek lub spawy nie są uszkodzone. Stosować wyłącznie w przypadku, gdy worek jest
nieuszkodzony, a spawy są nienaruszone (tzn. zawartość 3 komór nie została wymieszana), roztwory
aminokwasów i glukozy są przezroczyste, bezbarwne lub lekko żółte, praktycznie pozbawione
widocznych cząsteczek oraz gdy emulsja tłuszczowa jest jednorodna o mlecznym wyglądzie.
Mieszanie roztworów i emulsji
Przed rozerwaniem spawów należy się upewnić, że produkt ma temperaturę pokojową.
Zaczynając od góry worka (przy uchwycie), zrolować worek oburącz. Spawy będą zanikać od strony
portów. Kontynuować zwijanie worka aż do momentu rozerwania spawów do połowy ich długości.
Wymieszać, obracając worek co najmniej 3-krotnie.
Po zmieszaniu produkt ma postać jednorodnej emulsji o mlecznym wyglądzie.
Dodatkowe składniki
Pojemność worka jest wystarczająca, aby umożliwić dodanie witamin, elektrolitów i pierwiastków
śladowych.
Wszelkie dodatki (w tym witaminy) powinny być wprowadzone do gotowej emulsji (po rozerwaniu
spawów i po wymieszaniu zawartości 3 komór).
Witaminy można także dodawać do komory zawierającej glukozę przed przygotowaniem gotowej emulsji
(przed rozerwaniem spawów i przed wymieszaniem zawartości trzech komór).
Dodatkowe składniki muszą być wprowadzone przez wykwalifikowany personel w warunkach
aseptycznych.
Do produktu OLIMEL N12E można dodawać elektrolity, fosforany nieorganiczne/organiczne oraz
dostępne na rynku produkty wielowitaminowe (takie jak Cernevit) i produkty zawierające kilka
pierwiastków śladowych (takie jak Nutryelt). Maksymalne całkowite stężenie dodatkowych składników
wymienionych w poniższej tabeli, zostało wskazane na podstawie danych dotyczących stabilności i nie
powinno być uważane za zalecenia dotyczące dawkowania. Suplementacja powinna być podyktowana
potrzebami klinicznymi pacjenta i nie powinna wykraczać poza wytyczne żywieniowe. Przy osiąganiu
maksymalnego całkowitego stężenia należy uwzględnić ilość elektrolitów znajdujących się już w worku.
Zgodność z produktami pochodzącymi z różnych źródeł może być różna, a pracownicy służby zdrowia
powinni przeprowadzać odpowiednie kontrole podczas mieszania produktu OLIMEL N12E z innymi
roztworami do podawania pozajelitowego.
| Możliwe dodatkowe składniki na 1000 ml produktu OLIMEL N12E (dla dzieci i młodzieży) | |||
| Zawartość | Maksymalny dodatek | Maksymalna zawartość | |
| Sód | 35 mmol | 115 mmol | 150 mmol |
| Potas | 30 mmol | 120 mmol | 150 mmol |
| Magnez | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Wapń | 3,5 mmol | 1,5 mmol | 5,0 mmol |
| Fosforany nieorganiczne | 0 mmol | 10 mmol Pi lub 10 mmol Pob | 10 mmol Pi + 15 mmol Po lub 25 mmol Poa,b |
| Fosforany organiczne | 15 mmola | ||
| Pozostałe dodatkowe składniki (pierwiastki śladowe, witaminy, selen i cynk)c | |||
| Pierwiastki śladowe – Nutryelt Pediatricd | 1 fiolka na worek (10 ml roztworu koncentratu) | ||
| Witaminye | 1 fiolka (liofilizat) | ||
| Selen | 60 µg na worek | ||
| Cynk | 3 mg na worek | ||
| Możliwe dodatkowe składniki na 1000 ml produktu OLIMEL N12E (dla dorosłych) | |||
| Zawartość | Maksymalny dodatek | Maksymalna zawartość | |
| Sód | 35 mmol | 115 mmol | 150 mmol |
| Potas | 30 mmol | 120 mmol | 150 mmol |
| Magnez | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Wapń | 3,5 mmol | 1,5 mmol | 5,0 mmol |
| Fosforany nieorganiczne | 0 mmol | 10 mmol Pi lub 10 mmol Pob | 10 mmol Pi + 15 mmol Po lub 25 mmol Poa,b |
| Fosforany organiczne | 15 mmola | ||
| Pozostałe dodatkowe składniki (pierwiastki śladowe, witaminy, selen i cynk)c | |||
| Pierwiastki śladowe - Nutryeltd | 2 fiolki na worek (10 ml roztworu koncentratu) | ||
| Witaminy - Cernevite | 1 fiolka (5 ml liofilizatu) | ||
| Selen | 500 µg na worek | ||
| Cynk | 20 mg na worek | ||
Wprowadzając dodatkowe składniki należy:
- kontrolować warunki aseptyki,
- przygotować miejsce wstrzyknięcia w worku,
- przekłuć miejsce wstrzyknięcia i wstrzyknąć dodatkowe składniki za pomocą igły do wstrzykiwań lub urządzenia do przygotowania produktu leczniczego,
- wymieszać zawartość worka z dodatkowymi składnikami.
Okres ważności po zmieszaniu
Wykazano chemiczną i fizyczną stabilność w trakcie stosowania przez 7 dni w temperaturze od 2°C do
8°C i następnie przez 48 godzin przechowywania w temperaturze nieprzekraczającej 30°C.
Z mikrobiologicznego punktu widzenia, produkt należy zużyć natychmiast. Jeśli produkt nie zostanie
zużyty natychmiast, podczas stosowania za czas i warunki przechowywania do momentu zastosowania
odpowiada użytkownik a przechowywanie nie powinno trwać dłużej niż 24 godziny w temperaturze od
2°C do 8°C, chyba że rekonstytucja nastąpiła w kontrolowanych i zwalidowanych warunkach
aseptycznych.
Okres ważności po wprowadzeniu dodatkowych składników
Po wprowadzeniu dodatkowych składników, wykazano chemiczną i fizyczną stabilność w trakcie
stosowania przez 7 dni w temperaturze od 2°C do 8°C i następnie przez 48 godzin przechowywania w
temperaturze nieprzekraczającej 30°C.
Z mikrobiologicznego punktu widzenia, produkt należy zużyć natychmiast. Jeśli produkt nie zostanie
zużyty natychmiast, podczas stosowania za czas i warunki przechowywania do momentu zastosowania
odpowiada użytkownik a przechowywanie nie powinno trwać dłużej niż 24 godziny w temperaturze od
2°C do 8°C, chyba że dodanie dodatkowych składników nastąpiło w kontrolowanych i zwalidowanych
warunkach aseptycznych.
Przygotowanie infuzji
Kontrolować warunki aseptyki.
Zawiesić worek.
Usunąć plastikowy ochraniacz z portu do podawania produktu leczniczego.
Zdecydowanie wprowadzić iglicę zestawu do infuzji do portu do podawania produktu leczniczego.
Rysunek 1. Etapy przygotowania produktu OLIMEL do podania


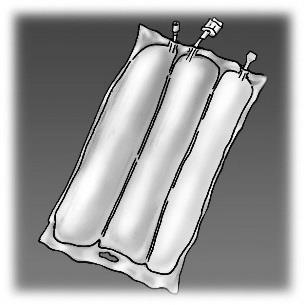
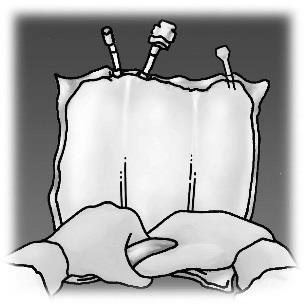
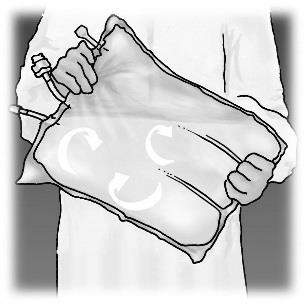
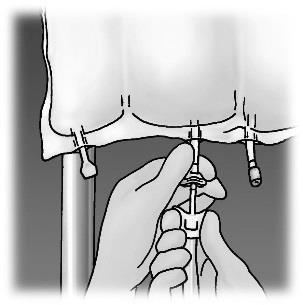
Podawanie
Wyłącznie do jednorazowego stosowania.
Podawać produkt wyłącznie po rozerwaniu spawów dzielących 3 komory i wymieszaniu ich zawartości.
Należy upewnić się, czy w gotowej emulsji do infuzji nie następuje rozdzielanie faz.
Po otwarciu worka zawartość musi zostać natychmiast wykorzystana. Nie wolno przechowywać
otwartego worka do następnej infuzji. Nie podłączać ponownie częściowo zużytych worków.
W celu uniknięcia możliwości powstania zatorów powietrznych, spowodowanych obecnością gazu
zawartego w pierwszym worku, nie podłączać worków seryjnie.
Wszelkie resztki niewykorzystanego produktu lub jego odpady oraz cały zestaw do infuzji należy
zniszczyć.
Wynaczynienie
Miejsce założenia cewnika należy regularnie monitorować pod kątem oznak wynaczynienia.
W przypadku wynaczynienia należy natychmiast przerwać podawanie produktu, pozostawiając na
miejscu wprowadzony cewnik lub kaniulę w celu natychmiastowego wdrożenia postępowania
leczniczego. O ile to możliwe, przed wyjęciem wprowadzonego cewnika/kaniuli należy dokonać aspiracji
płynu przez cewnik/kaniulę w celu zmniejszania ilości płynu w tkankach.
W zależności od rodzaju wynaczynionego produktu (w tym produktu(-ów) mieszanych z produktem
OLIMEL N12E, jeśli dotyczy) oraz stopnia/rozległości ewentualnego urazu, należy podjąć właściwe
szczególne
środki
zaradcze.
Opcje
postępowania
leczniczego
mogą
obejmować
leczenie
niefarmakologiczne, farmakologiczne i (lub) interwencję chirurgiczną. W przypadku dużego
wynaczynienia należy przed upływem 72 godzin skonsultować się z chirurgiem plastycznym.
Miejsce wynaczynienia należy monitorować co najmniej co cztery godziny w okresie pierwszych
24 godzin, a następnie raz na dobę.
Nie należy wznawiać wlewu do tej samej żyły centralnej.
Baxter i Olimel są znakami towarowymi Baxter International Inc.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterBaxter S.A.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Olimel N12EPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez recepty
Odpowiedniki Olimel N12E w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Olimel N12E – Hiszpania
Odpowiednik Olimel N12E – Ukraina
Lekarze online w sprawie Olimel N12E
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Olimel N12E – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














