

Kabiven Peripheral

Zapytaj lekarza o receptę na Kabiven Peripheral

Jak stosować Kabiven Peripheral
Ulotka dołączona do opakowania: informacja dla użytkownika
Kabiven Peripheral, emulsja do infuzji
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Kabiven Peripheral i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Kabiven Peripheral
- 3. Jak stosować Kabiven Peripheral
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Kabiven Peripheral
- 6. Zawartość opakowania i inne informacje
1. Co to jest Kabiven Peripheral i w jakim celu się go stosuje
Kabiven Peripheral jest lekiem zawierającym: aminokwasy (składniki niezbędne do tworzenia białek),
tłuszcze, glukozę i elektrolity. Zapewnia dożylne dostarczenie energii (z cukru i tłuszczów) oraz
aminokwasów, gdy żywienie doustne jest niemożliwe, niewystarczające lub przeciwwskazane.
Kabiven Peripheral jest wskazany do stosowania jako składnik kompleksowej diety dożylnej, razem
z solami, pierwiastkami śladowymi oraz witaminami.
2. Informacje ważne przed zastosowaniem leku Kabiven Peripheral
Kiedy nie stosować leku Kabiven Peripheral
Nie należy stosować leku:
- jeśli pacjent ma uczulenie(nadwrażliwość) na Kabiven Peripheral, na substancje czynne lub na którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli pacjent ma uczulenie (nadwrażliwość) na jaja, soję lub orzeszki ziemne;
- jeśli u pacjenta występuje zbyt wysokie stężenie tłuszczów(np. cholesterolu) we krwi;
- jeśli pacjent ma ciężką chorobę wątroby;
- jeśli u pacjenta występuje ostry wstrząs(spowodowany utratą dużej ilości krwi lub uczuleniem);
- jeśli pacjent ma zaburzenia układu krzepnięcia(zespół hemofagocytarny) lub jeśli krew niekrzepnie prawidłowo;
- jeśli pacjent ma zaburzenia metabolizmu białek lub aminokwasów;
- jeśli pacjent ma ciężką chorobę nerek;
- jeśli pacjent ma hiperglikemię ( zbyt duża ilość cukru we krwi) wymagającą podania więcej niż 6 jednostek insuliny na godzinę;
- jeśli pacjent ma podwyższone stężenie elektrolitów(soli) we krwi;
- jeśli pacjent ma kwasicę metaboliczną(nagromadzenie we krwi i tkankach nadmiernych ilości kwaśnych substancji);
- jeśli pacjent ma za dużo płynuw organizmie (przewodnienie);
- jeśli pacjent ma płyn w płucach(ostry obrzęk płuc);
- jeśli pacjent jest w śpiączce;
- jeśli pacjent ma problemy z sercem;
- jeśli pacjent jest odwodnionyoraz ma niskie stężenie soli;
- jeśli u pacjenta występuje ciężka ogólnoustrojowa reakcja zapalna(stan, w którym w organizmie występuje ciężkie zakażenie).
Nie należy stosować leku Kabiven Peripheral u noworodków i dzieci w wieku poniżej 2 lat.
Ostrzeżenia i środki ostrożności
Należy poinformować lekarza, jeśli u pacjenta występują:
- zaburzenia czynności wątroby;
- nieleczona cukrzyca;
- zaburzenia metabolizmu tłuszczów;
- choroby nerek;
- jakiekolwiek choroby trzustki;
- choroby tarczycy- niedoczynność tarczycy;
- ogólnoustrojowa reakcja zapalna(stan, w którym w organizmie występuje zakażenie);
- zaburzenia usuwania elektrolitów z organizmu;
- niewystarczające dostarczenie tlenudo komórek;
- zwiększona osmolarność surowicy.
Jeśli podczas infuzji wystąpi gorączka, wysypka, dreszcze lub trudności w oddychaniu, należy
niezwłocznie powiadomić o tym fachowy personel medyczny. Objawy te mogą być spowodowane
reakcją alergiczną lub podano zbyt dużą dawkę leku (patrz punkt 4).
Ten lek wpływa na wyniki niektórych badań. Należy poinformować lekarza o stosowaniu tego leku
przed wykonaniem badania.
Lekarz może zalecić regularne badanie krwi, aby potwierdzić prawidłowe działanie leku Kabiven
Peripheral.
Kabiven Peripheral a inne leki
Należy powiedzieć lekarzowi lub pielęgniarce o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje stosować.
Należy poinformować lekarza, jeśli pacjent stosuje:
- heparynę - lek, który zapobiega powstawaniu skrzepów oraz pomaga w ich rozpuszczaniu;
- warfarynę, ponieważ witamina K , która występuje w oleju sojowym, może mieć wpływ na zdolność krzepnięcia krwi;
- insulinę - lek stosowany w leczeniu cukrzycy.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Brak jest danych dotyczących stosowania leku Kabiven Peripheral u kobiet w okresie ciąży lub
podczas karmienia piersią. Jeśli podanie żywienia dożylnego (pozajelitowego) jest wymagane
u kobiet w okresie ciąży lub podczas karmienia piersią, lekarz zastosuje Kabiven Peripheral tylko po
dokładnym rozważeniu korzyści i ryzyka.
3. Jak stosować Kabiven Peripheral
Kabiven Peripheral podaje się w infuzji.
Dawkowanie oraz wielkość zastosowanego opakowania ustala się w zależności od masy ciała pacjenta
oraz jego zdolności do metabolizowania tłuszczów i cukrów. Kabiven Peripheral podaje się
w powolnej infuzji trwającej od 12 do 24 godzin. Dawkowanie ustala lekarz indywidualnie każdemu
pacjentowi.
Personel medyczny może kontrolować stan zdrowia pacjenta w trakcie leczenia.
Nie należy stosować leku Kabiven Peripheral u noworodków i dzieci w wieku poniżej 2 lat.
Zastosowanie większej niż zalecana dawki leku Kabiven Peripheral
Jest mało prawdopodobne, aby pacjent otrzymał zbyt dużą dawkę leku Kabiven Peripheral, ponieważ
lek ten jest podawany przez fachowy personel medyczny. Objawami przedawkowania są nudności,
wymioty, nadmierna potliwość i zatrzymanie płynów w organizmie. Obserwowano także
hiperglikemię (zbyt dużo cukru we krwi) i zaburzenia gospodarki elektrolitowej. W przypadku
przedawkowania istnieje ryzyko przyjęcia zbyt dużej ilości tłuszczów. Ten objaw to „zespół
przedawkowania tłuszczu”. W celu zapoznania się ze szczegółowymi informacjami - patrz punkt 4.
Możliwe działania niepożądane. Jeśli pacjent zauważy powyższe objawy lub uważa, że otrzymał
większą niż zalecana dawkę leku Kabiven Peripheral, powinien niezwłocznie poinformować o tym
lekarza lub pielęgniarkę. Mogą oni zmniejszyć szybkość infuzji lub przerwać ją.
Wszystkie te objawy na ogół ustępują lub zmniejszają się po przerwaniu infuzji.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza, pielęgniarki lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Bardzo rzadko (rzadziej niż u 1 na 10 000 pacjentów) Kabiven Peripheral może powodować uczulenie (nadwrażliwość). Należy natychmiast poinformować lekarza o wystąpieniu:
- guzowatej i swędzącej wysypki na ciele;
- bardzo wysokiej temperatury;
- trudności w oddychaniu.
Często występujące działania niepożądane (rzadziej niż u 1 na 10 pacjentów, ale częściej niż u 1 na 100 pacjentów):
- podwyższenie temperatury ciała;
- zapalenie żyły, do której podano lek.
Niezbyt często występujące działania niepożądane (rzadziej niż u 1 na 100 pacjentów, ale częściej niż u 1 na 1000 pacjentów):
- dreszcze;
- zmęczenie;
- bóle brzucha;
- bóle głowy;
- nudności;
- wymioty;
- zwiększenie aktywności enzymów wątrobowych. Lekarz poinformuje pacjenta o wystąpieniu tego działania niepożądanego.
Pozostałe działania niepożądane występują bardzo rzadko (rzadziej niż u 1 na 10 000 pacjentów):
- podwyższone lub obniżone ciśnienie krwi;
- przyspieszony oddech;
- wydłużona, bolesna erekcja u mężczyzn;
- zaburzenia obrazu krwi.
Zespół przedawkowania tłuszczu
Zespół przedawkowania tłuszczu występuje, gdy organizm ma problem z metabolizmem tłuszczów
w związku z otrzymaniem nadmiernej ilości leku Kabiven Peripheral. Może on także wystąpić
z powodu nagłej zmiany stanu zdrowia pacjenta (np. problemy z nerkami lub wątrobą). Możliwe
objawy to gorączka, zwiększona ilość tłuszczu we krwi, komórkach i tkankach, zaburzenia
w funkcjonowaniu wielu organów i śpiączka. Wszystkie te objawy na ogół ustępują po przerwaniu
infuzji.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane
można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych
Al. Jerozolimskie 181C, 02-222 Warszawa
tel.: +48 22 49 21 301, faks: +48 22 49 21 309
strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Kabiven Peripheral
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Lekarz lub farmaceuta są odpowiedzialni za zapewnienie właściwych warunków przechowywania,
stosowania i usuwania leku Kabiven Peripheral.
Nie przechowywać w temperaturze powyżej 25°C. Przechowywać w worku zewnętrznym.
Nie zamrażać.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu.
Nie stosować, jeśli opakowanie jest uszkodzone.
Do jednorazowego użycia. Niezużyta pozostałość leku nie nadaje się do dalszego stosowania.
6. Zawartość opakowania i inne informacje
Co zawiera Kabiven Peripheral
Kabiven Peripheral jest dostępny w trójkomorowych workach.
Worki zawierające 3 komory produkowane są w trzech pojemnościach.
Każdy trójkomorowy worek zawiera następujące, różne objętości składników:
| 2400 ml | 1920 ml | 1440 ml | |
| glukoza 11% | 1475 ml | 1180 ml | 885 ml |
| roztwór aminokwasów z elektrolitami | 500 ml | 400 ml | 300 ml |
| emulsja tłuszczowa (Intralipid 20%) | 425 ml | 340 ml | 255 ml |
Odpowiada to następującym składom:
| Substancje czynne: | 2400 ml | 1920 ml | 1440 ml |
| olej sojowy oczyszczony | 85 g | 68 g | 51 g |
| glukoza jednowodna co odpowiada glukozie bezwodnej | 178 g 162 g | 143 g 130 g | 107 g 97 g |
| alanina | 8,0 g | 6,4 g | 4,8 g |
| arginina | 5,6 g | 4,5 g | 3,4 g |
| kwas asparaginowy | 1,7 g | 1,4 g | 1,0 g |
| kwas glutaminowy | 2,8 g | 2,2 g | 1,7 g |
| glicyna (kwas aminooctowy) | 4,0 g | 3,2 g | 2,4 g |
| histydyna | 3,4 g | 2,7 g | 2,0 g |
| izoleucyna | 2,8 g | 2,2 g | 1,7 g |
| leucyna | 4,0 g | 3,2 g | 2,4 g |
| lizyny chlorowodorek | 5,6 g | 4,5 g | 3,4 g |
| co odpowiada lizynie bezwodnej | 4,5 g | 3,6 g | 2,7 g |
| metionina | 2,8 g | 2,2 g | 1,7 g |
| fenyloalanina | 4,0 g | 3,2 g | 2,4 g |
| prolina | 3,4 g | 2,7 g | 2,0 g |
| seryna | 2,2 g | 1,8 g | 1,4 g |
| treonina | 2,8 g | 2,2 g | 1,7 g |
| tryptofan | 0,95 g | 0,76 g | 0,57 g |
| tyrozyna | 0,12 g | 0,092 g | 0,069 g |
| walina | 3,6 g | 2,9 g | 2,2 g |
| wapnia chlorek dwuwodny co odpowiada wapnia chlorkowi | 0,49 g 0,37 g | 0,39 g 0,30 g | 0,29 g 0,22 g |
| sodu glicerofosforan co odpowiada sodu glicerofosforanowi bezwodnemu | 2,5 g | 2,0 g | 1,5 g |
| magnezu siarczan siedmiowodny co odpowiada magnezu siarczanowi | 1,6 g 0,8 g | 1,3 g 0,64 g | 0,99 g 0,48 g |
| potasu chlorek | 3,0 g | 2,4 g | 1,8 g |
| sodu octan trójwodny co odpowiada sodu octanowi | 4,1 g 2,4 g | 3,3 g 2,0 g | 2,5 g 1,5 g |
Pozostałe składniki (substancje pomocnicze) to:fosfolipidy jaja kurzego oczyszczone, glicerol,
sodu wodorotlenek (do ustalenia pH), kwas octowy lodowaty (do ustalenia pH) i woda do
wstrzykiwań.
Jak wygląda Kabiven Peripheral i co zawiera opakowanie
Roztwory glukozy i aminokwasów z elektrolitami są przezroczyste, bezbarwne do lekko żółtych,
a emulsja tłuszczowa jest biała i jednorodna. Opakowanie leku Kabiven Peripheral składa się
z trójkomorowego worka wewnętrznego i worka zewnętrznego. Pomiędzy workiem wewnętrznym
a zewnętrznym znajduje się pochłaniacz tlenu, który należy usunąć przed zastosowaniem leku. Worek
wewnętrzny jest podzielony na trzy komory zgrzewami, które pękają w toku przygotowania worka do
użycia. Zawartość wszystkich trzech komór należy zmieszać przed zastosowaniem.
Wielkości opakowań:
1440 ml, 1920 ml, 2400 ml.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Fresenius Kabi AB
S-751 74 Uppsala
Szwecja
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do przedstawiciela podmiotu
odpowiedzialnego:
Fresenius Kabi Polska Sp. z o.o.
Al. Jerozolimskie 134
02-305 Warszawa
tel.: +48 22 345 67 89
Data ostatniej aktualizacji ulotki:16.11.2023 r.
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
W celu uniknięcia zagrożeń związanych ze zbyt dużą szybkością infuzji, zaleca się jej
przeprowadzanie w sposób ciągły i odpowiednio kontrolowany, w miarę możliwości z użyciem
pompy objętościowej.
Ponieważ wykorzystanie żyły centralnej do infuzji wiąże się ze zwiększonym ryzykiem zakażenia,
podczas zakładania i obsługi cewnika zalecane jest dokładne przestrzeganie zasad postępowania
aseptycznego, aby uniknąć jakiegokolwiek zakażenia.
Zaleca się również kontrolowanie stężenia glukozy i elektrolitów w surowicy, osmolarności jak
również bilansu płynowego, równowagi kwasowo-zasadowej oraz wykonywanie enzymatycznych
prób wątrobowych (fosfataza alkaliczna, AspAT, AlAT).
W przypadku wystąpienia jakichkolwiek oznak lub jakiegokolwiek objawu reakcji anafilaktycznej
należy natychmiast przerwać infuzję.
Nie należy podawać leku Kabiven Peripheral jednocześnie z krwią w tym samym zestawie
infuzyjnym, ze względu na ryzyko wystąpienia pseudoaglutynacji.
Podobnie, jak w przypadku innych roztworów hipertonicznych do infuzji, podczas podawania do żył
obwodowych może wystąpić zakrzepowe zapalenie żył.
Sposób podawania
Podanie dożylne, infuzja do żyły obwodowej lub do żyły centralnej.
W celu zapewnienia pełnego żywienia pozajelitowego należy stosować dodatkowo - w zależności
od potrzeb pacjenta - pierwiastki śladowe, witaminy i elektrolity (uwzględniając elektrolity zawarte
w leku Kabiven Peripheral).
Szybkość infuzji
Maksymalna szybkość infuzji glukozy wynosi 0,25 g/kg mc./godzinę.
Dawka aminokwasów nie powinna być większa niż 0,1 g/kg mc./godzinę.
Dawka tłuszczów nie powinna być większa niż 0,15 g/kg mc./godzinę.
Szybkość infuzji nie powinna być większa niż 3,7 ml/kg mc./godzinę (co odpowiada 0,25 g glukozy,
0,09 g aminokwasów i 0,13 g tłuszczów na kg masy ciała). Zalecany czas trwania infuzji wynosi
od 12 do 24 godzin.
Zgodność
Dane dotyczące zgodności dostępne są dla leków Dipeptiven, Addamel N/Supliven, Glycophos,
Addiphos, Vitalipid N Adult/Infant i Soluvit N w określonych ilościach i w elektrolitach o określonym
stężeniu. Podczas dodawania elektrolitów, należy uwzględnić ich ilości już obecne w worku w celu
zaspokojenia potrzeb klinicznych pacjenta. Dostępne dane potwierdzają możliwość dodawania ww.
leków do aktywowanego worka zgodnie z poniższą tabelą:
Zakres zgodności: stabilny przez 8 dni, tj. 6 dni przechowywany w temperaturze 2-8 C, a następnie
48 godzin w temperaturze 20-25 C.
| Jednostka | Maksymalna całkowita zawartość | |||
| Wielkość worka Kabiven Peripheral | ml | 1440 | 1920 | 2400 |
| Dodatek | Objętość | |||
| Dipeptiven | ml |
|
|
|
| Supliven/Addamel N | ml |
|
|
|
| Soluvit N | fiolka |
|
|
|
| Vitalipid N Adult/Infant | ml |
|
|
|
| Limity elektrolitów1 | Ilość na worek | |||
| Sód | mmol | ≤ 216 | ≤ 288 | ≤ 360 |
| Potas | mmol | ≤ 216 | ≤ 288 | ≤ 360 |
| Wapń | mmol | ≤ 7,2 | ≤ 9,6 | ≤ 12 |
| Magnez | mmol | ≤ 7,2 | ≤ 9,6 | ≤ 12 |
| Fosforan nieorganiczny (Addiphos) lub Fosforan organiczny (Glycophos) | mmol | ≤ 22 | ≤ 29 | ≤ 36 |
Uwaga: tabela ta ma na celu wykazanie zgodności. Nie stanowi ona wytycznych dotyczących
dawkowania. Przed przepisaniem ww. leków należy zapoznać się z zatwierdzonymi drukami
informacyjnymi.
Informacje na temat zgodności z innymi dodatkami oraz czasów przechowywania różnych mieszanin
będą dostępne na życzenie.
Wszelkie dodatki należy łączyć z lekiem w warunkach aseptycznych.
Wszelkie niewykorzystane resztki leku lub jego odpady należy usunąć zgodnie z lokalnymi
przepisami.
Okres ważności i warunki przechowywania
Nie przechowywać w temperaturze powyżej 25°C. Przechowywać w worku zewnętrznym.
Nie zamrażać.
Okres ważności po zmieszaniu zawartości komór worka
Wykazano stabilność fizyczną i chemiczną zmieszanej zawartości worka trójkomorowego przez
48 godzin w temperaturze 20-25 C, włączając czas trwania infuzji. Z mikrobiologicznego punktu
widzenia lek należy zużyć natychmiast. W przeciwnym razie, za okres przechowywania podczas
użytkowania i za warunki przechowywania przed zastosowaniem odpowiada użytkownik. Okres ten
nie powinien zasadniczo przekraczać 24 godzin w temperaturze 2-8 C, chyba że mieszanie miało
miejsce w kontrolowanych i zwalidowanych warunkach aseptycznych.
Okres ważności po zmieszaniu z dodatkowymi substancjami
Po przerwaniu zabezpieczeń i zmieszaniu zawartości komór worka, można dodać inne składniki przez
port do podawania dodatkowych substancji.
Wykazano stabilność fizyko-chemiczną zmieszanej zawartości worka trójkomorowego
z dodatkowymi substancjami przez okres do 8 dni, tj. 6 dni w temperaturze 2-8 C, a następnie
48 godzin w temperaturze 20-25 C, włączając czas trwania infuzji. Z mikrobiologicznego punktu
widzenia lek należy zużyć natychmiast po dodaniu innych składników. W przeciwnym razie, za okres
przechowywania podczas użytkowania i za warunki przechowywania przed zastosowaniem
odpowiada użytkownik. Okres ten nie powinien zasadniczo przekraczać 24 godzin w temperaturze
2-8 C, chyba że mieszanie miało miejsce w kontrolowanych i zwalidowanych warunkach
aseptycznych.
Usuwanie pozostałości leku
Nie stosować jeśli opakowanie jest uszkodzone.
Stosować wyłącznie wtedy, gdy roztwory aminokwasów z elektrolitami i glukozy są przezroczyste,
bezbarwne do lekko żółtych, a emulsja tłuszczowa jest biała i jednorodna .Zawartość wszystkich
trzech komór należy zmieszać przed użyciem.
Po usunięciu zabezpieczeń należy natychmiast kilkakrotnie odwrócić worek tak, aby otrzymać przed
infuzją jednorodną mieszaninę.
Do jednorazowego użycia. Niezużyta pozostałość leku nie nadaje się do dalszego stosowania.
Wszelkie niewykorzystane resztki leku lub jego odpady należy usunąć zgodnie z lokalnymi
przepisami.
Kabiven Peripheral - Instrukcja przygotowania worka typu Biofine do użycia
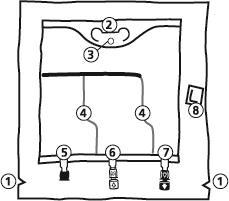
- 1. Nacięcie w worku zewnętrznym
- 2. Uchwyt worka
- 3. Otwór do zawieszenia worka
- 4. Zgrzewy oddzielające poszczególne komory worka
- 5. Port ślepy (używany tylko w produkcji)
- 6. Port do podawania dodatkowych substancji
- 7. Port infuzyjny
- 8. Pochłaniacz tlenu
1. Usuwanie worka zewnętrznego
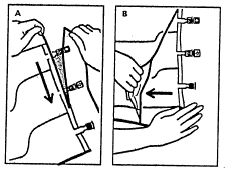
- Aby usunąć worek zewnętrzny, należy ułożyć go poziomo i zaczynając od nacięcia znajdującego się blisko portów rozrywać wzdłuż górnego brzegu (A).
- Następnie rozerwać worek zewnętrzny wzdłuż długiego brzegu, zdjąć go i wyrzucić razem z pochłaniaczem tlenu (B).
2. Mieszanie
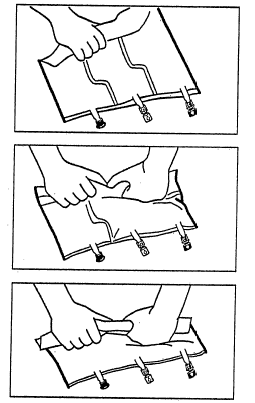
- Ułożyć worek na płaskiej powierzchni.
- Zaczynając od strony uchwytu mocno zrolować worek w kierunku portów, najpierw prawą ręką, a następnie wywierając stały ucisk lewą, aż do pęknięcia zgrzewów pionowych. Otwierają się one pod działaniem ciśnienia płynu. Zgrzewy można również otworzyć przed usunięciem worka zewnętrznego. Uwaga:płyn miesza się łatwo, mimo że zgrzew poziomy pozostaje nienaruszony.
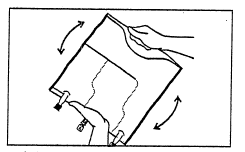
- Wymieszać zawartość trzech komór odwracając trzykrotnie worek, co powinno zapewnić dokładne wymieszanie składników.
3. Końcowe czynności przygotowawcze
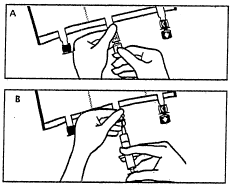
- Ponownie umieścić worek na płaskiej, równej powierzchni. Tuż przed podaniem dodatkowych substancji oderwać oznakowaną strzałką zatyczkę jednorazowego użytku zabezpieczającą biały port do podawania dodatkowych substancji (A). Uwaga:membrana portu służącego do podawania dodatkowych substancji jest jałowa.
- Przytrzymać podstawę portu służącego do podawania dodatkowych substancji. Wprowadzić igłę, wstrzyknąć dodatkowe substancje (o znanej zgodności) przez środek miejsca do wstrzykiwań (B).
- Wymieszać dokładnie zawartość worka po dodaniu każdego składnika obracając trzykrotnie worek po każdym dodaniu. Stosować strzykawki z igłami o średnicy 18 do 23 G i o długości maksymalnej 40 mm.
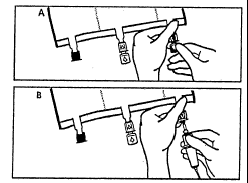
- Tuż przed podłączeniem zestawu do infuzji oderwać zatyczkę jednorazowego użytku zabezpieczającą niebieski port infuzyjny (A). Uwaga:membrana portu infuzyjnego jest jałowa.
- Stosować zestawy infuzyjne bez odpowietrznika lub zamknąć odpowietrznik.
- Przytrzymać podstawę portu infuzyjnego.
- Wkłuć ostrze aparatu do infuzji do portu infuzyjnego. Aby zapewnić dobre umocowanie ostrza, należy wkłuć całą jego długość. Uwaga:Wewnętrzna powierzchnia portu infuzyjnego jest jałowa.
4. Zawieszanie worka
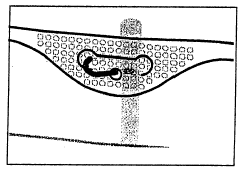
- Zawiesić worek wykorzystując otwór znajdujący się poniżej uchwytu.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyNie
- Producent
- ImporterFresenius Kabi AB
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Kabiven PeripheralPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez receptyPostać farmaceutyczna: Roztwór, -Substancja czynna: combinationsBez recepty
Odpowiedniki Kabiven Peripheral w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Kabiven Peripheral – Hiszpania
Odpowiednik Kabiven Peripheral – Ukraina
Lekarze online w sprawie Kabiven Peripheral
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Kabiven Peripheral – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














