
Fibrovein

Zapytaj lekarza o receptę na Fibrovein

Jak stosować Fibrovein
Ulotka dołączona do opakowania: informacja dla pacjenta
Fibrovein, 0,2%, 0,5%, 1% oraz 3%, roztwór do wstrzykiwań
Natrii tetradecylis sulfas
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona ważne informacje dla pacjenta.
Należy zachować tę ulotkę̨ , aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub pielęgniarki.
Jeśli u pacjenta wystąpią̨ jakiekolwiek poważne objawy niepożądane, w tym wszelkie objawy
niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce.
Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Fibrovein i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Fibrovein
- 3. Jak stosować lek Fibrovein
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Fibrovein
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Fibrovein i w jakim celu się go stosuje
Lek Fibrovein zawiera substancję czynną siarczan sodowy tetradecylu.
Lek Fibrovein dostępny w różnych stężeniach stosowany jest w leczeniu żylaków, dużych, średnich
i małych rozszerzonych naczynek i pajączków naczyniowych.
Substancja czynna leku należy do tzw. leków obliterujących. Leki obliterujące to środki chemiczne,
których wstrzyknięcie do zmienionej chorobowo żyły powoduje spuchnięcie jej wewnętrznej
powierzchni i sklejenie jej ścian. Przepływ krwi przez żyłę staje się niemożliwy i ostatecznie następuje
zwłóknienie tkanki bliznowatej. Po kilku tygodniach żyła z reguły przestaje być widoczna.
Lek Fibrovein przeznaczony jest wyłącznie do stosowania u osób dorosłych.
2. Informacje ważne przed zastosowaniem leku Fibrovein
Kiedy nie stosować leku Fibrovein:
- jeśli u pacjenta stwierdzono uczulenie na siarczan sodowy tetradecylu albo na którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6) lub jeśli pacjent ma chorobę uczuleniową;
- jeśli pacjent nie może chodzić z dowolnej przyczyny lub jest obłożnie chory;
- jeśli u pacjenta występuje ryzyko powstania zakrzepów krwi w układzie żylnym z powodu:
- dziedzicznie uwarunkowanej choroby krwi np. trombofilia;
- stosowania hormonalnych leków antykoncepcyjnych lub hormonalnej terapii zastępczej;
- znacznej otyłości;
- palenia tytoniu;
- długotrwałego unieruchomienia;
- jeśli u pacjenta wystąpiły niedawno zakrzepy krwi w żyłach powierzchownych lub głębokich albo w płucach;
- jeśli pacjent był niedawno operowany;
- jeśli u pacjenta występują skręcone żyły (żylaki kończyn dolnych) powodowane przez guzy znajdujące się w obrębie miednicy lub w jamie brzusznej, o ile guz nie został usunięty;
- jeśli u pacjenta występuje niekontrolowana choroba układowa taka jak cukrzyca, nadczynność tarczycy, astma, nieprawidłowości w obrazie krwi, zakażenie krwi lub niedawno występujące zaburzenia skóry lub trudności z oddychaniem;
- jeśli u pacjenta występuje obrzęk lub zaczerwienienie skóry, gorące lub wrażliwe w dotyku (zapalenie tkanki łącznej);
- jeśli u pacjenta występuje jakiekolwiek zakażenie;
- jeśli u pacjenta występuje postępujący nowotwór;
- jeśli u pacjenta stwierdzono nieprawidłowe zamykanie zastawek żył głębokich (niewydolność zastawek);
- jeśli u pacjenta występuje zator w tętnicy;
- jeśli u pacjenta stwierdzono ostre zapalenie żył kończyn dolnych (ostre zapalenie żył);
- jeśli u pacjenta mieć objawową dziurę w sercu (jedynie w przypadku zastosowania sklerosantu w postaci piany).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Fibrovein należy omówić to z lekarzem jeśli:
pacjent jest uczulony na dowolne pokarmy lub leki, lub jeśli występuje u niego jakakolwiek
inna alergia, przed przyjęciem leku powinien skonsultować się z lekarzem, aby można było
mu podać dawkę próbną na 24 godziny przed dalszym leczeniem;
u pacjenta występowały w przeszłości zakrzepy w żyłach powierzchownych lub
głębokich, albo w płucach;
u pacjenta mieć objawową dziurę w sercu (w przypadku zastosowania sklerosantu w postaci
piany).
u pacjentamieć objawową dziurę w sercu (w przypadku zastosowania sklerosantu w postaci
piany).
pacjent ma migreny;
jeśli pacjent ma zaburzenia żył w nogach, co wiąże się z długotrwałym stanem, powodującym
obrzęk tkanek ciała (obrzęk limfatyczny). Lek Fibrovein może nasilać miejscowy ból i stan
zapalny przez kilka dni lub kilka tygodni;
pacjent w przeszłości chorował na nadciśnienie płucne;
pacjent przebył przemijający napad niedokrwienia mózgu (TIA), udar lub poważny incydent
mózgowy;
u pacjenta zdiagnozowano chorobę tętnic lub żył (miażdżyca naczyń krwionośnych);
u pacjenta zdiagnozowano zakrzepy i zapalenie tętnic i żył dłoni i stóp (choroba Buergera);
pacjent ma trudności z oddychaniem, które są kontrolowane za pomocą leczenia (astma).
Lek Fibrovein może być podawany wyłącznie przez lekarza, a jeśli pozwalają na to wytyczne krajowe,
lek może być pod nadzorem lekarza podawany przez odpowiednio wykwalifikowany personel
medyczny, posiadające doświadcznie z zakresu anatomii układu żylnego i zaznajomiony z prawidłową
techniką nastrzykiwania. Przed wykonaniem wstrzyknięcia lekarz może przeprowadzić ocenę
wydolności zastawek żył pacjenta.
Przed przystąpieniem do zabiegu, lekarz zada pacjentowi kilka pytań o stan zdrowia i przekaże
informacje o potencjalnych działaniach niepożądanych związanych z zabiegiem.
Podczas leczenia
Lekarz w czasie i po zabiegu skleroterapii będzie prowadzić obserwację pacjenta pod kątem
nadwrażliwości (zaczerwienienia, świądu, kaszlu) lub objawów neurologicznych (zaburzenia widzenia,
migreny, mrowienie lub drętwienie).
Lekarz zaleci pacjentowi przyjście na wizytę kontrolną.
Dzieci i młodzież
Nie ustalono bezpieczeństwa stosowania i skuteczności leku Fibrovein u dzieci i młodzieży.
Lek Fibrovein a inne leki
Jeśli pacjentka przyjmuje hormonalne leki antykoncepcyjne (tzw. pigułki) lub stosuje hormonalną
terapię zastępczą, może wystąpić u niej ryzyko powstania zakrzepów w żyłach (patrz „Kiedy nie
stosować leku Fibrovein”). Należy powiedzieć o tym lekarzowi lub pielęgniarce.
Należy powiedzieć lekarzowi lub pielęgniarce o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować, również o tych, które
wydawane są̨ bez recepty.
Ciąża i karmienie piersią̨
Pacjentka musi powiedzieć lekarzowi jeśli:
jest w ciąży lub przypuszcza, że może być w ciąży;
planuje zajść w ciążę;
karmi piersią.
Bezpieczeństwo stosowania leku Fibrovein podczas ciąży nie zostało określone. Leku Fibrovein nie
należy stosować u kobiet w ciąży, jeżeli nie jest to zdecydowanie niezbędne. Lekarz zadecyduje, czy
stosowanie leku Fibrovein jest odpowiednie dla pacjenta.
Nie wiadomo czy Fibrovein przenika do mleka kobiet karmiących piersią. Jeśli pacjentka karmi
piersią, lekarz zdecyduje, czy Fibrovein jest dla niej odpowiednim lekiem.
Prowadzenie pojazdów i obsługiwanie maszyn
Po zastosowaniu leku Fibrovein, w celu zmniejszenia ryzyka zapalenia i przebarwienia skóry lekarz
może zalecić odpowiednie bandażowanie nóg i (lub) noszenie pończoch uciskowych, które mogą
wpłynąć na zdolność do prowadzenia pojazdów.
Lek Fibrovein zawiera sód, potas i alkohol benzylowy
Ten lek zawiera:
mniej niż 1 mmol (23 mg) sodu na fiolkę/ampułkę, to znaczy lek uznaje się za „wolny od
sodu”.
mniej niż 1 mmol (39 mg) potasu na fiolkę/ampułkę, to znaczy lek uznaje się za „wolny od
potasu”.
40 mg alkoholu benzylowego w każdej 2 ml ampułce lub 100 mg alkoholu benzylowego
w każdej 5 ml fiolce, co odpowiada 20 mg/ml. Alkohol benzylowy może powodować reakcje
alergiczne. W przypadku ciąży, karmienia piersią lub choroby wątroby lub nerek należy
poradzić się lekarza lub farmaceuty. Dzieje się tak dlatego, że w organizmie mogą gromadzić
się duże ilości alkoholu benzylowego, co może powodować działania niepożądane
(tzw. „kwasicę metaboliczną”).
3. Jak stosować lek Fibrovein
Nie wolnopodejmować prób samodzielnego wstrzykiwania leku Fibrovein. Leczenie powinien zawsze
prowadzić doświadczony lekarz, przeszkolony w zakresie prawidłowych technik wykonywania
wstrzykiwań.
Leczenie polega na bardzo ostrożnym i powolnym wstrzykiwaniu leku przy użyciu jak najmniejszych
igieł do zmienionych chorobowo żył, co umożliwia usunięcie z nich krwi. Lek można zmieszać ręcznie
za pomocą dwóch strzykawek i kranika, aby stworzyć mieszankę z powietrzem i wytworzyć piankę,
która pomoże usunąć krew z większych żył. W takim przypadku lek musi zostać podany pacjentowi
przez lekarza przeszkolonego w zakresie prawidłowych technik wytwarzania i podawania leku
w postaci piany.
W przypadku leczenia niewidocznych żylaków kończyn dolnych i do skleroterapii pianą zabieg
powinien zostać wykonany pod kontrolą USG.
Lekarz zdecyduje, jakie stężenie leku Fibrovein użyć i które obszary leczyć. Zalecane dawki:
Osoby dorosłe i w wieku podeszłym
- od 0,1 ml do 2 ml leku Fibrovein na każde wstrzyknięcie. Lekarz maksymalnie może wstrzyknąć do 10 ml trzech mniejszych stężeń leku Fibrovein, ale nie więcej niż 4 ml w przypadku zastosowania największego stężenia.
Z uwagi na ograniczenia dotyczące maksymalnej dobowej dawki sklerosantu, może zaistnieć potrzeba
kilkukrotnego powtórzenia zabiegu.
Po zakończeniu leczenia lekiem Fibrovein należy stosować się do zaleceń lekarza. Lekarz może zalecić
odpowiednie bandażowanie nóg i (lub) noszenie pończoch uciskowych, aby zmniejszyć ryzyko
wystąpienia zapalenia i przebarwienia skóry.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Mogą wystąpić poważne działania niepożądane. Należy przerwać leczenie lekiem Fibrovein i natychmiast skontaktować się z lekarzem lub udać się do oddziału ratunkowego najbliższego szpitala, jeśli wystąpi którykolwiek z poniższych objawów:
Niezbyt często (mogą wystąpić do 1 na 100 osób)
- Zakrzepy krwi w żyłach głębokich (zakrzepica żył głębokich najprawdopodobniej spowodowana chorobą podstawową). Objawy obejmują ból, obrzęk i uczucie tkliwości w jednej nodze (zazwyczaj w łydce), silny ból w zmienionym chorobowo obszarze, zwiększone ucieplenie skóry w obszarze powstania zakrzepu lub zaczerwienienie skóry, szczególnie w tylnej części nogi poniżej kolana.
Rzadko (mogą wystąpić do 1 na 1000 osób)
- Miejscowa martwica tkanek skóry lub rzadziej nerwów. Objawy obejmują ból, zmianę zabarwienia skóry (zaczerwienienie), obrzęk lub gromadzenie się płynu, pęcherze na skórze (mogą być wypełnione bezbarwnym płynem lub krwią), ciemnoczerwony, purpurowy lub czarny kolor skóry, nieprawidłowe odczucia (mrowienie, kłucie, pieczenie), drętwienie lub utrata czucia
Bardzo rzadko (mogą wystąpić do 1 na 10 000 osób)
- Najpoważniejszym działaniem niepożądanym jest silna reakcja alergiczna (wstrząs anafilaktyczny), która może powodować trudności z oddychaniem lub gwałtowny spadek ciśnienia tętniczego, powodujący uczucie omdlenia lub utratę przytomności. Wstrząs anafilaktyczny występuje rzadko, ale może prowadzić do zgonu, dlatego w razie jego wystąpienia należy natychmiast podać pacjentowi odpowiednie leczenie.
- Zablokowanie tętnicy spowodowane zakrzepem, co może prowadzić do:
o
udaru lub przerwania dopływu krwi do mózgu lub oka (przejściowy atak niedokrwienny).
Objawy mogą obejmować osłabienie, drętwienie lub paraliż twarzy, ręki lub nogi,
zazwyczaj po jednej stronie ciała, niewyraźną lub zniekształconą mowę lub trudności
w zrozumieniu innych, ślepotę w jednym lub obu oczach lub podwójne widzenie.
o
zatoru płucnego. Objawy mogą obejmować nagłą duszność, nagły, ostry ból w klatce
piersiowej, który może nasilać się podczas głębokiego oddychania lub kaszlu, szybkiego
bicia serca lub przyspieszenie oddychania.
Aby zabezpieczyć pacjentów przed tym bardzo rzadkim działaniem niepożądanym, nie wolno
stosować tego leku u pacjentów, u których występuje zwiększone ryzyko powstawania
zakrzepów krwi w żyłach i tętnicach (ryzyko zakrzepicy).
- Niewydolność krążenia. Objawy mogą obejmować uczucie zmęczenia, zamroczenie, omdlenie, ból w klatce piersiowej, duszność, osłabienie, zawroty głowy, wymioty i kołatanie serca.
- Martwica tkanek w przypadku wstrzyknięcia do tętnicy. Objawy mogą się różnić w zależności od ilości wstrzykniętego leku, miejsca wstrzyknięcia i szybkości otrzymania pomocy medycznej. Mogą one obejmować zakres od bólu, ale bez długotrwałego uszkodzenia, do utraty dużych powierzchni tkanek, w tym stopy, co może prowadzić do wystąpienia konieczności amputacji kończyny .
Inne działania niepożądane, które mogą wystąpić obejmują:
Bardzo często (mogą wystąpić u więcej, niż u 1 na 10 osób):
- Zapalenie żył powierzchownych.
Często (mogą wystąpić do 1 na 10 osób)
- Ból lub pieczenie (krótkotrwałe w miejscu wstrzyknięcia);
- Pigmentacja skóry;
- Rozszerzenie podskórnych naczyń włosowatych w miejscu ostrzykiwanym (tzw. matting).
Niezbyt często (mogą wystąpić do 1 na 100 osób):
- Miejscowe reakcje alergiczne lub niealergiczne skóry np. zaczerwienie, świąd, wysypka lub obrzęk;
- Zaburzenia widzenia;
- Migrena.
Rzadko (mogą wystąpić do 1 na 1 000 osób):
- Kaszel, duszność, uczucie gniecenia/ucisku w klatce piersiowej;
- Pieczenie, mrowienie, kłucie lub świąd skóry;
- Ból głowy, uczucie omdlenia;
- Dezorientacja, zawroty głowy, utrata przytomności.
Bardzo rzadko (mogą wystąpić do 1 na 10 000 osób):
- Gorączka, uderzenia gorąca, czerwona swędząca skóra (pokrzywka);
- Nudności, wymioty, biegunka, uczucie opuchniętego języka lub zwiększonej objętości języka, suchość w jamie ustnej;
- Zapalenie żył.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Działania niepożądane można
zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych, Al. Jerozolimskie 181 C, 02-222 Warszawa, Tel.: +48 22 49 21 301, Fax: + 48 22 49 21
309, Strona internetowa : https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Fibrovein
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Brak specjalnych zaleceń dotyczących temperatury przechowywania leku.
- Nie zamrażać.
- Folki i ampułki należy przechowywać w opakowaniu zewnętrznym, w celu ochrony przed światłem.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku tekturowym po: „Termin ważności (EXP)”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Tylko do jednorazowego użytku. Zawartość opakowania należy zużyć bezpośrednio po otwarciu.
Wszelkie resztki niewykorzystanego produktu należy usunąć́.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpady. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Fibrovein
Substancją czynną leku jest sodu tetradecylu siarczan.
W przypadku stężenia 0,2%
Każdy ml roztworu do wstrzykiwań zawiera 2 mg sodu tetradecylu siarczanu.
Każda 5 ml fiolka zawiera 10 mg sodu tetradecylu siarczanu.
W przypadku stężenia 0,5%
Każdy ml roztworu do wstrzykiwań zawiera 5 mg sodu tetradecylu siarczanu.
Każda 2 ml ampułka zawiera 10 mg sodu tetradecylu siarczanu.
W przypadku stężenia 1%
Każdy ml roztworu do wstrzykiwań zawiera 10 mg sodu tetradecylu siarczanu.
Każda 2 ml ampułka zawiera 20 mg sodu tetradecylu siarczanu.
W przypadku stężenia 3%
Każdy ml roztworu do wstrzykiwań zawiera 30 mg sodu tetradecylu siarczanu.
Każda 2 ml ampułka zawiera 60 mg sodu tetradecylu siarczanu.
Każda 5 ml fiolka zawiera 150 mg sodu tetradecylu siarczanu.
Pozostałe składniki leku to: alkohol benzylowy (20 mg/ml), disodu fosforan dwunastowodny, potasu
diwodorofosforan, woda do wstrzykiwań, sodu wodorotlenek (do regulacji pH). Patrz punkt 2 „Lek
Fibrovein zawiera sód i potas”.
Jak wygląda lek Fibrovein i co zawiera opakowanie
Lek Fibrovein to roztwór do wstrzykiwań zawarty w szklanych ampułkach lub fiolkach. Roztwór jest
przejrzysty, bezbarwny, jałowy, bez widocznych cząstek stałych.
Fibrovein, 0,2%: opakowanie zawiera 2, 5 lub 10 fiolek po 5 ml.
Fibrovein, 0,5%: opakowanie zawiera 5 ampułek po 2 ml.
Fibrovein, 1%: opakowanie zawiera 5 ampułek po 2 ml.
Fibrovein, 3%: opakowanie zawiera 5 ampułek po 2 ml lub 2, 5 lub 10 fiolek po 5 ml.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i Wytwórca:
Podmiot odpowiedzialny:
STD Pharmaceutical (Ireland) Limited
Block 1, Blanchardstown Corporate Park, Ballycoolen Road, Blanchardstown, Dublin 15
D15 AKK1, Irlandia
+353 1588 6916
Wytwórca:
Medipha Sante
Les Fjords-Immeuble Oslo
19 Avenue de Norvege
91953 Courtaboeuf CEDEX
Francja
Chemische Fabrik Kreussler & Co. GmbH
Rheingaustrasse 87-93
65203 Wiesbaden,
Niemcy
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Fibrovein
Bułgaria, Republika Czeska, Francja, Niemcy,
Irlandia, Holandia, Polska, Rumunia
Austria, Hiszpania
Veinfibro
Data ostatniej aktualizacji ulotki:05/2024
Inne źródła informacji:
Szczegółowa informacja o tym leku jest dostępna na stronie internetowej Urzędu Rejestracji
Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
www.urpl.gov.pl
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Fibrovein, 0,2%, roztwór do wstrzykiwań
Fibrovein, 0,5%, roztwór do wstrzykiwań
Fibrovein, 1%, roztwór do wstrzykiwań
Fibrovein, 3%, roztwór do wstrzykiwań
Dodatkowe informacje dotyczące niniejszego produktu znajdują się w Charakterystyce Produktu
Leczniczego (ChPL).
Dawkowanie i sposób podawania
Dawkowanie
Produkt leczniczy Fibrovein przeznaczony jest wyłącznie do podawania dożylnego. W zależności od
rozmiaru i ciężkości zmian żylnych wymagane jest zastosowanie innych stężeń. Pajączki naczyniowe
należy leczyć tylko 0,2% stężeniem, a żylaki siatkowe 0,5%. Stężenie 1% najkorzystniej działa na małe
i średnie żylaki, natomiast 3% na większe zmiany żylne. Rozmiar niewidocznych żylaków należy
ustalić pod kontrolą USG.
Sklerosant należy podawać dożylnie w małych równych porcjach do miejsc wzdłuż przebiegu
zmienionej chorobowo żyły. Fibrovein o stężeniu 0,2% i 0,5% należy podawać w postaci płynu.
Fibrovein o stężeniu 1% i 3% można podawać w postaci postaci płynnego sklerosantu lub mieszanki
sklerosantu z powietrzem (postać pianki) zgodnie z opisem podanym w poniższej tabeli. Celem zabiegu
jest uzyskanie optymalnego zniszczenia ścianek naczynia po zastosowaniu sklerosantu o minimalnym
skutecznym stężeniu potrzebnym do efektywnego leczenia. Zbyt wysokie stężenie produktu
leczniczego może prowadzić do pojawienia się martwicy tkanek lub innych powikłań.
Dorośli
| Stężenie | Standardowa dawka do wstrzykiwania dożylnego w wyznaczonych miejscach na zabieg | Maksymalna całkowita dawka do wstrzyknięcia na zabieg | ||
| Płyn | Pianka* | Płyn | Pianka* | |
| Fibrovein, 0,2% i 0,5% | od 0,1 do 1,0 ml | Nie dotyczy | 10 ml | Nie dotyczy |
| Fibrovein, 1% | od 0,1 do 1,0 ml | od 0,5 do 2,0 ml | 10 ml | 16 ml |
| Fibrovein, 3% | od 0,5 do 2,0 ml | od 0,5 do 2,0 ml | 4 ml | 16 ml |
*Suma objętości płynu i powietrza
W przypadkach, gdy wskazana jest szczególna ostrożność, zaleca się wykonanie próby uczuleniowej,
podając pacjentowi od 0,25 do 0,5 ml produktu leczniczego Fibrovein i obserwowanie pacjenta przez
kilka godzin, a następnie podanie mu drugiej lub większej dawki.
Zabieg często wymaga powtórzenia (średnio pacjent potrzebuje 2 do 4 dodatkowych zabiegów)
z powodu ograniczonej dawki, którą można zastosować podczas jednego zabiegu. Aby chronić pacjenta
przed reakcją alergiczną, na początku każdego zabiegu zaleca się podanie niewielkiej dawki próbnej
produktu leczniczego Fibrovein.
Fibrovein, 1% i 3% roztwór do wstrzykiwań
W przypadku podania sklerosantu w postaci pianki
Piankę przeznaczoną do leczenia większych żył można przygotować z użyciem produktu leczniczego
Fibrovein o stężeniu 1% i 3%. Piankę należy przygotować tuż przed jej podaniem. Musi być ona
podana pacjentowi przez lekarza odpowiednio przeszkolonego w zakresie prawidłowych technik
wytwarzania i podawania produktu leczniczego w postaci piany. Najlepiej, jeśli zabieg skleroterapii
pianą zostanie wykonany pod kontrolą USG.
Fibrovein, 0,2% roztwór do wstrzykiwań
W przypadku pajączków naczyniowych do wstrzykiwania należy użyć jak najmniejszych igieł
(np. 30 G) i wstrzykiwać produkt leczniczy powoli, aby umożliwić usunięcie krwi z leczonych naczyń
żylnych. Do leczenia pajączków naczyniowych można również użyć techniki polegającej na
dodatkowym podaniu powietrza, tzw. air-block.
Osoby w podeszłym wieku
Nie ma specjalnych zaleceń dotyczących dawkowania.
Dzieci i młodzież
Nie ustalono bezpieczeństwa stosowania i skuteczności produktu leczniczego produktu leczniczego
Fibrovein u dzieci i młodzieży. Brak danych.
Sposób podawania
Poniżej znajdują się instrukcje dotyczące przygotowania pianki. Przedstawiona metoda przygotowania
pianki to technika Tessariego. Można również użyć innych technik (np. DSS, Easyfoam, Sterivein).
Podczas przygotowania leku Fibrovein do podania należy zachować rygorystyczne warunki aseptyczne.
Lek Fibrovein przeznaczony jest do jednorazowego użytku i stosowania pozajelitowego Po otwarciu
fiolki lub ampułki produkt należy natychmiast zużyć, a niewykorzystany roztwór usunąć.
Przed użyciem należy przeprowadzić kontrolę wzrokową pod kątem obecności cząstek stałych. Jeśli
roztwór zawiera cząstki stałe, nie należy go stosować.
Najlepiej, jeśli zabieg skleroterapii pianą zostanie wykonany pod kontrolą USG. W takim przypadku
produkt musi zostać podany przez lekarza odpowiednio przeszkolonego w zakresie prawidłowych
technik wytwarzania i podawania leku w postaci piany.
Niezgodności farmaceutyczne
Tego produktu leczniczego nie należy mieszać z heparyną.
Nie mieszać produktu leczniczego z innymi produktami leczniczymi, ponieważ nie wykonano badań
dotyczących zgodności.
Specjalne ostrzeżenia i środki ostrożności
Lek Fibrovein powinien być podawany wyłącznie przez lekarza, a jeśli pozwalają na to wytyczne
krajowe, produkt może pod nadzorem lekarza podawać odpowiednio wykwalifikowany personel
medyczny, który posiada doświadczenie w zakresie anatomii układu żylnego, diagnostyce i leczeniu
chorób układu żylnego oraz zna prawidłową technikę nastrzykiwania.
Zgłaszano również wystąpienie reakcji alergicznych, w tym wstrząsu anafilaktycznego, dlatego lekarz
podający ten produkt powinien być przygotowany do zastosowania leczenia przeciwwstrząsowego.
Podczas zabiegu lekarz musi mieć bezpośredni dostęp do ratunkowego sprzętu reanimacyjnego.
Ze względu na szczególną ostrożność, pacjent powinien być leczony w szpitalu.
W przypadku wynaczynienia mogą wystąpić poważne, miejscowe działania niepożądane, łącznie
z martwicą tkanek, dlatego należy zachować szczególną ostrożność podczas wkłuwania igły
i wstrzykiwać minimalną skuteczną dawkę w każdym nastrzykiwanym miejscu. Roztwór należy
wstrzykiwać powoli.
Należy zachować szczególną ostrożność , aby nie wstrzyknąć roztworu do tętnicy, ponieważ może
powodować to martwicę tkanek, mogącą prowadzić do wystąpienia konieczności amputacji kończyny.
Należy zachować szczególną ostrożność przy wykonywaniu wstrzyknięć w stopę oraz powyżej i pod
kostką ( malleolus) z uwagi na ryzyko dla jednej z tętnic. W leczeniu żył o mniejszej powierzchni należy
zastosować ucisk, ponieważ prawdopodobieństwo pigmentacji może być większe, jeśli nastąpi
wynaczynienie krwi w miejscu wstrzyknięcia.
Wytwarzanie pianki i przygotowanie do wstrzyknięcia
Zalecenia ogólne
Jakość pianki zależy od określonych warunków:
Stężenia produktu: Piankę można przygotować wyłącznie z użyciem sodu tetradecylu siarczanu
o stężeniu od 1% do 3%.
Proporcji płynu do powietrza: Zwykle stosunek ten wynosi 1 objętość cieczy na 3 do 4 objętości
powietrza.
Wielokrotność przepompowań mieszkanki z jednej do drugiej strzykawki: Lekarz powinien
zastosować się do wielokrotności przepompowań określonych dla każdej techniki.
Konsystencja makroskopowa pianki: Przed podaniem pianki należy skontrolować jej jakość poza
strzykawką. Pianka powinna być jednolita, miękka i spójna bez widocznych dużych pęcherzyków.
Jeśli pianka zawiera duże pęcherzyki, należy ją wyrzucić i przygotować nową piankę.
Całkowity czas przygotowania pianki: Przygotowanie pianki powinno zająć około 10 sekund od
pierwszego do ostatniego przepompowania płynu z jednej strzykawki do drugiej.
Maksymalny czas pomiędzy przygotowaniem a wstrzyknięciem pianki: Piankę sklerosantu trzeba
zużyć w ciągu sześćdziesięciu sekund od jej przygotowania. Po upłynięciu sześćdziesięciu sekund
należy wyrzucić resztki niewykorzystanej pianki. W razie potrzeby należy przygotować więcej
pianki.
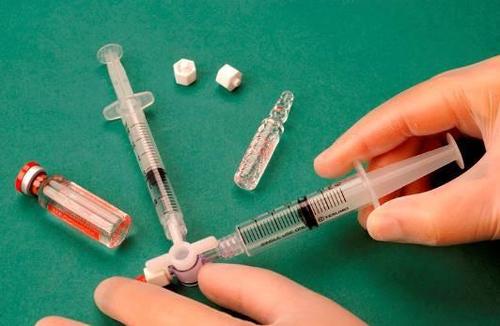
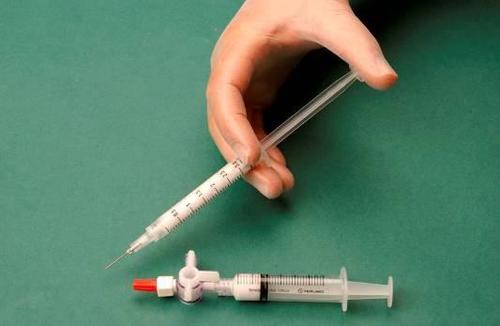
Wytwarzanie pianki (technika Tessariego)
Podczas wytwarzania pianki należy zachować rygorystyczne warunki aseptyczne.
Aby wytworzyć piankę do jednej jałowej strzykawki nabiera się 1 ml płynnego sklerosantu, a do
drugiej jałowej strzykawki 3 ml lub 4 ml jałowego powietrza. Powietrze zasysanie jest do strzykawki
przez 0,2 μm filtr sterylizacyjny, co gwarantuje jego jałowość. Strzykawki złączane są przy użyciu
jałowego kranika/łącznika trójdrożnego (rys. 1). Podczas wykonywania pianki zaleca się stosowanie
strzykawek typu Luer Lock oraz ochronę oczu. Podłączenie strzykawki ze złączem typu Luer slip do
kranika trójdrożnego pod ciśnieniem może zakończyć się niepowodzeniem co prowadzi do
niekontrolowanego wycieku produktu.
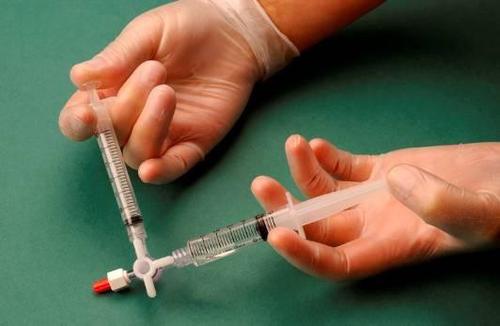
Po połączeniu strzykawek, mieszankę sklerosant/powietrze dynamicznie przepompowuje się około
20 razy z jednej strzykawki do drugiej przez łącznik trójdrożny aż do momentu uzyskania pianki
o jednolitej, gładkiej konsystencji (rys. 2 i 3).
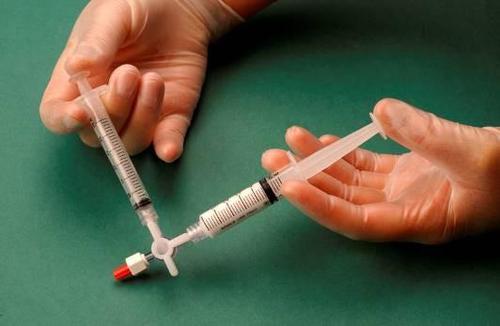
Strzykawka zawierająca piankę jest wyciągana z łącznika i przy jej użyciu natychmiast wykonuje się
wkłucie dożylne, przez które podaje się piankę do naczynia (rys. 4).
Piankę sklerosantu należy zużyć w ciągu sześćdziesięciu sekund od jej przygotowania. Po upłynięciu
sześćdziesięciu sekund należy wyrzucić resztki niewykorzystanej pianki. W razie potrzeby należy
przygotować więcej pianki.
Przed podaniem pianki należy skontrolować jej jakość. Pianka powinna mieć jednolitą konsystencję,
być białej barwy i nie zawierać widocznych dla gołego oka dużych pęcherzyków.
Substancje pomocnicze
Ten produkt leczniczy zawiera:
mniej niż 1 mmol (23 mg) sodu na fiolkę/ampułkę, to znaczy lek uznaje się za „wolny od
sodu”.
mniej niż 1 mmol (39 mg) potasu na fiolkę/ampułkę, to znaczy lek uznaje się za „wolny od
potasu”.
40 mg alkoholu benzylowego w każdej 2 ml ampułce lub 100 mg alkoholu benzylowego
w każdej 5 ml fiolce, co odpowiada 20 mg/ml. Alkohol benzylowy może powodować reakcje
alergiczne. Może powodować kwasicę metaboliczną w przypadku ciąży, karmienia piersią lub
choroby wątroby lub nerek.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyNie
- ImporterChemische Fabrik Kreussler Co.GmbH Medipha Sante
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki FibroveinPostać farmaceutyczna: Roztwór, 0,5% (5 mg/ml)Substancja czynna: sodium tetradecyl sulfateBez receptyPostać farmaceutyczna: Roztwór, 1% (10 mg/ml)Substancja czynna: sodium tetradecyl sulfateBez receptyPostać farmaceutyczna: Roztwór, 3% (30 mg/ml)Substancja czynna: sodium tetradecyl sulfateBez recepty
Odpowiedniki Fibrovein w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Fibrovein – Espanha
Lekarze online w sprawie Fibrovein
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Fibrovein – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














