
Jak stosować Divina
Ulotka dołączona do opakowania: informacja dla pacjenta
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Divina i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Divina
- 3. Jak stosować lek Divina
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Divina
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Divina i w jakim celu się go stosuje
Lek Divina jest cyklicznym, dwufazowym lekiem przeznaczonym do stosowania w hormonalnej terapii
zastępczej (HTZ). Lek ten zawiera dwa rodzaje żeńskich hormonów, estradiolu walerianian (estrogen)
i medroksyprogesteronu octan (progestagen).
Lek Divina jest stosowany w celu:
Łagodzenia objawów występujących po menopauzie
Podczas menopauzy zmniejsza się ilość estrogenu produkowanego przez organizm kobiety. Może to
skutkować objawami takimi jak uczucie gorąca na twarzy, szyi i klatce piersiowej („uderzenia gorąca”). Lek
Divina łagodzi te objawy, występujące po menopauzie. Lek Divina jest przepisywany tylko w przypadkach,
gdy objawy w znacznym stopniu wpływają niekorzystnie na życie codzienne pacjentki.
Zapobiegania osteoporozie
Po menopauzie u niektórych kobiet rozwija się kruchość kości (osteoporoza). Wszystkie dostępne
opcje należy przedyskutować z lekarzem prowadzącym. Jeśli pacjentka jest narażona na zwiększone ryzyko
złamań z powodu osteoporozy i inne leki nie są odpowiednie, można stosować lek Divina w celu
zapobiegania osteoporozie.
Doświadczenia w leczeniu pacjentek w wieku powyżej 65 lat są ograniczone.
2. Informacje ważne przed zastosowaniem leku Divina
Historia choroby oraz regularne badania kontrolne
Stosowanie hormonalnej terapii zastępczej (HTZ) wiąże się z ryzykiem, które należy uwzględnić
podejmując decyzję o rozpoczęciu lub kontynuowaniu terapii.
Przypadki stosowania terapii u kobiet z przedwczesną menopauzą (spowodowaną niewydolnością jajników
lub zabiegami chirurgicznymi) są nieliczne. W przypadku kobiet z przedwczesną menopauzą ryzyko
stosowania HTZ może być inne. Należy skonsultować się z lekarzem.
Przed rozpoczęciem (lub ponownym stosowaniem) HTZ lekarz przeprowadzi wywiad lekarski dotyczący
pacjentki i jej rodziny. Lekarz może też przeprowadzić badanie fizykalne, w tym badanie piersi i (lub)
narządów wewnętrznych, jeżeli zajdzie taka konieczność.
Po rozpoczęciu leczenia z użyciem leku Divina należy regularnie zgłaszać się na wizyty kontrolne (co
najmniej raz w roku). Podczas tych wizyt należy omówić z lekarzem zalety i ryzyko dalszego stosowania
leku Divina.
Należy regularnie badać piersi, zgodnie z zaleceniami lekarza.
Kiedy nie stosować leku Divina:
Jeżeli którykolwiek z poniższych punktów dotyczy pacjentki lub jeżeli pacjentka ma wątpliwości odnośnie
któregokolwiek z poniższych punktów, powinna skonsultować się z lekarzemprzed zastosowaniem leku
Divina.
Nie należy stosować leku Divina:
- jeśli pacjentka ma uczulenie na substancje czynnelub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- jeżeli pacjentka choruje lub chorowała w przeszłości na nowotwór złośliwy piersilub jeśli występuje jego podejrzenie,
- jeżeli pacjentka choruje na nowotwór złośliwy, wrażliwy na działanie estrogenów, jak na przykład nowotwór śluzówki macicy (endometrium) lub jeśli występuje jego podejrzenie,
- jeśli występuje krwawienie z pochwy o nieznanej przyczynie,
- jeżeli występuje nieleczone nadmierne pogrubienie błony śluzowej macicy(hiperplazja endometrium),
- jeżeli pacjentka ma lub miała zakrzep żylny(żylna choroba zakrzepowo-zatorowa) kończyn dolnych (zakrzepica żył głębokich) lub płuc (zator tętnicy płucnej),
- jeżeli pacjentka choruje na zaburzenie krzepnięcia krwi(takie jak niedobór białka C, białka S lub antytrombiny),
- jeżeli pacjentka ma lub w niedalekiej przeszłości miała zaburzenia zakrzepowo-zatorowe tętnic, na przykład zawał serca udarlub dusznicę bolesną,
- jeżeli pacjentka choruje lub chorowała w przeszłości na chorobę wątrobyi wyniki testów wątrobowych nie powróciły do wartości prawidłowych,
- jeżeli pacjentka choruje na rzadkie dziedziczne schorzenie krwi zwane porfirią.
Jeżeli którykolwiek z powyższych czynników wystąpi po raz pierwszy podczas stosowania leku Divina,
należy natychmiast zaprzestać stosowania leku i bezzwłocznie skontaktować się z lekarzem.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Divina należy omówić to z lekarzem lub farmaceutą.
Przed rozpoczęciem leczenia należy poinformować lekarza o zaistnieniu, obecnie lub w przeszłości,
któregokolwiek z wymienionych stanów, jako że mogą one nawracać lub nasilać się w okresie leczenia
z zastosowaniem leku Divina. W następujących przypadkach należy zwiększyć częstotliwość wizyt
kontrolnych:
- mięśniaki macicy (włókniaki macicy),
- rozrost błony śluzowej macicy poza jamą macicy (endometrioza) lub wcześniejsze przypadki nadmiernego rozrostu błony śluzowej macicy (hiperplazja endometrium),
- zwiększone ryzyko zaburzeń zakrzepowo-zatorowych (zobacz „Zakrzepy w żyłach (zakrzepica)”),
- zwiększone ryzyko nowotworu złośliwego, wrażliwego na estrogen (na przykład, gdy matka, siostra lub babka pacjentki chorowała na nowotwór złośliwy piersi),
- wysokie ciśnienie krwi,
- zaburzenia czynności wątroby, na przykład łagodny guz wątroby,
- cukrzyca ze zmianami naczyniowymi lub bez,
- kamica żółciowa,
- silne bóle głowy lub bóle głowy typu migrenowego,
- choroba układu odpornościowego, która wpływa na wiele narządów w organizmie (toczeń rumieniowaty układowy, SLE),
- padaczka,
- astma,
- choroba wpływająca na błonę bębenkową i słuch (otoskleroza),
- bardzo wysokie stężenie tłuszczów (triglicerydów) w organizmie pacjentki,
- zatrzymanie płynów z powodu zaburzeń czynności serca lub nerek,
- dziedziczny lub nabyty obrzęk naczynioruchowy (choroba charakteryzująca się występowaniem obrzęków najczęściej twarzy, kończyn i okolic stawów).
Należy przerwać stosowanie leku Divina i bezzwłocznie skontaktować się z lekarzem
Jeśli pacjentka podczas stosowania HTZ zauważy którykolwiek z poniższych objawów:
- którakolwiek z chorób wymienionych w punkcie „Kiedy nie stosować leku Divina”,
- zażółcenie skóry lub białek oczu (żółtaczka); mogą być to oznaki choroby wątroby,
- obrzęk twarzy, języka i (lub) gardła i (lub) trudności w połykaniu lub pokrzywka, jednocześnie z trudnościami w oddychaniu, mogące wskazywać na wystąpienie obrzęku naczynioruchowego,
- znaczne zwiększenie ciśnienia tętniczego krwi (możliwe objawy to bóle głowy, zmęczenie, zawroty głowy),
- bóle głowy typu migrenowego, które pojawiają się po raz pierwszy,
- jeżeli pacjentka zajdzie w ciążę,
- jeżeli zauważy oznaki powstawania zakrzepu, takie jak:
- bolesna opuchlizna i zaczerwienienie kończyn dolnych,
- gwałtowny ból w klatce piersiowej,
- trudności z oddychaniem. Więcej informacji dostępnych jest w punkcie „Zakrzepy w żyłach (zakrzepica)”.
Uwaga:Divina nie jest lekiem antykoncepcyjnym. Jeżeli od ostatniej miesiączki minęło mniej niż
12 miesięcy lub gdy pacjentka ma poniżej 50 lat, konieczne mogą być dodatkowe środki antykoncepcyjne,
aby zapobiec zajściu w ciążę. Należy poradzić się lekarza.
HTZ i nowotwory złośliwe
Nadmierne pogrubienie śluzówki macicy (hiperplazja endometrium) oraz nowotwór złośliwy błony śluzowej macicy (nowotwór endometrium)
Stosowanie wyłącznie estrogenowej HTZ zwiększa ryzyko nadmiernego pogrubienia błony śluzowej macicy
(hiperplazji endometrium) oraz nowotworu złośliwego śluzówki macicy (nowotworu endometrium).
Stosowanie estrogenów w skojarzeniu z progestagenem, przez co najmniej 12 dni na cykl lub ciągłe
stosowanie terapii skojarzonej, pozwala znacznie zmniejszyć to dodatkowe ryzyko.
W przypadku kobiet z zachowaną macicą, które nie stosują HTZ, średnio u 5 z 1000 w wieku od 50 do 65 lat
zdiagnozowany zostanie nowotwór endometrium.
W przypadku kobiet z zachowaną macicą, które stosują wyłącznie estrogenową HTZ, u 10 do 60 na
1000 kobiet zdiagnozowany zostanie nowotwór endometrium (tj. od 5 do 55 dodatkowych przypadków),
w zależności od dawki oraz okresu przyjmowania leku.
Nieregularne krwawienia
Mogą wystąpić nieregularne krwawienia lub plamienia w czasie pierwszych 3-6 miesięcy stosowania leku
Divina. Jeżeli nieregularne krwawienie:
- trwa dłużej niż przez pierwsze 6 miesięcy,
- pojawia się, gdy pacjentka stosuje lek Divina przez ponad 6 miesięcy,
- utrzymuje się po odstawieniu leku Divina, należy bezzwłocznie udać się do lekarza.
Rak piersi
Dane potwierdzają, że przyjmowanie hormonalnej terapii zastępczej (HTZ) w postaci skojarzenia estrogenu
i progestagenu lub samego estrogenu zwiększa ryzyko wystąpienia raka piersi. Dodatkowe ryzyko zależy od
tego, jak długo pacjentka stosuje HTZ. To dodatkowe ryzyko ujawnia się po 3 latach stosowania HTZ. Po
zakończeniu HTZ dodatkowe ryzyko będzie się z czasem zmniejszać, ale ryzyko może się utrzymywać
przez 10 lat lub dłużej, jeśli HTZ trwała ponad 5 lat.
Porównanie
W przypadku kobiet w wieku od 50 do 54 lat, które nie stosują HTZ, rak piersi zostanie rozpoznany
u średnio 13 do 17 na 1000 kobiet w okresie 5 lat.
W przypadku kobiet w wieku 50 lat, które rozpoczną pięcioletnią estrogenową HTZ, liczba zachorowań
wyniesie 16–17 na 1000 pacjentek (tj. dodatkowe 0 do 3 przypadków).
W przypadku kobiet w wieku od 50 lat, które rozpoczną pięcioletnią estrogenowo-progestagenową HTZ,
liczba zachorowań wyniesie 21 na 1000 pacjentek (tj. dodatkowe 4 do 8 przypadków).
W przypadku kobiet w wieku od 50 do 59 lat, które nie stosują HTZ, rak piersi zostanie rozpoznany
u średnio 27 na 1000 kobiet w okresie 10 lat.
W przypadku kobiet w wieku 50 lat, które rozpoczną 10-letnią estrogenową HTZ, liczba zachorowań
wyniesie 34 na 1000 pacjentek (tj. dodatkowe 7 przypadków).
W przypadku kobiet w wieku 50 lat, które rozpoczną 10-letnią estrogenowo-progestagenową HTZ, liczba
zachorowań wyniesie 48 na 1000 pacjentek (tj. dodatkowe 21 przypadków).
Należy regularnie badać piersi.Należy skontaktować się z lekarzem, jeżeli pojawią się zmiany takie jak:
- zmarszczenia skóry,
- zmiany w obrębie sutka,
- wszelkie widoczne lub wyczuwalne zgrubienia.
Dodatkowo, zaleca się udział w oferowanych programach przesiewowych badań mammograficznych.
Ważne jest, aby w przypadku przesiewowej mammografii poinformować fachowy personel medyczny,
wykonujący badanie, o stosowaniu HTZ, ponieważ ten lek może powodować zwiększenie radiologicznej
gęstości piersi, co może wpływać na wynik mammografii. W miejscach o zwiększonej gęstości
mammografia może nie wykazać wszystkich guzków.
Nowotwór jajników
Nowotwór jajników występuje rzadko - znacznie rzadziej, niż nowotwór piersi. Stosowanie HTZ
obejmującej tylko estrogeny lub skojarzenie estrogenów i progestagenów wiąże się z nieznacznie
zwiększonym ryzykiem nowotworu jajnika.
Ryzyko nowotworu jajnika zależy od wieku. Na przykład u kobiet w wieku 50-54 lat, które nie stosują HTZ,
nowotwór jajnika zostanie rozpoznany w okresie 5 lat u około 2 na 2 000 kobiet. U kobiet, które
przyjmowały HTZ przez 5 lat, wystąpi u około 3 kobiet na 2 000 pacjentek korzystających z terapii
(tzn. około 1 przypadek więcej).
Wpływ HTZ na serce i krążenie
Zakrzepy w żyłach (zakrzepica)
Ryzyko rozwinięcia żylnej choroby zakrzepowo-zatorowejjest ok. 1,3-3 krotnie większe w przypadku
kobiet stosujących HTZ niż osób, które z niej nie korzystają, zwłaszcza w pierwszym roku terapii.
Zakrzepy mogą mieć poważne skutki i jeśli skrzep dostanie się do płuc, może spowodować ból klatki
piersiowej, duszność, omdlenie lub nawet śmierć.
Prawdopodobieństwo powstawania zakrzepów w żyłach zwiększa się z wiekiem i w zależności od
występowania następujących czynników. Należy poinformować lekarza, jeżeli ma miejsce którakolwiek
z poniższych sytuacji:
- pacjentka nie może chodzić przez dłuższy czas z powodu poważnego zabiegu chirurgicznego, urazu lub choroby (zobacz również punkt 3 „Jeżeli potrzebujesz operacji”),
- pacjentka jest otyła (WMC >30 kg/m ),
- pacjentka ma zaburzenia krzepnięcia krwi, wymagające długoterminowego leczenia z wykorzystaniem leku przeciwzakrzepowego,
- jeżeli którykolwiek z bliskich krewnych miał zakrzep w kończynie dolnej, płucu lub innym narządzie,
- pacjentka miała rozległy zabieg chirurgiczny,
- pacjentka choruje na toczeń rumieniowaty układowy,
- pacjentka ma nowotwór,
- jeśli pacjentka jest w ciąży lub w okresie poporodowym.
Objawy zakrzepu można znaleźć w punkcie „Należy przerwać stosowanie leku Divina i bezzwłocznie
skontaktować się z lekarzem”.
Porównanie
W przypadku kobiet w wieku od 50 do 59 lat, które nie stosują HTZ, w ciągu 5 lat średnio u 4 do 7 na 1000
prawdopodobnie wystąpi zakrzep żylny.
Spośród kobiet w wieku od 50 do 59 lat, które stosowały złożoną estrogenowo-progestagenową HTZ przez
ponad 5 lat, w 9 do 12 przypadkach na 1000 wystąpi zakrzep żylny (tzn. o 5 przypadków więcej).
Choroba serca (zawał mięśnia sercowego)
Brak jest dowodów naukowych potwierdzających, że HTZ może zapobiegać zawałom serca.
Kobiety w wieku powyżej 60 lat, które stosują złożoną estrogenowo-progestagenową HTZ, są nieznacznie
bardziej narażone na choroby serca niż kobiety, które nie korzystają z HTZ.
Udar niedokrwienny mózgu
Ryzyko wystąpienia udaru niedokrwiennego mózgu jest ok. 1,5-krotnie większe u osób stosujących HTZ niż
u tych, które z niej nie korzystają. Liczba dodatkowych przypadków udaru mózgu spowodowanego
stosowaniem HTZ zwiększa się z wiekiem.
Porównanie
W przypadku kobiet w wieku od 50 do 59 lat, które nie stosują HTZ, średnio u 8 na 1000 w ciągu 5 lat
prawdopodobnie wystąpi udar mózgu. U kobiet w wieku 50-59 lat, które stosują HTZ, wystąpi 11 takich
przypadków na 1000 pacjentek, w ciągu 5 lat (tzn. o 3 przypadki więcej).
Inne stany chorobowe
- HTZ nie zapobiega utracie funkcji poznawczych. Istnieją dowody na zwiększone ryzyko otępienia u kobiet, które rozpoczęły HTZ w wieku powyżej 65 lat. Należy poradzić się lekarza.
- Estrogeny mogą powodować zatrzymywanie płynów, szczególnie u pacjentek z zaburzeniami czynności serca bądź nerek.
- HTZ może wpływać na wyniki niektórych badań endokrynologicznych oraz testów czynności wątroby. Należy poinformować lekarza o zażywaniu leku Divina przed wykonaniem tego typu badań.
- Pacjentka powinna poinformować lekarza, jeśli wie, że ma wysokie stężenie triglicerydów we krwi. W bardzo rzadkich przypadkach zaobserwowano, że istotne zwiększenie stężenia triglicerydów we krwi podczas terapii estrogenami może prowadzić do zapalenia trzustki.
- Lek Divina nie zapobiega ciąży. Dlatego nie należy go stosować jako środka antykoncepcyjnego.
Lek Divina a inne leki
Niektóre leki mogą zakłócać działanie leku Divina. Może to prowadzić do nieregularnych krwawień. Odnosi
się to do następujących leków:
- leków stosowanych w leczeniu padaczki(jak np. fenobarbital, fenytoina i karbamazepina),
- leków stosowanych w leczeniu gruźlicy(jak np. ryfampicyna, ryfabutyna),
- leków stosowanych w leczeniu infekcji HIV wirusem zapalenia wątroby typu C
- (tzw. inhibitory proteazy i nienukleozydowe inhibitory odwrotnej transkryptazy (np. newirapina, efawirenz, rytonawir i nelfinawir),
- leków ziołowych zawierających ziele dziurawca zwyczajnego ( Hypericum perforatum).
Hormonalna terapia zastępcza z estrogenem może wpływać na to, jak działają inne leki. Odnosi się to do
następujących leków:
- leku stosowanego w leczeniu padaczki- lamotryginy, gdyż może to zwiększyć ryzyko drgawek.
- leków stosowanych w leczeniu zapalenia wątroby typu C (HCV) (takich jak schemat leczenia skojarzonego za pomocą ombitaswiru/parytaprewiru/rytonawiru z dazabuwirem lub bez dazabuwiru oraz schemat leczenia skojarzonego za pomocą glekaprewiru/pibrentaswiru), ponieważ mogą one powodować zwiększenie wartości wyników badań krwi określających czynność wątroby [zwiększenie
aktywności enzymu wątrobowego, aminotransferazy alaninowej (AlAT)] u kobiet stosujących złożone
hormonalne produkty antykoncepcyjne, zawierające etynyloestradiol. Nie wiadomo, czy podczas
jednoczesnego stosowania leku Divina z tymi schematami leczenia HCV może wystąpić zwiększenie
aktywności enzymu AlAT.
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych obecnie, ostatnio lub
potencjalnie w przyszłości, również o tych, które wydawane są bez recepty, o lekach ziołowych lub innych
produktach naturalnych. Lekarz udzieli pacjentce porady na ten temat.
Badania laboratoryjne
Jeżeli konieczne jest przeprowadzenie badania krwi, należy poinformować personel laboratorium
o stosowaniu leku Divina, ponieważ może on wpłynąć na wyniki niektórych badań.
Ciąża i karmienie piersią
Lek Divina jest przeznaczony do stosowania wyłącznie przez kobiety po menopauzie. W przypadku zajścia
w ciążę należy przerwać stosowanie leku Divina i skontaktować się z lekarzem.
Stosowanie leku Divina jest przeciwwskazane w okresie karmienia piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie stwierdzono wpływu leku na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Divina zawiera laktozę.
Jeśli stwierdzono wcześniej u pacjentki nietolerancję niektórych cukrów, pacjentka powinna skontaktować
się z lekarzem przed przyjęciem leku.
Jedna biała tabletka zawiera 86,6 mg laktozy, jedna niebieska tabletka zawiera 72,0 mg laktozy.
3. Jak stosować lek Divina
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy zwrócić się do
lekarza. Lekarz będzie starał się przepisać najmniejszą dawkę potrzebną do leczenia objawów, przez
możliwie najkrótszy okres. Jeżeli zdaniem pacjentki dawka jest zbyt duża lub zbyt mała, należy
poinformować o tym lekarza.
Lek Divina należy przyjmować zgodnie z informacjami zawartymi na opakowaniu kalendarzowym, jedna
tabletka na dobę w cyklach 21-dniowych bez przerwy w przyjmowaniu tabletek, po których następuje 7 dni
przerwy w przyjmowaniu tabletek. W okresie przerwy w przyjmowaniu tabletek u większości kobiet
występuje krwawienie z odstawienia podobne do miesiączki. Zaleca się, aby tabletkę zażywać wieczorem.
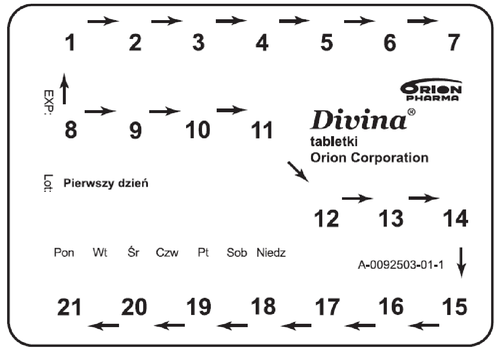
- 1. Na każdym blistrze znajduje się napis „Pierwszy dzień” wraz z zaznaczonymi kolejnymi dniami tygodnia. Należy zaznaczyć na blistrze (np. robiąc dziurkę) dzień tygodnia, w którym rozpoczyna się kurację. Dzięki temu można łatwo sprawdzić, czy tabletki były przyjmowane zgodnie z harmonogramem.
- 2. Pacjentki po menopauzie mogą zacząć leczenie od razu. Pacjentki, które w dalszym ciągu miesiączkują, powinny zacząć leczenie w piątym dniu cyklu miesiączkowego (w piątym dniu od rozpoczęcia miesiączki).
- 3. U kobiet niestosujących HTZ lub w przypadku kobiet przechodzących z innego złożonego leku do HTZ stosowanego w sposób ciągły, leczenie lekiem Divina można rozpocząć dowolnego, dogodnego dnia.
- 4. U kobiet przechodzących z cyklicznego lub ciągłego sekwencyjnego leczenia HTZ, leczenie należy rozpocząć w dniu następnym po zakończeniu wcześniejszego cyklu leczenia (trwającego 28 dni).
- 5. Tabletki należy brać w kolejności pokazanej na opakowaniu - najpierw białe, następnie niebieskie. Po tym czasie następuje siedem dni przerwy. W tym czasie u większości kobiet występuje krwawienie z odstawienia.
- 6. Następny cykl przyjmowania tabletek należy rozpocząć w tym samym dniu tygodnia, w którym rozpoczęty był pierwszy cykl. Jest możliwe, że niektóre kobiety nie będą miały krwawienia w okresie 7-dniowej przerwy w terapii lub krwawienie wystąpi tylko w niektórych cyklach.
W razie wystąpienia krwawień
W czasie pierwszych kilku miesięcy leczenia mogą wystąpić krwawienia i plamienia z dróg rodnych. Należy
skontaktować się z lekarzem w razie wystąpienia długotrwałych lub nieregularnych krwawień. Pomocnym
może być zapisywanie dat wystąpienia krwawień, ponieważ lekarz może zapytać pacjentkę o ich
występowanie podczas wizyt.
Jeśli pacjentka odnosi wrażenie, że działanie leku Divina jest zbyt mocne lub niewystarczające, nie powinna
zmieniać dawki lub zaprzestawać przyjmowania leku bez uprzedniej konsultacji z lekarzem.
Jeżeli konieczna jest operacja
Przed operacją należy poinformować chirurga o stosowaniu leku Divina. Możliwe, że konieczne będzie
zaprzestanie stosowania leku Divina na 4 do 6 tygodni przed operacją, w celu ograniczenia ryzyka
wystąpienia zakrzepu (patrz punkt 2 „Zakrzepy w żyłach”). Należy poradzić się lekarza odnośnie momentu,
od którego można ponownie rozpocząć stosowanie leku Divina.
Zastosowanie większej niż zalecana dawki leku Divina
Nie zaobserwowano poważnych objawów przedawkowania po spożyciu dużych dawek doustnych środków
stosowanych w HTZ. Przedawkowanie estrogenu może wywołać nudności, bóle głowy oraz krwawienie
z dróg rodnych. W razie przyjęcia większej niż zalecana dawki leku należy niezwłocznie zwrócić się do
lekarza lub farmaceuty.
Pominięcie zastosowania dawki leku Divina
Jeżeli nie zostanie przyjęta jedna tabletka, należy ją przyjąć następnego dnia rano, a wieczorem zażyć
tabletkę przeznaczoną na dany dzień. Jeśli pacjentka w ogóle nie zażyje tabletki, należy kontynuować
leczenie z następną tabletką. Może wtedy wystąpić niewielkie krwawienie w czasie cyklu.
W razie planowania dłuższego wyjazdu pacjentka powinna upewnić się, że dysponuje wystarczającym
zapasem tabletek.
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Divina
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do
lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Lek Divina może powodować działania niepożądane, szczególnie w pierwszych miesiącach leczenia. Są one
zwykle łagodne i ustępują w trakcie trwania leczenia.
Najczęstszymi działaniami niepożądanymi podczas leczenia lekiem Divina są ból głowy i bolesność piersi
(u 10% pacjentek).
Następujące choroby są zgłaszane częściej w przypadku kobiet stosujących HTZ niż tych, które z niej nie
korzystają:
- nowotwór piersi,
- nieprawidłowy rozrost lub nowotwór błony śluzowej macicy (hiperplazja endometrium lub nowotwór endometrium),
- nowotwór jajników,
- zakrzepy w żyłach kończyn dolnych lub płucach (zaburzenia zakrzepowo-zatorowe żył),
- choroby serca,
- udar mózgu,
- ryzyko otępienia, jeżeli stosowanie HTZ rozpoczęto w wieku powyżej 65 lat.
Więcej informacji dotyczących powyższych działań niepożądanych znajduje się w punkcie 2.
Często (mogą wystąpić do 1 na 10 osób)
- zwiększenie masy ciała,
- zmniejszenie masy ciała,
- bóle głowy, zawroty głowy,
- nudności, wymioty, kurcze żołądka, gazy jelitowe,
- upławy, choroby sromu i (lub) pochwy, zaburzenia cyklu menstruacyjnego,
- podrażnienie skóry, świąd w miejscu podania, ból, zwiększona intensywność pocenia,
- wrażliwość lub bolesność piersi,
- krwawienia lub plamienie, nieregularne miesiączki,
- depresja, nerwowość, letarg (bezwład, brak reakcji na większość bodźców),
- obrzęk,
- uderzenia gorąca.
Niezbyt często (mogą wystąpić do 1 na 100 osób)
- zmiany nastroju, zaburzenia popędu płciowego, niepokój, bezsenność, apatia, niestabilność emocjonalna, zaburzenia koncentracji, euforia, pobudzenie,
- migrena, drętwienie, drgawki,
- zaburzenia widzenia, suchość oczu,
- nadciśnienie, zapalenie żył powierzchniowych, plamica,
- duszność, katar,
- łagodny nowotwór piersi lub endometrium,
- zwiększenie apetytu, duże stężenie cholesterolu we krwi,
- kołatanie serca,
- zaparcia, niestrawność, biegunka, choroba odbytu,
- trądzik, łysienie, suchość skóry, choroby paznokci, guzki skórne, nadmierne owłosienie, rumień guzowaty, pokrzywka,
- dolegliwości stawów, skurcze mięśni,
- częstsze oddawanie moczu i (lub) zwiększona potrzeba oddawania moczu, nietrzymanie moczu, zapalenie pęcherza moczowego, przebarwienie moczu, krwiomocz,
- wrażliwość lub obrzęk piersi, nieprawidłowy rozrost błony śluzowej macicy, choroba macicy,
- zmęczenie, nieprawidłowe wyniki badań laboratoryjnych, osłabienie, gorączka, grypa, złe samopoczucie,
- nadwrażliwość.
Rzadko (mogą wystąpić do 1 na 1000 osób)
- żylna choroba zakrzepowo-zatorowa (np. zakrzepica żył głębokich kończyn dolnych lub żył miednicy i zatorowość płucna),
- zaburzenia czynności wątroby i przepływu żółci,
- wysypka,
- nietolerancja soczewek kontaktowych,
- bolesne miesiączkowanie, zespół napięcia przedmiesiączkowego.
Nieznana (częstość nie może być określona na podstawie dostępnych danych)
- mięśniaki macicy,
- nasilenie dziedzicznego lub nabytego obrzęku naczynioruchowego,
- zaburzenia krążenia mózgowego (epizody niedokrwienia mózgu),
- ból brzucha, wzdęcia,
- choroby wątroby powodujące zażółcenie skóry (żółtaczka cholestatyczna),
- wyprysk.
Następujące działania niepożądane zostały zaobserwowane w przypadku innych HTZ:
- zawał mięśnia sercowego,
- choroby pęcherzyka żółciowego,
- różne zaburzenia skóry i tkanki podskórnej:
- przebarwienia skóry, zwłaszcza na twarzy lub szyi, znane jako „plamy ciążowe” (ostuda),
- bolesne guzki skórne (rumień guzowaty),
- wysypka z rumieniowymi zmianami w kształcie pierścieni lub owrzodzeniami (rumień wielopostaciowy).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej
ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych
Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych
Al. Jerozolimskie 181C, 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Divina
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku po „Termin ważności
(EXP)”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w temperaturze powyżej 25°C.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Divina
Jedna biała tabletka zawiera:
- Substancją czynną leku jest: 2 mg estradiolu walerianianu.
- Pozostałe składniki to: laktoza jednowodna, skrobia kukurydziana, żelatyna, talk, magnezu stearynian.
Jedna niebieska tabletka zawiera:
- Substancjami czynnymi leku są: 2 mg estradiolu walerianianu i 10 mg medroksyprogesteronu octanu.
- Pozostałe składniki to: laktoza jednowodna, skrobia kukurydziana, indygotyna (E 132), żelatyna, poliwidon, talk, magnezu stearynian.
Jak wygląda lek Divina i co zawiera opakowanie
Wielkość opakowania
Blister zawiera 21 tabletek (11 białych + 10 niebieskich).
1 lub 3 blistry w tekturowym pudełku.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
CS 50070
Lys Lez Lannoy 59452
Francja
W celu uzyskania bardziej szczegółowych informacji dotyczących tego leku należy zwrócić się do
miejscowego przedstawiciela podmiotu odpowiedzialnego:
Orion Pharma Poland Sp. z o.o.
[email protected]
Data ostatniej aktualizacji ulotki:
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterDELPHARM LILLE S.A.S. Orion Corporation
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki DivinaPostać farmaceutyczna: Tabletki, 2 mg (białe), 2 mg + 0,5 mg (jasnobrązowe)Substancja czynna: norgestrel and estrogenProducent: Bayer AG Bayer Weimar GmbH und Co. KGWymaga receptyPostać farmaceutyczna: Tabletki, 1 mg (biała), 1 mg + 10 mg (szara)Substancja czynna: dydrogesterone and estrogenProducent: Abbott Biologicals B.V.Wymaga receptyPostać farmaceutyczna: Tabletki, 1 mg (białe), 1 mg + 10 mg (szare)Substancja czynna: dydrogesterone and estrogenWymaga recepty
Odpowiedniki Divina w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Divina – Hiszpania
Lekarze online w sprawie Divina
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Divina – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.






