
Cutaquig

Zapytaj lekarza o receptę na Cutaquig

Jak stosować Cutaquig
Ulotka dołączona do opakowania: Informacja dla użytkownika
CUTAQUIG 165 mg/mlroztwór do wstrzykiwań
Immunoglobulina ludzka normalna (SCIg)
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Cutaquig i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Cutaquig
- 3. Jak stosować lek Cutaquig
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Cutaquig
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Cutaquig i w jakim celu się go stosuje
Co to jest lek Cutaquig
Lek Cutaquig należy do klasy leków określanych jako „normalne ludzkie immunoglobuliny”.
Immunoglobuliny nazywa się też przeciwciałami; są to białka występujące we krwi zdrowych ludzi.
Przeciwciała stanowią część układu odpornościowego (naturalnego mechanizmu obronnego
organizmu) i pomagają organizmowi w zwalczaniu zakażeń (infekcji).
Jak działa lek Cutaquig
Lek Cutaquig zawiera immunoglobuliny, które zostały uzyskane z krwi zdrowych ludzi. Lek ten
działa dokładnie w ten sam sposób, co immunoglobuliny naturalnie obecne we krwi.
W jakim celu stosuje się lek Cutaquig
Lek Cutaquig stosuje się u pacjentów, którzy nie mają ilości przeciwciał wystarczających do
zwalczania zakażeń i tym samym często występują u nich zakażenia. Regularne podawanie
odpowiednich dawek leku Cutaquig może zwiększyć nieprawidłowo małe stężenie immunoglobulin
we krwi pacjenta do prawidłowego poziomu (terapia zastępcza).
Lek Cutaquig przepisuje się dorosłym i dzieciom (w wieku 0-18 lat) w następujących sytuacjach:
Leczenie pacjentów, którzy urodzili się ze zmniejszona zdolnością lub niezdolnością do wytwarzania
immunoglobulin (pierwotny niedobór odporności).
Pacjenci z nabytym niedoborem przeciwciał (wtórny niedobór odporności) z powodu określonych
chorób lub leczenia, u których występują ciężkie lub nawracające zakażenia.
2. Informacje ważne przed zastosowaniem leku Cutaquig
Kiedy NIE stosować leku Cutaquig:
- jeśli pacjent ma uczulenie na normalną ludzką immunoglobulinę lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
NIE wstrzykiwać leku Cutaquig do naczyń krwionośnych.
Ostrzeżenia i środki ostrożności:
Przed rozpoczęciem stosowania leku Cutaquig należy omówić to z lekarzem lub farmaceutą.
Pacjent może być uczulony (nadwrażliwy) na immunoglobuliny nawet nie wiedząc o tym.
Rzeczywiste reakcje alergiczne, tak jak nagły spadek ciśnienia krwi lub wstrząs anafilaktyczny
(gwałtowny spadek ciśnienia krwi w połączeniu z innymi objawami, takimi jak obrzęk gardła,
trudności z oddychaniem i wysypka skórna) zdarzają się rzadko, mogą jednak wystąpić, nawet jeśli
pacjent utrzymywał uprzednio ludzkie immunoglobuliny i dobrze je tolerował. Może do tego dojść w
szczególności w sytuacji, gdy we krwi pacjenta nie ma wystarczającej liczby immunoglobulin typu A
(niedobór IgA) i ma on przeciwciała przeciwko IgA.
- Przed leczeniem należy powiedzieć lekarzowi lub innemu członkowi personelu medycznego, jeśli pacjent ma niedobór immunoglobulin typu A (IgA). Lek Cutaquig zawiera minimalną ilość IgA, która może wywołać reakcję alergiczną. W takich rzadkich przypadkach mogą wystąpić reakcje alergiczne, jak nagły spadek ciśnienia krwi lub wstrząs (patrz także punkt 4). Objawy i oznaki takich rzadkich reakcji alergicznych są następujące:
- uczucie oszołomienia, zawroty głowy lub omdlenie,
- wysypka i swędzenie skóry, obrzęk jamy ustnej lub gardła, trudności z oddychaniem, świszczący oddech,
- nieprawidłowa częstość akcji serca, ból w klatce piersiowej, siny kolor warg lub palców dłoni i stóp,
- nieostre widzenie. Jeżeli podczas infuzji leku Cutaquig pacjent zauważy takie objawy, należy niezwłocznie powiedzieć o tym lekarzowi. Lekarz zdecyduje czy należy zmniejszyć szybkość infuzji, czy też całkiem ją przerwać.
- Należy poinformować lekarza, jeżeli pacjent miał w przeszłości chorobę serca lub naczyń krwionośnych, lub zakrzepy krwi lub jeśli był przez pewien czas unieruchomiony. Wiadomo, że takie okoliczności zwiększają ryzyko występowania zakrzepów krwi po zastosowaniu leku Cutaquig. Należy także powiedzieć lekarzowi o wszystkich lekach stosowanych aktualnie przez pacjenta, bowiem pewne leki, takie jak zawierające hormon estrogen (np. tabletki antykoncepcyjne), mogą zwiększać ryzyko wystąpienia zakrzepu krwi. Jeżeli u pacjenta po zastosowaniu leku Cutaquig wystąpią takie objawy lub oznaki, jak duszność, ból w klatce piersiowej, ból i obrzęk kończyny, czy osłabienie lub drętwienie jednej strony ciała należy niezwłocznie skontaktować się z lekarzem.
- Jeżeli u pacjenta po zastosowaniu leku Cutaquig wystąpią takie objawy lub oznaki, jak silny ból głowy, sztywność karku, senność, gorączka, światłowstręt, mdłości i wymioty należy skontaktować się z lekarzem. Mogą to być objawy aseptycznego zapalenia opon mózgowo- rdzeniowych. Lekarz zdecyduje, czy koniczne jest wykonanie dodatkowych testów i czy należy kontynuować stosowanie leku Cutaquig.
- Lek Cutaquig zawiera przeciwciała przeciw grupom krwi, które mogą spowodować zniszczenie czerwonych krwinek i tym samy anemię (zbyt mała liczba czerwonych krwinek).
Lekarz zmniejszy ryzyko wystąpienia możliwych powikłań, upewniając się:
- że pacjent nie jest uczulony na normalną ludzką immunoglobulinę. Na początku lek musi być podawany z małą szybkością infuzji. Należy ściśle przestrzegać zalecanych szybkości infuzji podanych w punkcie 3.
- że pacjent jest starannie monitorowany pod kątem jakichkolwiek objawów przez cały czas infuzji, zwłaszcza jeśli: o pacjent otrzymuje normalną ludzką immunoglobulinę po raz pierwszy, o pacjent zmienił właśnie inny lek na lek Cutaquig, o od poprzedniej infuzji upłynęło dużo czasu (ponad osiem tygodni).
W takich przypadkach zaleca się monitorowanie pacjenta podczas pierwszej infuzji i przez
godzinę po jej zakończeniu. Jeśli powyższe punkty nie dotyczą pacjenta, zaleca się obserwację
przez co najmniej 20 minut po podaniu leku.
Dzieci i młodzież
Wymienione ostrzeżenia i środki ostrożności dotyczą zarówno dorosłych, jak i dzieci.
Lek Cutaquig a inne leki
- Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które pacjent planuje stosować.
- Nie wolno mieszać z leku Cutaquig z żadnym innym lekiem.
- Przed szczepieniem należy powiedzieć lekarzowi wykonującemu szczepienie o leczeniu lekiem Cutaquig. Cutaquig (tak jak wszystkie inne leki zawierające normalną ludzką immunoglobulinę) może zakłócić działanie niektórych szczepionek zawierających żywe wirusy, takiej jak szczepionki przeciwko odrze, różyczce, śwince i ospie wietrznej. W związku z tym, po zastosowaniu leku Cutaquig pacjent może musieć odczekać do 3 miesięcy przed szczepieniem żywą atenuowaną szczepionką. W przypadku szczepienia przeciwko odrze takie upośledzenie skuteczności może utrzymywać się przez okres do jednego roku.
- Badanie stężenia glukozy we krwi Niektóre typy systemów stosowanych do oznaczania stężenia glukozy we krwi (tak zwane glukometry) błędnie rozpoznają maltozę zawartą w leku Cutaquig jako glukozę. To może prowadzić do błędnego zawyżania odczytów stężenia glukozy podczas infuzji oraz przez okres około 15 godzin po zakończeniu infuzji, a w konsekwencji do niewłaściwego zastosowania insuliny skutkującego zagrażającą życiu hipoglikemią (tj. obniżonym poziomem cukru we krwi). Także w przypadkach prawdziwej hipoglikemii może nie nastąpić leczenie z uwagi na fałszywie zmienione odczyty podwyższonego stężenia glukozy. Zatem podczas podawania leku Cutaquig lub innych produktów zawierających maltozę należy oznaczyć stężenie glukozy we krwi za pomocą systemu badania wykorzystującego metodę swoistą dla glukozy. Nie powinno się stosować systemów opartych na metodach wykorzystujących dehydrogenazę glukozową pirolochinolinochinonu (GDH-PQQ) lub oksydoreduktazę glukozową. Należy uważnie przeczytać informacje dotyczące systemu oznaczania stężenia glukozy, w tym pasków testowych, aby stwierdzić czy dany system jest odpowiedni do badania podczas jednoczesnego stosowania leków podawanych pozajelitowo, zawierających maltozę. W przypadku pojawienia się wątpliwości należy skontaktować się z lekarzem prowadzącym leczenie w celu ustalenia, czy dany system oznaczania stężenia glukozy nadaje się do badania podczas jednoczesnego stosowania leków podawanych pozajelitowo, zawierających maltozę.
Cutaquig z jedzeniem, piciem i alkoholem
Nie zaobserwowano żadnego wpływu.
Ciąża, karmienie piersią i wpływ na płodność
W ciąży i w okresie karmienia piersią lub gdy istnieje podejrzenie, że kobieta jest w ciąży, lub gdy
planuje ciążę, przed zastosowaniem tego leku należy poradzić się lekarza lub farmaceuty. Lek ten
powinien być stosowany w okresie ciąży lub karmienia piersią tylko po konsultacji z lekarzem lub
farmaceutą.
Nie przeprowadzono klinicznych badań leku Cutaquig u kobiet w okresie ciąży. Jednakże leki
zawierające immunoglobuliny są stosowane u kobiet w ciąży lub karmiących piersią od wielu lat i nie
zaobserwowano żadnych działań szkodliwych dla przebiegu ciąży ani dla płodu czy noworodka.
Jeżeli pacjentka karmi piersią i otrzymuje lek Cutaquig, immunoglobuliny zawarte w tym leku przejdą
również do mleka matki. Dzięki temu dziecko będzie chronione przed pewnymi zakażeniami.
Doświadczenie dotyczące stosowania immunoglobulin nie wskazuje na szkodliwy wpływ na
płodność.
Prowadzenie pojazdów i obsługiwanie maszyn
Pewne działania niepożądane związane z lekiem Cutaquig mogą upośledzić zdolność prowadzenia
pojazdów i obsługiwania maszyn. Pacjenci, u których podczas leczenia wystąpią działania
niepożądane, powinni poczekać na ich ustąpienie przed prowadzeniem pojazdu lub obsługiwaniem
maszyn.
Lek Cutaquig zawiera sód
Ten lek zawiera 33,1 mg sodu (główny składnik soli kuchennej) na fiolkę po 48 ml i 13,8 mg sodu na
fiolkę po 20 ml. Stanowi to odpowiednio 1,7% i 0,7% zalecanego maksymalnego dziennego spożycia
sodu w diecie przez dorosłych.
Informacje na temat pochodzenia leku Cutaquig
Lek Cutaquig otrzymywany jest z osocza ludzkiej krwi (jest to płynny składnik krwi). Gdy leki
wytwarzane są z ludzkiej krwi lub osocza, podejmowane są określone środki ostrożności, aby
zapobiec przenoszeniu zakażeń na pacjentów. Obejmują one:
- staranną selekcję dawców krwi i osocza, w celu wykluczenia dawców mogących być nosicielami zakażeń,
- badanie każdej donacji i puli zebranego osocza w celu wykrycia obecności wirusów/zakażeń,
- włączenie do procesu przetwarzania krwi lub osocza etapów mających na celu inaktywację lub usunięcie wirusów. Mimo tych środków ostrożności w przypadku podawania leków przygotowanych z ludzkiej krwi lub osocza nie można całkowicie wykluczyć możliwości przeniesienia zakażenia. Dotyczy to również nieznanych lub pojawiających się od niedawna wirusów lub innych rodzajów zakażeń.
Podejmowane środki są uważane za skuteczne wobec wirusów otoczkowych, takich jak wirus
ludzkiego niedoboru odporności (HIV - wirus powodujący AIDS), wirus zapalenia wątroby typu B i
wirus zapalenia wątroby typu C.
Podejmowane środki ostrożności mogą mieć ograniczoną skuteczność wobec wirusów
bezotoczkowych, takich jak wirus zapalenia wątroby typu A i parwowirus B19.
Nie stwierdzono związku produktów immunoglobulin z wirusowym zapaleniem wątroby typu A lub
zakażeniem parwowirusem B19, przypuszczalnie dlatego, że przeciwciała przeciwko tym zakażeniom
zawarte w tym produkcie mają działanie ochronne.
Zaleca się usilnie, aby w każdym przypadku podawania leku Cutaquig pacjentowi odnotować nazwę i
numer serii leku w celu udokumentowania użytej serii (patrz także Aneks I: Wytyczne dotyczące
podawania).
3. Jak stosować lek Cutaquig
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości
należy zwrócić się z do lekarza lub farmaceuty.
Lek Cutaquig musi być podawany w infuzji pod skórę (podanie podskórne).
Leczenie zostanie rozpoczęte przez lekarza prowadzącego pacjenta lub pielęgniarkę z doświadczeniem
w leczeniu pacjentów z osłabionym układem odpornościowym.
Gdy lekarz/pielęgniarka określi właściwą dawkę i szybkość infuzji dla pacjenta i gdy pacjent otrzyma
kilka pierwszych infuzji pod nadzorem, pacjent może otrzymać zgodę na samodzielne stosowanie
leczenia w domu lub na podawanie leczenia w domu przez przeszkolonego opiekuna. Lekarzem lub
pielęgniarka z doświadczeniem w prowadzeniu pacjentów stosujących leczenie domowe upewni się,
że pacjent lub jego opiekun otrzyma przeszkolenie i dokładne informacje na temat
- zasady prowadzenia infuzji w warunkach aseptycznych,
- stosowania urządzenia do infuzji (w razie potrzeby),
- prowadzenia dzienniczka leczenia,
- działań, jakie należy podjąć w razie wystąpienia poważnych działań niepożądanych (patrz również punkt 4). Gdy tylko pacjent będzie w stanie stosować leczenie samodzielnie, a podczas leczenia nie pojawią się żadne działania niepożądane, lekarz zezwoli pacjentowi na kontynuowanie leczenia w domu.
Dawkowanie
Dawkowanie i szybkość infuzji dla indywidualnego pacjenta zostaną ustalone przez lekarza, który
dostosuje dawkę do pacjenta biorąc pod uwagę masę ciała, leczenie otrzymywane uprzednio przez
pacjenta oraz jego reakcję na leczenie. Należy zawsze stosować się do instrukcji lekarza.
Terapia zastępcza w zespołach pierwotnego niedoboru odporności:
Lekarz określi, czy pacjent wymaga dawki nasycającej (dla dorosłych i dzieci) wynoszącej co
najmniej 1,2 do 3,0 ml/kg masy ciała podzielonej na kilka dni. Następnie pacjent będzie otrzymać lek
Cutaquig w regularnych odstępach czasu, od podawania codziennie do podawania co dwa tygodnie.
Dawka skumulowana podana w ciągu miesiąca wyniesie około 2,4 do 4,8 ml/kg masy ciała. Lekarz
lub pielęgniarka może skorygować dawkę w zależności od reakcji pacjenta na leczenie.
Terapia zastępcza we wtórnych niedoborach odporności:
Zalecana dawka produktu leczniczego Cutaquig to skumulowana dawka miesięczna wynosząca 1,2–
2,4 ml/kg podawana w równych odstępach czasu (około raz w tygodniu). Może istnieć konieczność
wstrzykiwania każdej dawki w inne miejsce. Lekarz może dostosować dawkę w zależności od
odpowiedzi na leczenie.
Nie wolno zmieniać dawki ani częstości podawania leku bez konsultacji ze swoim lekarzem. Jeśli
pacjent uzna, że powinien otrzymywać lek Cutaquig częściej lub rzadziej, należy porozmawiać ze
swoim lekarzem. Jeśli pacjent uzna, że pominął dawkę, powinien jak najszybciej porozmawiać o tym z
lekarzem.
Sposób i droga podania
Wybór miejsca (miejsc) infuzji:
Sugerowane obszary do podskórnej infuzji leku Cutaquig to brzuch, uda, górne części ramion oraz
obszar górnych części nóg/bioder. Można podawać infuzję w więcej niż jednym miejscu jednocześnie.
Nie ma ograniczeń liczby miejsc infuzji, ale poszczególne miejsca powinny być oddalone od siebie o
co najmniej 5 cm. Podczas każdego podawania należy zmieniać miejsca infuzji zgodnie z zaleceniem
lekarza lub pielęgniarki.
Objętość infuzji podawana w jedno miejsce jest różna, ale zaleca się podzielenie dużych objętości
infuzji (> 30 ml) i podanie ich w kilka różnych miejsc. U noworodków i dzieci miejsca infuzji można
zmienić po podaniu 5-15 ml.
Szybkość infuzji:
Lekarz określi odpowiednią dla pacjenta szybkość infuzji, biorąc pod uwagę indywidualną dawkę,
częstotliwość dawkowania i tolerancję produktu.
Zalecana początkowa szybkość infuzji wynosi 15 ml/godz./miejsce, jeśli pacjent nie był uprzednio
leczony SCIG. W przypadku pacjenta już leczonego SCIG i przechodzącego na lek Cutaquig zaleca
się stosowanie poprzednio stosowanej szybkości podawania w początkowych infuzjach. W kolejnych
infuzjach, jeśli lek jest dobrze tolerowany, szybkość podawania można stopniowo zwiększać
o ok. 10 ml/godz./miejsce co 2-4 tygodnie u dorosłych (≥40 kg) oraz maksymalnie do
10 ml/godz./miejsce co 4 tygodnie u dzieci i młodzieży (<40 kg).
Następnie, jeśli pacjent toleruje początkowe infuzje przy pełnej dawce na miejsce i maksymalnej
szybkości, można rozważyć zwiększenie szybkości kolejnych infuzji, aż do osiągnięcia maksymalnej
szybkości przepływu 67,5 ml/godz./miejsce u dorosłych (≥40 kg) i 25 ml/godz./miejsce u dzieci
i młodzieży (<40 kg).
Dokładna instrukcja stosowania podana jest niżej.
Lek Cutaquig jest przeznaczony wyłącznie do podawania podskórnego (pod skórę). Nie wstrzykiwać
leku do naczyń krwionośnych.
Lek Cutaquig może stosować w domu dopiero po otrzymaniu właściwych instrukcji i przeszkolenia
przez lekarza lub pielęgniarkę.
Podczas stosowania leku Cutaquig należy dokładnie przestrzegać każdego punktu wytycznych
dotyczących podawania zamieszczonych na końcu niniejszej ulotki (Aneks I) i stosować zasady
aseptyki (technikę jałową).
Stosować rękawiczki, jeżeli lekarz zalecił je nosić podczas przygotowywania infuzji.
Stosowanie u dzieci i młodzieży
W przypadku dzieci i młodzieży (od 0 do 18 lat) zastosowanie mają te same wskazania, dawki i
częstość infuzji, co u dorosłych.
Zastosowanie większej niż zalecana dawki leku Cutaquig
Jeśli pacjent uzna, że podał w infuzji zbyt dużą dawkę leku, należy jak najszybciej skontaktować się
ze swoim lekarzem lub pielęgniarką.
Pominięcie zastosowania leku Cutaquig
Jeśli pacjent pominął dawkę, należy jak najszybciej poinformować o tym swojego lekarza lub
pielęgniarską. Nie należy podawać w infuzji podwójnej dawki leku Cutaquig w celu uzupełnienia
pominiętej dawki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, jak dreszcze, ból głowy, zawroty
głowy, gorączka, wymioty, reakcje alergiczne, mdłości, ból stawów, niskie ciśnienie krwi i
umiarkowany ból okolicy lędźwiowej, chociaż nie u każdego one wystąpią.
Pewne działania niepożądane, takie jak ból głowy, dreszcze czy ból ciała można ograniczyć przez
zmniejszenie szybkości infuzji.
W badaniach klinicznych oceniających bezpieczeństwo stosowania leku Cutaquig nie zaobserwowano
poważnych działań niepożądanych leku u pacjentów, u których go stosowano.
Pacjent może być uczulony (nadwrażliwy) na immunoglobuliny i mogą u niego wystąpić reakcje
alergiczne, takie jak nagły spadek ciśnienia krwi lub, w pojedynczych przypadkach, wstrząs. Lekarze
są świadomi tych potencjalnych działań niepożądanych i będą monitorować pacjenta podczas kilku
pierwszych infuzji i po ich zakończeniu.
Jeśli u pacjenta wystąpi którykolwiek z poniższych objawów, należy natychmiast powiedzieć o tym
lekarzowi:
- uczucie oszołomienia, zawroty głowy lub omdlenie,
- wysypka i swędzenie skóry, obrzęk jamy ustnej lub gardła, trudności z oddychaniem, świszczący oddech,
- nieprawidłowa częstość akcji serca, ból w klatce piersiowej, siny kolor warg lub palców dłoni i stóp,
- nieostre widzenie. W razie stosowania leku Cutaquig w domu, pacjent może wykonać infuzję w obecności opiekuna, który będzie obserwować pacjenta pod kątem objawów reakcji alergicznej. W razie wystąpienia jakichkolwiek objawów reakcji alergicznej należy przerwać infuzję i w razie potrzeby wezwać pomoc. Informacje na temat ryzyka reakcji alergicznych podane są również w punkcie 2 niniejszej ulotki. Następujące działania niepożądane występują bardzo często (mogą wystąpić przy więcej niż 1 na 10 infuzji):
- Reakcje w miejscu infuzji, takie jak zaczerwienie, obrzęk, swędzenie i dyskomfort.
Następujące działania niepożądane występują niezbyt często (mogą wystąpić przy więcej niż 1 na
1000 infuzji do mniej niż 1 na 100 infuzji):
- Ból głowy
- Nudności
- Zmęczenie
Następujące działania niepożądane występują rzadko (mogą wystąpić przy więcej niż 1 na
10 000 infuzji):
- Zawroty głowy
- Ból brzucha
- Rozdęcie jamy brzusznej
- Wymioty
- Odruch wymiotny
- Ból mięśni
- Ból stawów
- Gorączka
- Dreszcze
- Dyskomfort w klatce piersiowej
- Objawy grypopodobne
- Ból
- Ogólne złe samopoczucie
- Dodatni wynik testu krwi w kierunku przeciwciał
- Nieprawidłowe wyniki testów krwi wskazujące na niszczenie czerwonych krwinek.
- Zwiększenie stężenia hemoglobiny
- Zwiększenie stężenia kreatyniny we krwi
- Wysypka
- Reakcje skórne
- Zwiększenie aktywności określonych enzymów wątrobowych nazywanych transaminazami
Inne działania niepożądane, które nie wystąpiły w badaniach klinicznych, ale były również zgłaszane,
to:
- Nadwrażliwość (np. rumień, pokrzywka)
- Podwyższone ciśnienie krwi
- Problemy związane z tworzeniem się zakrzepów krwi w naczyniach krwionośnych (np. zakrzepica żył głębokich, udar)
- Zakrzepy w naczyniach krwionośnych (patrz również punkt 2 „Ostrzeżenia i środki ostrożności”)
- Swędzenie
- Ból pleców
Działania niepożądane obserwowane przy stosowaniu podobnych leków
Następujące dodatkowe działania niepożądane obserwowano przy podawaniu podskórnej infuzji
normalnej ludzkiej immunoglobuliny. Możliwe jest, że wystąpią one u jakiegoś pacjenta stosującego
ten lek.
- dreszcze,
- bladość,
- biegunka,
- ból w miejscu wstrzyknięcia,
- szybko postępujące zaczerwienienie okolic szyi/twarzy,
- uczucie ciepła,
- uczucie zimna,
- osłabienie,
- ucisk w gardle,
- trudności w oddychaniu,
- objawy przypominające astmę,
- kaszel,
- obrzęk twarzy,
- zespół nazywany „aseptycznym zapaleniem opon mózgowo-rdzeniowych” (patrz również punkt 2 „Ostrzeżenia i środki ostrożności”).
Jeśli u pacjenta wystąpi którykolwiek z poniższych objawów, należy natychmiast powiedzieć o tym
lekarzowi: Mogą to być objawy poważnego problemu.
- Silny ból głowy w połączeniu z takimi objawami, jak mdłości, wymioty, sztywność karku, gorączka i nadwrażliwość na światło. Mogą to być objawy przejściowego i odwracalnego niezakaźnego obrzęku błon otaczających mózg i rdzeń kręgowy (zapalenie opon mózgowo- rdzeniowych).
- Ból, obrzęk, wzrost temperatury, zaczerwienienie lub guzek w obrębie ręki lub nogi, duszność bez widocznej przyczyny, ból lub dyskomfort w klatce piersiowej, który nasila się przy głębokim oddychaniu, przyspieszenie tętna bez widocznej przyczyny, drętwienie lub osłabienie jednej strony ciała, nagłe splątanie lub trudności z mówieniem. Mogą to być objawy zakrzepu krwi.
Takie działania niepożądane mogą wystąpić nawet jeśli pacjent otrzymywał uprzednio ludzkie
immunoglobuliny i dobrze je tolerował.
Dodatkowe informacje na temat okoliczności zwiększających ryzyko działań niepożądanych podane
są w punkcie 2.
Zgłaszanie działań niepożądanych
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane
niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania niepożądane
można zgłaszać bezpośrednio do krajowego systemu zgłaszania:
Departament Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL-02 222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
e-mail: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Cutaquig
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i na pudełku po
„EXP”. Termin ważności oznacza ostatni dzień danego miesiąca.
Przechowywać w lodówce (2°C – 8 ° C). Nie zamrażać. Przechowywać fiolkę w pudełku zewnętrznym
w celu ochrony przed światłem.
W okresie ważności lek może być przechowywany w temperaturze pokojowej (nie przechowywać w
temperaturze przekraczającej 25°C) przez okres do 9 miesięcy bez konieczności przechowywania w
lodówce w tym okresie; jeśli lek nie zostanie zużyty w tym okresie, musi być usunięty po jego
upływie.
Po pierwszym otwarciu opakowania lek należy zużyć natychmiast.
Nie stosować leku Cutaquig, jeśli roztwór jest mętny lub zawiera cząstki stałe.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Cutaquig
Substancją czynną jest immunoglobulina ludzka normalna w stężeniu 165 mg/ml (co najmniej 95%
stanowi immunoglobulina G).
- IgG ……….. 71%
- IgG ……….. 25%
- IgG ……….. 3%
- IgG ………… 2%
Pozostałe składniki to: maltoza, polisorbat 80 i woda do wstrzykiwań.
Maksymalna zawartość IgA wynosi 300 mikrogramów/ml.
Lek Cutaquig zawiera sód w ilości ≤ 30 mmol/l.
Jak wygląda lek Cutaquig i co zawiera opakowanie
Lek Cutaquig jest to roztwór do wstrzykiwań.
Roztwór jest przejrzysty i bezbarwny.
Podczas przechowywania roztwór może stać się lekko opalizujący i blado żółtawy.
Cutaquig dostępny jest w postaci:
6, 10, 12, 20, 24 lub 48 ml roztworu w fiolce (ze szkła typu I) z korkiem z gumy bromobutylowej -
opakowania zawierające 1, 10 lub 20 fiolek.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny:
Octapharma (IP) SPRL
Allée de la Recherche 65
1070 Anderlecht
Belgia
Wytwórca:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Strasse 235
1100 Wiedeń
Austria
Octapharma AB
Lars Forssells gata 23
112 75 Stockholm
Szwecja
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Bułgaria, Chorwacja, Czechy, Dania, Estonia,
Finlandia, Francja, Hiszpania, Holandia, Irlandia, Islandia, Litwa,
Łotwa, Luksemburg, Malta, Niemcy, Norwegia, Polska,
Portugalia, Rumunia, Słowacja, Słowenia, Szwecja, Węgry,
Wielka Brytania (Irlandia Północna), Włochy:
Cutaquig
Data ostatniej aktualizacji ulotki: 11/2023
Aneks I – Wytyczne dotyczące podawania
1. Przygotować konieczną liczbę fiolek leku Cutaquig
- Jeśli fiolki są przechowywane w lodówce, przenieść je do temperaturze pokojowej na co najmniej 90 minut przed infuzją.
- Nie podgrzewać fiolek ani nie umieszczać ich w kuchence mikrofalowej.
- Nie wstrząsać fiolkami, aby uniknąć tworzenia się piany.
2. Przygotowanie infuzji
- Wybrać i przygotować czysty obszar roboczy przy użyciu chusteczek antyseptycznych lub roztworu dezynfekującego (Rysunek 1).
Rysunek 1
- Przygotować sprzęt i materiały do infuzji:
- pompa infuzyjna (opcjonalnie) i zgodna strzykawkę (lub strzykawki),
- igła (do pobrania produktu z fiolki),
- zestaw infuzyjny,
- przewód do infuzji i złącze Y (trójnik) (jeśli jest potrzebny),
- alkohol i chusteczki nasączone alkoholem/chusteczki antyseptyczne,
- gazik lub przezroczysty opatrunek i plaster mocujący (bez opatrunku),
- pojemnik na ostre odpady,
- dzienniczek leczenia i długopis.
- Umyć starannie ręce i odczekać aż wyschną (Rysunek 2). Użyć żelu dezynfekcyjnego, tak jak przedstawiono to na szkoleniu.
Rysunek 2
- W razie potrzeby zaprogramować pompę zgodnie z instrukcją jej obsługi i tak jak to przedstawiono na szkoleniu przeprowadzonym przez lekarza lub pielęgniarkę.
3. Sprawdzenie i otwarcie fiolek
- Sprawdzić dokładnie każdą fiolkę:
- pod kątem prawidłowo oznakowanej dawki zgodnej z dawką przepisaną przez lekarza,
- wyglądu roztworu (powinien być przezroczysty i bezbarwny do bladożółtego lub jasnobrązowego),
- upewnić się, że osłona ochronna jest na swoim miejscy i jest nienaruszona,
- sprawdzić termin ważności i numer serii.
- Nie używać roztworu, który jest mętny lub zawiera cząstki stałe.
- Zdjąć osłonę ochronną.
- Zdezynfekować gumowy korek chusteczką antyseptyczną i odczekać aż wyschnie (Rysunek 3).

Rysunek 3
4. Przygotowanie i napełnienie strzykawki
- Odtworzyć opakowanie z jałową strzykawką i igłą.
- Przykręcić igłę do strzykawki.
- Odciągnąć tłok strzykawki, by nabrać do niej objętość powietrza w przybliżeniu równą objętości roztworu, jaka ma być pobrana z fiolki.
- Wkłuć igłę do fiolki i odwrócić fiolkę do góry dnem. Wstrzyknąć powietrze, upewniając się, że końcówka igły znajduje się ponad roztworem, by uniknąć tworzenia piany.
- Następnie powoli pobrać odpowiednią objętość leku Cutaquig upewniając się, że końcówka igły cały czas pozostaje w roztworze (Rysunek 4).
Rysunek4
- Wyciągnąć igłę z fiolki.
- Konieczne może być powtórzenie tej procedury, jeśli wyliczona dawka wymaga pobrania leku z więcej niż jednej fiolki.
- Po zakończeniu odłączyć igłę i wyrzucić ją do pojemnika na ostre odpady.
- Przejść niezwłocznie do kolejnego etapu, ponieważ roztwór IgG należy zużyć jak najszybciej.
5. Przygotowanie pompy infuzyjnej i przewodu (opcjonalnie)
- Należy przygotować pompę zgodnie z instrukcją załączoną przez jej producenta.
- Aby wstępnie wypełnić przewód do infuzji, podłączyć wypełnioną strzykawkę przewodu do infuzji i delikatnie nacisnąć tłok strzykawki, aby wypełnić przewód lekiem Cutaquig i usunąć z niego całe powietrze. (Rysunek 5).
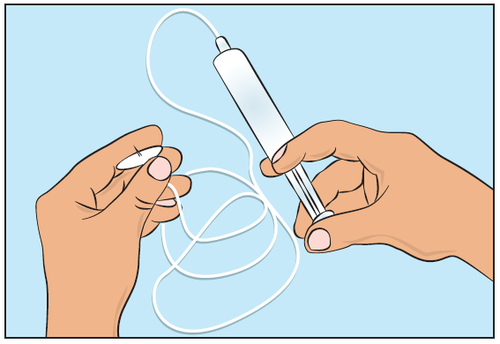
Rysunek 5
6. Wybór miejsc infuzji i wkłucie igły (igieł) do infuzji
- Infuzje leku Cutaquig można podawać w następujące obszary: brzuch, uda, górne części ramion oraz obszar górnych części nóg/bioder (Rysunek 6).
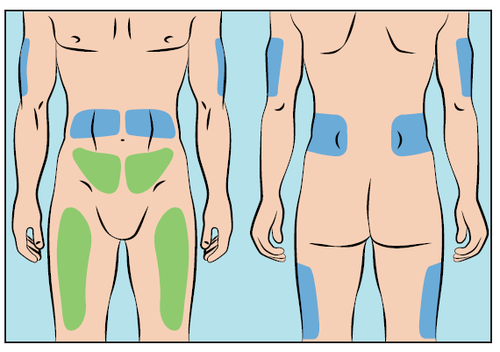
Rysunek 6
- Poszczególne miejsca infuzji powinny być oddalone od siebie o co najmniej 5 cm.
- Należy użyć miejsc infuzji innych niż użyte przy poprzednim podaniu leku.
- Unikać wkłuwania igły w blizny, tatuaże, rozstępy i obszary skóry uszkodzonej/objętej zapaleniem/zaczerwienionej.
- Oczyścić skórę w wybranym miejscu (miejscach) infuzji antyseptyczną chusteczką do skóry i odczekać, aż skóra wyschnie.
- Ścisnąć fałd skóry wokół miejsca infuzji pomiędzy kciukiem i palcem wskazującym (Rysunek 7), zdjąć ostrożnie osłonę z igły i wkłuć igłę w skórę (Rysunek 8). Kąt wkłucia igły zależy od typu stosowanego zestawu do infuzji.

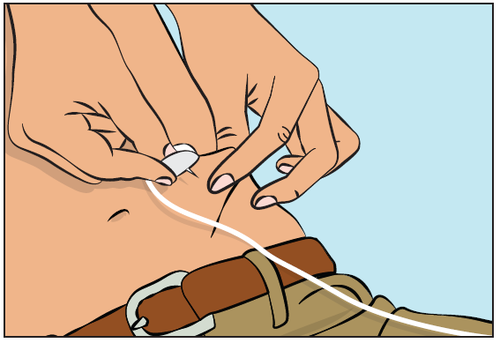
Rysunek 7
Rysunek 8
7. Sprawdzenie infuzji
- Nie wolno podawać roztworu do naczynia krwionośnego.
- Unieruchomić igłę na miejscu używając jałowego gazika i plastra bez opatrunku lub przezroczystego opatrunku (Rysunek 9).
8. Rozpoczęcie infuzji
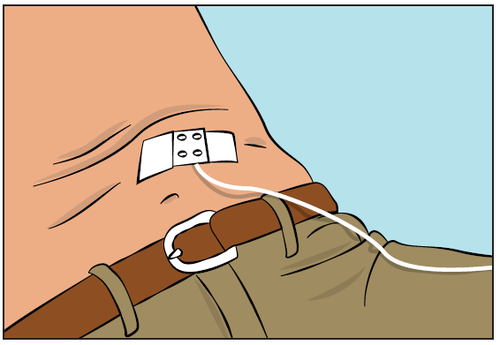
Rysunek 9
- Rozpocząć infuzję. Jeśli lek podawany jest przez pompę infuzyjną, należy stosować się do instrukcji producenta.
9. Odnotowanie infuzji
- Na każdej fiolce leku Cutaquig znajduje się odrywana część etykiety z danymi nt. numeru serii. Należy wkleić tę etykietę do dzienniczka leczenia pacjenta lub do rejestru infuzji. Odnotować informacje na temat dawki, daty, godziny, lokalizacji miejsc infuzji oraz wszelkich zakażeń i działań niepożądanych, jak również wszelkie uwagi związane z daną infuzją.
10. Po zakończeniu infuzji
- Delikatnie wyciągnąć igłę (igły) ze skóry i natychmiast wyrzucić do pojemnika na ostre odpady.
- W razie konieczności nałożyć mały gazik na miejsca po igle i założyć opatrunek.
- Wyrzucić wszystkie zużyte materiały jednorazowe, jak również niezużyty lek i puste fiolki w sposób zalecony przez lekarza lub pielęgniarkę i zgodnie z miejscowymi wymogami. Posprzątać i schować w bezpieczne miejsce cały sprzęt wielokrotnego użytku (np. pompę) do czasu następnej infuzji.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterOctapharma AB Octapharma GmbH Octapharma Pharmazeutika Produktionsges.m.g.H.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki CutaquigPostać farmaceutyczna: Roztwór, 200 mg/mlSubstancja czynna: immunoglobulins, normal human, for extravascular adm.Producent: Baxalta Belgium Manufacturing S.A.Wymaga receptyPostać farmaceutyczna: Roztwór, 200 mg/mlSubstancja czynna: immunoglobulins, normal human, for extravascular adm.Producent: Instituto Grifols, S.A.Wymaga receptySubstancja czynna: immunoglobulins, normal human, for intravascular adm.Producent: Baxalta Belgium Manufacturing S.A.Wymaga recepty
Odpowiedniki Cutaquig w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Cutaquig – Hiszpania
Odpowiednik Cutaquig – Ukraina
Lekarze online w sprawie Cutaquig
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Cutaquig – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














