
Cosopt PF

Zapytaj lekarza o receptę na Cosopt PF

Jak stosować Cosopt PF
ULOTKA DLA PACJENTA
Ulotka dołączona do opakowania: informacja dla użytkownika
COSOPT PF, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym
Dorzolamid + Tymolol
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek COSOPT PF i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku COSOPT PF
- 3. Jak stosować lek COSOPT PF
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek COSOPT PF
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek COSOPT PF i w jakim celu się go stosuje
COSOPT PF zawiera dwa leki: dorzolamid i tymolol.
- Dorzolamid należy do grupy leków zwanych „inhibitorami anhydrazy węglanowej”.
- Tymolol należy do grupy leków zwanych „inhibitorami receptorów beta-adrenergicznych” (beta-adrenolitykami). Leki te powodują obniżenie ciśnienia śródgałkowego na drodze dwóch różnych mechanizmów.
COSOPT PF zalecany jest w leczeniu jaskry w celu obniżenia podwyższonego ciśnienia
śródgałkowego, kiedy nie wystarcza stosowanie kropli do oczu zawierających tylko inhibitor receptora
beta-adrenergicznego.
2. Informacje ważne przed zastosowaniem leku COSOPT PF
Kiedy nie stosować leku COSOPT PF
- jeśli pacjent ma uczulenie na chlorowodorek dorzolamidu, maleinian tymololu lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
- jeśli obecnie lub w przeszłości u pacjenta stwierdzono zaburzenia układu oddechowego, takie jak astma lub ciężkie przewlekłe obturacyjne zapalenie oskrzeli (poważna choroba płuc, która może objawiać się świszczącym oddechem, problemami z oddychaniem i (lub) długo utrzymującym się kaszlem);
- jeśli u pacjenta stwierdza się zwolnienie akcji serca, niewydolność serca lub zaburzenia rytmu serca (nieregularną akcję serca);
- jeśli u pacjenta stwierdzono ciężką chorobę nerek lub ciężkie zaburzenia funkcji nerek albo kamicę nerkową w wywiadzie;
- jeśli u pacjenta stwierdza się nadmierne zakwaszenie krwi w wyniku nagromadzenia jonów chlorkowych w organizmie (kwasica hiperchloremiczna).
W przypadku wątpliwości, czy można stosować ten lek, należy zwrócić się do lekarza lub farmaceuty.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania COSOPT PF należy omówić to z lekarzem.
Należy poinformować lekarza o wszystkich występujących obecnie lub w przeszłości zaburzeniach
oka i chorobach:
- chorobie niedokrwiennej serca (jej objawy to między innymi ból lub uczucie ucisku w klatce piersiowej, duszność lub uczucie dławienia się), niewydolność serca, niskie ciśnienie krwi;
- zaburzenia częstości akcji serca, na przykład zwolnienie akcji serca;
- problemy z oddychaniem, astma lub przewlekła obturacyjna choroba płuc;
- choroby związane ze słabym krążeniem krwi (takie jak choroba Raynauda lub zespół Raynauda);
- cukrzyca, ponieważ tymolol może maskować przedmiotowe i podmiotowe objawy hipoglikemii (małe stężenie cukru we krwi);
- nadczynność tarczycy, ponieważ tymolol może maskować jej objawy przedmiotowe i podmiotowe.
Przed zabiegiem operacyjnym należy poinformować lekarza prowadzącego o stosowaniu leku
COSOPT PF ,ponieważ tymolol może zmienić działanie niektórych leków stosowanych do
znieczulenia.
Należy także powiedzieć lekarzowi o uczuleniu na jakiekolwiek leki lub reakcjach anafilaktycznych.
Należy powiadomić lekarza, jeśli u pacjenta wystąpiło osłabienie siły mięśniowej lub rozpoznano
miastenię ( Myasthenia gravis).
W przypadku wystąpienia podrażnienia oka lub jakiegokolwiek nowego problemu z okiem, takiego
jak zaczerwienienie oka albo obrzęk powiek, należy natychmiast zgłosić się do lekarza.
Jeżeli pacjent podejrzewa, że lek COSOPT PF wywołuje reakcję alergiczną lub nadwrażliwość
(np. wysypka na skórze, ciężka reakcja skórna lub zaczerwienie skóry i swędzenie oka), należy
przerwać stosowanie tego leku i natychmiast skontaktować się z lekarzem.
Należy powiadomić lekarza w przypadku stwierdzenia infekcji oka, doznania urazu oka, po operacji
gałki ocznej lub wystąpieniu reakcji, której towarzyszy pojawienie się nowych lub nasilenie
dotychczasowych objawów.
Po podaniu do oka lek COSOPT PF może wywołać działania ogólnoustrojowe.
Nie przeprowadzono badań dotyczących stosowania tego leku u pacjentów używających soczewek
kontaktowych.
Przed zastosowaniem leku COSOPT PF osoby używające miękkich soczewek kontaktowych powinny
zasięgnąć porady lekarskiej.
Stosowanie u dzieci
Doświadczenia związane ze stosowaniem leku COSOPT (postać ze środkiem konserwującym)
u niemowląt i dzieci są ograniczone.
Stosowanie u osób w podeszłym wieku
W badaniach prowadzonych z zastosowaniem leku COSOPT (postać ze środkiem konserwującym),
lek COSOPT wywoływał zbliżone działania u osób w podeszłym wieku i młodszych.
Stosowanie u pacjentów z zaburzeniami czynności wątroby
Należy poinformować lekarza o istniejących obecnie lub w przeszłości chorobach wątroby.
COSOPT PF a inne leki
COSOPT PF może wpływać na działanie innych leków lub też inne stosowane przez pacjenta leki,
mogą wpływać na działanie leku COSOPT PF. Dotyczy to także innych przeciwjaskrowych leków
okulistycznych. Należy powiedzieć lekarzowi o przyjmowaniu lub zamiarze przyjmowania leków
obniżających ciśnienie krwi, leków nasercowych lub przeciwcukrzycowych. Należy powiedzieć
lekarzowi lub farmaceucie o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio,
a także o lekach, które pacjent planuje stosować. Jest to szczególnie istotne w przypadku:
- przyjmowania leków obniżających ciśnienie krwi lub stosowanych w chorobach serca (takich jak leki blokujące kanał wapniowy, antagoniści receptorów beta-adrenergicznych czy digoksyna);
- przyjmowania leków stosowanych w zaburzeniach rytmu serca czy przywracających regularny rytm serca (takich jak leki blokujące kanał wapniowy, antagoniści receptorów beta-adrenergicznych czy digoksyna);
- stosowania innych kropli do oczu zawierających leki z grupy antagonistów receptorów beta-adrenergicznych;
- przyjmowania innych inhibitorów anhydrazy węglanowej, takich jak acetazolamid;
- przyjmowania inhibitorów monoaminooksydazy (MAOI);
- przyjmowania leków o działaniu parasympatykomimetycznym (cholinergicznym), które mogą być stosowane w zaburzeniach oddawania moczu. Leki parasympatykomimetyczne są także czasami stosowane w celu przywrócenia prawidłowej motoryki (ruchomości) jelit;
- przyjmowania narkotyków, takich jak morfina, stosowanych w leczeniu umiarkowanie silnych lub silnych bólów;
- przyjmowania leków przeciwcukrzycowych;
- przyjmowania leków przeciwdepresyjnych takich jak fluoksetyna i paroksetyna;
- przyjmowania chemioterapeutyków z grupy sulfonamidów;
- przyjmowania chinidyny (leku stosowanego w leczeniu chorób serca i pewnych postaci malarii).
Ciąża i karmienie piersią
Przed zastosowaniem jakiegokolwiek leku należy poradzić się lekarza lub farmaceuty.
Stosowanie w ciąży
Nie należy stosować tego leku w czasie ciąży, chyba że lekarz uzna to za konieczne.
Stosowanie podczas karmienia piersią
Nie należy stosować tego leku podczas karmienia piersią. Tymolol może przenikać do pokarmu
kobiecego .Przed przyjęciem jakiegokolwiek leku w okresie karmienia piersią należy poradzić się
lekarza prowadzącego.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie przeprowadzono badań nad wpływem na zdolność prowadzenia pojazdów lub obsługiwania
maszyn. Niektóre działania niepożądane związane ze stosowaniem leku COSOPT PF, takie jak
niewyraźne widzenie, mogą wpływać na zdolność prowadzenia pojazdów i (lub) obsługiwania
maszyn. Pacjenci, którzy źle się czują lub widzą niewyraźnie, nie powinni prowadzić pojazdów ani
obsługiwać maszyn.
3. Jak stosować lek COSOPT PF
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy zwrócić
się do lekarza lub farmaceuty. Lekarz ustala właściwą dawkę leku i czas leczenia.
Zalecana dawka to jedna kropla do chorego oka (chorych oczu) rano i wieczorem.
Jeżeli oprócz leku COSOPT PF równocześnie stosowane są inne krople do oczu, należy zachować co
najmniej 10 minut przerwy przed podaniem następnego leku.
Nie należy zmieniać dawki leku bez porozumienia z lekarzem.
W przypadku trudności z zastosowaniem kropli, należy zwrócić się o pomoc do członka rodziny lub
opiekuna.
Nie dopuszczać, aby którakolwiek część pojemnika jednodawkowego dotknęła oka lub jego okolic.
Może to prowadzić do obrażeń oka, jak również do zanieczyszczenia pojemnika bakteriami, które
mogą spowodować zakażenie oka prowadzące do jego poważnego uszkodzenia, a nawet utraty
wzroku. Aby uniknąć możliwego zanieczyszczenia pojemnika jednodawkowego, należy umyć ręce
przed zastosowaniem tego leku i unikać kontaktu końcówki pojemnika jednodawkowego
z jakąkolwiek powierzchnią. Nowy pojemnik jednodawkowy powinien być otwarty bezpośrednio
przed każdym użyciem. Każdy pojemnik zawiera roztwór w ilości wystarczającej do podania
odpowiedniej dawki produktu leczniczego do obu oczu, jeśli lekarz zaleci stosowanie do obu oczu.
Otwarty pojemnik z jakąkolwiek pozostałą zawartością wyrzucić natychmiast po użyciu.
Instrukcja stosowania
Otworzyć foliową saszetkę zawierającą pojemniki jednodawkowe. Należy zapisać datę pierwszego
otwarcia na saszetce.
Użycie produktu leczniczego COSOPT PF
- 1. Należy umyć ręce.
- 2. Wyjąć pasek pojemników z saszetki.
- 3. Oderwać od paska jeden pojemnik jednodawkowy.
- 4. Włożyć pasek z pozostałymi pojemnikami z powrotem i złożyć krawędź, aby zamknąć saszetkę.
- 5. Jeśli roztwór nie znajduje się na końcówce pojemnika, stuknij kilka razy palcem w nieotwarty pojemnik trzymając końcówkę dozującą skierowaną do dołu, aby roztwór dostał się do końcówki.
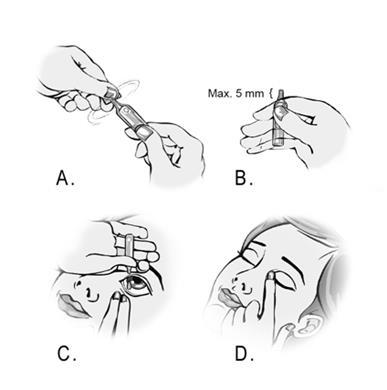
- 6. Otworzyć pojemnik, odkręcając jego górną część. (Rysunek A).
- 7. Trzymać pojemnik między kciukiem a palcem wskazującym. Należy pamiętać, że końcówka pojemnika nie może wystawać więcej niż 5 mm ponad krawędź palca wskazującego. (Rysunek B).
- 8. Przechylić głowę do tyłu lub położyć się. Położyć dłoń na czole. Palec wskazujący powinien być ułożony wzdłuż łuku brwiowego lub spoczywać na grzbiecie nosa. Należy spojrzeć w górę i drugą ręką odciągnąć dolną powiekę w dół. Nie dopuścić, aby którakolwiek część pojemnikadotknęła oka lub jego okolic. Wpuścić jedną kroplę do przestrzeni między powieką a gałką oczną poprzez delikatne ściśnięcie pojemnika. (Rysunek C). Nie należy mrugać podczas wpuszczania kropli do oka. Każdy pojemnik jednodawkowy zawiera roztwór w ilości wystarczającej do podania odpowiedniej dawki produktu leczniczego do obu oczu.
- 9. Zamknąć oko i naciskać wewnętrzny kącik oka palcem przez około dwie minuty. Pomaga to zapobiec przedostaniu się leku do całego organizmu. (Rysunek D).
- 10. Zetrzeć nadmiar roztworu ze skóry wokół oczu.
Jeśli lekarz zaleci stosowanie kropli do obu oczu, powyższe kroki należy powtórzyć dla
drugiego oka.
Aby uniknąć zanieczyszczenia roztworu, który nie zawiera konserwantów, natychmiast po
zakropleniu produktu leczniczego do oka (oczu) pojemnik jednodawkowy należy wyrzucić,
nawet jeśli pozostało w nim trochę roztworu.
Pozostałe pojemniki należy przechowywać w foliowej saszetce; mogą być używane w ciągu 15
dni po otwarciu saszetki. Jeśli po upływie 15 dni od daty otwarcia saszetki pozostały w niej
jeszcze jakiekolwiek pojemniki, należy je usunąć w sposób bezpieczny dla środowiska i
otworzyć nową saszetkę. Ważne jest, aby krople do oczu stosowane były nieprzerwanie w
sposób zalecony przez lekarza.
W razie wątpliwości dotyczących sposobu podawania produktu leczniczego, należy zwrócić się
do lekarza, farmaceuty lub pielęgniarki.
Zastosowanie większej niż zalecana dawki leku COSOPT PF
W przypadku podania do oka zbyt wielu kropli lub połknięcia zawartości pojemnika, wśród innych
objawów mogą wystąpić zawroty głowy, trudności w oddychaniu lub uczucie zwolnionej czynności
serca. Należy natychmiast skontaktować się z lekarzem.
Pominięcie zastosowania leku COSOPT PF
COSOPT PF należy przyjmować zgodnie ze wskazaniami lekarza.
W razie pominięcia dawki leku należy ją zastosować jak najszybciej. Jeżeli jednak do przyjęcia
następnej dawki pozostało niewiele czasu, nie należy podawać pominiętej dawki i powrócić do
regularnego schematu dawkowania.
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku COSOPT PF
Przed odstawieniem leku należy skonsultować się z lekarzem.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem leku należy zwrócić się do
lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Działania niepożądane:
Jeśli wystąpi którekolwiek z następujących działań niepożądanych, należy zaprzestać stosowania tego
leku i zwrócić się natychmiast po pomoc lekarską, ponieważ mogą to być objawy reakcji na lek.
Uogólnione reakcje alergiczne, w tym obrzęk pod skórą, mogą występować w okolicach twarzy
i kończyn oraz powodować niedrożność dróg oddechowych i trudności z przełykaniem, duszność,
pokrzywkę lub swędzącą wysypkę, wysypkę miejscową i uogólnioną, świąd oraz ciężką, nagłą
i zagrażającą życiu reakcję alergiczną.
Leczenie kroplami można na ogół kontynuować, chyba że działania niepożądane są ciężkie. W razie
obaw należy skontaktować się z lekarzem lub farmaceutą. Nie należy przerywać leczenia lekiem
COSOPT PF bez konsultacji z lekarzem
Podczas badań klinicznych lub po wprowadzeniu leku do obrotu zgłoszono następujące
działania niepożądane związane z lekiem COSOPT PF lub jednym z jego składników
czynnych:
Bardzo często (mogą występować u więcej niż 1 na 10 osób)
Uczucie palenia i kłucia w oku, zmiana odczuwania smaku
Często (mogą występować u nie więcej niż 1 na 10 osób)
Zaczerwienienie gałek ocznych i skóry wokół oka (oczu), łzawienie lub swędzenie oka (oczu),
nadżerki rogówki (uszkodzenia przedniej warstwy gałki ocznej), obrzęk i (lub) podrażnienie
gałek ocznych i skóry wokół oka (oczu), uczucie ciała obcego w oku, zmniejszenie
wrażliwości rogówki (nie odczuwanie ciała obcego w oku oraz nie odczuwanie bólu), ból oka,
suche oczy, niewyraźne widzenie, ból głowy, zapalenie zatok (uczucie napięcia lub
wypełnienia nosa), nudności, osłabienie i uczucie zmęczenia.
Niezbyt często (mogą występować u nie więcej niż 1 na 100 osób)
Zawroty głowy, depresja, zapalenie tęczówki, zaburzenia widzenia, w tym zmiany refrakcji
(w niektórych przypadkach z powodu odstawienia leków zwężających źrenicę), zwolnienie
akcji serca, omdlenia, duszność, niestrawność oraz kamica nerkowa.
Rzadko (mogą występować u nie więcej niż 1 na 1000 osób)
Toczeń rumieniowaty układowy (choroba autoimmunologiczna, która może powodować
zapalenie narządów wewnętrznych) ,mrowienie lub drętwienie dłoni albo stóp, bezsenność,
koszmary senne, utrata pamięci, nasilenie objawów przedmiotowych oraz podmiotowych
miastenii (zaburzenie mięśni), osłabienie popędu płciowego, udar mózgu, przemijająca
krótkowzroczność, która może ustąpić po odstawieniu leku, odwarstwienie po zabiegach
filtracyjnych leżącej pod siatkówką warstwy, w której znajdują się naczynia krwionośne,
mogące powodować zaburzenia wzroku, opadanie powiek (powieki są w połowie zamknięte),
podwójne widzenie, tworzenie się strupów na powiekach, obrzęk rogówki (z objawami
podmiotowymi zaburzenia widzenia), małe ciśnienie w oku, dzwonienie w uszach, obniżenie
ciśnienia krwi, zaburzenie rytmu serca, zmiany rytmu lub tempa pracy serca, zastoinowa
niewydolność serca (choroba serca objawiająca się zadyszką i obrzękiem stóp i nóg z powodu
nagromadzenia płynu), obrzęk (nagromadzenie płynu), niedokrwienie mózgu (zmniejszony
dopływ krwi do mózgu), ból w klatce piersiowej silne bicie serca, które może być szybkie lub
nieregularne (kołatanie serca), zawał serca, choroba Raynauda, obrzęk dłoni i stóp lub zimne
dłonie i stopy oraz osłabienie krążenia w kończynach górnych i dolnych, skurcze mięśni nóg
i (lub) bóle nóg podczas chodzenia (chromanie), duszność, niewydolność oddechowa,
zapalenie błony śluzowej nosa (nieżyt), krwawienia z nosa, zwężenie dróg oddechowych
w płucach, kaszel, podrażnienie gardła, suchość jamy ustnej, biegunka, kontaktowe zapalenie
skóry, wypadanie włosów, biało-srebrzysta wysypka (wysypka łuszczycopodobna), choroba
Peyroniego (w przebiegu której może dojść do skrzywienia penisa), reakcje alergiczne, takie
jak wysypka, pokrzywka, świąd, w rzadkich przypadkach możliwy też obrzęk warg, obrzęki
powiek i jamy ustnej, świszczący oddech lub ciężkie reakcje skórne (zespół Stevensa-
Johnsona, martwica toksyczno-rozpływna naskórka).
Tak jak inne leki podawane miejscowo do oczu, tymolol wchłania się do krwiobiegu, w wyniku
czego mogą wystąpić działania niepożądane podobne do obserwowanych po doustnym podaniu leków
blokujących receptory beta-adrenergiczne. Działania niepożądane występują rzadziej po zastosowaniu
kropli do oczu miejscowo, niż po podaniu tych leków na przykład doustnie lub we wstrzyknięciach.
Wśród wymienionych dodatkowych działań niepożądanych uwzględniono reakcje typowe dla grupy
terapeutycznej leków o działaniu beta-adrenolitycznym stosowanych w schorzeniach okulistycznych:
Nieznana (częstość nie może być określona na podstawie dostępnych danych)
Małe stężenie cukru we krwi, niewydolność serca, zaburzenia rytmu serca, ból brzucha, wymioty, bóle
mięśni niezwiązane z wysiłkiem fizycznym, zaburzenia funkcji seksualnych, halucynacja, uczucie
ciała obcego w oku (uczucie, że w oku coś się znajduje), przyspieszone tętno i zwiększone ciśnienie
tętnicze krwi.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych
Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych,
Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309,
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu. Dzięki zgłaszaniu
działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa
stosowania leku.
5. Jak przechowywać lek COSOPT PF
Lek ten należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować nieotwartych saszetek COSOPT PF po upływie terminu ważności (sześć cyfr po skrócie
EX lub EXP) zamieszczonego na opakowaniu foliowym. Pierwsze dwie cyfry oznaczają miesiąc,
a ostatnie cztery – rok. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w temperaturze powyżej 25°C.
Przechowywać w oryginalnej foliowej saszetce w celu ochrony przed światłem.
Lek COSOPT PF można używać w okresie 15 dni po pierwszym otwarciu saszetki.
Po tym czasie należy wyrzucić wszelkie niewykorzystane pojemniki jednodawkowe.
Otwarte opakowanie jednodawkowe należy wyrzucić natychmiast po pierwszym użyciu, nawet jeśli
znajdują się w nim jakiekolwiek pozostałości leku.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek COSOPT PF
- Substancjami czynnymi leku są dorzolamid i tymolol.
W każdym mililitrze roztworu znajduje się 20 mg dorzolamidu (22,26 mg chlorowodorku
dorzolamidu) i 5 mg tymololu (6,83 mg maleinianu tymololu).
- Pozostałe składniki to: hydroksyetyloceluloza, mannitol, sodu cytrynian, sodu wodorotlenek i woda do wstrzykiwań.
Jak wygląda lek COSOPT PF i co zawiera opakowanie
Lek COSOPT PF jest przejrzystym, bezbarwnym lub prawie bezbarwnym, lekko lepkim roztworem.
W każdej foliowej saszetce znajduje się 15 lub 10 pojemników jednodawkowych z polietylenu niskiej
gęstości zawierających po 0,2 ml roztworu.
Wielkości opakowań:
30 x 0,2 ml (2 saszetki z 15 pojemnikami jednodawkowymi lub 3 saszetki z 10 pojemnikami
jednodawkowymi)
60 x 0,2 ml (4 saszetki z 15 pojemnikami jednodawkowymi lub 6 saszetek z 10 pojemnikami
jednodawkowymi)
120 x 0,2 ml (8 saszetek z 15 pojemnikami jednodawkowymi lub 12 saszetek z 10 pojemnikami
jednodawkowymi)
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Santen Oy
Niittyhaankatu 20
33720 Tampere
Finlandia
Wytwórca
Fareva Mirabel
Route de Marsat, Riom;
63963 Clermont-Ferrand, Cedex 9
Francja
Santen Oy
Kelloportinkatu 1
33100 Tampere
Finlandia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Zjednoczonym Królestwie (Irlandii Północnej) pod następującymi nazwami:
Cosopt
Finlandia, Francja, Litwa, Portugalia, Szwecja
Cosopt brez konzervansa
Słowenia
Cosopt Conserveermiddelvrij
Holandia
Cosopt fără conservant
Rumunia
Cosopt Free
Słowacja
Cosopt Free bez konzervačních přísad
Czechy
Cosopt monodose
Włochy
Cosopt PF
Bułgaria, Łotwa, Polska
Cosopt PF “Χωρίς συντηρητικό”
Grecja
Cosopt Preservative-free
Irlandia, Zjednoczone Królestwo (Irlandia Północna)
Cosopt-S
Niemcy
Cosopt sine
Austria
Cosopt Ukonserveret
Dania
Cosopt Unit Dose
Belgia, Luksemburg
Cosopt Uno
Węgry
Data ostatniej aktualizacji ulotki: 09/2023
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterLaboratories Merck Sharp & Dohme – Chibret Santen Oy
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Cosopt PFPostać farmaceutyczna: Krople, 50 mcg/ml + 5 mg/mlSubstancja czynna: timolol, combinationsProducent: Pharmaselect International Beteiligungs GmbHBez receptyPostać farmaceutyczna: Krople, (0,3 mg + 5 mg)/mlSubstancja czynna: timolol, combinationsWymaga receptyPostać farmaceutyczna: Krople, 0,3 mg/ml + 5 mg/mlSubstancja czynna: timolol, combinationsProducent: Genetic S.p.AWymaga recepty
Odpowiedniki Cosopt PF w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Cosopt PF – Hiszpania
Odpowiednik Cosopt PF – Ukraina
Lekarze online w sprawie Cosopt PF
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Cosopt PF – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














