
Boostrix Polio

Zapytaj lekarza o receptę na Boostrix Polio

Jak stosować Boostrix Polio
Ulotka dołączona do opakowania: informacja dla użytkownika
Boostrix Polio, Zawiesina do wstrzykiwań w ampułko-strzykawce
Szczepionka przeciw błonicy, tężcowi, krztuścowi (bezkomórkowa, złożona) i poliomyelitis
(inaktywowana), adsorbowana, o zmniejszonej zawartości antygenów
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem szczepionki, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest szczepionka Boostrix Polio i w jakim celu się ją stosuje
- 2. Informacje ważne przed zastosowaniem szczepionki Boostrix Polio
- 3. Jak stosować szczepionkę Boostrix Polio
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać szczepionkę Boostrix Polio
- 6. Zawartość opakowania i inne informacje
1. Co to jest szczepionka Boostrix Polio i w jakim celu się ją stosuje
Boostrix Polio jest szczepionką stosowaną do szczepienia przypominającego dzieci w wieku od 3
lat, młodzieży oraz dorosłych w celu zapobiegania czterem chorobom: błonicy, tężcowi,
krztuścowi (kokluszowi) i poliomyelitis (polio). Szczepionka powoduje powstawanie w organizmie
własnej odporności (przeciwciał) przeciwko wymienionym chorobom.
- Błonica:Błonica najczęściej atakuje drogi oddechowe i czasami skórę. Zazwyczaj w drogach oddechowych dochodzi do stanu zapalnego i obrzęku, co powoduje poważne trudności w oddychaniu, a czasami duszenie się. Bakterie błonicy wytwarzają także toksyny (trucizny), które mogą powodować uszkodzenie nerwów, choroby serca, a nawet mogą doprowadzić do zgonu.
- Tężec:Bakterie tężca dostają się do organizmu człowieka w miejscu przecięcia, zadrapania lub rany skóry. Obrażenia, które stwarzają największe ryzyko zakażenia tężcem, to: oparzenia, złamania, rany głębokie lub rany zanieczyszczone glebą, kurzem, odchodami końskimi, drzazgami drzewnymi. Bakterie te produkują toksyny (trucizny), które mogą wywoływać sztywność mięśni, bolesne skurcze mięśni, drgawki, a nawet zgon. Skurcze mięśni mogą być tak silne, że prowadzą do złamania kości kręgosłupa.
- Krztusiec (koklusz):Krztusiec jest chorobą o bardzo dużej zakaźności. Choroba atakuje drogi oddechowe, powodując ciężkie napady kaszlu, które mogą utrudniać normalne oddychanie. Kaszel występujący w tej chorobie jest bardzo charakterystyczny - mówi się, że osoby chore na krztusiec „zanoszą się kaszlem”. Kaszel może utrzymywać się przez 1-2 miesiące lub dłużej. Bakterie krztuśca mogą także wywoływać zakażenia uszu, zapalenie oskrzeli, które może trwać bardzo długo, zapalenie płuc, drgawki, uszkodzenie mózgu, a nawet zgon.
- Poliomyelitis(Polio):Poliomyelitis, czasami po prostu nazywane polio, jest zakażeniem wirusowym, które charakteryzuje się wieloma objawami. Często stanowi ono łagodnie przebiegającą chorobę, ale u niektórych osób może powodować trwałe uszkodzenia, a nawet zgon. W najcięższej postaci tej choroby dochodzi do paraliżu mięśni (mięśnie nie mogą spełniać swoich funkcji), może to być paraliż mięśni oddechowych lub zapewniających możliwość poruszania się o własnych siłach. Kończyny dotknięte tym schorzeniem mogą być zniekształcone i bolesne.
Żaden ze składników szczepionki nie może wywołać błonicy, tężca lub krztuśca i poliomyelitis.
Zastosowanie szczepionki Boostrix Polio podczas ciąży pomaga chronić dziecko przed krztuścem
podczas pierwszych kilku miesięcy życia dziecka, zanim otrzyma ono szczepienie pierwotne.
2. Informacje ważne przed zastosowaniem szczepionki Boostrix Polio
Kiedy nie stosować szczepionki Boostrix Polio:
- jeśli kiedykolwiek wystąpiła reakcja alergiczna (uczuleniowa) na Boostrix Polio lub którykolwiek składnik tej szczepionki (wymieniony w punkcie 6) jak również neomycynę, polimyksynę (antybiotyki) lub formaldehyd. Wśród objawów uczulenia należy wymienić: swędzącą wysypkę skórną, trudności w oddychaniu, obrzęk twarzy lub języka.
- jeśli kiedykolwiek wystąpiła reakcja alergiczna na którąkolwiek szczepionkę przeciwko błonicy, tężcowi, krztuścowi (kokluszowi) lub poliomyelitis.
- jeśli doszło do jakichkolwiek zaburzeń układu nerwowego w ciągu 7 dni od uprzedniego podania szczepionki przeciwko krztuścowi (kokluszowi).
- jeżeli po uprzednich szczepieniach przeciwko błonicy lub tężcowi dochodziło do przejściowego obniżenia liczby płytek krwi (które zwiększa ryzyko wystąpienia krwawienia lub siniaków) lub też występowały zaburzenia mózgu i nerwów.
- jeśli występuje wysoka gorączka (powyżej 38,0 ° C). Łagodna infekcja, taka jak np. przeziębienie, nie powinna być przeciwwskazaniem do szczepienia, ale najpierw należy o tym powiedzieć lekarzowi.
Ostrzeżenia i środki ostrożności
Przed przyjęciem szczepionki Boostrix Polio należy zwrócić się do lekarza, lub farmaceuty:
- jeśli kiedykolwiek przedtem po szczepieniu szczepionką Boostrix Polio lub inną szczepionką przeciwko krztuścowi (kokluszowi), wystąpiły problemy zdrowotne, a w szczególności:
- Wysoka gorączka (powyżej 40 ° C) w ciągu 48 godzin od podania szczepionki
- Zapaść lub stan podobny do wstrząsu w ciągu 48 godzin od podania szczepionki
- Nieustający płacz trwający co najmniej trzy godziny w ciągu 48 godzin od podania szczepionki
- Drgawki lub napady drgawek z towarzyszącą gorączką lub bez w ciągu 3 dni od podania szczepionki
- jeśli dziecko choruje na niezdiagnozowaną lub postępującą chorobę mózgu albo na niepoddającą się leczeniu padaczkę. Szczepionka powinna być podana po opanowaniu choroby
- jeśli występują krwawienia lub łatwo dochodzi do powstawania siniaków
- jeśli występują skłonności do drgawek związanych z gorączką, lub takie przypadki miały miejsce w rodzinie
- jeśli, z różnych przyczyn, występują długotrwałe zaburzenia odporności (w tym zakażenie wirusem HIV). W takich przypadkach szczepionka Boostrix Polio może zostać podana, ale zaszczepieni pacjenci mogą nie uzyskać tak dobrej ochrony przeciw zakażeniom jak osoby z prawidłowym działaniem układu odpornościowego.
Po lub nawet przed podaniem każdej szczepionki w postaci wstrzyknięcia może dojść do omdlenia
(szczególnie u nastolatków). W związku z tym należy poinformować lekarza lub pielęgniarkę, jeżeli u
pacjenta kiedyś wystąpiło omdlenie podczas podawania zastrzyku.
Tak jak w przypadku każdej szczepionki, może nie dojść do wytworzenia ochronnej odpowiedzi
immunologicznej u wszystkich zaszczepionych osób.
Szczepionka Boostrix Polio a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych obecnie lub
ostatnio, a także o lekach, które pacjent planuje przyjmować oraz o otrzymanych ostatnio
szczepionkach.
Szczepionka Boostrix Polio może być podawana w tym samym czasie co niektóre inne szczepionki.
Każda szczepionka będzie podana w inne miejsce.
Szczepionka Boostrix Polio może nie zadziałać właściwie, jeśli zostanie zastosowana w tym samym
czasie co leki zmniejszające zdolność układu immunologicznego (odpornościowego) do zwalczania
infekcji.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tej szczepionki.
Nie wiadomo, czy Boostrix Polio przechodzi do mleka. Lekarz przedyskutuje z pacjentką ewentualne
ryzyko oraz korzyści przy zastosowaniu szczepionki Boostrix Polio w okresie karmienia piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Jest mało prowdopodobne, aby szczepionka Boostrix Polio miała wpływ na zdolność prowadzenia
pojazdów i obsługę maszyn.
Boostrix Polio zawiera neomycynę i polimyksynę
Szczepionka Boostrix Polio zawiera neomycynę i polimyksynę (antybiotyki). Należy powiedzieć
lekarzowi, jeśli wcześniej występowały reakcje alergiczne (uczuleniowe) na te substancje.
Szczepionka Boostrix Polio zawiera kwas para-aminobenzoesowy, fenyloalaninę, sód i potas
Boostrix Polio zawiera kwas para-aminobenzoesowy. Może powodować reakcje alergiczne (możliwe
reakcje typu późnego) i wyjątkowo skurcz oskrzeli.
Szczepionka zawiera 0,0298 mikrograma fenyloalaniny w każdej dawce. Fenyloalanina może być
szkodliwa dla pacjentów z fenyloketonurią (PKU), rzadką chorobą genetyczną, w której fenyloalanina
gromadzi się w organizmie, ponieważ organizm nie usuwa jej w odpowiedni sposób.
Ta szczepionka zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, to znaczy szczepionkę uznaje się
za „wolną od sodu”.
Ta szczepionka zawiera potas, mniej niż 1 mmol (39 mg) potasu na dawkę, to znaczy szczepionkę
uznaje się za „wolną od potasu”.
3. Jak stosować szczepionkę Boostrix Polio
- Szczepionka Boostrix Polio będzie podana jako wstrzyknięcie domięśniowe.
- W żadnym wypadku szczepionki nie można podać donaczyniowo.
- Pacjent otrzyma pojedynczą dawkę szczepionki.
- Lekarz ustali, czy pacjent został wcześniej zaszczepiony przeciwko błonicy, tężcowi, krztuścowi i / lub poliomyelitis.
- Szczepionka Boostrix Polio może zostać zastosowana w przypadku, gdy istnieje podejrzenie zakażenia tężcem z powodu zranienia. Lekarz podejmie także dodatkowe działania takie jak
opatrzenie rany i/lub podanie antytoksyny przeciwtężcowej w celu zmniejszenia ryzyka
wystąpienia choroby.
- Lekarz poinformuje, jeśli konieczne będzie podanie powtórnej dawki szczepionki.
4. Możliwe działania niepożądane
Jak każdy lek, ta szczepionka może powodować działania niepożądane, chociaż nie u każdego one
wystąpią.
Tak jak w przypadku wszystkich szczepionek w postaci wstrzyknięć, istnieje bardzo małe ryzyko (do
1 na 10 000 dawek szczepionki) wystąpienia reakcji alergicznych (anafilaktycznych i
anafilaktoidalnych). Stan taki można rozpoznać na podstawie następujących objawów:
- Wysypka, która może być swędząca lub pęcherzowa,
- Obrzęk okolicy oczu i twarzy,
- Trudności w oddychaniu i połykaniu,
- Nagły spadek ciśnienia krwi i utrata przytomności.Reakcje takie występują zazwyczaj przed opuszczeniem gabinetu lekarskiego. Jednakże, w każdym takim przypadku należy natychmiast skontaktować się z lekarzem.
Działania niepożądane, które występowały w badaniach klinicznych u dzieci w wieku 4 do 8 lat:
Bardzo często(mogą wystąpić częściej niż 1 na 10 dawek szczepionki): ból, zaczerwienienie i obrzęk
w miejscu podania, senność.
Często(mogą wystąpić do 1 na 10 dawek szczepionki): gorączka równa lub wyższa niż 37,5 °C (w
tym gorączka wyższa niż 39 °C), krwawienie, świąd i twardy guzek w miejscu podania, rozległy
obrzęk kończyny, w którą podano szczepionkę, utrata apetytu, rozdrażnienie, ból głowy.
Niezbyt często(mogą wystąpić do 1 na 100 dawek szczepionki): biegunka, nudności, wymioty, ból
brzucha, obrzęk węzłów chłonnych szyjnych, pachowych lub pachwinowych (limfadenopatia),
problemy ze spaniem, apatia, suchość gardła, zmęczenie.
Jednoczesne podawanie ze szczepionką przeciw odrze, śwince i różyczce (MMR) albo odrze, śwince,
różyczce i ospie wietrznej (MMRV) u dzieci w wieku 3 – 6 lat
W badaniach, w których szczepionka Boostrix Polio była podawana w tym samym czasie co
szczepionka MMR lub MMRV, regularnie zgłaszano występowanie wysypki skórnej i zapalenia
górnych dróg oddechowych (w tym wycieku z nosa i bólu gardła). Gorączka, rozdrażnienie,
zmęczenie, utrata apetytu oraz zaburzenia żołądka i jelit (w tym biegunka i wymioty) były zgłaszane z
większą częstością (bardzo często) niż w badaniach, w których podawano tylko szczepionkę Boostrix
Polio.
Działania niepożądane, które występowały w badaniach klinicznych u dorosłych, młodzieży i dzieci w
wieku od 10 lat:
Bardzo często(mogą wystąpić częściej niż 1 na 10 dawek szczepionki): ból, zaczerwienienie i obrzęk
w miejscu podania, zmęczenie, ból głowy.
Często(mogą wystąpić do 1 na 10 dawek szczepionki): gorączka równa lub wyższa niż 37,5 °C,
krwiak, świąd, twardy guzek, uczucie ciepła, zdrętwienie w miejscu podania, ból brzucha, nudności,
wymioty.
Niezbyt często(mogą wystąpić do 1 na 100 dawek szczepionki): gorączka powyżej 39 °C, rozległy
obrzęk kończyny, w którą podano szczepionkę, dreszcze, ból, zawroty głowy, ból stawów i ból mięśni,
świąd, opryszczka wargowa, obrzęk węzłów chłonnych szyjnych, pachowych lub pachwinowych
(limfadenopatia), zmniejszenie apetytu, mrowienie lub zdrętwienie dłoni lub stóp (parestezja),
senność, astma.
Następujące działania niepożądane wystąpiły podczas rutynowego stosowania szczepionki Boostrix
Polio i nie są specyficzne dla żadnej grupy wiekowej: omdlenia lub okresy utraty przytomności lub
braku świadomości, obrzęk twarzy, warg, jamy ustnej, języka lub gardła, który może powodować
trudności z przełykaniem lub oddychaniem (obrzęk naczyniowo-ruchowy), drgawki (z gorączką lub
bez), pęcherze (pokrzywka), nietypowe osłabienie (astenia).
Dodatkowo zgłaszano następujące działania niepożądane podczas badań klinicznych innej szczepionki
przeciw błonicy, tężcowi i krztuścowi (bezkomórkowej) o zmniejszonej zawartości antygenów
GlaxoSmithKline Biologicals (Boostrix):
Działania niepożądane, które występowały w badaniach klinicznych u dzieci w wieku 4 do 8 lat:
Niezbyt często(mogą wystąpić do 1 na 100 dawek szczepionki): zaburzenia uwagi, wydzielina i
świąd oczu, ropienie powiek (zapalenie spojówek), ból.
Działania niepożądane, które występowały w badaniach klinicznych u dorosłych, młodzieży i dzieci w
wieku od 10 lat:
Bardzo często(mogą wystąpić częściej niż 1 na 10 dawek szczepionki): ogólne złe samopoczucie.
Często(mogą wystąpić do 1 na 10 dawek szczepionki): twardy guzek lub ropień w miejscu podania.
Niezbyt często(mogą wystąpić do 1 na 100 dawek szczepionki): zapalenie górnych dróg
oddechowych, ból gardła i trudności w przełykaniu (zapalenie gardła), omdlenie, kaszel, biegunka,
wzmożone pocenie się, wysypka, sztywność stawów, sztywność stawowo-mięśniowa, objawy
grypowe, takie jak gorączka, ból gardła, katar, kaszel i dreszcze.
Po podaniu szczepionek przeciwko tężcowi bardzo rzadko (do 1 na 10 000 dawek szczepionki)
zgłaszano przemijające zapalenie nerwów, powodujące ból, osłabienie i porażenie kończyn, często
obejmujące także klatkę piersiową i twarz (syndrom Guillain-Barré).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane
niewymienione w ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych:
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: 22 49 21 301
Faks: 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać szczepionkę Boostrix Polio
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tej szczepionki po upływie terminu ważności zamieszczonego na opakowaniu
kartonowym oraz na etykiecie ampułko-strzykawki po „EXP”. Termin ważności oznacza ostatni dzień
podanego miesiąca.
Przechowywać w lodówce (2˚C – 8˚C).
Nie zamrażać. Zamrożenie niszczy szczepionkę.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera szczepionka Boostrix Polio
- Substancjami czynnymi szczepionki są:
Toksoid błoniczy
nie mniej niż 2 jednostki międzynarodowe (j.m.) (2,5 Lf)
Toksoid tężcowy
nie mniej niż 20 jednostek międzynarodowych (j.m.) (5 Lf)
Antygeny Bordetella pertussis
Toksoid krztuścowy
8 mikrogramów
Hemaglutynina włókienkowa
8 mikrogramów
Pertaktyna
2,5 mikrograma
Inaktywowany poliowirus
typ 1 (szczep Mahoney)
40 jednostek antygenu D
typ 2 (szczep MEF-1)
8 jednostek antygenu D
typ 3 (szczep Saukett)
32 jednostki antygenu D
adsorbowane na wodorotlenku glinu, uwodnionym (Al(OH) )
0,3 miligrama Al
i na fosforanie glinu (AlPO )
0,2 miligrama Al
namnażany w hodowli komórkowej VERO
Wodorotlenek glinu i fosforan glinu pełnią w tej szczepionce rolę adiuwantów. Adiuwanty to
substancje wchodzące w skład niektórych szczepionek, mające za zadanie przyspieszenie,
wzmocnienie i/lub przedłużenie ochronnego działania szczepionki.
- Pozostałe składniki szczepionki Boostrix Polio to: Medium 199 (zawierające aminokwasy (w tym fenyloalaninę), sole mineralne (w tym sód i potas), witaminy (w tym kwas para- aminobenzoesowy) i inne substancje), chlorek sodu, woda do wstrzykiwań.
Jak wygląda szczepionka Boostrix Polio i co zawiera opakowanie
Zawiesina do wstrzykiwań w ampułko-strzykawce.
Boostrix Polio jest białym, lekko mlecznym płynem w ampułko-strzykawce (0,5 ml).
Szczepionka Boostrix Polio jest dostępna w postaci 1-dawkowej ampułko-strzykawki,
w opakowaniach po 1 lub 10 sztuk, z dołączonymi igłami lub bez igieł.
Nie wszystkie rodzaje opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
GlaxoSmithKline Biologicals S.A.
rue de l’Institut 89
1330 Rixensart, Belgia
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego
Obszaru Gospodarczego pod następującymi nazwami:
Boostrix Polio:Austria, Belgia, Bułgaria, Czechy, Dania, Finlandia, Grecja, Hiszpania, Holandia,
Islandia, Litwa, Luksemburg, Łotwa, Niemcy, Norwegia, Polska, Portugalia, Słowacja, Słowenia,
Szwecja, Węgry
Boostrix Tetra:Francja
IPV-Boostrix:Irlandia, Malta
Polio Boostrix:Włochy
Boostrix IPV:Rumunia
Data ostatniej aktualizacji ulotki:04/2023
Inne źródła informacji
Szczegółowa informacja o tym leku jest dostępna na stronie internetowej: Urzędu Rejestracji
Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
-------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Przed zastosowaniem szczepionka powinna osiągnąć temperaturę pokojową. Ampułko-strzykawką
należy mocno wstrząsnąć w celu uzyskania jednorodnej mętnej, białej zawiesiny.
Przed podaniem, szczepionkę należy ocenić wzrokowo pod kątem występowania jakichkolwiek
obcych cząstek i (lub) zmiany wyglądu fizycznego szczepionki. W przypadku ich stwierdzenia, nie
należy podawać szczepionki.
Instrukcje dotyczące ampułko-strzykawki
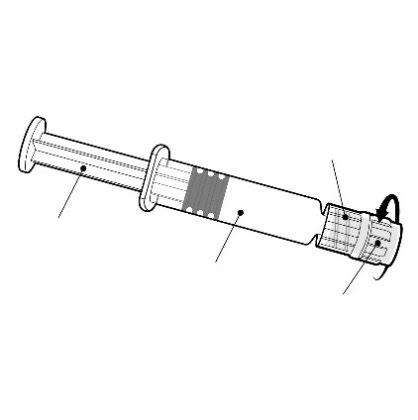
Należy trzymać ampułko-strzykawkę za
korpus, a nie za tłok.
Należy odkręcić nasadkę ampułko-
strzykawki poprzez przekręcenie jej w
kierunku przeciwnym do ruchu wskazówek
zegara.
Adapter
typu Luer Lock
Tłok
Korpus
Nasadka
Należy przymocować igłę do ampułko-
strzykawki poprzez przyłączenie nasadki igły do
adaptera Luer Lock (ang. Luer Lock Adaptor,
LLA) i obrócenie jej ćwierć obrotu w kierunku
zgodnym z ruchem wskazówek zegara, do chwili
aż poczuje się zablokowanie igły.
Nie wolno wyciągać tłoka z korpusu ampułko-
strzykawki. Jeśli tak się stanie, nie należy
podawać szczepionki.
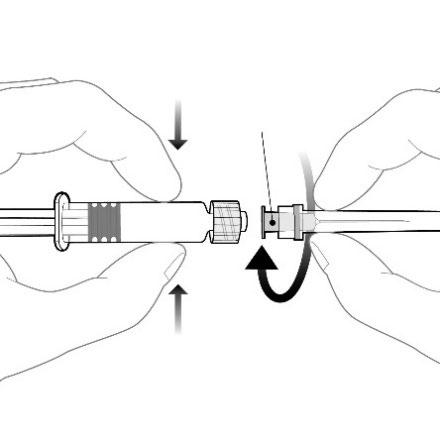
Nasadka igły
Usuwanie
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z
lokalnymi przepisami.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterGlaxoSmithKline Biologicals S.A.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Boostrix PolioPostać farmaceutyczna: Zawiesina, 0,5 mlSubstancja czynna: diphtheria-pertussis-poliomyelitis-tetanusProducent: Sanofi-Aventis Zrt.Wymaga receptyPostać farmaceutyczna: Zawiesina, 1 dawka (0,5 ml)Substancja czynna: diphtheria-pertussis-poliomyelitis-tetanusProducent: GlaxoSmithKline Biologicals S.A.Wymaga receptyPostać farmaceutyczna: Proszek, 32 jednostek antygenu D + 10 mcg + nie mniej niż 40 j.m. + 8 jednostek antygenu D + 40 jednostek antygenu D + nie mniej niż 30 j.m. + 25 mcg + 25 mcgSubstancja czynna: diphtheria-pertussis-poliomyelitis-tetanusWymaga recepty
Odpowiedniki Boostrix Polio w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Boostrix Polio – Hiszpania
Odpowiednik Boostrix Polio – Ukraina
Lekarze online w sprawie Boostrix Polio
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Boostrix Polio – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














