

Vagirux

Consulta con un médico sobre la receta médica de Vagirux

Cómo usar Vagirux
Hoja de instrucciones del paquete: información para el usuario
Atención! Conservar la hoja de instrucciones. Información en el embalaje primario en idioma extranjero.
Vagirux, 10 microgramos, tabletas vaginales
Estradiol
Es importante leer atentamente el contenido de la hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para una persona. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones
- 1. Qué es Vagirux y para qué se utiliza
- 2. Información importante antes de usar Vagirux
- 3. Cómo usar Vagirux
- 4. Posibles efectos adversos
- 5. Cómo conservar Vagirux
- 6. Contenido del embalaje y otra información
1. Qué es Vagirux y para qué se utiliza
Vagirux contiene estradiol.
- El estradiol es una hormona femenina.
- Pertenece a un grupo de hormonas llamadas estrógenos.
- Es idéntico al estradiol producido por los ovarios de la mujer.
Vagirux pertenece a un grupo de medicamentos llamados terapia hormonal sustitutiva (THS) para administración vaginal.
El medicamento Vagirux se utiliza paraaliviar los síntomas de la menopausia que ocurren en la vagina, como la sequedad o la irritación. En terminología médica, este fenómeno se conoce como "inflamación vaginal atrófica". Está causado por la disminución de los niveles de estrógenos en el cuerpo y ocurre naturalmente después de la menopausia.
El medicamento Vagirux actúareemplazando el estrógeno que produce el ovario de la mujer.
El medicamento se administra vaginalmente, por lo que la hormona se libera allí donde es necesaria. Esto puede aliviar la sensación de incomodidad en la vagina.
2. Información importante antes de usar Vagirux
Historial médico y controles regulares
El uso de la THS conlleva un riesgo que debe ser considerado cuando la paciente decide si debe usar o continuar con la terapia hormonal sustitutiva.
La experiencia en el tratamiento de mujeres en la menopausia prematura (debido a la insuficiencia ovárica o a una cirugía) es limitada. Si la paciente está experimentando una menopausia prematura, el riesgo asociado con el uso de la THS puede ser diferente. Debe hablar con su médico.
Antes de iniciar (o reanudar) el uso de la THS, el médico debe realizar un historial médico, incluyendo el historial familiar. El médico puede decidir realizar un examen, como un examen de senos y (o) un examen ginecológico, si es necesario.
Si la paciente comienza a usar Vagirux, debe consultar a su médico al menos una vez al año. Durante las visitas de control, debe discutir con su médico los beneficios y los riesgos de continuar usando Vagirux.
Las pacientes deben realizar exámenes de detección de senos de acuerdo con las recomendaciones de su médico.
Cuándo no usar Vagirux
En caso de que se produzca alguno de los trastornos o dudas mencionados a continuación, debe consultar a un médicoantes de iniciar el uso de Vagirux.
No use Vagirux si la paciente:
- ha sido diagnosticada con, ha tenido en el pasado o se sospecha que tiene cáncer de seno;
- ha sido diagnosticada con, ha tenido en el pasado o se sospecha que tiene tumor dependiente de estrógenos, como el cáncer de endometrio (cáncer de la capa mucosa del útero);
- ha tenido sangrado vaginal inexplicable;
- ha tenido engrosamiento excesivo de la capa mucosa del útero(hiperplasia endometrial) que no ha sido tratado;
- ha sido diagnosticada con o ha tenido en el pasado coágulos de sangre en las venas(trombosis), como la trombosis venosa profunda en las extremidades inferiores o la embolia pulmonar;
- tiene un trastorno de coagulación de la sangre(como la deficiencia de proteína C, proteína S o antitrombina);
- ha tenido en el pasado o tiene actualmente una enfermedad causada por coágulos de sangre en las arterias, como infarto de miocardio, accidente cerebrovascularo angina de pecho;
- ha sido diagnosticada con o ha tenido en el pasado enfermedad hepáticay los resultados de las pruebas hepáticas no han vuelto a la normalidad;
- ha sido diagnosticada con una enfermedad rara de la sangrellamada porfiria, que se transmite de generación en generación (hereditaria).
- ha tenido alergiaa estradiolo a alguno de los demás componentes de Vagirux (enumerados en el punto 6);
Si alguna de las condiciones mencionadas anteriormente se produce por primera vez mientras se está usando Vagirux, debe dejar de usarlo de inmediato y ponerse en contacto con su médico lo antes posible.
Precauciones y advertencias
Antes de iniciar el tratamiento, debe informar a su médico si actualmente tiene o ha tenido en el pasado alguna de las siguientes enfermedades, ya que pueden volver a ocurrir o empeorar mientras se está usando Vagirux. En estos casos, el médico puede considerar necesario realizar controles más frecuentes.
- miomas uterinos;
- endometriosis (crecimiento de la capa mucosa del útero fuera del útero) o hiperplasia endometrial (crecimiento excesivo de la capa mucosa del útero) en el pasado;
- aumento del riesgo de coágulos de sangre (véase "Coágulos de sangre en las venas (trombosis)");
- aumento del riesgo de cáncer de seno (cáncer de seno en la madre, hermana o abuela);
- hipertensión arterial;
- enfermedad hepática, como un tumor benigno del hígado;
- diabetes;
- colelitiasis;
- migraña o dolores de cabeza severos;
- enfermedad del sistema inmunológico que afecta a muchos órganos, lupus eritematoso sistémico;
- epilepsia;
- asma;
- enfermedad que afecta la membrana del tímpano y la audición, otosclerosis;
- niveles muy altos de triglicéridos en la sangre;
- retención de líquidos debido a una disfunción cardíaca o renal;
- edema angioneurótico hereditario o adquirido.
Debe dejar de usar Vagirux y ponerse en contacto con su médico de inmediatosi se produce alguno de los siguientes estados mientras se está usando la THS:
- aparición de alguna de las enfermedades mencionadas en el punto "Cuándo no usar Vagirux" anteriormente;
- icoloración amarilla de la piel y los ojos (ictericia). Puede ser un signo de enfermedad hepática;
- hinchazón de la cara, la lengua y (o) la garganta y (o) dificultad para tragar o urticaria junto con dificultad para respirar, que sugieren edema angioneurótico;
- aumento significativo de la presión arterial (síntomas como dolor de cabeza, sensación de cansancio y mareo);
- dolor de cabeza tipo migraña que aparece por primera vez;
- si la paciente está embarazada;
- si la paciente experimenta síntomas de coágulos de sangre, como:
- dolor y hinchazón en las extremidades inferiores,
- dolor súbito en el pecho,
- dificultad para respirar. Para más información, véase "Coágulos de sangre en las venas (trombosis)".
Advertencia:Vagirux no es un medicamento anticonceptivo. Si han pasado menos de 12 meses desde la última menstruación o la paciente tiene menos de 50 años, puede ser necesario usar un método adicional de anticoncepción. Debe consultar a su médico.
THS y cáncer
Hiperplasia endometrial (engrosamiento excesivo de la capa mucosa del útero) y cáncer de endometrio
El uso a largo plazo de la THS en forma de tabletas que contienen solo estrógeno puede aumentar el riesgo de desarrollar cáncer de endometrio (capa mucosa del útero).
No se sabe si existe un riesgo similar durante el uso repetido o prolongado (más de un año) de Vagirux. Sin embargo, Vagirux se absorbe muy poco en la sangre y, por lo tanto, no es necesario agregar progestágeno.
Sangradoo manchadono es usualmente una causa de preocupación, pero debe consultar a su médico. Puede ser un signo de hiperplasia endometrial.
Los riesgos descritos se refieren a medicamentos usados en la terapia hormonal sustitutiva (THS) que se absorben en la sangre. Vagirux se usa localmente en la vagina y su absorción en la sangre es muy baja. Es menos probable que las afecciones mencionadas se agraven o reaparezcan mientras se usa Vagirux, pero si tiene dudas, debe consultar a su médico.
Cáncer de seno
Los datos indican que el uso de Vagirux no aumenta el riesgo de cáncer de seno en mujeres que nunca han tenido cáncer de seno.
No se sabe si Vagirux puede usarse de manera segura en mujeres que han tenido cáncer de seno.
Debe examinar regularmente los senos. Debe ponerse en contacto con su médico si nota alguno de los siguientes cambios:
- hundimiento de la piel,
- cambios en el pezón,
- presencia de bultos que son visibles o palpables.
Además, se recomienda realizar exámenes de detección de senos de acuerdo con las recomendaciones de su médico.
Cáncer de ovario
El cáncer de ovario es raro, mucho menos común que el cáncer de seno. El uso de la THS que solo contiene estrógeno se asocia con un aumento leve del riesgo de cáncer de ovario.
Comparación
El riesgo de cáncer de ovario depende de la edad. Por ejemplo, en mujeres de 50 a 54 años que no usan la THS, el cáncer de ovario se diagnostica en un período de 5 años en aproximadamente 2 de cada 2000 mujeres. En mujeres que han usado la THS durante 5 años, ocurre en aproximadamente 3 de cada 2000 mujeres que la usan (es decir, aproximadamente 1 caso adicional).
Efecto de la THS en el corazón y la circulación
Coágulos de sangre en las venas (trombosis venosa)
El riesgo de desarrollar coágulos de sangre en las venases de 1,3 a 3 veces mayor en mujeres que usan la THS en comparación con las que no la usan, especialmente durante el primer año de uso.
La formación de coágulos de sangre puede tener consecuencias graves y, si se desplazan a los pulmones, pueden causar dolor en el pecho, dificultad para respirar, pérdida de conciencia e incluso la muerte.
El riesgo de coágulos de sangre en las venas es mayor si la paciente es mayor o si alguna de las siguientes situaciones se aplica a la paciente. Debe informar a su médico si alguna de las siguientes situaciones se aplica a la paciente:
- la paciente no puede caminar durante un período prolongado debido a una operación importante, lesión o enfermedad (véase también el punto 3, "Si se planea una operación");
- la paciente tiene un índice de masa corporal (IMC) mayor de 30 kg/m2;
- la paciente tiene trastornos tromboembólicos que requieren la ingesta a largo plazo de medicamentos para prevenir la formación de coágulos de sangre;
- la paciente o algún familiar cercano ha tenido coágulos de sangre en las extremidades inferiores, los pulmones u otros órganos en el pasado;
- la paciente tiene lupus eritematoso sistémico;
- se ha diagnosticado cáncer.
Si se producen síntomas de coágulos de sangre, véase "Debe dejar de usar Vagirux y ponerse en contacto con su médico de inmediato".
Comparación
En mujeres de 50 a 59 años que no usan la THS, el número de casos de coágulos de sangre en las venas en un período de 5 años se estima en 4 a 7 por cada 1000 mujeres.
En mujeres de 50 a 59 años que usan la THS que solo contiene estrógeno durante más de 5 años, el número de casos es de 5 a 8 por cada 1000 (es decir, 1 caso adicional).
Enfermedad cardíaca (infarto de miocardio)
En mujeres que usan la THS que solo contiene estrógeno, no se produce un aumento del riesgo de desarrollar enfermedad cardíaca.
Accidente cerebrovascular
El riesgo de sufrir un accidente cerebrovascular es aproximadamente 1,5 veces mayor en mujeres que usan la THS en comparación con las que no la usan. El número de casos adicionales de accidente cerebrovascular causados por el uso de la THS aumenta con la edad.
Comparación
En mujeres de 50 a 59 años que no usan la THS, el número de casos de accidente cerebrovascular en un período de 5 años se estima en 8 por cada 1000 mujeres. En mujeres de 50 a 59 años que usan la THS, el número de casos en un período de 5 años es de 11 por cada 1000 mujeres (es decir, 3 casos adicionales).
Otras afecciones
La THS no previene la pérdida de memoria. El riesgo de pérdida de memoria probable puede ser ligeramente mayor en mujeres que comienzan a usar la THS a una edad superior a 65 años. Debe consultar a su médico.
Vagirux y otros medicamentos
Debe informar a su médico o farmacéutico sobre todos los medicamentos que esté usando actualmente o ha usado recientemente, incluyendo aquellos que se venden sin receta, medicamentos a base de hierbas o otros productos naturales.
La probabilidad de interacción con otros medicamentos es baja, ya que Vagirux se usa localmente en la vagina. Vagirux puede afectar otros tratamientos locales usados en la vagina.
Embarazo y lactancia
Vagirux está indicado solo para mujeres en la menopausia. Si la paciente queda embarazada, debe dejar de usar Vagirux y ponerse en contacto con su médico.
Conducción de vehículos y uso de máquinas
No se conocen efectos de Vagirux en la conducción de vehículos o el uso de máquinas.
3. Cómo usar Vagirux
Este medicamento debe usarse siempre según las indicaciones de su médico. En caso de dudas, debe consultar a su médico o farmacéutico.
Uso del medicamento
- El uso de Vagirux puede iniciarse en cualquier día.
- Para uso vaginal exclusivo. No debe tomar las tabletas por vía oral.
- La tableta vaginal debe insertarse en la vagina con el aplicador.
La "INSTRUCCIÓN DE USO" al final de esta hoja de instrucciones contiene instrucciones detalladas. Antes de usar Vagirux, debe leer atentamente la instrucción.
El aplicador de tabletas vaginales está diseñado para uso múltiple hasta 24 veces para una paciente (una tableta por aplicación). Después de esto, debe desechar el aplicador con los residuos domésticos. No debe usar aplicadores que muestren signos visibles de daño.
Qué dosis de Vagirux debe usar?
- Durante las primeras 2 semanas, debe usar una tableta vaginal al día.
- Después de esto, debe usar una tableta vaginal dos veces a la semana. Debe dejar un intervalo de 3 a 4 días entre las dosis.
Información general sobre el tratamiento de los síntomas de la menopausia
- El médico determina la dosis más baja de Vagirux que sea efectiva para tratar los síntomas durante el período más corto posible. Debe consultar a su médico si la dosis recomendada parece demasiado alta o insuficiente.
- El tratamiento debe continuar solo si los beneficios superan los riesgos. Debe hablar con su médico sobre esto.
Uso de una dosis mayor de la recomendada de Vagirux
- En caso de que se ingiera una dosis mayor de la recomendada de Vagirux, debe ponerse en contacto con su médico o farmacéutico.
- Vagirux está diseñado para uso local en la vagina. La dosis de estradiol es tan baja que se necesitaría una cantidad significativa de tabletas para alcanzar la dosis usualmente usada en el tratamiento oral.
Olvido de una dosis de Vagirux
- En caso de que se olvide una dosis, debe usar la tableta olvidada lo antes posible.
- No debe usar una dosis doble para compensar la dosis olvidada.
Interrupción del uso de Vagirux
No debe interrumpir el tratamiento con Vagirux sin consultar a su médico. El médico explicará las consecuencias de interrumpir el tratamiento y discutirá otras posibles opciones de tratamiento.
Si se planea una operación
Si se planea una operación, la paciente debe informar al cirujano de que está usando Vagirux. Puede ser necesario interrumpir el uso de Vagirux 4 a 6 semanas antes de la operación para reducir el riesgo de coágulos de sangre (véase el punto 2, "Coágulos de sangre en las venas (trombosis)").
Antes de reanudar el uso de Vagirux, debe consultar a su médico.
En caso de dudas adicionales sobre el uso de este medicamento, debe consultar a su médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, Vagirux puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
En mujeres que usan la THS en forma de medicamentos que se absorben en la sangre, se han informado con más frecuencia los siguientes trastornos en comparación con las que no usan la THS. Los siguientes riesgos son menos probable que se apliquen a medicamentos administrados vaginalmente, como Vagirux:
- cáncer de ovario;
- coágulos de sangre en las venas de las piernas o los pulmones (enfermedad tromboembólica venosa);
- accidente cerebrovascular;
- pérdida de memoria probable, si se inicia el uso de la THS a una edad superior a 65 años.
Para obtener más información, véase el punto 2, "Información importante antes de usar Vagirux".
Frecuente: puede afectar hasta 1 de cada 10 mujeres
- dolor de cabeza;
- dolor abdominal;
- sangrado vaginal, flujo o malestar.
Poco frecuente: puede afectar hasta 1 de cada 100 mujeres
- infecciones por hongos en los genitales;
- malestar general (náuseas);
- erupción cutánea;
- aumento de peso;
- sofocos;
- hipertensión arterial.
Muy raro: puede afectar hasta 1 de cada 10,000 mujeres
- diarrea;
- retención de líquidos;
- empeoramiento de la migraña;
- hipersensibilidad generalizada (por ejemplo, reacción anafiláctica o choque anafiláctico).
Se han informado los siguientes efectos adversos durante el uso de estrógenos administrados por vía sistémica:
- colelitiasis;
- diferentes trastornos de la piel:
- decoloración de la piel, especialmente en la cara o el cuello, llamada melasma;
- erupción cutánea con enrojecimiento o dolor;
- erupción cutánea con enrojecimiento característico o dolor (eritema multiforme).
Informes de efectos adversos
Si se producen efectos adversos, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos pueden informarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Sanidad, Consumo y Bienestar Social, C/ Alcalá 56, 28071 Madrid, teléfono: +34 91 596 34 00, fax: +34 91 596 34 01, sitio web: https://www.aemps.gob.es/.
Al informar los efectos adversos, se pueden recopilar más datos sobre la seguridad del medicamento.
5. Cómo conservar Vagirux
El medicamento debe conservarse en un lugar donde no pueda ser visto o alcanzado por los niños.
Conservar en el embalaje original para protegerlo de la luz.
No use este medicamento después de la fecha de caducidad impresa en el embalaje. La fecha de caducidad es el último día del mes indicado.
No deseche los medicamentos por el desagüe o en los contenedores de residuos domésticos. Debe preguntar a su farmacéutico cómo desechar los medicamentos que ya no se necesitan. Este comportamiento ayudará a proteger el medio ambiente. Este medicamento puede representar un riesgo para el medio ambiente acuático.
6. Contenido del embalaje y otra información
Qué contiene Vagirux
- El principio activo de Vagirux es estradiol. Cada tableta vaginal contiene estradiol hemihidratado equivalente a 10 microgramos de estradiol.
- Los demás componentes son: hipromelosa, lactosa monohidratada, almidón de maíz y estearato de magnesio. Cubierta de la tableta: hipromelosa y macrogol.
Cómo es Vagirux y qué contiene el embalaje
Las tabletas vaginales son blancas, redondas, recubiertas con la letra "E" grabada en un lado, de aproximadamente 6 mm de diámetro.
Tamaños del embalaje:
18 tabletas vaginales en blister de PVC/PVDC/Aluminio con aplicador vaginal para uso múltiple en bolsa de protección. Todo en una caja de cartón.
Para obtener más información detallada, debe consultar al titular de la autorización de comercialización o al importador paralelo.
Título de la autorización de comercialización en Grecia, país de exportación:
Gedeon Richter Plc.
Gyömrői út 19-21.
H-1103 Budapest
Hungría
Fabricante:
Haupt Pharma Münster GmbH
Schleebrüggenkamp 15
48159 Münster
Alemania
Gedeon Richter Plc.
Gyömrői út 19-21.
H-1103 Budapest
Hungría
Importador paralelo:
InPharm Sp. z o.o.
ul. Strumykowa 28/11
03-138 Varsovia
Reempaquetado por:
InPharm Sp. z o.o. Services sp. k.
ul. Chełmżyńska 249
04-458 Varsovia
Número de autorización en Grecia, país de exportación:20658/12-03-2021
Número de autorización de importación paralela:81/24
Fecha de aprobación de la hoja de instrucciones: 28.02.2024
Este medicamento está autorizado para su comercialización en los estados miembros del Espacio Económico Europeo bajo los siguientes nombres:
Hungría
Vagirux 10 microgramos tabletas vaginales
Austria
Revellfem 10 microgramos tabletas vaginales
Liechtenstein
Revellfem
República Checa
Vagirux
Eslovaquia
Vagirux 10 microgramos tabletas vaginales
Dinamarca
Revellfem
Islandia
Revellfem
Noruega
Vagirux
Finlandia
Vagirux
Suecia
Vagirux
Estonia
VAGIRUX
Letonia
Vagirux 10 microgramos tabletas vaginales
Lituania
VAGIRUX 10 microgramos tabletas vaginales
Croacia
Vagirux 10 microgramos tabletas vaginales
Eslovenia
Vagirux 10 microgramos tabletas vaginales
Irlanda
Vagirux
Malta
Vagirux 10 microgramos tabletas vaginales
España
Vagirux 10 microgramos tabletas vaginales
Italia
Vagirux
Polonia
Vagirux
[Información sobre la marca registrada]
INSTRUCCIONES DE USO
Cómo usar Vagirux
- 1. Retire la cubierta protectora del aplicador. Abra desde el lado que se muestra en la figura.
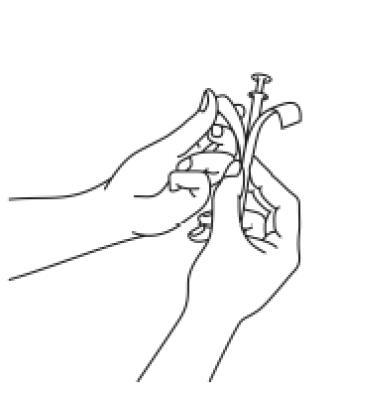
- 2. Sostenga el tubo, tire del émbolo del aplicador hasta que se detenga. Saque una tableta vaginal del blister separado y colóquela firmemente en el mango (extremo ancho) del tubo del aplicador.
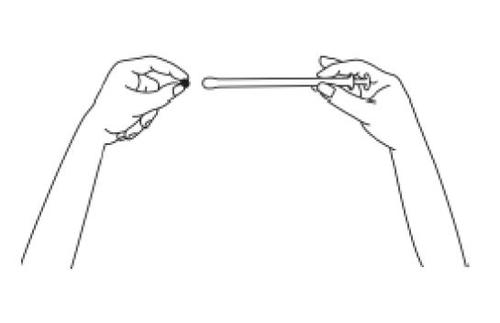
- 3. Introduzca el aplicador en la vagina con cuidado, hasta que sienta resistencia (8-10 cm).
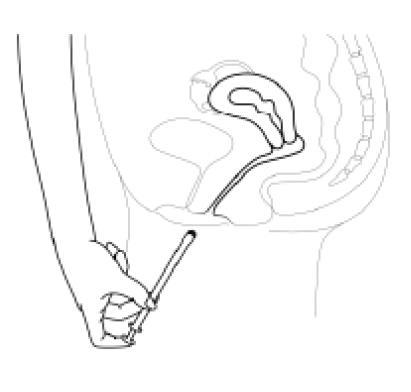
- 4. Para liberar la tableta, presione el émbolo hasta que sienta resistencia. La tableta se adhirirá inmediatamente a la pared vaginal. La tableta no se caerá cuando esté de pie o caminando.
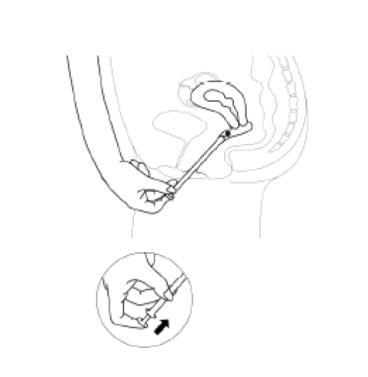
- 5. Después de cada uso, antes del siguiente uso, debe limpiar el aplicador según las siguientes instrucciones de limpieza:
- Retire el émbolo del aplicador.
- Limpie tanto el tubo como el émbolo con un jabón suave y enjuague bien con agua tibia del grifo. Enjuague tanto la superficie interna como la externa del tubo.
- Si es necesario, retire cualquier exceso de agua del tubo y del émbolo sacudiéndolos brevemente.
- Deje que el tubo y el émbolo se sequen al aire en una superficie limpia (por ejemplo, en una toalla de papel).
- Vuelva a introducir el émbolo en el tubo del aplicador para su uso posterior.
- 6. Debe usar el aplicador hasta que se acabe el embalaje (18 veces), y luego desechar el aplicador con los residuos domésticos.
- País de registro
- Principio activo
- Requiere recetaSí
- Titular de la autorización de comercialización (TAC, MAH)Gedeon Richter Plc.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a VagiruxForma farmacéutica: Gel, 0.5 mgPrincipio activo: EstradiolFabricante: Orion CorporationRequiere recetaForma farmacéutica: Gel, 1 mgPrincipio activo: EstradiolFabricante: Orion CorporationRequiere recetaForma farmacéutica: Gel, 1 mg/gPrincipio activo: EstradiolRequiere receta
Alternativas a Vagirux en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Vagirux en España
Alternativa a Vagirux en Ucrania
Médicos online para Vagirux
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Vagirux – sujeta a valoración médica y normativa local.










