
Prilotekal

Consulta con un médico sobre la receta médica de Prilotekal

Cómo usar Prilotekal
Hoja de instrucciones del paquete: información para el usuario
Prilotekal
20 mg/ml, solución para inyección
Clorhidrato de prilocaína
Debe leer el contenido de la hoja de instrucciones antes de tomar el medicamento, ya que contiene información importante para el paciente.
Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
Debe consultar a un médico o farmacéutico si tiene alguna duda adicional.
Si el paciente experimenta algún efecto adverso, incluidos los efectos adversos no mencionados en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Prilotekal y para qué se utiliza
- 2. Información importante antes de tomar Prilotekal
- 3. Cómo tomar Prilotekal
- 4. Posibles efectos adversos
- 5. Cómo conservar Prilotekal
- 6. Contenido del paquete y otra información
1. Qué es Prilotekal y para qué se utiliza
Prilotekal 20 mg/ml solución para inyección es un tipo de medicamento llamado anestésico local,
pertenece al grupo de los amidas y es una solución para inyección. Prilotekal solución para inyección se
utiliza para anestesiar ciertas partes del cuerpo y prevenir el dolor durante las operaciones en personas
adultas.
Prilotekal se inyecta en la parte inferior de la columna vertebral del paciente. Ayuda a detener el dolor
rápidamente en el paciente desde la cintura hacia abajo durante un período limitado (procedimientos quirúrgicos de corta duración).
2. Información importante antes de tomar Prilotekal
Cuándo no tomar Prilotekal
si el paciente es alérgico (hipersensible) al clorhidrato de prilocaína, otros medicamentos anestésicos
locales del grupo de las amidas o a cualquiera de los demás componentes de este medicamento (enumerados en el punto
- 6), si el paciente tiene problemas graves de conducción cardíaca, si el paciente tiene anemia aguda, si el paciente tiene insuficiencia cardíaca descompensada, si el paciente tiene choque hipovolémico y cardiogénico, si el paciente tiene metahemoglobinemia congénita o adquirida, si el paciente tiene contraindicaciones generales o específicas para la técnica de anestesia subaracnoidea. No se debe administrar Prilotekal en un vaso sanguíneo. No se debe utilizar Prilotekal en niños menores de 6 meses.
Precauciones y advertencias
En caso de cualquier problema mencionado a continuación, debe informar a su médico antesde tomar este medicamento.
si el paciente ha experimentado alguna vez una reacción adversa a un medicamento anestésico
si el paciente tiene una infección de la piel en el sitio de inyección propuesto o en sus alrededores
si el paciente padece alguna de las siguientes afecciones:
- enfermedades del sistema nervioso central, como: meningitis, polio y problemas con la médula espinal debido a la anemia,
- dolor de cabeza severo,
- tumores cerebrales, de la médula espinal o cualquier otro,
- tuberculosis de la médula espinal,
- lesión reciente de la médula espinal,
- presión arterial muy baja o volumen de sangre bajo,
- problemas de coagulación de la sangre,
- porfiria aguda,
- líquido en los pulmones,
- sepsis (infección de la sangre). si el paciente tiene enfermedad cardíaca (incluyendo bloqueo cardíaco total o parcial, insuficiencia cardíaca descompensada, arritmia) si el paciente tiene problemas hepáticos o renales si el paciente tiene una afección neurológica, como esclerosis múltiple, parálisis, parálisis transversa o trastornos neuromusculares si el paciente tiene debilidad general del cuerpo. La anestesia espinal solo debe ser administrada por un médico con la experiencia y conocimientos necesarios. El médico es responsable de tomar las medidas necesarias para evitar la inyección en un vaso sanguíneo y tener la capacidad de reconocer y tratar los efectos adversos.
Niños y adolescentes
No se recomienda el uso de Prilotekal en niños y adolescentes. La eficacia y seguridad de Prilotekal
en niños y adolescentes no han sido establecidas. No hay datos disponibles al respecto.
El uso de Prilotekal en niños menores de 6 meses está contraindicado debido al mayor riesgo de desarrollar metahemoglobinemia.
Prilotekal y otros medicamentos
Debe informar a su médico sobre todos los medicamentos que esté tomando actualmente o recientemente, así
como sobre los medicamentos que planea tomar, incluyendo los medicamentos que se venden sin receta.
Especially si está tomando medicamentos para tratar un ritmo cardíaco irregular (medicamentos antiarrítmicos de clase III) y analgésicos.
Embarazo, lactancia
Si la paciente está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener
un hijo, debe consultar a su médico, quien decidirá si debe recibir Prilotekal en inyección o no. No se debe administrar prilocaína para anestesia local o regional durante el parto.
No se sabe si la prilocaína pasa a la leche materna. La lactancia materna puede reanudarse después de 24 horas de la administración del medicamento.
Conducción de vehículos y uso de máquinas
No debe conducir vehículos ni operar máquinas, ya que Prilotekal puede afectar las reacciones y la coordinación muscular durante un período de tiempo.
Prilotekal contiene sodio
El medicamento contiene menos de 1 mmol (23 mg) de sodio por dosis (dosis máxima equivalente a 4
ml de solución para inyección de Prilotekal), es decir, el medicamento se considera "libre de sodio".
3. Cómo tomar Prilotekal
Este medicamento se administra al paciente por un médico que determinará la dosis adecuada para el paciente. La dosis habitual en adultos es de 40-60 mg de clorhidrato de prilocaína (2-3 ml de Prilotekal);
la dosis máxima es de 80 mg de clorhidrato de prilocaína (4 ml de Prilotekal).
El médico inyecta Prilotekal en la parte inferior de la columna vertebral del paciente, y el paciente adopta una posición sentada o acostada.
Prilotekal no se recomienda para su uso en niños y adolescentes. La seguridad y eficacia de Prilotekal
en niños y adolescentes no han sido evaluadas. El uso de Prilotekal en niños menores de 6 meses está contraindicado debido al mayor riesgo de desarrollar metahemoglobinemia.
En pacientes con mal estado general y enfermedades concomitantes (por ejemplo, enfermedad vascular, arteriosclerosis, neuropatía diabética y mal funcionamiento hepático o renal), se recomienda una dosis reducida.
En caso de deterioro de la función renal o hepática, se recomienda el uso de dosis más bajas.
Prilotekal se inyecta por vía subaracnoidea.
El equipo, los medicamentos y el personal capacitado para actuar en caso de emergencia deben estar disponibles de inmediato. En casos raros, se han informado reacciones graves después de la administración de medicamentos anestésicos locales, incluso en ausencia de hipersensibilidad en la historia del paciente individual.
Sobredosis de Prilotekal
Es poco probable que el paciente reciba demasiado Prilotekal si se administra mediante un médico experimentado en anestesia espinal. Sin embargo, si se inyecta accidentalmente una dosis directamente en la sangre, el paciente puede experimentar problemas de visión o audición, temblor muscular, convulsiones, ataques epilépticos y pérdida de conciencia en un corto período de tiempo. En cualquier caso, si el paciente recibe Prilotekal, el equipo de tratamiento debe estar disponible para tratar una posible sobredosis.
Si tiene alguna duda adicional sobre el uso de este medicamento, debe consultar a un médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, Prilotekal puede causar efectos adversos, aunque no todos los pacientes los experimentarán.
Al igual que con todos los medicamentos anestésicos locales, pueden ocurrir con frecuencia una disminución de la presión arterial y una frecuencia cardíaca más lenta.
El paciente puede experimentar náuseas, tener presión arterial baja o frecuencia cardíaca lenta. Otros posibles efectos adversos incluyen: dolor de cabeza después de la operación, vómitos y dificultad para orinar.
Los posibles efectos adversos son:
Muy frecuentes: pueden ocurrir en más de 1 de cada 10 personas
Presión arterial baja, náuseas.
Frecuentes: pueden ocurrir en 1 de cada 10 personas
Parestesias, mareos, vómitos.
Poco frecuentes: pueden ocurrir en 1 de cada 100 personas
Convulsiones, parestesias alrededor de la boca, pérdida de conciencia, temblor, sensación de entumecimiento de la lengua, problemas para hablar, problemas para escuchar, tinnitus, problemas para ver, dolor de espalda, debilidad muscular transitoria. Frecuencia cardíaca lenta, presión arterial elevada.
Raros: pueden ocurrir en 1 de cada 1.000 personas
Metahemoglobinemia, cianosis, shock anafiláctico, reacciones anafilácticas, reacciones alérgicas,
picazón.
Inflamación de la pia mater, neuropatía, cambios en los nervios periféricos.
Visión doble. Paro cardíaco, frecuencia cardíaca irregular. Depresión de la función respiratoria.
Es poco probable que la solución para inyección de Prilotekal cause efectos adversos graves, a menos que se administre accidentalmente de manera incorrecta o se use junto con otros medicamentos anestésicos locales. En tal caso, pueden ocurrir: entumecimiento de la lengua, mareo, mareos, temblor y convulsiones. En casos muy raros, el uso de prilocaína puede causar: infarto de miocardio, problemas para respirar, pérdida de sensación en las partes inferiores del cuerpo y reacciones alérgicas, que pueden causar erupciones, hinchazón o presión arterial muy baja.
Un efecto adverso raro pero grave en la anestesia espinal es el bloqueo espinal alto o total, junto con la depresión de la función cardiovascular y respiratoria.
Notificación de efectos adversos
Si ocurren cualquier efecto adverso, incluidos los efectos adversos no mencionados en la hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos se pueden notificar directamente al Departamento de Vigilancia de Medicamentos de la Agencia Reguladora de Medicamentos, Calle Jerozolimskie 181C, 02-222 Varsovia, Tel.: +48 22 49 21 301, Fax: +48 22 49 21 309,
Página web: https://smz.ezdrowie.gov.pl
Los efectos adversos también se pueden notificar al titular de la autorización de comercialización.
La notificación de efectos adversos puede ayudar a recopilar más información sobre la seguridad del medicamento.
5. Cómo conservar Prilotekal
El medicamento debe conservarse en un lugar donde no pueda ser visto ni alcanzado por los niños.
No debe usar Prilotekal después de la fecha de caducidad indicada en los frascos y el paquete exterior. La fecha de caducidad (EXP) es el último día del mes dado.
No debe conservar a una temperatura superior a 25°C. No debe conservar en el refrigerador ni congelar.
Debe conservar en el paquete original para protegerlo de la luz.
Debe usar inmediatamente después de abrir por primera vez.
No debe usar Prilotekal si se observa que la solución no es clara y libre de partículas.
Debe eliminar cualquier residuo del producto o desecho según las regulaciones locales. Debido a la restricción de uso en el hospital, la eliminación de los residuos del medicamento se realiza directamente por el hospital. Este procedimiento ayudará a proteger el medio ambiente.
6. Contenido del paquete y otra información
Qué contiene Prilotekal?
El principio activo del medicamento es clorhidrato de prilocaína.
1 ml de solución para inyección contiene 20 mg de clorhidrato de prilocaína (lo que equivale al 2%).
1 frasco de 5 ml de solución contiene 100 mg de clorhidrato de prilocaína.
Los demás componentes son: glucosa anhidra o glucosa monohidratada, agua para inyección, hidróxido de sodio 1N (para ajustar el pH).
Cómo se presenta Prilotekal y qué contiene el paquete?
Solución para inyección. Solución clara e incolora.
Prilotekal se suministra en frascos de vidrio incoloro tipo I.
Caja de 10 frascos, cada uno conteniendo 5 ml de solución para inyección.
Título de la autorización de comercialización
B.Braun Melsungen AG
Carl-Braun-Strasse 1
34212 Melsungen
Alemania
Fabricante:
Sirton Pharmaceuticals SPA
Piazza XX Settembre 2
22079 Villa Guardia (CO)
Italia
Sintetica GmbH
Albersloher Weg 11
- 48155 - Münster Alemania
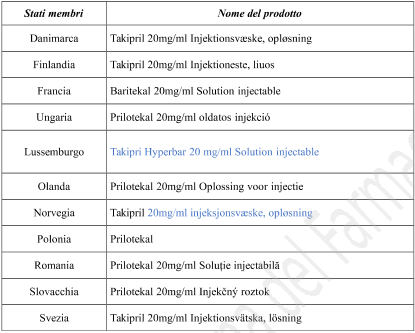
Este medicamento está autorizado para su comercialización en los países miembros del Espacio Económico Europeo bajo los siguientes nombres:
Nombres del producto en diferentes países
| País miembro | Nombre del producto |
| Austria | Takipril hyperbar 2% Injektionslösung |
| Alemania | Takipril 20 mg/ml Injektionslösung |
| Italia | Prilotekal |
| España | Takipril hiperbárica, 20mg/ml solución inyectable |
| Reino Unido | Prilotekal 20mg/ml solución para inyección |
| Bélgica | Tachipri Hyperbar 20 mg/ml Oplossing voor injectie Tachipri Hyperbar 20 mg/ml Solution injectable Tachipri Hyperbar 20 mg/ml Injektionslösung |
| Bulgaria | Takipril 20 mg/ml Инжекционен разтвор |
| República Checa | Takiprin |
| Dinamarca | Takipril 20 mg/ml Injektionsvæske, opløsning |
| Finlandia | Takipril 20 mg/ml Injektioneste, liuos |
| Francia | Baritekal 20 mg/ml Solution injectable |
| Hungría | Prilotekal 20 mg/ml oldatos injekció |
| Luxemburgo | Tachipri Hyperbar 20 mg/ml Solution injectable |
| Países Bajos | Prilotekal 20 mg/ml Oplossing voor injectie |
| Noruega | Takipril 20 mg/ml injeksjonsvæske, oppløsning |
| Polonia | Prilotekal |
| Rumania | Prilotekal 20 mg/ml Soluţie injectabilă |
| Eslovaquia | Prilotekal 20 mg/ml Injekčný roztok |
| Suecia | Takipril 20 mg/ml Injektionsvätska, lösning |
Fecha de la última actualización de la hoja de instrucciones: septiembre 2020
La siguiente información está destinada exclusivamente al personal médico especializado:
{ La ChPL se agrega al final de la hoja de instrucciones impresa, como parte de la sección desprendible.}
- País de registro
- Principio activo
- Requiere recetaNo
- ImportadorSintetica GmbH Sirton Pharmaceuticals SpA.
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a PrilotekalForma farmacéutica: Crema, (25 mg + 25 mg)/gPrincipio activo: lidocaine, combinationsFabricante: Pierre Fabre Medicament ProductionRequiere recetaForma farmacéutica: Gel, 0.5 g/100 gPrincipio activo: LidocainaNo requiere recetaForma farmacéutica: Aerosol, 96 mg/gPrincipio activo: LidocainaFabricante: Aflofarm Farmacja Polska Sp. z o.o.No requiere receta
Alternativas a Prilotekal en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Prilotekal en España
Médicos online para Prilotekal
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Prilotekal – sujeta a valoración médica y normativa local.














