

Ovestin

Consulta con un médico sobre la receta médica de Ovestin

Cómo usar Ovestin
Hoja de instrucciones del paquete: información para el paciente
Atención! Conservar la hoja de instrucciones. Información en el embalaje primario en un idioma extranjero.
Ovestin
1 mg/g, crema vaginal
Estriol
Es importante leer atentamente el contenido de la hoja de instrucciones antes de usar el medicamento, ya que contiene información importante para el paciente.
- Debe conservar esta hoja de instrucciones para poder volver a leerla si es necesario.
- En caso de dudas, debe consultar a un médico o farmacéutico.
- Este medicamento ha sido recetado específicamente para una persona. No debe dárselo a otros. El medicamento puede ser perjudicial para otra persona, incluso si los síntomas de su enfermedad son los mismos.
- Si el paciente experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Véase el punto 4.
Índice de la hoja de instrucciones:
- 1. Qué es Ovestin y para qué se utiliza
- 2. Información importante antes de usar Ovestin
- 3. Cómo usar Ovestin
- 4. Posibles efectos adversos
- 5. Cómo conservar Ovestin
- 6. Contenido del embalaje y otra información
1. Qué es Ovestin y para qué se utiliza
Ovestin pertenece a un grupo de medicamentos llamados terapia hormonal sustitutiva (THS) para uso vaginal. El medicamento contiene el hormona femenino estriol (estrógeno). Ovestin se utiliza en mujeres posmenopáusicas, al menos 12 meses después de la última menstruación.
Ovestin se utiliza para aliviar los síntomas de la menopausia que ocurren en la vagina, como la sequedad o la irritación. En terminología médica, este fenómeno se conoce como "atrophie vaginitis". Está causado por la disminución de los niveles de estrógeno en el cuerpo y ocurre naturalmente después de la menopausia.
Si antes de la menopausia se extirpan los ovarios quirúrgicamente (un procedimiento llamado ooforectomía), la producción de estrógeno disminuye rápidamente.
La falta de estrógeno puede causar sequedad y sensibilidad aumentada de las paredes de la vagina, lo que es la causa de las relaciones sexuales dolorosas y la aparición de inflamaciones y picazón en la vagina. La falta de estrógeno también puede causar síntomas de incontinencia urinaria y cistitis recurrente. Estos síntomas suelen desaparecer después de usar medicamentos que contienen estrógeno. La mejora es generalmente notable después de unos días o semanas de iniciar el tratamiento.
Ovestin actúa reemplazando el estrógeno que normalmente produce el ovario de la mujer. El medicamento se administra vaginalmente, por lo que el hormona se libera donde es necesario.
Esto puede aliviar la sensación de incomodidad en la vagina.
La mejora puede ser notable solo después de unos días o incluso semanas.
Además de las indicaciones descritas anteriormente, Ovestin también se puede usar para:
- acelerar la curación de heridas quirúrgicas en mujeres sometidas a operaciones vaginales
- evaluar con precisión la citología vaginal en mujeres en la posmenopausia.
2. Información importante antes de usar Ovestin
Historia clínica y controles regulares
El uso de la THS conlleva un riesgo que debe considerarse al tomar la decisión de iniciar o continuar la terapia hormonal sustitutiva.
La experiencia con el tratamiento de mujeres con menopausia prematura (debido a la insuficiencia ovárica o después de una operación quirúrgica) es limitada. En mujeres con menopausia prematura, el riesgo asociado con el uso de la THS puede variar. Siempre debe consultar a un médico.
Antes de iniciar (o reanudar) el uso de la THS, el médico realizará una historia clínica sobre el estado de salud de la paciente y las enfermedades que ocurren en la familia. También puede decidir realizar un examen físico, incluyendo, si es necesario, un examen de mama y (o) un examen ginecológico vaginal.
Después de iniciar el uso de Ovestin, debe asistir regularmente a controles con su médico (al menos una vez al año). Durante el control, debe discutir con su médico los beneficios y riesgos asociados con la continuación del uso de Ovestin.
Debe realizar exámenes de mama regularmente según las recomendaciones de su médico.
Cuándo no usar Ovestin:
No use Ovestin si alguna de las siguientes situaciones se aplica a usted. En caso de duda, antes de usar Ovestin, debe consultar a un médico.
Cuándo no usar Ovestin:
- si es alérgico al estriol o a alguno de los demás componentes de este medicamento (enumerados en el punto 6 "Contenido del embalaje y otra información").
- si tiene o ha tenido cáncer de mama o si se sospecha cáncer de mama.
- si tiene o ha tenido un tumor dependiente de estrógeno, como el cáncer de endometrio (revestimiento del útero), o si se sospecha un tumor de este tipo.
- si tiene sangrado vaginal de causa desconocida.
- si tiene hiperplasia endometrial no tratada (crecimiento excesivo del revestimiento del útero).
- si tiene o ha tenido trombosis en los vasos sanguíneos (trombosis venosa), como la trombosis venosa profunda o la embolia pulmonar.
- si tiene trastornos de coagulación sanguínea (como la deficiencia de proteína C, la deficiencia de proteína S o la deficiencia de antitrombina).
- si tiene enfermedades causadas por la presencia de trombos en los vasos sanguíneos, como el infarto de miocardio, el accidente cerebrovascular o la angina de pecho.
- si tiene o ha tenido enfermedad hepática, y los resultados de las pruebas de función hepática no han vuelto a la normalidad.
- si tiene porfiria, una enfermedad rara de la sangre que se transmite de generación en generación.
Si alguno de los estados mencionados anteriormente ocurre por primera vez mientras usa Ovestin, debe dejar de usarlo de inmediato y consultar a un médico lo antes posible.
Precauciones y advertencias
Antes de iniciar el tratamiento, debe informar a su médico si alguna de las siguientes condiciones se aplica a usted, ya que durante el uso de Ovestin, estos síntomas pueden regresar o empeorar. Si esto sucede, debe asistir a controles con su médico con más frecuencia:
- miomas uterinos (mioma uterino)
- crecimiento de las células del revestimiento del útero (endometrio) fuera del útero (endometriosis) o crecimiento excesivo del revestimiento del útero (hiperplasia endometrial) en el pasado
- aumento del riesgo de formación de trombos sanguíneos [ver el punto "Trombosis venosa"]
- aumento del riesgo de desarrollar un tumor dependiente de estrógeno (como el cáncer de mama en la madre, hermana o abuela)
- hipertensión
- trastornos hepáticos, como los tumores hepáticos benignos
- diabetes con o sin cambios en los vasos sanguíneos
- colelitiasis
- migraña o dolor de cabeza severo
- enfermedad del sistema inmunológico que afecta muchos órganos internos (lupus eritematoso sistémico; enfermedad crónica de tejido conjuntivo con cambios en la piel en todo el cuerpo)
- epilepsia
- asma
- enfermedad que afecta el oído y causa pérdida de audición (otosclerosis)
- retención de líquidos en el cuerpo debido a enfermedades cardíacas o renales
- edema angioneurótico hereditario o adquirido.
Debe informar a su médico si tiene hepatitis C y está recibiendo tratamiento que incluye medicamentos como ombitasvir/paritaprevir/ritonavir y dasabuvir, administrados con ribavirina o sin ella. La administración conjunta de estos medicamentos con algunos medicamentos que contienen estrógeno puede causar un aumento en los resultados de las pruebas de función hepática (aumento de la actividad de la enzima hepática ALT); el riesgo de que esto suceda con Ovestin es desconocido en este momento.
Debe decirle a su médico si nota algún cambio en su estado mientras usa Ovestin.
Debe dejar de usar Ovestin y consultar a un médico de inmediatosi mientras usa la THS, ocurre alguno de los siguientes síntomas:
- cualquiera de los estados mencionados en el punto "Cuándo no usar Ovestin"
- ictericia (color amarillo de la piel y las membranas mucosas), que puede ser un signo de enfermedad hepática
- hinchazón de la cara, la lengua y/o la garganta y/o dificultad para tragar o urticaria, junto con dificultad para respirar, que sugieren angioedema.
- aumento significativo de la presión arterial (posibles síntomas: dolor de cabeza, fatiga, mareo)
- dolores de cabeza de tipo migrañoso que ocurren por primera vez
- embarazo
- síntomas que indican la formación de trombos sanguíneos, como:
- hinchazón y enrojecimiento dolorosos de las piernas
- dolor súbito en el pecho
- dificultad para respirar. Más información en el punto "Trombosis venosa".
Advertencia:Ovestin no es un medicamento anticonceptivo. Si han pasado menos de 12 meses desde la última menstruación o si tiene menos de 50 años, puede ser necesario usar un método anticonceptivo adicional. Debe consultar a un médico.
THS y cáncer
Hiperplasia endometrial y cáncer de endometrio
El uso de la THS con estrógeno solo en forma de tabletas durante un período prolongado puede aumentar el riesgo de desarrollar cáncer de endometrio.
No hay certeza de si existe un riesgo similar en el caso de la administración repetida o prolongada (más de un año) de Ovestin. Sin embargo, se ha demostrado que Ovestin se absorbe muy poco en la sangre y, por lo tanto, no es necesario agregar progestágeno.
El sangrado o la mancha no es generalmente una causa de preocupación, pero debe consultar a un médico. Puede ser un signo de hiperplasia endometrial.
Para evitar la estimulación del endometrio, no debe exceder la dosis máxima ni tomarla durante más de unas semanas (como máximo 4 semanas).
Los riesgos descritos a continuación se relacionan con los medicamentos de THS que se absorben en la sangre. Sin embargo, Ovestin se administra localmente en la vagina y se absorbe en la sangre en cantidades muy pequeñas. Es menos probable que los estados mencionados a continuación empeoren o reaparezcan mientras se usa Ovestin, pero en caso de duda, debe consultar a un médico.
Cáncer de mama
Los datos indican que el uso de Ovestin no aumenta el riesgo de cáncer de mama en mujeres que nunca han tenido cáncer de mama antes. No se sabe si Ovestin puede usarse de manera segura en mujeres que han tenido cáncer de mama.
Debe examinar regularmente sus senos y consultar a un médico si nota algún cambio, como:
- hundimiento de la piel
- cambios en los pezones
- cualquier bulto visible o palpable.
Además, se recomienda realizar exámenes de mamografía de screening según las recomendaciones de su médico.
Cáncer de ovario
El cáncer de ovario es raro, mucho menos común que el cáncer de mama. El uso de la THS con estrógeno solo se asocia con un aumento leve del riesgo de cáncer de ovario.
El riesgo de cáncer de ovario depende de la edad. Por ejemplo, en mujeres de 50 a 54 años que no usan THS, el cáncer de ovario se diagnostica en un período de 5 años en aproximadamente 2 de cada 2000 mujeres. En mujeres que usan THS durante 5 años, el cáncer de ovario se diagnostica en aproximadamente 3 mujeres de cada 2000 que lo usan (es decir, aproximadamente 1 caso adicional).
Efecto de la THS en el corazón o la circulación sanguínea
Trombosis venosa
El riesgo de formación de trombos sanguíneos en las venas es aproximadamente 1,3 a 3 veces mayor en mujeres que usan THS que en aquellas que no la usan, especialmente en el primer año de tratamiento.
La formación de trombos sanguíneos puede tener consecuencias graves y, si un trombo llega a los pulmones, puede causar dolor en el pecho, dificultad para respirar, pérdida de conocimiento o incluso la muerte.
La probabilidad de formación de trombos en las venas aumenta con la edad y en los casos mencionados a continuación. Si alguna de las siguientes situaciones se aplica a usted, debe informar a su médico:
- inmovilización durante un período prolongado debido a una operación quirúrgica, lesión o enfermedad (ver también el punto 3 "Necesidad de una operación")
- obesidad severa (índice de masa corporal superior a 30 kg/m2)
- trastornos de coagulación sanguínea que requieren el uso prolongado de medicamentos anticoagulantes
- trombosis venosa en las piernas, los pulmones o otro órgano en un familiar cercano
- lupus eritematoso sistémico (enfermedad crónica de tejido conjuntivo con cambios en la piel en todo el cuerpo)
- enfermedad maligna.
Los síntomas de la trombosis venosa se describen en el punto "Cuándo debe dejar de usar Ovestin y consultar a un médico de inmediato".
Comparación
En mujeres de más de 50 años que no usan THS, se puede esperar que la trombosis venosa ocurra en un período de 5 años en aproximadamente 4 a 7 de cada 1000 mujeres.
En mujeres de más de 50 años que han usado THS con estrógeno durante más de 5 años, el número de casos es de 5 a 8 de cada 1000 mujeres (es decir, 1 caso adicional).
Enfermedad cardíaca (infarto de miocardio)
En mujeres que usan THS con estrógeno solo, el riesgo de desarrollar enfermedad cardíaca no aumenta.
Accidente cerebrovascular
El riesgo de sufrir un accidente cerebrovascular es aproximadamente 1,5 veces mayor en mujeres que usan THS que en aquellas que no la usan. El número de casos adicionales de accidente cerebrovascular asociados con el uso de THS aumenta con la edad.
Comparación
En mujeres de más de 50 años que no usan THS, se puede esperar que el accidente cerebrovascular ocurra en un período de 5 años en aproximadamente 8 de cada 1000 mujeres, y en mujeres de la misma edad que usan THS, la tasa es de 11 casos de cada 1000 mujeres en un período de 5 años (es decir, 3 casos adicionales).
Otras condiciones
La THS no previene la pérdida de memoria. Algunas pruebas sugieren un mayor riesgo de pérdida de memoria en mujeres que comienzan a usar THS después de los 65 años. Debe consultar a un médico al respecto.
Ovestin y otros medicamentos
Debe decirle a su médico o farmacéutico todos los medicamentos que está tomando actualmente o recientemente, así como los que planea tomar, incluyendo aquellos que se venden sin receta, medicamentos herbales o otros productos naturales.
Algunos medicamentos pueden afectar la acción de Ovestin, lo que puede provocar sangrado irregular. Esto se aplica a los siguientes medicamentos:
- medicamentos antiepilépticos(como fenobarbital, fenitoína y carbamazepina)
- medicamentos usados para tratar la tuberculosis(como rifampicina, rifabutina)
- medicamentos usados para tratar el VIH(como nevirapina, efavirenz, ritonavir y nelfinavir)
- productos herbales que contienen hypericum(Hypericum perforatum)
Análisis de laboratorio
Si es necesario realizar análisis de sangre, debe informar a su médico o al personal del laboratorio que está usando Ovestin, ya que puede afectar los resultados de algunas pruebas.
Ovestin con alimentos y bebidas
Los alimentos y bebidas no afectan la acción de Ovestin.
Embarazo y lactancia
Si está embarazada o en período de lactancia, cree que puede estar embarazada o planea tener un hijo, debe consultar a un médico o farmacéutico antes de usar este medicamento.
Ovestin está destinado exclusivamente para uso en mujeres posmenopáusicas.
En caso de embarazo, debe dejar de usar Ovestin y consultar a un médico.
Las mujeres en período de lactancia deben consultar a un médico antes de usar Ovestin.
Conducción de vehículos y uso de maquinaria
El uso de Ovestin no debe afectar la capacidad de conducir vehículos o operar maquinaria. Sin embargo, la reacción individual al medicamento puede variar.
Ovestin contiene alcohol cetílico y alcohol estearílico.
El medicamento puede causar una reacción cutánea local (como dermatitis de contacto).
3. Cómo usar Ovestin
Este medicamento debe usarse siempre según las recomendaciones de su médico o farmacéutico. En caso de duda, debe consultar a un médico o farmacéutico.
En caso de cambios atróficos en el tracto urogenital inferior, la dosis recomendada es 1 aplicación al día durante las primeras semanas (como máximo 4 semanas), luego la dosis se reduce gradualmente a 1 aplicación dos veces a la semana.
Para mejorar la curación de heridas en mujeres posmenopáusicas sometidas a operaciones vaginales, la dosis recomendada es 1 aplicación al día durante 2 semanas antes de la operación y 1 aplicación dos veces a la semana durante 2 semanas después de la operación.
Para facilitar la interpretación de los resultados de la citología vaginal en mujeres posmenopáusicas, la dosis recomendada es 1 aplicación cada dos días en la semana anterior a la toma de la citología.
Ovestin crema debe usarse vaginalmente con un aplicador, preferiblemente antes de acostarse por la noche.
1 aplicación (aplicador lleno hasta el nivel de la marca circular) contiene 0,5 g de crema, lo que equivale a 0,5 mg de estriol.
- 1. Debe quitar la tapa del tubo, girarla y abrir el tubo con el extremo afilado.
- 2. Enrosque el aplicador en el tubo. Asegúrese de que el émbolo esté completamente insertado en el aplicador.
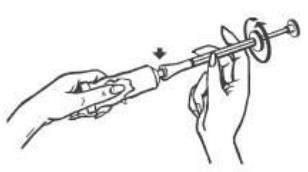
- 3. Presione lentamente la crema en el aplicador hasta que sienta resistencia en el émbolo (el émbolo se detendrá en el lugar marcado por la banda roja indicada por las flechas en la ilustración a continuación).
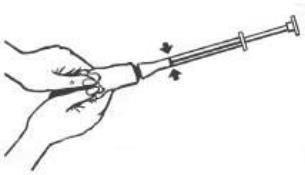
- 4. Desenrosque el aplicador del tubo y vuelva a colocar la tapa en el tubo.
- 5. En posición acostada, coloque la punta del aplicador con crema profundamente en la vagina.
- 6. Presione lentamente todo el contenido de la crema en la vagina mediante el émbolo.
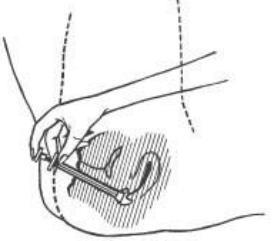
- 7. Después de usar, debe sacar el émbolo del aplicador superando el punto de resistencia y lavar ambos componentes con agua tibia y jabón. No use detergentes. Después de lavar, enjuague bien ambos componentes.
- 8. NO COLOQUE EL APLICADOR EN AGUA CALIENTE O HIRVIENDO.
- 9. El dispositivo se puede volver a armar insertando el émbolo en el aplicador para superar el punto de resistencia.
Después de vaciar el tubo, el aplicador debe desecharse.
Su médico tratará de recetar la dosis más baja posible que deba tomar durante el período más corto necesario para aliviar los síntomas que experimenta.
Si siente que el efecto de Ovestin es demasiado fuerte o demasiado débil, debe consultar a un médico.
Uso de una dosis mayor de la recomendada de Ovestin
En caso de uso de una dosis mayor de la recomendada, debe consultar a un médico o farmacéutico de inmediato.
En caso de ingestión de la crema, no supone un peligro para la salud y la vida. Sin embargo, debe informar a su médico. Los síntomas de sobredosis son generalmente náuseas y vómitos. En mujeres, también puede ocurrir sangrado genital después de unos días.
Olvido de una dosis de Ovestin
No debe usar una dosis doble para compensar una dosis olvidada.
En caso de olvido de una dosis, el medicamento debe usarse lo antes posible, a menos que sea el día de la próxima aplicación. Si el olvido se detecta el día de la próxima aplicación, debe omitir la dosis olvidada y usar las siguientes según el esquema establecido anteriormente.
Necesidad de una operación
Las personas que deban someterse a una operación deben informar a su cirujano de que están usando Ovestin. Es posible que sea necesario suspender el uso de Ovestin aproximadamente 4 a 6 semanas antes de la operación para reducir el riesgo de formación de trombos sanguíneos (ver el punto 2 "Trombosis venosa"). Debe preguntar a su médico cuándo puede volver a usar Ovestin.
En caso de dudas adicionales sobre el uso de este medicamento, debe consultar a un médico o farmacéutico.
4. Posibles efectos adversos
Como cualquier medicamento, Ovestin puede causar efectos adversos, aunque no todos los experimentarán.
Las siguientes enfermedades se informan con más frecuencia en mujeres que usan THS en forma de medicamentos que se absorben en la sangre que en aquellas que no usan THS. Estos riesgos son menos probables en medicamentos administrados vaginalmente, como Ovestin:
- cáncer de ovario
- trombosis venosa en las venas de las piernas o los pulmones (enfermedad tromboembólica venosa)
- accidente cerebrovascular
- pérdida de memoria posible, si el uso de la THS comienza después de los 65 años. Más información sobre estos efectos adversos en el punto 2.
Dependiendo de las dosis utilizadas y la sensibilidad de la paciente, pueden ocurrir los siguientes efectos adversos:
- hinchazón y sensibilidad aumentada de los senos
- sangrado vaginal leve
- aumento de la secreción vaginal
- náuseas
- retención de líquidos en el cuerpo, generalmente manifestada como hinchazón en los tobillos o los pies
- irritación o picazón local
- síntomas similares a los de la gripe.
En la mayoría de las pacientes, estos síntomas desaparecen después de las primeras semanas de tratamiento.
Se han informado los siguientes efectos adversos durante el uso de otros medicamentos de THS:
- colecistitis
- diversas afecciones de la piel
- decoloración de la piel, especialmente en la cara o el cuello, conocida como "melasma" (manchas oscuras)
- erupciones cutáneas con bultos rojos dolorosos (eritema nodoso)
- erupción con placas rojas y ampollas (eritema multiforme).
Notificación de efectos adversos
Si experimenta algún efecto adverso, incluyendo cualquier efecto adverso no mencionado en esta hoja de instrucciones, debe informar a su médico o farmacéutico. Los efectos adversos pueden notificarse directamente al Departamento de Vigilancia de Medicamentos del Ministerio de Salud.
5. Cómo conservar Ovestin
Debe conservar este medicamento en un lugar fuera del alcance de los niños.
No use este medicamento después de la fecha de caducidad que se indica en el embalaje. La fecha de caducidad es el último día del mes indicado.
No conserve en temperaturas superiores a 25°C. No congele.
No deseche los medicamentos por el desagüe o en los contenedores de basura doméstica. Debe preguntar a su farmacéutico cómo eliminar los medicamentos que ya no necesita. Este comportamiento ayudará a proteger el medio ambiente.
6. Contenido del embalaje y otra información
Qué contiene Ovestin
- El principio activo de Ovestin es estriol. Un gramo de crema contiene 1 mg de estriol.
- Los demás componentes son: alcoholes de cadena larga, palmítico de cetilo, glicerol (E 422), alcohol cetílico, alcohol estearílico, polisorbato 60, estearato de sorbitano, ácido láctico, clorhexidina dihidrocloruro, hidróxido de sodio, agua purificada.
Cómo se presenta Ovestin y contenido del embalaje
Ovestin es una crema blanca a casi blanca, homogénea, suave y con una consistencia cremosa y un olor característico débil.
Se presenta en un tubo de aluminio con una tapa de polietileno y un aplicador con un cilindro de estireno-acrilonitrilo y un émbolo de polietileno, en una caja de cartón.
Tamaño del embalaje: 15 g de crema en el tubo.
Para obtener información más detallada, debe consultar al titular de la autorización de comercialización o al importador paralelo.
Título de la autorización de comercialización en Austria, país de exportación:
Aspen Pharma Trading Limited
3016 Lake Drive
Citywest Business Campus
Dublin 24, Irlanda
Fabricante:
Aspen Bad Oldesloe GmbH
Industriestrasse 32-36
D-23843 Bad Oldesloe
Alemania
Importador paralelo:
InPharm Sp. z o.o.
ul. Strumykowa 28/11
03-138 Varsovia
Reempaquetado por:
InPharm Sp. z o.o. Services sp. k.
ul. Chełmżyńska 249
04-458 Varsovia
Número de autorización en Austria, país de exportación:17453
Número de autorización de importación paralela:128/24
Fecha de aprobación de la hoja de instrucciones: 20.03.2024
[Información sobre la marca registrada]
- País de registro
- Principio activo
- Requiere recetaSí
- Titular de la autorización de comercialización (TAC, MAH)Aspen Pharma Trading Limited
- Esta información ha sido traducida con IA y es solo orientativa. No constituye asesoramiento médico. Consulta siempre con un médico antes de tomar cualquier medicamento.
- Alternativas a OvestinForma farmacéutica: Gel, 50 mcg/gPrincipio activo: EstriolFabricante: Italfarmaco S.A.Requiere recetaForma farmacéutica: Supositorios, 0.5 mgPrincipio activo: EstriolFabricante: Dr. Kade Pharmazeutische Fabrik GmbHRequiere recetaForma farmacéutica: Supositorios, 0.5 mgPrincipio activo: EstriolRequiere receta
Alternativas a Ovestin en otros países
Las mejores alternativas con el mismo principio activo y efecto terapéutico.
Alternativa a Ovestin en Ukraine
Alternativa a Ovestin en Spain
Médicos online para Ovestin
Consulta sobre dosis, efectos secundarios, interacciones, contraindicaciones y renovación de la receta de Ovestin – sujeta a valoración médica y normativa local.










